 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: Retinopathy of prematurity (ROP), Anti-vascular endothelial growth factor (anti-VEGF), laser coagulation, Epistemonikos, GRADE.
INTRODUCCIÓN
La retinopatía del prematuro es una patología que afecta a recién nacidos de pretérmino, siendo la segunda causa de ceguera infantil a nivel mundial. Los tratamientos más utilizados son la crioterapia o la fotocoagulación láser, pero en el último tiempo, los fármacos anti factor del crecimiento vascular endotelial (anti-VEGF) gradualmente han ganado más adeptos, principalmente en el tratamiento de pacientes con retinopatía del prematuro tipo 1 (ET-ROP). Por lo anterior, es importante realizar un resumen de la evidencia existente para evaluar la eficacia y seguridad de los fármacos anti-VEGF en retinopatía del prematuro tipo 1.
MÉTODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, analizamos los datos de los estudios primarios, realizamos un metaanálisis y preparamos una tabla de resumen de los resultados utilizando el método GRADE.
RESULTADOS Y CONCLUSIONES
Identificamos seis revisiones sistemáticas que en conjunto incluyeron 15 estudios primarios, de los cuales cinco corresponden a ensayos aleatorizados.
Concluimos que el uso de anti-VEGF en comparación con la fotocoagulación con láser, probablemente disminuye el riesgo de errores refractivos. Por otro lado, el uso de anti-VEGF podría resultar en poca o nula diferencia en la mortalidad al alta hospitalaria, opacidad de cristalino o córnea que requiera cirugía y desprendimiento completo o parcial de retina, pero la certeza de la evidencia es baja. Finalmente, no es posible establecer con claridad si los anti-VEGF comparados con la fotocoagulación láser aumenta la recurrencia de la retinopatía del prematuro, debido a que la certeza de la evidencia existente ha sido evaluada como muy baja.
La retinopatía del prematuro (ROP) es un trastorno vasoproliferativo de la retina que afecta a los recién nacidos de pretérmino (RNPT) resultando en la segunda causa de ceguera infantil en el mundo. La ablación de la retina avascular con crioterapia o con fotocoagulación con láser han sido consideradas como tratamientos útiles y eficaces para la retinopatía del prematuro [1] [2].
El rol y asociación del factor de crecimiento endotelial vascular (VEGF) en la patogénesis de la retinopatía del prematuro ha sido estudiado ampliamente. Se ha encontrado que la neovascularización retinal causante de la tracción que lleva finalmente al desprendimiento de retina, se debe principalmente al desarrollo y efecto de factores de crecimiento endotelial vascular (VEGF) [3], [4], [5]. Dado lo anterior, el uso de agentes anti-VEGF intravítreos ha ganado adeptos gradualmente e incluso ha sido recomendado por algunos oftalmólogos como terapia de primera línea para tratar la retinopatía del prematuro posterior agresiva y la enfermedad de la zona I. El objetivo de esta revisión es evaluar la eficacia y seguridad del uso de fármacos anti-VEGF cuando se usa como monoterapia en recién nacidos prematuros con retinopatía del prematuro tipo 1 en comparación con la terapia con fotocoagulación con láser.
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y re analizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia |
Véase matriz de evidencia en Epistemonikos más abajo.Encontramos seis revisiones sistemáticas [6], [7], [8], [9], [10], [11], que incluyeron 15 estudios primarios reportados en 17 referencias [12], [13], [14], [15], [16], [17], [18], [19], [20], [21], [22], [23], [24], [25], [26], [27], [28], de los cuales cinco corresponden a ensayos aleatorizados reportados en siete referencias [12], [13], [15], [19], [23], [25], [27]. La tabla y el resumen en general se basan en los ensayos aleatorizados, dado que los estudios observacionales no aumentaban la certeza de la evidencia existente, ni entregaban información adicional relevante |
|
Qué tipo de pacientes incluyeron los estudios* |
Todos los ensayos incluyeron recién nacidos prematuros con retinopatía del prematuro tipo 1 [13], [15], [19], [25], [29]. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Todos los ensayos compararon terapia con anti-VEGF versus fotocoagulación con láser (tratamiento estándar) [13], [15], [19], [25], [29]. Los anti-VEGF usados fueron bevacizumab en cuatro ensayos [13], [15], [25], [27] y ranibizumab en un ensayo [19]. |
|
Qué tipo de desenlaces midieron |
Los ensayos reportaron múltiples desenlaces, los cuales fueron agrupados por las revisiones sistemáticas de la siguiente manera:
El seguimiento promedio de los ensayos fue de seis meses con un rango que fluctuó entre ocho semanas y dos años [13], [15], [19], [25], [29]. |
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
La información sobre los efectos de anti-VEGF está basada en cinco ensayos aleatorizados que incluyeron pacientes prematuros con retinopatía del prematuro tipo 1 [13], [15], [19], [25], [27]. Dos ensayos midieron el desenlace recurrencia de retinopatía del prematuro (193 pacientes) [13], [19]. Dos ensayos midieron el desenlace mortalidad al alta hospitalaria (229 pacientes) [13], [27]. Cuatro ensayos midieron el desenlace desprendimiento completo o parcial de retina (393 pacientes) [13], [15], [19], [27]. Tres ensayos midieron el desenlace opacidad del cristalino (catarata) que requiere remoción (544 pacientes) [13], [19], [27]. Un ensayo evaluó el desenlace opacidad corneal que requiere trasplante de córnea (286 pacientes) [13]. Un ensayo midió el desenlace error de refracción (miopía) (211 pacientes) [13].
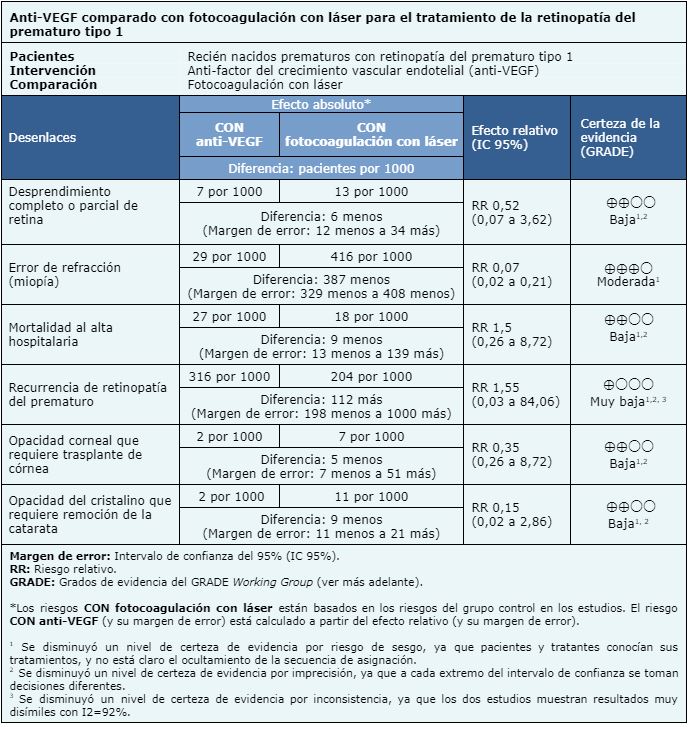
El resumen de los resultados es el siguiente:
Siga el enlace para acceder a la versión interactiva de esta tabla (Interactive Summary of Findings - iSoF)

| A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos, recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
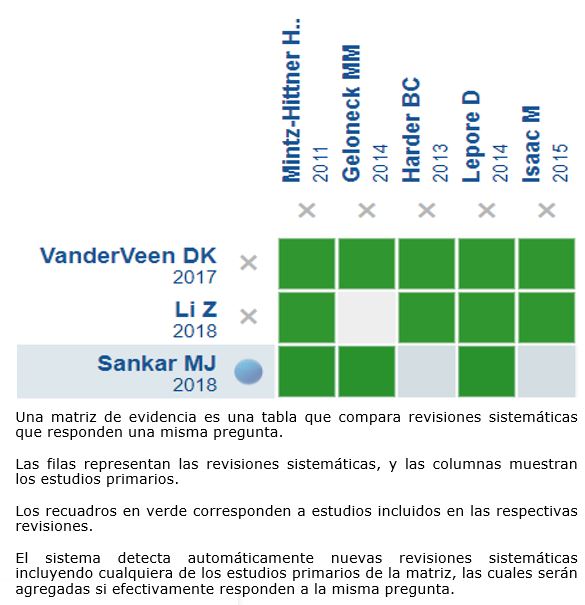
Siga el enlace para acceder a la versión interactiva: Anti-VEGF comparado con fotocoagulación con láser para la retinopatía del prematuro tipo 1.
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí.
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos.
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.

INTRODUCTION
Retinopathy of prematurity (ROP) is a condition that affects preterm infants, being the second leading cause of childhood blindness worldwide. The most commonly used treatments are cryotherapy or laser photocoagulation, but over the last few years, anti-vascular endothelial growth factor (anti-VEGF) drugs have gradually gained more adherents, mainly in the treatment of patients with type 1 retinopathy of prematurity (ET- ROP) Therefore, it is important to summarize the existing evidence to evaluate the efficacy and safety of anti-VEGF drugs in type 1 retinopathy of prematurity.
METHODS
We searched in Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified six systematic reviews including 15 studies overall, of which five were randomized trials.
We conclude that the use of anti-VEGF compared to laser photocoagulation, probably reduces the risk of refractive errors. On the other hand, the use of anti-VEGF may result in little or no difference in the mortality at hospital discharge, lens or corneal opacity requiring surgery, and complete or partial retinal detachment, but the certainty of the evidence is low. Finally, it is not possible to clearly establish whether anti-VEGF compared with laser photocoagulation, increases the recurrence of retinopathy of prematurity, because the certainty of the existing evidence has been assessed as very low.
 Autores:
Raúl González C.[1,2], Marcela Díaz C.[2,3], Rodolfo Garretón C.[1,2]
Autores:
Raúl González C.[1,2], Marcela Díaz C.[2,3], Rodolfo Garretón C.[1,2]

Citación: González C. , Díaz C. , Garretón C. . Anti-vascular endothelial growth factor (VEGF) drugs compared to laser photocoagulation for treatment of type 1 retinopathy of prematurity. Medwave 2022;22(01):e8506 doi: DOI 10.5867/medwave.2022.01.8507
Fecha de envío: 8/10/2019
Fecha de aceptación: 26/12/2019
Fecha de publicación: 17/1/2022
Origen: Este artículo es producto del Epistemonikos Evidence Synthesis Project de la Fundación Epistemonikos, en colaboración con Medwave para su publicación.
Tipo de revisión: Con revisión por pares sin ciego por parte del equipo metodológico del Centro Evidencia UC Synthesis Project

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity. Preliminary results. Arch Ophthalmol. 1988;106:471-479.
Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity. Preliminary results. Arch Ophthalmol. 1988;106:471-479.  Early Treatment for Retinopathy of Prematurity Cooperative Group. Revised indications for the treatment of retinopathy of prematurity: results of the Early Treatment for Retinopathy of Prematurity randomized trial. Arch Ophthalmol. 2003;121: 1684-1694.
Early Treatment for Retinopathy of Prematurity Cooperative Group. Revised indications for the treatment of retinopathy of prematurity: results of the Early Treatment for Retinopathy of Prematurity randomized trial. Arch Ophthalmol. 2003;121: 1684-1694.  Smith LE. IGF-1 and retinopathy of prematurity in the preterm infant. Biol Neonate. 2005;88:237-244.
Smith LE. IGF-1 and retinopathy of prematurity in the preterm infant. Biol Neonate. 2005;88:237-244.  Pierce EA, Avery RL, Foley ED, et al. Vascular endothelial growth factor/vascular permeability factor expression in a mouse model of retinal neovascularization. Proc Natl Acad Sci USA. 1995;92:905-909.
Pierce EA, Avery RL, Foley ED, et al. Vascular endothelial growth factor/vascular permeability factor expression in a mouse model of retinal neovascularization. Proc Natl Acad Sci USA. 1995;92:905-909.  Hartnett ME. Pathophysiology and mechanisms of severe retinopathy of prematurity. Ophthalmology. 2015;122:200-210.
Hartnett ME. Pathophysiology and mechanisms of severe retinopathy of prematurity. Ophthalmology. 2015;122:200-210.  Sankar, M. J., Sankar, J., & Chandra, P. Anti-vascular endothelial growth factor (VEGF) drugs for treatment of retinopathy of prematurity. Cochrane Database of Systematic Reviews. 2018 Jan 8;1:CD009734.
Sankar, M. J., Sankar, J., & Chandra, P. Anti-vascular endothelial growth factor (VEGF) drugs for treatment of retinopathy of prematurity. Cochrane Database of Systematic Reviews. 2018 Jan 8;1:CD009734.  VanderVeen, D. K., Melia, M., Yang, M. B., Hutchinson, A. K., Wilson, L. B., & Lambert, S. Anti-Vascular Endothelial Growth Factor Therapy for Primary Treatment of Type 1 Retinopathy of Prematurity: A Report by the American Academy of Ophthalmology.Ophthalmology, 2017; 24(5), 619–633.
VanderVeen, D. K., Melia, M., Yang, M. B., Hutchinson, A. K., Wilson, L. B., & Lambert, S. Anti-Vascular Endothelial Growth Factor Therapy for Primary Treatment of Type 1 Retinopathy of Prematurity: A Report by the American Academy of Ophthalmology.Ophthalmology, 2017; 24(5), 619–633.  Abri Aghdam, K., Khadamy, J., Falavarjani, K. G., & Tsui, I. Refractive outcomes following the treatment of retinopathy of prematurity in the anti-VEGF era: a literature review. Journal of American Association for Pediatric Ophthalmology and Strabismus, 2016;20(6), 539–540.
Abri Aghdam, K., Khadamy, J., Falavarjani, K. G., & Tsui, I. Refractive outcomes following the treatment of retinopathy of prematurity in the anti-VEGF era: a literature review. Journal of American Association for Pediatric Ophthalmology and Strabismus, 2016;20(6), 539–540.  Pertl, L., Steinwender, G., Mayer, C., Hausberger, S., Pöschl, E.-M., Wackernagel, W., Haas, A. A Systematic Review and Meta-Analysis on the Safety of Vascular Endothelial Growth Factor (VEGF) Inhibitors for the Treatment of Retinopathy of Prematurity. PLOS ONE, 2015,10(6)
Pertl, L., Steinwender, G., Mayer, C., Hausberger, S., Pöschl, E.-M., Wackernagel, W., Haas, A. A Systematic Review and Meta-Analysis on the Safety of Vascular Endothelial Growth Factor (VEGF) Inhibitors for the Treatment of Retinopathy of Prematurity. PLOS ONE, 2015,10(6)  Mihai Mititelu, MD, MPH; Khurram M. Chaudhary, MD; Ronni M. Lieberman, MD.An Evidence-Based Meta-analysis of Vascular Endothelial Growth Factor Inhibition in Pediatric Retinal Diseases: Part 1. Retinopathy of Prematurity.Journal of Pediatric Ophthalmology and Strabismus. 2012;49(6):332-340
Mihai Mititelu, MD, MPH; Khurram M. Chaudhary, MD; Ronni M. Lieberman, MD.An Evidence-Based Meta-analysis of Vascular Endothelial Growth Factor Inhibition in Pediatric Retinal Diseases: Part 1. Retinopathy of Prematurity.Journal of Pediatric Ophthalmology and Strabismus. 2012;49(6):332-340  Li Z, Zhang Y, Liao Y, Zeng R, Zeng P, Lan Y. Comparison of efficacy between anti-vascular endothelial growth factor (VEGF) and laser treatment in Type-1 and threshold retinopathy of prematurity (ROP). BMC Ophthalmology. 2018;18(1).
Li Z, Zhang Y, Liao Y, Zeng R, Zeng P, Lan Y. Comparison of efficacy between anti-vascular endothelial growth factor (VEGF) and laser treatment in Type-1 and threshold retinopathy of prematurity (ROP). BMC Ophthalmology. 2018;18(1).  Geloneck, M. M., Chuang, A. Z., Clark, W. L., Hunt, M. G., Norman, A. A., Packwood, E. A.,Mintz-Hittner, H. A. (2014). Refractive Outcomes Following Bevacizumab Monotherapy Compared With Conventional Laser Treatment. JAMA Ophthalmology, 132(11), 1327
Geloneck, M. M., Chuang, A. Z., Clark, W. L., Hunt, M. G., Norman, A. A., Packwood, E. A.,Mintz-Hittner, H. A. (2014). Refractive Outcomes Following Bevacizumab Monotherapy Compared With Conventional Laser Treatment. JAMA Ophthalmology, 132(11), 1327  Mintz-Hittner, H. A., Kennedy, K. A., & Chuang, A. Z. (2011). Efficacy of Intravitreal Bevacizumab for Stage 3+ Retinopathy of Prematurity. New England Journal of Medicine, 364(7), 603–615.
Mintz-Hittner, H. A., Kennedy, K. A., & Chuang, A. Z. (2011). Efficacy of Intravitreal Bevacizumab for Stage 3+ Retinopathy of Prematurity. New England Journal of Medicine, 364(7), 603–615.  Harder, B. C., Schlichtenbrede, F. C., von Baltz, S., Jendritza, W., Jendritza, B., & Jonas, J. B. (2013). Intravitreal Bevacizumab for Retinopathy of Prematurity: Refractive Error Results. American Journal of Ophthalmology, 155(6), 1119–1124.
Harder, B. C., Schlichtenbrede, F. C., von Baltz, S., Jendritza, W., Jendritza, B., & Jonas, J. B. (2013). Intravitreal Bevacizumab for Retinopathy of Prematurity: Refractive Error Results. American Journal of Ophthalmology, 155(6), 1119–1124.  Lepore, D., Quinn, G. E., Molle, F., Baldascino, A., Orazi, L., Sammartino, M. Romagnoli, C. (2014). Intravitreal Bevacizumab versus Laser Treatment in Type 1 Retinopathy of Prematurity. Ophthalmology, 121(11), 2212–2219.
Lepore, D., Quinn, G. E., Molle, F., Baldascino, A., Orazi, L., Sammartino, M. Romagnoli, C. (2014). Intravitreal Bevacizumab versus Laser Treatment in Type 1 Retinopathy of Prematurity. Ophthalmology, 121(11), 2212–2219.  Isaac, M., Mireskandari, K., & Tehrani, N. (2015). Treatment of type 1 retinopathy of prematurity with bevacizumab versus laser. Journal of American Association for Pediatric Ophthalmology and Strabismus, 19(2), 140–144.
Isaac, M., Mireskandari, K., & Tehrani, N. (2015). Treatment of type 1 retinopathy of prematurity with bevacizumab versus laser. Journal of American Association for Pediatric Ophthalmology and Strabismus, 19(2), 140–144.  Harder, B. C., von Baltz, S., Schlichtenbrede, F. C., & Jonas, J. B. (2012). Early Refractive Outcome After Intravitreous Bevacizumab for Retinopathy of Prematurity. Archives of Ophthalmology, 130(6).
Harder, B. C., von Baltz, S., Schlichtenbrede, F. C., & Jonas, J. B. (2012). Early Refractive Outcome After Intravitreous Bevacizumab for Retinopathy of Prematurity. Archives of Ophthalmology, 130(6).  Moran, S., O’Keefe, M., Hartnett, C., Lanigan, B., Murphy, J., & Donoghue, V. (2014). Bevacizumab versus diode laser in stage 3 posterior retinopathy of prematurity. Acta Ophthalmologica, 92(6), e496–e497.
Moran, S., O’Keefe, M., Hartnett, C., Lanigan, B., Murphy, J., & Donoghue, V. (2014). Bevacizumab versus diode laser in stage 3 posterior retinopathy of prematurity. Acta Ophthalmologica, 92(6), e496–e497.  Zhang, G., Yang, M., Zeng, J., Vakros, G., Su, K., Chen, M. Zhuang, R. (2017). Comparison of intravitreal injection of Ranibizumab versus laser therapy for Zone II treatment- requiring retinopathy of prematury . Retina, 37(4), 710–717.
Zhang, G., Yang, M., Zeng, J., Vakros, G., Su, K., Chen, M. Zhuang, R. (2017). Comparison of intravitreal injection of Ranibizumab versus laser therapy for Zone II treatment- requiring retinopathy of prematury . Retina, 37(4), 710–717.  Hwang, C. K., Hubbard, G. B., Hutchinson, A. K., & Lambert, S. R. (2015). Outcomes after Intravitreal Bevacizumab versus Laser Photocoagulation for Retinopathy of Prematurity. Ophthalmology, 122(5), 1008–1015.
Hwang, C. K., Hubbard, G. B., Hutchinson, A. K., & Lambert, S. R. (2015). Outcomes after Intravitreal Bevacizumab versus Laser Photocoagulation for Retinopathy of Prematurity. Ophthalmology, 122(5), 1008–1015.  Lee, J. Y., Chae, J. B., Yang, S. J., Yoon, Y. H., & Kim, J.-G. (2010). Effects of intravitreal bevacizumab and laser in retinopathy of prematurity therapy on the development of peripheral retinal vessels. Graefe’s Archive for Clinical and Experimental Ophthalmology, 248(9), 1257–1262
Lee, J. Y., Chae, J. B., Yang, S. J., Yoon, Y. H., & Kim, J.-G. (2010). Effects of intravitreal bevacizumab and laser in retinopathy of prematurity therapy on the development of peripheral retinal vessels. Graefe’s Archive for Clinical and Experimental Ophthalmology, 248(9), 1257–1262  Gunay, M., Celik, G., Tuten, A., Karatekin, G., Bardak, H., & Ovali, F. (2016). Characteristics of Severe Retinopathy of Prematurity in Infants with Birth Weight above 1500 Grams at a Referral Center in Turkey. PLOS ONE, 11(8), e0161692.
Gunay, M., Celik, G., Tuten, A., Karatekin, G., Bardak, H., & Ovali, F. (2016). Characteristics of Severe Retinopathy of Prematurity in Infants with Birth Weight above 1500 Grams at a Referral Center in Turkey. PLOS ONE, 11(8), e0161692.  Helen Mintz-Hittner, MD, The University of Texas Health Science Center, Houston. Bevacizumab Eliminates the Angiogenic Threat for Retinopathy of Prematurity (BEAT-ROP).ClinicalTrials.gov Identifier: NCT00622726 June 6, 2017
Helen Mintz-Hittner, MD, The University of Texas Health Science Center, Houston. Bevacizumab Eliminates the Angiogenic Threat for Retinopathy of Prematurity (BEAT-ROP).ClinicalTrials.gov Identifier: NCT00622726 June 6, 2017
 Mueller, B., Salchow, D. J., Waffenschmidt, E., Joussen, A. M., Schmalisch, G., Czernik, C.,Winterhalter, S. (2016). Treatment of type I ROP with intravitreal bevacizumab or laser photocoagulation according to retinal zone. British Journal of Ophthalmology, bjophthalmol–2016
Mueller, B., Salchow, D. J., Waffenschmidt, E., Joussen, A. M., Schmalisch, G., Czernik, C.,Winterhalter, S. (2016). Treatment of type I ROP with intravitreal bevacizumab or laser photocoagulation according to retinal zone. British Journal of Ophthalmology, bjophthalmol–2016  O'Keeffe N, Murphy J, O'Keefe M, Lanigan B.Bevacizumab compared with diode laser in stage 3 posterior retinopathy of prematurity: A 5 year follow up.Ir Med J. 2016 Feb 19;109(2):355.
O'Keeffe N, Murphy J, O'Keefe M, Lanigan B.Bevacizumab compared with diode laser in stage 3 posterior retinopathy of prematurity: A 5 year follow up.Ir Med J. 2016 Feb 19;109(2):355.  Gunay, M., Sukgen, E. A., Celik, G., & Kocluk, Y. (2016). Comparison of Bevacizumab, Ranibizumab, and Laser Photocoagulation in the Treatment of Retinopathy of Prematurity in Turkey. Current Eye Research, 42(3), 462–469.
Gunay, M., Sukgen, E. A., Celik, G., & Kocluk, Y. (2016). Comparison of Bevacizumab, Ranibizumab, and Laser Photocoagulation in the Treatment of Retinopathy of Prematurity in Turkey. Current Eye Research, 42(3), 462–469.  Karkhaneh, R., Khodabande, A., Riazi-Eafahani, M., Roohipoor, R., Ghassemi, F., Imani, M.,Torabi, H. (2016). Efficacy of intravitreal bevacizumab for zone-II retinopathy of prematurity. Acta Ophthalmologica, 94(6), e417–e420.
Karkhaneh, R., Khodabande, A., Riazi-Eafahani, M., Roohipoor, R., Ghassemi, F., Imani, M.,Torabi, H. (2016). Efficacy of intravitreal bevacizumab for zone-II retinopathy of prematurity. Acta Ophthalmologica, 94(6), e417–e420.  Kuo, H.-K., Sun, I.-T., Chung, M.-Y., & Chen, Y.-H. (2015). Refractive Error in Patients with Retinopathy of Prematurity after Laser Photocoagulation or Bevacizumab Monotherapy. Ophthalmologica, 234(4), 211–217.
Kuo, H.-K., Sun, I.-T., Chung, M.-Y., & Chen, Y.-H. (2015). Refractive Error in Patients with Retinopathy of Prematurity after Laser Photocoagulation or Bevacizumab Monotherapy. Ophthalmologica, 234(4), 211–217.  American Academy of Ophthalmology, Weisenthal RW, Staff AA of O, Ophthalmology EB of. 2018-2019 Basic and Clinical Science Course (BCSC) [Internet]. American Academy of Ophthalmology; 2018. (Basic and clinical science course). | Link |
American Academy of Ophthalmology, Weisenthal RW, Staff AA of O, Ophthalmology EB of. 2018-2019 Basic and Clinical Science Course (BCSC) [Internet]. American Academy of Ophthalmology; 2018. (Basic and clinical science course). | Link | MINISTERIO DE SALUD. Guía Clínica RETINOPATÍA DEL PREMATURO. Santiago: Minsal, 2010.
MINISTERIO DE SALUD. Guía Clínica RETINOPATÍA DEL PREMATURO. Santiago: Minsal, 2010.  Longueira C, Perapoch J, Mart N. Retinopatía de la prematuridad. 2008
Longueira C, Perapoch J, Mart N. Retinopatía de la prematuridad. 2008