 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Palabras clave: Cannabinoids, cannabis abuse disorder, Epistemonikos, GRADE.
INTRODUCCIėN
El cannabis se erige como la droga ilĒcita mßs consumida en el mundo. Actualmente no existen alternativas farmacol¾gicas especĒficas para el tratamiento de su adicci¾n, por lo que se ha postulado la utilidad del uso de cannabinoides como herramienta terapķutica. Ellos actuarĒan principalmente a travķs de la disminuci¾n de sĒntomas de abstinencia y craving (deseo o compulsi¾n por consumir), pero su efectividad a·n no estß clara.
M╔TODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemßticas en salud a nivel mundial, la cual es mantenida mediante b·squedas en m·ltiples fuentes de informaci¾n, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios, realizamos un metanßlisis y preparamos una tabla de resumen de los resultados utilizando el mķtodo GRADE.
RESULTADOS Y CONCLUSIONES
Identificamos siete revisiones sistemßticas que en conjunto incluyeron 15 estudios primarios, de los cuales cuatro corresponden a ensayos aleatorizados. Concluimos que el uso de cannabinoides podrĒa resultar en poco o nulo aumento en la abstinencia al finalizar el tratamiento, y probablemente aumenta los efectos adversos.
El trastorno por abuso de sustancias es un problema epidemiológicamente relevante que se define por el desarrollo de patrones conductuales desadaptativos en relación al consumo de alguna sustancia, y que en general se acompaña de tolerancia, uno de los elementos diagnósticos de la dependencia. En este contexto, el cannabis se erige como una de las drogas ilícitas con potencial adictivo más consumidas en el mundo [1].
Si bien no existen alternativas farmacológicas específicas para el tratamiento del trastorno por abuso de cannabis, diversos estudios han postulado que el sistema endocannabinoide tiene un rol en la modulación de varios circuitos neuronales asociados a la adicción a drogas, y en este contexto se ha propuesto la utilización de cannabinoides como alternativa terapéutica en pacientes que sufren de trastorno por consumo de cannabis. Al igual que la terapia de reemplazo de nicotina se utiliza comúnmente para el cese del hábito tabáquico, se postula el uso de cannabinoides para la disminución de los síntomas de abstinencia y craving.
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y reanalizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia |
Encontramos siete revisiones sistemáticas [2],[3],[4], |
|
Qué tipo de pacientes incluyeron los estudios* |
Tres ensayos [9],[11],[12] incluyeron pacientes adultos con diagnóstico de dependencia a cannabis según criterios DSM - IV- TR, y uno [10] incluyó pacientes descritos como dependientes de cannabis reclutados de la comunidad sin especificar el criterio de dependencia. Tres ensayos [9],[11],[12] excluyeron pacientes que tuvieran comorbilidades psiquiátricas significativas o dependencia de otras sustancias (exceptuando nicotina y cafeína), y en uno no se especificó criterios de exclusión de los pacientes. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Dos ensayos evaluaron nabiximol (Sativex) como intervención durante 6 días [9] y durante 8 semanas [10]. Un ensayo [11] utilizó dronabinol vía oral como monoterapia y otro [12] utilizo dronabinol asociado a lofexidina (un agonista alfa-2 adrenérgico). Además, un ensayo [9] utilizó en paralelo terapia cognitivo conductual en ambos grupos. |
|
Qué tipo de desenlaces midieron |
Los ensayos evaluaron múltiples desenlaces, los cuales fueron agrupados por las distintas revisiones sistemáticas de la siguiente manera:
|
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
Cuál es la evidencia
La información sobre los efectos de cannabinoides está basada en cuatro ensayos aleatorizados que incluyen 338 pacientes [9],[10],[11],[12].
Un ensayo midió el desenlace abstinencia al fin del tratamiento (156 pacientes) [11], cuatro ensayos midieron el desenlace síntomas de abstinencia y craving (338 pacientes) [9],[10],[11],[12] y un ensayo midió el desenlace efectos adversos (156 pacientes) [11]. Respecto a los síntomas de abstinencia/craving, ninguna revisión permitió la extracción de datos de manera que pudieran ser incorporados a un metanálisis, por lo que la información de dicho desenlace se presenta como síntesis narrativa.
El resumen de los resultados es el siguiente:
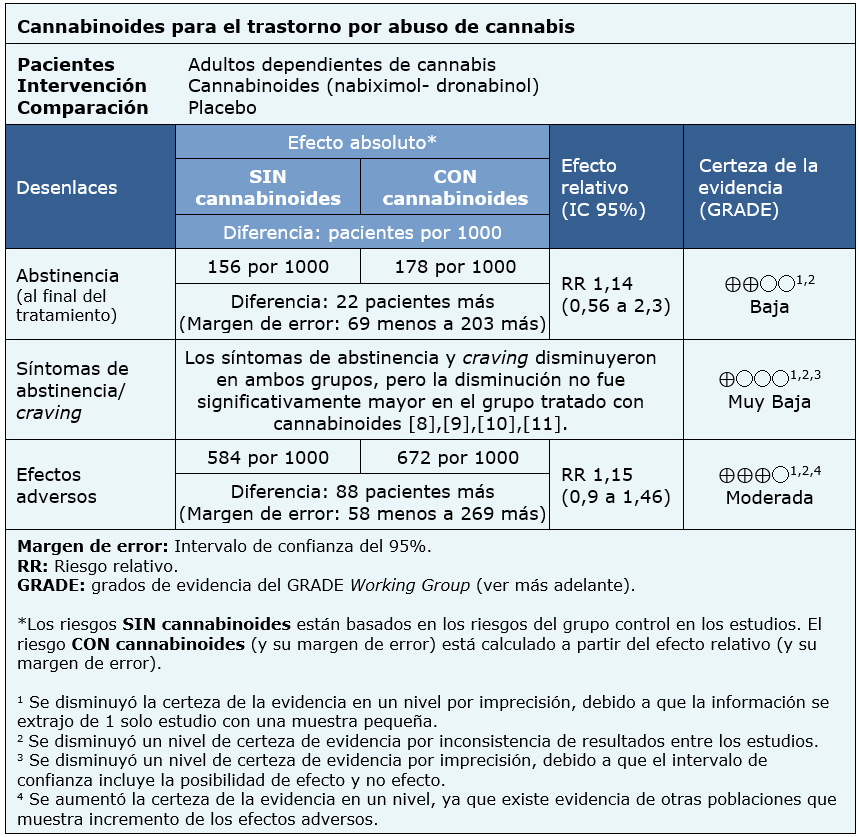
| Siga el enlace para acceder a la versión interactiva de esta tabla (Interactive Summary of Findings - iSoF) |
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
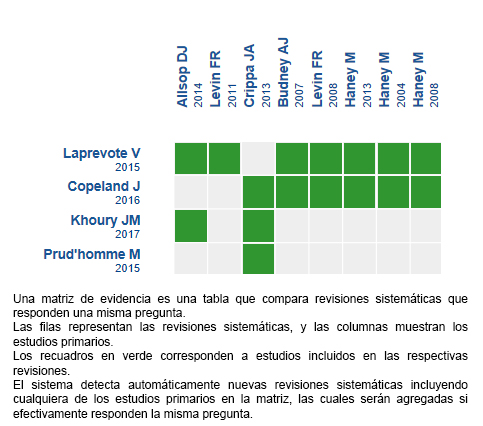
Siga el enlace para acceder a la versión interactiva: Cannabinoides para el trastorno por consumo de cannabis.
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

INTRODUCTION
Cannabis stands as the most used illegal drug in the world. Currently there are no pharmacologic alternatives to treat its addiction, so the use of Cannabinoids has been postulated as a therapeutic tool. They would act mainly through decrease in abstinence and craving symptoms but its effectiveness remains unclear.
METHODS
To answer this question we used Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified seven systematic reviews including 15 studies, of which four were randomized trials. We concluded the use of cannabinoids might result in little or no increase in abstinence at the end of treatment, and it probably increases adverse effects.
 Autores:
Andrķs RodrĒguez[1,2], Cynthia Zavala[2,3]
Autores:
Andrķs RodrĒguez[1,2], Cynthia Zavala[2,3]

Citaci¾n: RodrĒguez A, Zavala C. Cannabinoids for the treatment of cannabis abuse disorder. Medwave 2018;18(6):e7286 doi: 10.5867/medwave.2018.06.7286
Fecha de envĒo: 28/7/2018
Fecha de aceptaci¾n: 30/7/2018
Fecha de publicaci¾n: 11/10/2018
Origen: Este artĒculo es producto del Epistemonikos Evidence Synthesis Project de la Fundaci¾n Epistemonikos, en colaboraci¾n con Medwave para su publicaci¾n.
Tipo de revisi¾n: Con revisi¾n por pares sin ciego por parte del equipo metodol¾gico del Epistemonikos Evidence Synthesis Project.

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Oficina de las Naciones Unidas contra la Droga y el Delito, Informe Mundial sobre las Drogas 2017 (ISBN: 978-92-1-148291-1, eISBN: 978-92-1-060623-3, publicaci¾n de las Naciones Unidas, n·m. de venta S.17.XI.6).
Oficina de las Naciones Unidas contra la Droga y el Delito, Informe Mundial sobre las Drogas 2017 (ISBN: 978-92-1-148291-1, eISBN: 978-92-1-060623-3, publicaci¾n de las Naciones Unidas, n·m. de venta S.17.XI.6).  Marshall K, Gowing L, Ali R, Le Foll B. Pharmacotherapies for cannabis dependence. Cochrane Database of Systematic Reviews. 2014;12(12):CD008940.
Marshall K, Gowing L, Ali R, Le Foll B. Pharmacotherapies for cannabis dependence. Cochrane Database of Systematic Reviews. 2014;12(12):CD008940.  Kowal MA, Hazekamp A, Grotenhermen F. Review on clinical studies with cannabis and cannabinoids 2010-2014. Cannabinoids. 2016;11(special issue):1-18.
Kowal MA, Hazekamp A, Grotenhermen F. Review on clinical studies with cannabis and cannabinoids 2010-2014. Cannabinoids. 2016;11(special issue):1-18.  Laprevote V, Schwan R, Schwitzer T, Rolland B, Thome J. Is there a place for off-label pharmacotherapy in cannabis use disorder? A review on efficacy and safety. Current pharmaceutical design. 2015;21(23):3298-305.
Laprevote V, Schwan R, Schwitzer T, Rolland B, Thome J. Is there a place for off-label pharmacotherapy in cannabis use disorder? A review on efficacy and safety. Current pharmaceutical design. 2015;21(23):3298-305.  Marshall K, Gowing L, Ali R, Le Foll B. Pharmacotherapies for cannabis dependence. Cochrane Database of Systematic Reviews. 2014;12(12):CD008940.
Marshall K, Gowing L, Ali R, Le Foll B. Pharmacotherapies for cannabis dependence. Cochrane Database of Systematic Reviews. 2014;12(12):CD008940.  Prud'homme M, Cata R, Jutras-Aswad D. Cannabidiol as an Intervention for Addictive Behaviors: A Systematic Review of the Evidence. Substance abuse : research and treatment. 2015;9:33-8.
Prud'homme M, Cata R, Jutras-Aswad D. Cannabidiol as an Intervention for Addictive Behaviors: A Systematic Review of the Evidence. Substance abuse : research and treatment. 2015;9:33-8.  Bahji A., Mazhar M.N.. Treatment of cannabis dependence with synthetic cannabinoids: A systematic review. Canadian Journal of Addiction. 2016;7(4):8-13.
Bahji A., Mazhar M.N.. Treatment of cannabis dependence with synthetic cannabinoids: A systematic review. Canadian Journal of Addiction. 2016;7(4):8-13.  Copeland J, Pokorski I. Progress toward pharmacotherapies for cannabis-use disorder: an evidence-based review. Subst Abuse Rehabil. 2016 May 3;7:41-53. | CrossRef | PubMed | PMC |
Copeland J, Pokorski I. Progress toward pharmacotherapies for cannabis-use disorder: an evidence-based review. Subst Abuse Rehabil. 2016 May 3;7:41-53. | CrossRef | PubMed | PMC | Allsop DJ, Copeland J, Lintzeris N, Dunlop AJ, Montebello M, Sadler C, Rivas GR, Holland RM, Muhleisen P, Norberg MM, Booth J, McGregor IS. Nabiximols as an agonist replacement therapy during cannabis withdrawal: a randomized clinical trial. JAMA psychiatry. 2014;71(3):281-91.
Allsop DJ, Copeland J, Lintzeris N, Dunlop AJ, Montebello M, Sadler C, Rivas GR, Holland RM, Muhleisen P, Norberg MM, Booth J, McGregor IS. Nabiximols as an agonist replacement therapy during cannabis withdrawal: a randomized clinical trial. JAMA psychiatry. 2014;71(3):281-91.  Trigo JM, Lagzdins D, Rehm J, Selby P, Gamaleddin I, Fischer B, Barnes AJ, Huestis MA, Le Foll B. Effects of fixed or self-titrated dosages of Sativex on cannabis withdrawal and cravings. Drug and alcohol dependence. 2016;161:298-306.
Trigo JM, Lagzdins D, Rehm J, Selby P, Gamaleddin I, Fischer B, Barnes AJ, Huestis MA, Le Foll B. Effects of fixed or self-titrated dosages of Sativex on cannabis withdrawal and cravings. Drug and alcohol dependence. 2016;161:298-306.  Levin FR, Mariani JJ, Brooks DJ, Pavlicova M, Cheng W, Nunes EV. Dronabinol for the treatment of cannabis dependence: a randomized, double-blind, placebo-controlled trial. Drug and alcohol dependence. 2011;116(1-3):142-50.
Levin FR, Mariani JJ, Brooks DJ, Pavlicova M, Cheng W, Nunes EV. Dronabinol for the treatment of cannabis dependence: a randomized, double-blind, placebo-controlled trial. Drug and alcohol dependence. 2011;116(1-3):142-50.  Levin FR, Mariani JJ, Pavlicova M, Brooks D, Glass A, Mahony A, Nunes EV, Bisaga A, Dakwar E, Carpenter KM, Sullivan MA, Choi JC. Dronabinol and lofexidine for cannabis use disorder: A randomized, double-blind, placebo-controlled trial. Drug and alcohol dependence. 2016;159:53-60.
Levin FR, Mariani JJ, Pavlicova M, Brooks D, Glass A, Mahony A, Nunes EV, Bisaga A, Dakwar E, Carpenter KM, Sullivan MA, Choi JC. Dronabinol and lofexidine for cannabis use disorder: A randomized, double-blind, placebo-controlled trial. Drug and alcohol dependence. 2016;159:53-60.  Trigo JM, Soliman A, Staios G, Quilty L, Fischer B, George TP, Rehm J, Selby P, Barnes AJ, Huestis MA, Le Foll B. Sativex Associated With Behavioral-Relapse Prevention Strategy as Treatment for Cannabis Dependence: A Case Series. Journal of addiction medicine. 2016;10(4):274-9.
Trigo JM, Soliman A, Staios G, Quilty L, Fischer B, George TP, Rehm J, Selby P, Barnes AJ, Huestis MA, Le Foll B. Sativex Associated With Behavioral-Relapse Prevention Strategy as Treatment for Cannabis Dependence: A Case Series. Journal of addiction medicine. 2016;10(4):274-9.  Shannon S, Opila-Lehman J. Cannabidiol Oil for Decreasing Addictive Use of Marijuana: A Case Report. Integrative medicine (Encinitas, Calif.). 2015;14(6):31-5.
Shannon S, Opila-Lehman J. Cannabidiol Oil for Decreasing Addictive Use of Marijuana: A Case Report. Integrative medicine (Encinitas, Calif.). 2015;14(6):31-5.  Crippa JA, Hallak JE, Machado-de-Sousa JP, Queiroz RH, Bergamaschi M, Chagas MH, Zuardi AW. Cannabidiol for the treatment of cannabis withdrawal syndrome: a case report. Journal of clinical pharmacy and therapeutics. 2013;38(2):162-4.
Crippa JA, Hallak JE, Machado-de-Sousa JP, Queiroz RH, Bergamaschi M, Chagas MH, Zuardi AW. Cannabidiol for the treatment of cannabis withdrawal syndrome: a case report. Journal of clinical pharmacy and therapeutics. 2013;38(2):162-4.  Budney AJ, Vandrey RG, Hughes JR, Moore BA, Bahrenburg B. Oral delta-9-tetrahydrocannabinol suppresses cannabis withdrawal symptoms. Drug and alcohol dependence. 2007;86(1):22-9.
Budney AJ, Vandrey RG, Hughes JR, Moore BA, Bahrenburg B. Oral delta-9-tetrahydrocannabinol suppresses cannabis withdrawal symptoms. Drug and alcohol dependence. 2007;86(1):22-9.  Levin FR, Kleber HD. Use of dronabinol for cannabis dependence: two case reports and review. The American journal on addictions. 2008;17(2):161-4.
Levin FR, Kleber HD. Use of dronabinol for cannabis dependence: two case reports and review. The American journal on addictions. 2008;17(2):161-4.  Hart CL, Haney M, Ward AS, Fischman MW, Foltin RW. Effects of oral THC maintenance on smoked marijuana self-administration. Drug and alcohol dependence. 2002;67(3):301-9.
Hart CL, Haney M, Ward AS, Fischman MW, Foltin RW. Effects of oral THC maintenance on smoked marijuana self-administration. Drug and alcohol dependence. 2002;67(3):301-9.  Haney M, Cooper ZD, Bedi G, Vosburg SK, Comer SD, Foltin RW. Nabilone decreases marijuana withdrawal and a laboratory measure of marijuana relapse. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2013;38(8):1557-65.
Haney M, Cooper ZD, Bedi G, Vosburg SK, Comer SD, Foltin RW. Nabilone decreases marijuana withdrawal and a laboratory measure of marijuana relapse. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2013;38(8):1557-65.  Haney M, Hart CL, Vosburg SK, Nasser J, Bennett A, Zubaran C, Foltin RW. Marijuana withdrawal in humans: effects of oral THC or divalproex. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2004;29(1):158-70.
Haney M, Hart CL, Vosburg SK, Nasser J, Bennett A, Zubaran C, Foltin RW. Marijuana withdrawal in humans: effects of oral THC or divalproex. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2004;29(1):158-70.  Haney M, Hart CL, Vosburg SK, Comer SD, Reed SC, Foltin RW. Effects of THC and lofexidine in a human laboratory model of marijuana withdrawal and relapse. Psychopharmacology. 2008;197(1):157-68.
Haney M, Hart CL, Vosburg SK, Comer SD, Reed SC, Foltin RW. Effects of THC and lofexidine in a human laboratory model of marijuana withdrawal and relapse. Psychopharmacology. 2008;197(1):157-68.  Morgan CJ, Freeman TP, Schafer GL, Curran HV. Cannabidiol attenuates the appetitive effects of Delta 9-tetrahydrocannabinol in humans smoking their chosen cannabis. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2010;35(9):1879-85.
Morgan CJ, Freeman TP, Schafer GL, Curran HV. Cannabidiol attenuates the appetitive effects of Delta 9-tetrahydrocannabinol in humans smoking their chosen cannabis. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology. 2010;35(9):1879-85.  Morgan CJ, Schafer G, Freeman TP, Curran HV. Impact of cannabidiol on the acute memory and psychotomimetic effects of smoked cannabis: naturalistic study: naturalistic study [corrected]. The British journal of psychiatry : the journal of mental science. 2010;197(4):285-90.
Morgan CJ, Schafer G, Freeman TP, Curran HV. Impact of cannabidiol on the acute memory and psychotomimetic effects of smoked cannabis: naturalistic study: naturalistic study [corrected]. The British journal of psychiatry : the journal of mental science. 2010;197(4):285-90.  Gabriel Rada, David Aceituno, Rubķn Allende, Gonzalo Bravo, RocĒo Bravo, Oscar Corsi, Juan Franco, Evelyn G¾mez, Rami Guinguis, Ariel Izcovich, Valentina Llovet, Diego Lobos, Eva Madrid, Macarena Morel, Luis Ortiz, Javier Pķrez-Bracchiglione, MatĒas Rocco, Jana Stojanova, Gerard Urr·tia, Cynthia Zavala. Therapeutic use of cannabis, cannabis-derived products and synthetic cannabinoids: a protocol for multiple systematic reviews. PROSPERO 2018 CRD42018097382. | Link |
Gabriel Rada, David Aceituno, Rubķn Allende, Gonzalo Bravo, RocĒo Bravo, Oscar Corsi, Juan Franco, Evelyn G¾mez, Rami Guinguis, Ariel Izcovich, Valentina Llovet, Diego Lobos, Eva Madrid, Macarena Morel, Luis Ortiz, Javier Pķrez-Bracchiglione, MatĒas Rocco, Jana Stojanova, Gerard Urr·tia, Cynthia Zavala. Therapeutic use of cannabis, cannabis-derived products and synthetic cannabinoids: a protocol for multiple systematic reviews. PROSPERO 2018 CRD42018097382. | Link |