 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: Células madre, enfermedad de Parkinson, Epistemonikos, GRADE.
INTRODUCCIÓN
Muchos pacientes con enfermedad de Parkinson tienen una respuesta limitada con el tratamiento farmacológico convencional. Se ha postulado el uso de células madre como una alternativa, aunque su efectividad sigue siendo un tema de controversia.
MÉTODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios, realizamos un metanálisis y preparamos una tabla de resumen de los resultados utilizando el método GRADE.
RESULTADOS Y CONCLUSIONES
Identificamos dos revisiones sistemáticas que en conjunto incluyeron 21 estudios primarios, de los cuales tres corresponden a ensayos aleatorizados. Concluimos que no está claro si las células madre podrían tener algún efecto sobre la sintomatología de la enfermedad de Parkinson porque la certeza de la evidencia disponible es muy baja.
La enfermedad de Parkinson es una condición progresiva y degenerativa caracterizada por la destrucción de neuronas dopaminérgicas localizadas en la sustancia nigra, específicamente en la vía nigroestriatal, lo cual lleva a una disminución progresiva de los niveles de dopamina. No obstante, en la enfermedad de Parkinson también se produce pérdida de otros grupos neuronales (serotoninérgicos, noradrenérgicos, etc) lo que afecta los niveles de otros neurotransmisores a medida que la enfermedad progresa. Lo anterior determina que con el avance de la enfermedad de Parkinson se produzca un descenso en el número de neuronas dopaminérgicas y no dopaminérgicas funcionales, resultando en una disminución de los beneficios terapéuticos [1].
El tratamiento farmacológico ha logrado grandes avances en la enfermedad de Parkinson, siendo principalmente la levodopa la droga más utilizada para controlar los síntomas de esta enfermedad. A pesar de esto, muchos pacientes siguen sintomáticos, incluso con complicaciones significativas secundarias al tratamiento como discinesias, acinesia y el deterioro de fin de dosis, por ejemplo. Por otro lado la enfermedad de Parkinson es progresiva y presenta otras manifestaciones adicionales como el deterioro cognitivo, que implica un desafío para el tratante [2].
Frente a este problema, se están investigando nuevas alternativas de tratamiento como el uso de factores neuroprotectores y el implante de células madre, cuyo potencial terapéutico podría ser de gran utilidad.
Las células madre están definidas como células precursoras que tienen la capacidad de autorrenovarse y generar múltiples tipos celulares maduros. Es necesario distinguir las células madre embrionarias de las adultas. Las primeras resultan del aislamiento y cultivo de células del blastocisto, que se forma 5 días después de la fertilización. Dentro de éstas, las células pluripotenciales pueden producir todos los tipos celulares del organismo adulto, lo cual les otorga una ventaja sobre las del adulto. Las células madre adultas o somáticas se mantienen quiescentes con capacidad de autorrenovación y de diferenciación limitadas. Se han aislado numerosos tipos de células precursoras desde tejidos adultos, llevando al concepto que todos los tejidos tienen su propio compartimento de células madres, responsables de repletar las células que mueren dentro de un órgano. Las células mesenquimáticas, por ejemplo, son de origen estromal y pueden ser aisladas virtualmente de cualquier tejido del organismo. El potencial más obvio de las células madre adultas es utilizarlas para restaurar o reemplazar tejidos que han sido dañados por enfermedades o heridas y evitar el problema ético que significa usar células derivadas de embrión, sin embargo el verdadero potencial terapéutico para tejidos no hematológicos sigue siendo motivo de investigación [3].
El trasplante de células madre constituye una alternativa novedosa en la enfermedad de Parkinson. Mediante su injerto en las regiones afectadas, busca desarrollar nuevas sinapsis y restaurar los niveles de dopamina en la vía nigroestriada. Sin embargo, la técnica requiere de neurocirugía estereotáctica para injertarlas directamente en las zonas requeridas, lo que no está exento de riesgos, por lo que aún existe controversia sobre el rol de esta intervención en la enfermedad de Parkinson.
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y reanalizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia |
Encontramos dos revisiones sistemáticas [1],[4], que incluyeron 21 estudios primarios [5],[6],[7],[8],[9], |
|
Qué tipo de pacientes incluyeron los estudios* |
Ambos ensayos incluyeron pacientes con enfermedad de Parkinson con al menos dos de los siguientes síntomas: bradicinesia, rigidez, temblor en reposo y estabilidad en su medicación. El rango de edad fue de 34 a 75 años. Un ensayo incluyó a pacientes con enfermedad de Parkinson por más de 7 años (duración promedio de 14 años) [5], mientras que el otros ensayo incluyó a pacientes con enfermedad de Parkinson avanzada, sin mencionar la duración de su enfermedad [7]. Ambos ensayos excluyeron a pacientes con neurocirugía previa o antecedente de enfermedad psiquiátrica. Un ensayo [5] excluyó a pacientes con puntaje de minimental (MMSE) menor a 24, alucinaciones con levodopa, epilepsia o accidente cerebrovascular, mientras que otro ensayo [7] excluyó el parkinsonismo atípico. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Todos los ensayos utilizaron como intervención el injerto de células de tejido mesencefálico de origen embrionario mediante cirugía estereotáctica. Todos los ensayos compararon contra placebo, que consistió en una cirugía simulada sin injerto de células fetales. Ningún ensayo reportó la dosis de levodopa administrada en caso de ser necesaria. |
|
Qué tipo de desenlaces midieron |
Todos los ensayos evaluaron:
Un ensayo [5] reportó desenlaces al primer año luego de la cirugía mientras que el segundo [7] los reportó a los dos años luego del procedimiento. |
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
Cuál es la evidencia
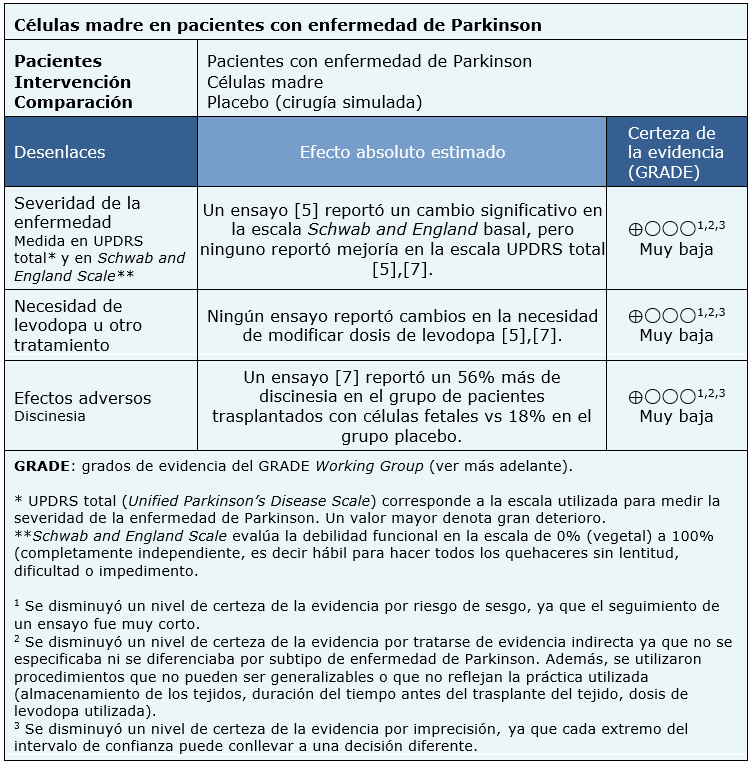
La información sobre los efectos del trasplante de células madre en pacientes con enfermedad de Parkinson está basada en dos ensayos aleatorizados [5],[7] que incluyeron a 74 pacientes en total.
Ninguna de las revisiones sistemáticas presentó metanálisis ni información que permitiera el reanálisis de los ensayos, por lo que la información presentada a continuación corresponde a una síntesis narrativa de la información obtenida desde las revisiones.
El resumen de los resultados es el siguiente:
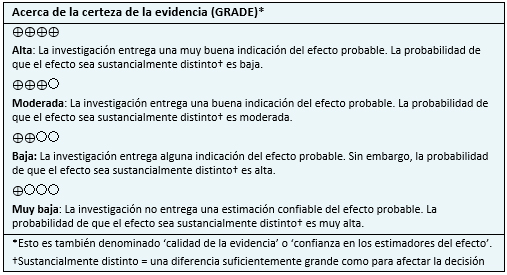
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Factibilidad |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
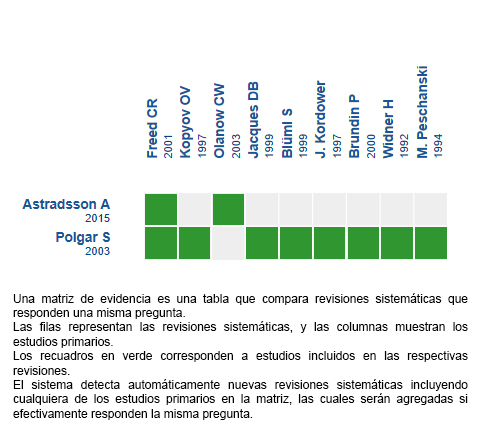
Siga el enlace para acceder a la versión interactiva: Células madre para la enfermedad de Parkinson
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

INTRODUCTION
There are many patients with Parkinson's disease who have a limited response to conventional pharmacological treatment. The use of stem cells has been postulated as an alternative, although its effectiveness remains a matter of controversy.
METHODS
To answer this question we used Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified two systematic reviews including 21 studies overall, of which three were randomized trials. We concluded it is not clear whether stem cells have any effect on the symptoms of Parkinson's disease because the certainty of the available evidence is very low.
 Autores:
Matías Rocco[1,2], Carlos Juri[2,3]
Autores:
Matías Rocco[1,2], Carlos Juri[2,3]

Citación: Rocco M, Juri C. Is treatment with stem cells effective in Parkinson's disease?. Medwave 2018;18(4):e7241 doi: 10.5867/medwave.2018.05.7241
Fecha de envío: 1/4/2018
Fecha de aceptación: 14/8/2018
Fecha de publicación: 12/9/2018
Origen: Este artículo es producto del Epistemonikos Evidence Synthesis Project de la Fundación Epistemonikos, en colaboración con Medwave para su publicación.
Tipo de revisión: Con revisión por pares sin ciego por parte del equipo metodológico del Epistemonikos Evidence Synthesis Project.

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Polgar S, Morris ME, Reilly S, Bilney B, Sanberg PR. Reconstructive neurosurgery for Parkinson's disease: a systematic review and preliminary
meta-analysis. Brain Res Bull. 2003 Apr 15;60(1-2):1-24. Review.
| PubMed |
Polgar S, Morris ME, Reilly S, Bilney B, Sanberg PR. Reconstructive neurosurgery for Parkinson's disease: a systematic review and preliminary
meta-analysis. Brain Res Bull. 2003 Apr 15;60(1-2):1-24. Review.
| PubMed | Jankovic J, Aguilar LG. Current approaches to the treatment of Parkinson's disease. Neuropsychiatr Dis Treat. 2008 Aug;4(4):743-57. | PubMed | PMC |
Jankovic J, Aguilar LG. Current approaches to the treatment of Parkinson's disease. Neuropsychiatr Dis Treat. 2008 Aug;4(4):743-57. | PubMed | PMC | Chagastelles PC, Nardi NB. Biology of stem cells: an overview. Kidney Int Suppl (2011). 2011 Sep;1(3):63-67. | PubMed | PMC |
Chagastelles PC, Nardi NB. Biology of stem cells: an overview. Kidney Int Suppl (2011). 2011 Sep;1(3):63-67. | PubMed | PMC | Astradsson A, Aziz TZ. Parkinson's disease: fetal cell or stem cell-derived treatments. BMJ Clin Evid. 2015 Apr 21;2015. pii: 1203. | PubMed | PMC |
Astradsson A, Aziz TZ. Parkinson's disease: fetal cell or stem cell-derived treatments. BMJ Clin Evid. 2015 Apr 21;2015. pii: 1203. | PubMed | PMC | Freed CR, Greene PE, Breeze RE, Tsai WY, DuMouchel W, Kao R, Dillon S, Winfield H, Culver S, Trojanowski JQ, Eidelberg D, Fahn S. Transplantation of embryonic dopamine neurons for severe Parkinson's disease. N Engl J Med. 2001 Mar 8;344(10):710-9. | PubMed |
Freed CR, Greene PE, Breeze RE, Tsai WY, DuMouchel W, Kao R, Dillon S, Winfield H, Culver S, Trojanowski JQ, Eidelberg D, Fahn S. Transplantation of embryonic dopamine neurons for severe Parkinson's disease. N Engl J Med. 2001 Mar 8;344(10):710-9. | PubMed | Kopyov OV, Jacques DS, Lieberman A, Duma CM, Rogers RL. Outcome following intrastriatal fetal mesencephalic grafts for Parkinson's patients is directly related to the volume of grafted tissue. Exp Neurol. 1997 Aug;146(2):536-45. | PubMed |
Kopyov OV, Jacques DS, Lieberman A, Duma CM, Rogers RL. Outcome following intrastriatal fetal mesencephalic grafts for Parkinson's patients is directly related to the volume of grafted tissue. Exp Neurol. 1997 Aug;146(2):536-45. | PubMed | Olanow CW, Goetz CG, Kordower JH, Stoessl AJ, Sossi V, Brin MF, Shannon KM, Nauert GM, Perl DP, Godbold J, Freeman TB. A double-blind controlled trial of bilateral fetal nigral transplantation in Parkinson's disease. Ann Neurol. 2003 Sep;54(3):403-14. | PubMed |
Olanow CW, Goetz CG, Kordower JH, Stoessl AJ, Sossi V, Brin MF, Shannon KM, Nauert GM, Perl DP, Godbold J, Freeman TB. A double-blind controlled trial of bilateral fetal nigral transplantation in Parkinson's disease. Ann Neurol. 2003 Sep;54(3):403-14. | PubMed | Jacques DB, Kopyov OV, Eagle KS, Carter T, Lieberman A. Outcomes and complications of fetal tissue transplantation in Parkinson's disease. Stereotact Funct Neurosurg. 1999;72(2-4):219-24. | PubMed |
Jacques DB, Kopyov OV, Eagle KS, Carter T, Lieberman A. Outcomes and complications of fetal tissue transplantation in Parkinson's disease. Stereotact Funct Neurosurg. 1999;72(2-4):219-24. | PubMed | Blüml S, Kopyov O, Jacques S, Ross BD. Activation of neurotransplants in humans. Exp Neurol. 1999 Jul;158(1):121-5. | PubMed |
Blüml S, Kopyov O, Jacques S, Ross BD. Activation of neurotransplants in humans. Exp Neurol. 1999 Jul;158(1):121-5. | PubMed | Kordower J., Goetz C., Freeman T., Olanow C. Dopaminergic transplants in patients with Parkinson’s disease: neuroanatomical correlates of clinical recovery. Exp. Neurol. 1997;144:41–46. | Link |
Kordower J., Goetz C., Freeman T., Olanow C. Dopaminergic transplants in patients with Parkinson’s disease: neuroanatomical correlates of clinical recovery. Exp. Neurol. 1997;144:41–46. | Link | Brundin P, Pogarell O, Hagell P, Piccini P, Widner H, Schrag A, Kupsch A, Crabb L, Odin P, Gustavii B, Björklund A, Brooks DJ, Marsden CD, Oertel WH, Quinn NP, Rehncrona S, Lindvall O. Bilateral caudate and putamen grafts of embryonic
mesencephalic tissue treated with lazaroids in Parkinson's disease. Brain. 2000 Jul;123 ( Pt 7):1380-90. | PubMed |
Brundin P, Pogarell O, Hagell P, Piccini P, Widner H, Schrag A, Kupsch A, Crabb L, Odin P, Gustavii B, Björklund A, Brooks DJ, Marsden CD, Oertel WH, Quinn NP, Rehncrona S, Lindvall O. Bilateral caudate and putamen grafts of embryonic
mesencephalic tissue treated with lazaroids in Parkinson's disease. Brain. 2000 Jul;123 ( Pt 7):1380-90. | PubMed | Widner H, Tetrud J, Rehncrona S, Snow B, Brundin P, Gustavii B, Björklund A, Lindvall O, Langston JW. Bilateral fetal mesencephalic grafting in two patients with parkinsonism induced by 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP). N Engl J Med. 1992 Nov 26;327(22):1556-63. | PubMed |
Widner H, Tetrud J, Rehncrona S, Snow B, Brundin P, Gustavii B, Björklund A, Lindvall O, Langston JW. Bilateral fetal mesencephalic grafting in two patients with parkinsonism induced by 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP). N Engl J Med. 1992 Nov 26;327(22):1556-63. | PubMed | Peschanski M, Defer G,N’Guyen J, Ricolfi F, Monfort J, Remy P. Bilateral motor improvement and alteration of l-Dopa effect in two patients with Parkinson’s disease following intrastriatal transplantation of foetal vental mesencephalon. Brain. 1994;117:487–499. | Link |
Peschanski M, Defer G,N’Guyen J, Ricolfi F, Monfort J, Remy P. Bilateral motor improvement and alteration of l-Dopa effect in two patients with Parkinson’s disease following intrastriatal transplantation of foetal vental mesencephalon. Brain. 1994;117:487–499. | Link | Kordower J, Rosenstein J, Collier T, Burke M, Chen E, Li J, Martel L, Levey A, Mufson E, Freeman T, Olanow C. Functional fetal nigral grafts in a patient with Parkinson’s disease: chemoanatomic, ultrastructural, and metabolic studies. J. Comp. Neurol. 1996;37:203–230. | Link |
Kordower J, Rosenstein J, Collier T, Burke M, Chen E, Li J, Martel L, Levey A, Mufson E, Freeman T, Olanow C. Functional fetal nigral grafts in a patient with Parkinson’s disease: chemoanatomic, ultrastructural, and metabolic studies. J. Comp. Neurol. 1996;37:203–230. | Link | Kopyov O, Jacques D, Lieberman A, Duma C, Rogers R. Clinical study of fetal mesencephalic intracerebral transplants for the treatment of Parkinson’s disease. Cell Transplant. 1996;5(2):327–337. | Link |
Kopyov O, Jacques D, Lieberman A, Duma C, Rogers R. Clinical study of fetal mesencephalic intracerebral transplants for the treatment of Parkinson’s disease. Cell Transplant. 1996;5(2):327–337. | Link | Hagell P, Schrag A, Piccini P, Jahanshahi M, Brown R, Rehncrona S, Widner H, Brundin P, Rothwell JC, Odin P, Wenning GK, Morrish P, Gustavii B, Björklund A,
Brooks DJ, Marsden CD, Quinn NP, Lindvall O. Sequential bilateral transplantation in Parkinson's disease: effects of the second graft. Brain. 1999 Jun;122 (Pt 6):1121-32. | PubMed |
Hagell P, Schrag A, Piccini P, Jahanshahi M, Brown R, Rehncrona S, Widner H, Brundin P, Rothwell JC, Odin P, Wenning GK, Morrish P, Gustavii B, Björklund A,
Brooks DJ, Marsden CD, Quinn NP, Lindvall O. Sequential bilateral transplantation in Parkinson's disease: effects of the second graft. Brain. 1999 Jun;122 (Pt 6):1121-32. | PubMed | Freed CR, Breeze RE, Schneck SA. Transplantation of fetal mesencephalic tissue in Parkinson's disease. N Engl J Med. 1995 Sep 14;333(11):730-1. | PubMed |
Freed CR, Breeze RE, Schneck SA. Transplantation of fetal mesencephalic tissue in Parkinson's disease. N Engl J Med. 1995 Sep 14;333(11):730-1. | PubMed | Schumacher JM, Ellias SA, Palmer EP, Kott HS, Dinsmore J, Dempsey PK, Fischman AJ, Thomas C, Feldman RG, Kassissieh S, Raineri R, Manhart C, Penney D, Fink JS, Isacson O. Transplantation of embryonic porcine mesencephalic tissue in patients with PD. Neurology. 2000 Mar 14;54(5):1042-50. | PubMed |
Schumacher JM, Ellias SA, Palmer EP, Kott HS, Dinsmore J, Dempsey PK, Fischman AJ, Thomas C, Feldman RG, Kassissieh S, Raineri R, Manhart C, Penney D, Fink JS, Isacson O. Transplantation of embryonic porcine mesencephalic tissue in patients with PD. Neurology. 2000 Mar 14;54(5):1042-50. | PubMed | Freeman T, Watts R, Hauser R, Bakay R, Elias S, Stoessl A, Eidelberg D, Dinsmore J, Fink S. A prospective, randomized, double-blind, surgical placebo-controlled trial of intrastriatal transplantation of fetal porcine ventral mesencephalic tissue (neurocellPD) in subjects with Parkinson’s disease. Experimental Neurology. 2002;175(2):426. | Link |
Freeman T, Watts R, Hauser R, Bakay R, Elias S, Stoessl A, Eidelberg D, Dinsmore J, Fink S. A prospective, randomized, double-blind, surgical placebo-controlled trial of intrastriatal transplantation of fetal porcine ventral mesencephalic tissue (neurocellPD) in subjects with Parkinson’s disease. Experimental Neurology. 2002;175(2):426. | Link | Defer GL, Geny C, Ricolfi F, Fenelon G, Monfort JC, Remy P, Villafane G, Jeny R, Samson Y, Keravel Y, Gaston A, Degos JD, Peschanski M, Cesaro P, Nguyen JP. Long-term outcome of unilaterally transplanted parkinsonian patients. I. Clinical approach. Brain. 1996 Feb;119 ( Pt 1):41-50. | PubMed |
Defer GL, Geny C, Ricolfi F, Fenelon G, Monfort JC, Remy P, Villafane G, Jeny R, Samson Y, Keravel Y, Gaston A, Degos JD, Peschanski M, Cesaro P, Nguyen JP. Long-term outcome of unilaterally transplanted parkinsonian patients. I. Clinical approach. Brain. 1996 Feb;119 ( Pt 1):41-50. | PubMed | Remy P, Samson Y, Hantraye P, Fontaine A, Defer G, Mangin J. Neural grafting in five parkinsonian patients: correlations between PET and clinical evolution. Ann. Neurol. 1995;38:580–588. | Link |
Remy P, Samson Y, Hantraye P, Fontaine A, Defer G, Mangin J. Neural grafting in five parkinsonian patients: correlations between PET and clinical evolution. Ann. Neurol. 1995;38:580–588. | Link | Wenning GK, Odin P, Morrish P, Rehncrona S, Widner H, Brundin P, Rothwell JC, Brown R, Gustavii B, Hagell P, Jahanshahi M, Sawle G, Björklund A, Brooks DJ,
Marsden CD, Quinn NP, Lindvall O. Short- and long-term survival and function of unilateral intrastriatal dopaminergic grafts in Parkinson's disease. Ann Neurol. 1997 Jul;42(1):95-107. | PubMed |
Wenning GK, Odin P, Morrish P, Rehncrona S, Widner H, Brundin P, Rothwell JC, Brown R, Gustavii B, Hagell P, Jahanshahi M, Sawle G, Björklund A, Brooks DJ,
Marsden CD, Quinn NP, Lindvall O. Short- and long-term survival and function of unilateral intrastriatal dopaminergic grafts in Parkinson's disease. Ann Neurol. 1997 Jul;42(1):95-107. | PubMed | Freeman TB, Olanow CW, Hauser RA, Nauert GM, Smith DA, Borlongan CV, Sanberg PR, Holt DA, Kordower JH, Vingerhoets FJ, et al. Bilateral fetal nigral transplantation into the postcommissural putamen in Parkinson's disease. Ann Neurol. 1995 Sep;38(3):379-88. | PubMed |
Freeman TB, Olanow CW, Hauser RA, Nauert GM, Smith DA, Borlongan CV, Sanberg PR, Holt DA, Kordower JH, Vingerhoets FJ, et al. Bilateral fetal nigral transplantation into the postcommissural putamen in Parkinson's disease. Ann Neurol. 1995 Sep;38(3):379-88. | PubMed | Lindvall O, Rehncrona S, Brundin P, Gustavii B, Astedt B, Widner H, Lindholm T, Björklund A, Leenders K, Rothwell J, Frackowiak R, Marsden C, Johnels B, Steg G, Freedman R, Hoffer B, Seiger A, Bygdeman M, Stromberg I, Olson L. Human fetal dopamine neurons grafted into the striatum in two patients with severe Parkinson’s disease: a detailed account of methodology and a 6-month follow-up. Arch. Neurol. 1990;46:615–631. | Link |
Lindvall O, Rehncrona S, Brundin P, Gustavii B, Astedt B, Widner H, Lindholm T, Björklund A, Leenders K, Rothwell J, Frackowiak R, Marsden C, Johnels B, Steg G, Freedman R, Hoffer B, Seiger A, Bygdeman M, Stromberg I, Olson L. Human fetal dopamine neurons grafted into the striatum in two patients with severe Parkinson’s disease: a detailed account of methodology and a 6-month follow-up. Arch. Neurol. 1990;46:615–631. | Link | Hauser RA, Freeman TB, Snow BJ, Nauert M, Gauger L, Kordower JH, Olanow CW. Long-term evaluation of bilateral fetal nigral transplantation in Parkinson disease. Arch Neurol. 1999 Feb;56(2):179-87. | PubMed |
Hauser RA, Freeman TB, Snow BJ, Nauert M, Gauger L, Kordower JH, Olanow CW. Long-term evaluation of bilateral fetal nigral transplantation in Parkinson disease. Arch Neurol. 1999 Feb;56(2):179-87. | PubMed | Fox SH, Katzenschlager R, Lim SY, Ravina B, Seppi K, Coelho M et al. (2011). The movement disorder society evidence‐based medicine review update: Treatments for the motor symptoms of Parkinson's disease. Movement Disorders, 26(S3), S2-S41.
Fox SH, Katzenschlager R, Lim SY, Ravina B, Seppi K, Coelho M et al. (2011). The movement disorder society evidence‐based medicine review update: Treatments for the motor symptoms of Parkinson's disease. Movement Disorders, 26(S3), S2-S41.  Grimes D, Gordon J, Snelgrove B, Lim-Carter I, Fon E, Martin W, et al. Canadian Guidelines on Parkinson's Disease. The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques. 2012. Jul;39 (4 Suppl 4):S1-30. | PubMed |
Grimes D, Gordon J, Snelgrove B, Lim-Carter I, Fon E, Martin W, et al. Canadian Guidelines on Parkinson's Disease. The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques. 2012. Jul;39 (4 Suppl 4):S1-30. | PubMed | National Collaborating Centre for Chronic Conditions (UK). Parkinson's Disease: National Clinical Guideline for Diagnosis and Management in Primary and Secondary Care. London: Royal College of Physicians (UK); 2006. | PubMed |
National Collaborating Centre for Chronic Conditions (UK). Parkinson's Disease: National Clinical Guideline for Diagnosis and Management in Primary and Secondary Care. London: Royal College of Physicians (UK); 2006. | PubMed | Hort J, O'Brien JT, Gainotti G, Pirttila T, Popescu BO, Rektorova I, et al; EFNS Scientist Panel on Dementia. EFNS guidelines for the diagnosis and management of Alzheimer's disease. Eur J Neurol. 2010 Oct;17(10):1236-48. | PubMed |
Hort J, O'Brien JT, Gainotti G, Pirttila T, Popescu BO, Rektorova I, et al; EFNS Scientist Panel on Dementia. EFNS guidelines for the diagnosis and management of Alzheimer's disease. Eur J Neurol. 2010 Oct;17(10):1236-48. | PubMed | Lige L, Zengmin T. Transplantation of Neural Precursor Cells in the Treatment of Parkinson Disease: An Efficacy and Safety Analysis. Turk Neurosurg. 2016;26(3):378-83. | CrossRef | PubMed |
Lige L, Zengmin T. Transplantation of Neural Precursor Cells in the Treatment of Parkinson Disease: An Efficacy and Safety Analysis. Turk Neurosurg. 2016;26(3):378-83. | CrossRef | PubMed | Yin F, Tian ZM, Liu S, Zhao QJ, Wang RM, Shen L, Wieman J, Yan Y. Transplantation of human retinal pigment epithelium cells in the treatment for Parkinson disease. CNS Neurosci Ther. 2012 Dec;18(12):1012-20. | CrossRef | PubMed |
Yin F, Tian ZM, Liu S, Zhao QJ, Wang RM, Shen L, Wieman J, Yan Y. Transplantation of human retinal pigment epithelium cells in the treatment for Parkinson disease. CNS Neurosci Ther. 2012 Dec;18(12):1012-20. | CrossRef | PubMed | Brazzini A, Cantella R, De la Cruz A, Yupanqui J, León C, Jorquiera T, Brazzini M, Ortega M, Saenz LN. Intraarterial autologous implantation of adult stem cells for patients with Parkinson disease. J Vasc Interv Radiol. 2010
Apr;21(4):443-51. Erratum in: J Vasc Interv Radiol. 2010 Jul;21(7):1141. | CrossRef | PubMed |
Brazzini A, Cantella R, De la Cruz A, Yupanqui J, León C, Jorquiera T, Brazzini M, Ortega M, Saenz LN. Intraarterial autologous implantation of adult stem cells for patients with Parkinson disease. J Vasc Interv Radiol. 2010
Apr;21(4):443-51. Erratum in: J Vasc Interv Radiol. 2010 Jul;21(7):1141. | CrossRef | PubMed | Venkataramana NK, Kumar SK, Balaraju S, Radhakrishnan RC, Bansal A, Dixit A, Rao DK, Das M, Jan M, Gupta PK, Totey SM. Open-labeled study of unilateral autologous bone-marrow-derived mesenchymal stem cell transplantation in Parkinson's disease. Transl Res. 2010 Feb;155(2):62-70. | CrossRef | PubMed |
Venkataramana NK, Kumar SK, Balaraju S, Radhakrishnan RC, Bansal A, Dixit A, Rao DK, Das M, Jan M, Gupta PK, Totey SM. Open-labeled study of unilateral autologous bone-marrow-derived mesenchymal stem cell transplantation in Parkinson's disease. Transl Res. 2010 Feb;155(2):62-70. | CrossRef | PubMed | Hayek M, A Study to Evaluate the Safety of Neural Stem Cells in Patients With Parkinson's Disease, NCT02452723. | Link |
Hayek M, A Study to Evaluate the Safety of Neural Stem Cells in Patients With Parkinson's Disease, NCT02452723. | Link | Lie J, A Study To Evaluate the Safety and Efficacy of Human Neural Stem Cells for Parkinson's Disease Patient hNSCPD, NCT03128450. | Link |
Lie J, A Study To Evaluate the Safety and Efficacy of Human Neural Stem Cells for Parkinson's Disease Patient hNSCPD, NCT03128450. | Link | Santos V, Pacheco C, Ferreira P. Clinical trials of stem-cell based therapy used in central nervous system disease a systematic review. | Link |
Santos V, Pacheco C, Ferreira P. Clinical trials of stem-cell based therapy used in central nervous system disease a systematic review. | Link |