 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Durante un episodio de sepsis, el fen¾meno de respuesta inflamatoria sistķmica desencadena un dķficit en la acci¾n y/o secreci¾n de cortisol. Se ha planteado que el uso de corticoides podrĒa tener un rol en el manejo de la sepsis, pero no existe consenso al respecto. Utilizando la base de datos Epistemonikos, la cual es mantenida mediante b·squedas en 30 bases de datos, identificamos 16 revisiones sistemßticas que en conjunto incluyen 64 estudios aleatorizados que responden esta pregunta. Realizamos un metanßlisis y tablas de resumen de los resultados utilizando el mķtodo GRADE. Concluimos que el uso de corticoides en cuadros sķpticos probablemente favorece la reversi¾n del shock, acorta brevemente la estadĒa en unidades de cuidado intensivo, y podrĒa disminuir la mortalidad, con escasos efectos adversos clĒnicamente relevantes.
La sepsis continúa siendo la principal causa de morbimortalidad en unidades de cuidados intensivos en todo el mundo. Su incidencia ha ido en aumento, con mayores complicaciones y con agentes infecciosos más resistentes. Si bien se ha observado cierta tendencia a la disminución de la mortalidad gracias a algunas intervenciones, las herramientas terapéuticas efectivas siguen siendo limitadas.
Durante un episodio de sepsis, el fenómeno de respuesta inflamatoria sistémica desencadena un déficit en la acción y/o secreción de cortisol secundario a citoquinas proinflamatorias. Por este motivo, se ha postulado que el uso de corticoides podría tener un rol en el manejo de la sepsis. Sin embargo, la evidencia ha sido contradictoria respecto a su real efecto, y aún no existe consenso sobre el rol que juega este tratamiento en la sepsis.
Utilizamos la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en 30 bases de datos, para identificar revisiones sistemáticas y sus estudios primarios incluidos. Con esta información generamos un resumen estructurado, siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios, tablas de resumen de resultados con el método GRADE, y tabla de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia. |
Encontramos dieciséis revisiones sistemáticas [1],[2],[3], |
|
Qué tipo de pacientes incluyeron los estudios |
Respecto a los tipos de pacientes, cabe destacar que diecinueve estudios fueron realizados previo al año 1991, año que se realiza el primer Consensus Definitions for Sepsis and Septic Shock [70], por lo que la definición y graduación de la severidad de la sepsis es heterogénea entre los diversos estudios, sumado al hecho del tercer Consensus Definitions for Sepsis and Septic Shock publicado recientemente [71]. |
|
Qué tipo de intervenciones incluyeron los estudios |
De los cincuenta y tres estudios, el tipo de corticoides más utilizado fue hidrocortisona (53,8%), luego dexametasona (21,1%), metilprednisolona (17,3%) y otros (ej: betametasona, prednisolona; 7,8%). La vía de administración siempre fue endovenosa en todos los estudios. Respecto a las dosis, al equiparar dosis equivalente a hidrocortisona, las dosis fueron desde 30 mg hasta 4200 mg por día. Las diferentes revisiones utilizaron definiciones distintas para considerar bajas dosis de corticoides. Algunas utilizaron una dosis equivalente < 300 mg de hidrocortisona al día, otras 400 y otras incluso 500. 50% de los estudios utilizó dosis menor o igual a 300 mg al día. Solamente dos estudios adicionaron mineralocorticoides como intervención [18],[28]. Todos los estudios compararon contra placebo o tratamiento estándar. |
|
Qué tipo de desenlaces midieron |
Las distintas revisiones sistemáticas evaluaron los siguientes desenlaces: - Mortalidad a 28 días |
La información sobre los efectos del uso de corticoides en sepsis está basada en 44 estudios aleatorizados que incluyen 5618 pacientes, 44 estudios midieron el desenlace mortalidad [17],[18],[19],[20],[21],[22],[23],[24],[25],[26],[27],[29],[30],[32],[33],[34],[39],[40],[41],[42],[43],[44],[45],[46],[47],[48],[51],[52],[53],[55],[56],[57],[58],[59],[60],[61],[62],[63],[64],[65],[66],[67],[68],[69]; 12 estudios midieron el desenlace reversión de shock [18],[19],[22],[23],[24],[25],[32],[34],[55],[57],[60],[61]; 12 estudios midieron el desenlace estadía en unidad de cuidados intensivos [18],[19], [22],[24],[25],[29],[32],[34],[44],[59],[61],[66]; 20 estudios midieron el desenlace hemorragia digestiva [18],[19],[20],[22],[24],[25],[27],[29],[32],[42],[44],[46],[55],[57],[59],[61],[63],[67],[68], [69]; 21 estudios midieron el desenlace sobreinfecciones [17],[18],[19],[20],[22],[23],[24],[25],[27],[29],[32],[39],[42],[46],[57],[59],[60],[61],[63],[68],[69]; 13 estudios midieron el desenlace hiperglicemia [18],[19],[22],[42],[44],[46],[57],[59],[60],[61],[63], [68],[69] y tres estudios midieron el desenlace mioneuropatía del paciente crítico [18],[19],[61]. El resumen de los resultados es el siguiente:
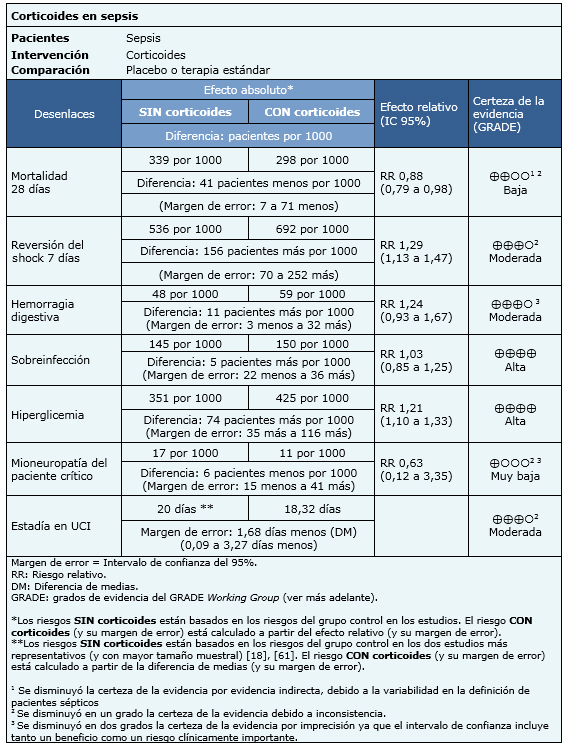

|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Qué piensan los pacientes y sus tratantes |
|
| Consideraciones de recursos |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
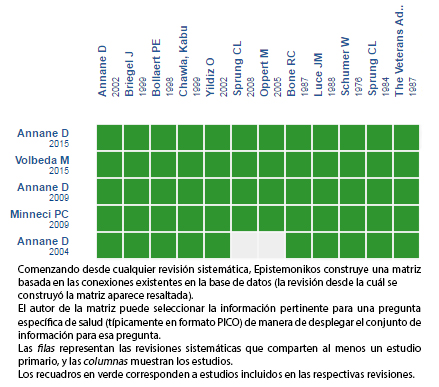
Siga el enlace para acceder a la versión interactiva: Corticoides para la sepsis
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más rápida.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta. El detalle de los métodos para elaborar este resumen están descritos aquí: http://dx.doi.org/10.5867/medwave.2014.06.5997.
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Los resúmenes de evidencia siguen un riguroso proceso de revisión por pares interno.
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

During an episode of sepsis, the systemic inflammatory response phenomenon triggers a deficit in the action and/or secretion of cortisol. It has been suggested that the use of corticosteroids may have a role in the management of sepsis, but there is no consensus. Searching in Epistemonikos database, which is maintained by screening 30 databases, we identified 16 systematic reviews including 66 randomized controlled trials addressing the question of this article. We combined the evidence using meta-analysis and generated a summary of findings following the GRADE approach. We concluded the use of corticosteroids during a sepsis episode probably favors reversal of shock, briefly shortens the stay in intensive care unit and might reduce mortality, with few clinically relevant adverse effects.
 Autores:
JoaquĒn Jerez[1,2], Ricardo Castro[2,3]
Autores:
JoaquĒn Jerez[1,2], Ricardo Castro[2,3]

Citaci¾n: Jerez J, Castro R. What is the role of corticosteroids in the management of sepsis?. Medwave 2016;16(Suppl3):e6522 doi: 10.5867/medwave.2016.6522
Fecha de publicaci¾n: 30/8/2016

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Annane D, Bellissant E, Bollaert PE, Briegel J, Keh D, Kupfer Y. Corticosteroids for treating sepsis. The Cochrane database of systematic reviews. 2015;12:CD002243. | Link |
Annane D, Bellissant E, Bollaert PE, Briegel J, Keh D, Kupfer Y. Corticosteroids for treating sepsis. The Cochrane database of systematic reviews. 2015;12:CD002243. | Link | Annane D, Bellissant E, Bollaert PE, Briegel J, Keh D, Kupfer Y. Corticosteroids for severe sepsis and septic shock: a systematic review and meta-analysis. BMJ. 2004 Aug 28;329(7464):480. | CrossRef | PubMed |
Annane D, Bellissant E, Bollaert PE, Briegel J, Keh D, Kupfer Y. Corticosteroids for severe sepsis and septic shock: a systematic review and meta-analysis. BMJ. 2004 Aug 28;329(7464):480. | CrossRef | PubMed | Annane D, Bellissant E, Bollaert PE, Briegel J, Confalonieri M, De Gaudio R,et al. Corticosteroids in the treatment of severe sepsis and septic shock in adults: a systematic review. JAMA. 2009 Jun 10;301(22):2362-75.
| CrossRef | PubMed |
Annane D, Bellissant E, Bollaert PE, Briegel J, Confalonieri M, De Gaudio R,et al. Corticosteroids in the treatment of severe sepsis and septic shock in adults: a systematic review. JAMA. 2009 Jun 10;301(22):2362-75.
| CrossRef | PubMed | Burry LD, Wax RS. Role of corticosteroids in septic shock. The Annals of pharmacotherapy. 2004;38(3):464-72. | Link |
Burry LD, Wax RS. Role of corticosteroids in septic shock. The Annals of pharmacotherapy. 2004;38(3):464-72. | Link | Cronin L, Cook DJ, Carlet J, Heyland DK, King D, Lansang MA, .Corticosteroid treatment for sepsis: a critical appraisal and meta-analysis of the literature. Crit Care Med. 1995 Aug;23(8):1430-9. | PubMed |
Cronin L, Cook DJ, Carlet J, Heyland DK, King D, Lansang MA, .Corticosteroid treatment for sepsis: a critical appraisal and meta-analysis of the literature. Crit Care Med. 1995 Aug;23(8):1430-9. | PubMed | Zhang F, Kramer CV.orticosteroids for dengue infection. Cochrane Database Syst Rev. 2014 Jul 1;(7):CD003488. | CrossRef | PubMed |
Zhang F, Kramer CV.orticosteroids for dengue infection. Cochrane Database Syst Rev. 2014 Jul 1;(7):CD003488. | CrossRef | PubMed | Ho KM, Tan JA. Use of L'Abbķ and pooled calibration plots to assess the relationship between severity of illness and effectiveness in studies ofcorticosteroids for severe sepsis. Br J Anaesth. 2011 Apr;106(4):528-36. | CrossRef | PubMed |
Ho KM, Tan JA. Use of L'Abbķ and pooled calibration plots to assess the relationship between severity of illness and effectiveness in studies ofcorticosteroids for severe sepsis. Br J Anaesth. 2011 Apr;106(4):528-36. | CrossRef | PubMed | Lefering R, Neugebauer EA. Steroid controversy in sepsis and septic shock: a meta-analysis. Crit Care Med. 1995 Jul;23(7):1294-303. | PubMed |
Lefering R, Neugebauer EA. Steroid controversy in sepsis and septic shock: a meta-analysis. Crit Care Med. 1995 Jul;23(7):1294-303. | PubMed | Menon K, McNally D, Choong K, Sampson M. A systematic review and meta-analysis on the effect of steroids in pediatric shock. Pediatr Crit Care Med. 2013 Jun;14(5):474-80.
| CrossRef | PubMed |
Menon K, McNally D, Choong K, Sampson M. A systematic review and meta-analysis on the effect of steroids in pediatric shock. Pediatr Crit Care Med. 2013 Jun;14(5):474-80.
| CrossRef | PubMed | Minneci PC, Deans KJ, Banks SM, Eichacker PQ, Natanson C. Meta-analysis: the effect of steroids on survival and shock during sepsis depends on the dose. Ann Intern Med. 2004 Jul 6;141(1):47-56. | PubMed |
Minneci PC, Deans KJ, Banks SM, Eichacker PQ, Natanson C. Meta-analysis: the effect of steroids on survival and shock during sepsis depends on the dose. Ann Intern Med. 2004 Jul 6;141(1):47-56. | PubMed | Minneci PC, Deans KJ, Eichacker PQ, Natanson C. The effects of steroids during sepsis depend on dose and severity of illness: an updated meta-analysis. Clin Microbiol Infect. 2009 Apr;15(4):308-18. | CrossRef | PubMed |
Minneci PC, Deans KJ, Eichacker PQ, Natanson C. The effects of steroids during sepsis depend on dose and severity of illness: an updated meta-analysis. Clin Microbiol Infect. 2009 Apr;15(4):308-18. | CrossRef | PubMed | Moran JL, Graham PL, Rockliff S, Bersten AD. Updating the evidence for the role of corticosteroids in severe sepsis and septic shock: a Bayesian meta-analytic perspective. Crit Care. 2010;14(4):R134. | CrossRef | PubMed |
Moran JL, Graham PL, Rockliff S, Bersten AD. Updating the evidence for the role of corticosteroids in severe sepsis and septic shock: a Bayesian meta-analytic perspective. Crit Care. 2010;14(4):R134. | CrossRef | PubMed | Patel GP, Balk RA. Systemic steroids in severe sepsis and septic shock. Am JRespir Crit Care Med. 2012 Jan 15;185(2):133-9. | CrossRef | PubMed |
Patel GP, Balk RA. Systemic steroids in severe sepsis and septic shock. Am JRespir Crit Care Med. 2012 Jan 15;185(2):133-9. | CrossRef | PubMed | Sherwin RL, Garcia AJ, Bilkovski R. Do low-dose corticosteroids improvemortality or shock reversal in patients with septic shock? A systematic reviewand position statement prepared for the American Academy of Emergency Medicine. J Emerg Med. 2012 Jul;43(1):7-12. | CrossRef | PubMed |
Sherwin RL, Garcia AJ, Bilkovski R. Do low-dose corticosteroids improvemortality or shock reversal in patients with septic shock? A systematic reviewand position statement prepared for the American Academy of Emergency Medicine. J Emerg Med. 2012 Jul;43(1):7-12. | CrossRef | PubMed | Sligl WI, Milner DA Jr, Sundar S, Mphatswe W, Majumdar SR. Safety andefficacy of corticosteroids for the treatment of septic shock: A systematic review and meta-analysis. Clin Infect Dis. 2009 Jul 1;49(1):93-101.
| CrossRef | PubMed |
Sligl WI, Milner DA Jr, Sundar S, Mphatswe W, Majumdar SR. Safety andefficacy of corticosteroids for the treatment of septic shock: A systematic review and meta-analysis. Clin Infect Dis. 2009 Jul 1;49(1):93-101.
| CrossRef | PubMed | Volbeda M, Wetterslev J, Gluud C, Zijlstra JG, van der Horst IC, Keus F.Glucocorticosteroids for sepsis: systematic review with meta-analysis and trialsequential analysis. Intensive Care Med. 2015 Jul;41(7):1220-34. | CrossRef | PubMed |
Volbeda M, Wetterslev J, Gluud C, Zijlstra JG, van der Horst IC, Keus F.Glucocorticosteroids for sepsis: systematic review with meta-analysis and trialsequential analysis. Intensive Care Med. 2015 Jul;41(7):1220-34. | CrossRef | PubMed | Abdelsalam Rezk N, Mohamed Ibrahim A. Effects of methyl prednisolone in early ARDS. Egyptian Journal of Chest Diseases and Tuberculosis. 2013;62(1):167-172. | CrossRef |
Abdelsalam Rezk N, Mohamed Ibrahim A. Effects of methyl prednisolone in early ARDS. Egyptian Journal of Chest Diseases and Tuberculosis. 2013;62(1):167-172. | CrossRef | Annane D, Sķbille V, Charpentier C, Bollaert PE, Franńois B, Korach JM, et al. Effect of treatment with low doses of hydrocortisone and fludrocortisone onmortality in patients with septic shock. JAMA. 2002 Aug 21;288(7):862-71.
| PubMed |
Annane D, Sķbille V, Charpentier C, Bollaert PE, Franńois B, Korach JM, et al. Effect of treatment with low doses of hydrocortisone and fludrocortisone onmortality in patients with septic shock. JAMA. 2002 Aug 21;288(7):862-71.
| PubMed | Arabi YM, Aljumah A, Dabbagh O, Tamim HM, Rishu AH, Al-Abdulkareem A, et al. Low-dose hydrocortisone in patients with cirrhosis and septic shock: a randomized controlled trial. CMAJ. 2010 Dec14;182(18):1971-7. | CrossRef | PubMed |
Arabi YM, Aljumah A, Dabbagh O, Tamim HM, Rishu AH, Al-Abdulkareem A, et al. Low-dose hydrocortisone in patients with cirrhosis and septic shock: a randomized controlled trial. CMAJ. 2010 Dec14;182(18):1971-7. | CrossRef | PubMed | Bennett IL Jr, Finland M, Hamburger M, Kass EH, Lepper M, Waisbren BA. Adouble-blind study of the effectiveness of cortisol in the management of severe infections. Trans Assoc Am Physicians. 1962;75:198-207. | PubMed |
Bennett IL Jr, Finland M, Hamburger M, Kass EH, Lepper M, Waisbren BA. Adouble-blind study of the effectiveness of cortisol in the management of severe infections. Trans Assoc Am Physicians. 1962;75:198-207. | PubMed | Bernard GR, Luce JM, Sprung CL, Rinaldo JE, Tate RM, Sibbald WJ, et al. High-dose corticosteroids in patients withthe adult respiratory distress syndrome. N Engl J Med. 1987 Dec 17;317(25):1565-70. | PubMed |
Bernard GR, Luce JM, Sprung CL, Rinaldo JE, Tate RM, Sibbald WJ, et al. High-dose corticosteroids in patients withthe adult respiratory distress syndrome. N Engl J Med. 1987 Dec 17;317(25):1565-70. | PubMed | Bollaert PE, Charpentier C, Levy B, Debouverie M, Audibert G, Larcan A. Reversal of late septic shock with supraphysiologic doses of hydrocortisone. Crit Care Med. 1998 Apr;26(4):645-50. | PubMed |
Bollaert PE, Charpentier C, Levy B, Debouverie M, Audibert G, Larcan A. Reversal of late septic shock with supraphysiologic doses of hydrocortisone. Crit Care Med. 1998 Apr;26(4):645-50. | PubMed | Bone RC, Fisher CJ Jr, Clemmer TP, Slotman GJ, Metz CA, Balk RA. A controlledclinical trial of high-dose methylprednisolone in the treatment of severe sepsis and septic shock. N Engl J Med. 1987 Sep 10;317(11):653-8. | PubMed |
Bone RC, Fisher CJ Jr, Clemmer TP, Slotman GJ, Metz CA, Balk RA. A controlledclinical trial of high-dose methylprednisolone in the treatment of severe sepsis and septic shock. N Engl J Med. 1987 Sep 10;317(11):653-8. | PubMed | Briegel J, Forst H, Haller M, Schelling G, Kilger E, Kuprat G, et al. Stress doses of hydrocortisonereverse hyperdynamic septic shock: a prospective, randomized, double-blind, single-center study. Crit Care Med. 1999 Apr;27(4):723-32. | PubMed |
Briegel J, Forst H, Haller M, Schelling G, Kilger E, Kuprat G, et al. Stress doses of hydrocortisonereverse hyperdynamic septic shock: a prospective, randomized, double-blind, single-center study. Crit Care Med. 1999 Apr;27(4):723-32. | PubMed | Chawla, Kabu, Kupfer, Yizhak, Goldman, Isa, Tessler, Sidney. Hydrocortisone reverses refractory septic shock. Critical Care Medicine. 1999;27(1). | Link |
Chawla, Kabu, Kupfer, Yizhak, Goldman, Isa, Tessler, Sidney. Hydrocortisone reverses refractory septic shock. Critical Care Medicine. 1999;27(1). | Link | Cicarelli DD, Vieira JE, Bense±or FE. Early dexamethasone treatment for septic shock patients: a prospective randomized clinical trial. Sao Paulo Med J. 2007 Jul 5;125(4):237-41. | PubMed |
Cicarelli DD, Vieira JE, Bense±or FE. Early dexamethasone treatment for septic shock patients: a prospective randomized clinical trial. Sao Paulo Med J. 2007 Jul 5;125(4):237-41. | PubMed | Cicarelli DD, Bense±or FE, Vieira JE. Effects of single dose of dexamethasoneon patients with systemic inflammatory response. Sao Paulo Med J. 2006 Mar 2;124(2):90-5. | PubMed |
Cicarelli DD, Bense±or FE, Vieira JE. Effects of single dose of dexamethasoneon patients with systemic inflammatory response. Sao Paulo Med J. 2006 Mar 2;124(2):90-5. | PubMed | COIITSS Study Investigators, Annane D, Cariou A, Maxime V, Azoulay E, D'honneur G, et al. Corticosteroid treatment and intensive insulin therapy for septic shock in adults: a randomized controlled trial. JAMA. 2010 Jan 27;303(4):341-8. | CrossRef | PubMed |
COIITSS Study Investigators, Annane D, Cariou A, Maxime V, Azoulay E, D'honneur G, et al. Corticosteroid treatment and intensive insulin therapy for septic shock in adults: a randomized controlled trial. JAMA. 2010 Jan 27;303(4):341-8. | CrossRef | PubMed | Confalonieri M, Urbino R, Potena A, Piattella M, Parigi P, Puccio G, et al. Hydrocortisone infusion forsevere community-acquired pneumonia: a preliminary randomized study. Am J Respir Crit Care Med. 2005 Feb 1;171(3):242-8. | PubMed |
Confalonieri M, Urbino R, Potena A, Piattella M, Parigi P, Puccio G, et al. Hydrocortisone infusion forsevere community-acquired pneumonia: a preliminary randomized study. Am J Respir Crit Care Med. 2005 Feb 1;171(3):242-8. | PubMed | de Gans J, van de Beek D. Dexamethasone in adults with bacterial meningitis. N Engl J Med. 2002 Nov 14;347(20):1549-56. | CrossRef | PubMed |
de Gans J, van de Beek D. Dexamethasone in adults with bacterial meningitis. N Engl J Med. 2002 Nov 14;347(20):1549-56. | CrossRef | PubMed | Gordon AC, Mason AJ, Perkins GD, Stotz M, Terblanche M, Ashby D, et al. The interaction of vasopressin and corticosteroids in septic shock: a ilotrandomized controlled trial. Crit Care Med. 2014 Jun;42(6):1325-33. | CrossRef | PubMed |
Gordon AC, Mason AJ, Perkins GD, Stotz M, Terblanche M, Ashby D, et al. The interaction of vasopressin and corticosteroids in septic shock: a ilotrandomized controlled trial. Crit Care Med. 2014 Jun;42(6):1325-33. | CrossRef | PubMed | Hoffman SL, Woodward TE, Hornick RB, Punjabi NH, Greisman SE. Effectivetreatment and prevention of typhoid fever: updated. Trans Am Clin Climatol Assoc. 1984;95:52-65. | PubMed |
Hoffman SL, Woodward TE, Hornick RB, Punjabi NH, Greisman SE. Effectivetreatment and prevention of typhoid fever: updated. Trans Am Clin Climatol Assoc. 1984;95:52-65. | PubMed | Hu B, Li JG, Liang H, Zhou Q, Yu Z, Li L, et al. [The effect oflow-dose hydrocortisone on requirement of norepinephrine and lactate clearance in patients with refractory septic shock]. Zhongguo Wei Zhong Bing Ji Jiu Yi Xue. 2009 Sep;21(9):529-31. | PubMed |
Hu B, Li JG, Liang H, Zhou Q, Yu Z, Li L, et al. [The effect oflow-dose hydrocortisone on requirement of norepinephrine and lactate clearance in patients with refractory septic shock]. Zhongguo Wei Zhong Bing Ji Jiu Yi Xue. 2009 Sep;21(9):529-31. | PubMed | Hughes GS Jr. Naloxone and methylprednisolone sodium succinate enhancesympathomedullary discharge in patients with septic shock. Life Sci. 1984 Dec 3;35(23):2319-26. | PubMed |
Hughes GS Jr. Naloxone and methylprednisolone sodium succinate enhancesympathomedullary discharge in patients with septic shock. Life Sci. 1984 Dec 3;35(23):2319-26. | PubMed | Huh, Jin Won, Lim, Chae-Man, Koh, Younsuck, Hong, Sang-Bum. Effect of low doses of hydrocortisone in patient with septic shock and relative adrenal insufficiency: 3 days versus 7 days treatment.: 369. Crit Care Med. 2006;34(12):A101-A101. | Link |
Huh, Jin Won, Lim, Chae-Man, Koh, Younsuck, Hong, Sang-Bum. Effect of low doses of hydrocortisone in patient with septic shock and relative adrenal insufficiency: 3 days versus 7 days treatment.: 369. Crit Care Med. 2006;34(12):A101-A101. | Link | Kaufmann I, Briegel J, Schliephake F, Hoelzl A, Chouker A, Hummel T, et al. Stress doses of hydrocortisone in septic shock: beneficial effects on opsonization-dependent neutrophil functions. Intensive Care Med. 2008 Feb;34(2):344-9. | PubMed |
Kaufmann I, Briegel J, Schliephake F, Hoelzl A, Chouker A, Hummel T, et al. Stress doses of hydrocortisone in septic shock: beneficial effects on opsonization-dependent neutrophil functions. Intensive Care Med. 2008 Feb;34(2):344-9. | PubMed | Keh D, Boehnke T, Weber-Cartens S, Schulz C, Ahlers O, Bercker S, et al. Immunologic and hemodynamic effects of "low-dose" hydrocortisone in septic shock: a double-blind, randomized, placebo-controlled, crossover study. Am J Respir Crit Care Med. 2003 Feb 15;167(4):512-20. | CrossRef | PubMed |
Keh D, Boehnke T, Weber-Cartens S, Schulz C, Ahlers O, Bercker S, et al. Immunologic and hemodynamic effects of "low-dose" hydrocortisone in septic shock: a double-blind, randomized, placebo-controlled, crossover study. Am J Respir Crit Care Med. 2003 Feb 15;167(4):512-20. | CrossRef | PubMed | Keh D, Boehnke T, Weber-Cartens S, Schulz C, Ahlers O, Bercker S, et al. Immunologic and hemodynamic effects of "low-dose" hydrocortisone in septic shock: a double-blind, randomized, placebo-controlled, crossover study. Am J Respir Crit Care Med. 2003 Feb 15;167(4):512-20. | PubMed |
Keh D, Boehnke T, Weber-Cartens S, Schulz C, Ahlers O, Bercker S, et al. Immunologic and hemodynamic effects of "low-dose" hydrocortisone in septic shock: a double-blind, randomized, placebo-controlled, crossover study. Am J Respir Crit Care Med. 2003 Feb 15;167(4):512-20. | PubMed | Klastersky J, Cappel R, Debusscher L. Effectiveness of betamethasone in management of severe infections. A double-blind study. N Engl J Med. 1971 Jun 3;284(22):1248-50. | PubMed |
Klastersky J, Cappel R, Debusscher L. Effectiveness of betamethasone in management of severe infections. A double-blind study. N Engl J Med. 1971 Jun 3;284(22):1248-50. | PubMed | Liu L, Li J, Huang YZ, Liu SQ, Yang CS, Guo FM, Qiu HB, Yang Y. [The effect of stress dose glucocorticoid on patients with acute respiratory distress syndrome combined with critical illness-related corticosteroid insufficiency]. Zhonghua Nei Ke Za Zhi. 2012 Aug;51(8):599-603. | PubMed |
Liu L, Li J, Huang YZ, Liu SQ, Yang CS, Guo FM, Qiu HB, Yang Y. [The effect of stress dose glucocorticoid on patients with acute respiratory distress syndrome combined with critical illness-related corticosteroid insufficiency]. Zhonghua Nei Ke Za Zhi. 2012 Aug;51(8):599-603. | PubMed | Lucas CE, Ledgerwood AM. The cardiopulmonary response to massive doses of steroids in patients with septic shock. Arch Surg. 1984 May;119(5):537-41. | PubMed |
Lucas CE, Ledgerwood AM. The cardiopulmonary response to massive doses of steroids in patients with septic shock. Arch Surg. 1984 May;119(5):537-41. | PubMed | Luce JM, Montgomery AB, Marks JD, Turner J, Metz CA, Murray JF. Ineffectiveness of high-dose methylprednisolone in preventing parenchymal lung injury and improving mortality in patients with septic shock. Am Rev Respir Dis. 1988 Jul;138(1):62-8. | PubMed |
Luce JM, Montgomery AB, Marks JD, Turner J, Metz CA, Murray JF. Ineffectiveness of high-dose methylprednisolone in preventing parenchymal lung injury and improving mortality in patients with septic shock. Am Rev Respir Dis. 1988 Jul;138(1):62-8. | PubMed | Marik P, Kraus P, Sribante J, Havlik I, Lipman J, Johnson DW. Hydrocortisone and tumor necrosis factor in severe community-acquired pneumonia. A randomized controlled study. Chest. 1993 Aug;104(2):389-92. | PubMed |
Marik P, Kraus P, Sribante J, Havlik I, Lipman J, Johnson DW. Hydrocortisone and tumor necrosis factor in severe community-acquired pneumonia. A randomized controlled study. Chest. 1993 Aug;104(2):389-92. | PubMed | Meduri GU, Golden E, Freire AX, Taylor E, Zaman M, Carson SJ, et al. Methylprednisolone infusion in early severe ARDS: results of a randomized controlled trial. Chest. 2007 Apr;131(4):954-63. | PubMed |
Meduri GU, Golden E, Freire AX, Taylor E, Zaman M, Carson SJ, et al. Methylprednisolone infusion in early severe ARDS: results of a randomized controlled trial. Chest. 2007 Apr;131(4):954-63. | PubMed | Meduri, Gianfranco U, Golden, Emmel, Umberger, Reba. PRospective double-blind randomized clinical trial on the effects of low-dose hydrocortisone infusion in patients with severe sepsis. Chest. 2009;136(4_MeetingAbstracts):45S-h-45S. | Link |
Meduri, Gianfranco U, Golden, Emmel, Umberger, Reba. PRospective double-blind randomized clinical trial on the effects of low-dose hydrocortisone infusion in patients with severe sepsis. Chest. 2009;136(4_MeetingAbstracts):45S-h-45S. | Link | Meijvis SC, Hardeman H, Remmelts HH, Heijligenberg R, Rijkers GT, van Velzen-Blad H, et al. Dexamethasone and length of hospital stay in patients with community-acquired pneumonia: a randomised, double-blind, placebo-controlled trial. Lancet. 2011 Jun 11;377(9782):2023-30. | CrossRef | PubMed |
Meijvis SC, Hardeman H, Remmelts HH, Heijligenberg R, Rijkers GT, van Velzen-Blad H, et al. Dexamethasone and length of hospital stay in patients with community-acquired pneumonia: a randomised, double-blind, placebo-controlled trial. Lancet. 2011 Jun 11;377(9782):2023-30. | CrossRef | PubMed | Mikami K, Suzuki M, Kitagawa H, Kawakami M, Hirota N, Yamaguchi H, et al. Efficacy of corticosteroids in the treatment of community-acquired pneumonia requiring hospitalization. Lung. 2007 Sep-Oct;185(5):249-55. | PubMed |
Mikami K, Suzuki M, Kitagawa H, Kawakami M, Hirota N, Yamaguchi H, et al. Efficacy of corticosteroids in the treatment of community-acquired pneumonia requiring hospitalization. Lung. 2007 Sep-Oct;185(5):249-55. | PubMed | Mirea, L, Ungureanu, R, Pavelescu, D, Grintescu, IC, Dumitrache, C, Grintescu, I, Mirea, D. Continuous administration of corticosteroids in septic shock can reduce risk of hypernatremia. Critical Care. 2014;18(Suppl 1):P239-P239. | CrossRef |
Mirea, L, Ungureanu, R, Pavelescu, D, Grintescu, IC, Dumitrache, C, Grintescu, I, Mirea, D. Continuous administration of corticosteroids in septic shock can reduce risk of hypernatremia. Critical Care. 2014;18(Suppl 1):P239-P239. | CrossRef | Mussack T, Briegel J, Schelling G, Biberthaler P, Jochum M. Effect of stress doses of hydrocortisone on S-100B vs. interleukin-8 and polymorphonuclear elastase levels in human septic shock. Clin Chem Lab Med. 2005;43(3):259-68. | PubMed |
Mussack T, Briegel J, Schelling G, Biberthaler P, Jochum M. Effect of stress doses of hydrocortisone on S-100B vs. interleukin-8 and polymorphonuclear elastase levels in human septic shock. Clin Chem Lab Med. 2005;43(3):259-68. | PubMed | Mussack T, Briegel J, Schelling G, Jochum M. Hemofiltrastion does not influence early S-100B serum levels in septic shock patients receiving stress doses of hydrocortisone or placebo. European journal of medical research. 2005;10(1):11-7. | Link |
Mussack T, Briegel J, Schelling G, Jochum M. Hemofiltrastion does not influence early S-100B serum levels in septic shock patients receiving stress doses of hydrocortisone or placebo. European journal of medical research. 2005;10(1):11-7. | Link | Nafae, Ramadan M., Ragab, Mostafa I., Amany, Fawzy M., Rashed, Shimaa B.. Adjuvant role of corticosteroids in the treatment of community-acquired pneumonia. Egyptian Journal of Chest Diseases and Tuberculosis. 2013;62(3):439-445. | Link |
Nafae, Ramadan M., Ragab, Mostafa I., Amany, Fawzy M., Rashed, Shimaa B.. Adjuvant role of corticosteroids in the treatment of community-acquired pneumonia. Egyptian Journal of Chest Diseases and Tuberculosis. 2013;62(3):439-445. | Link | Oppert M, Schindler R, Husung C, Offermann K, Grõf KJ, Boenisch O, et al. Low-dose hydrocortisone improves shock reversal and reduces cytokine levels in early hyperdynamic septic shock. Crit Care Med. 2005 Nov;33(11):2457-64. | PubMed |
Oppert M, Schindler R, Husung C, Offermann K, Grõf KJ, Boenisch O, et al. Low-dose hydrocortisone improves shock reversal and reduces cytokine levels in early hyperdynamic septic shock. Crit Care Med. 2005 Nov;33(11):2457-64. | PubMed | Rinaldi S, Adembri C, Grechi S, De Gaudio AR. Low-dose hydrocortisone during severe sepsis: effects on microalbuminuria. Crit Care Med. 2006 Sep;34(9):2334-9. | PubMed |
Rinaldi S, Adembri C, Grechi S, De Gaudio AR. Low-dose hydrocortisone during severe sepsis: effects on microalbuminuria. Crit Care Med. 2006 Sep;34(9):2334-9. | PubMed | Sabry, Nirmeen A., Omar, Emad El-Din. Corticosteroids and ICU Course of Community Acquired Pneumonia in Egyptian Settings. Pharmacology & Pharmacy. 2011;2:73-81. | CrossRef |
Sabry, Nirmeen A., Omar, Emad El-Din. Corticosteroids and ICU Course of Community Acquired Pneumonia in Egyptian Settings. Pharmacology & Pharmacy. 2011;2:73-81. | CrossRef | Scarborough M, Gordon SB, Whitty CJ, French N, Njalale Y, Chitani A, et al. Corticosteroids for bacterial meningitis in adults in sub-Saharan Africa. N Engl J Med. 2007 Dec 13;357(24):2441-50. | PubMed |
Scarborough M, Gordon SB, Whitty CJ, French N, Njalale Y, Chitani A, et al. Corticosteroids for bacterial meningitis in adults in sub-Saharan Africa. N Engl J Med. 2007 Dec 13;357(24):2441-50. | PubMed | Schumer W. Steroids in the treatment of clinical septic shock. Ann Surg. 1976 Sep;184(3):333-41. | PubMed |
Schumer W. Steroids in the treatment of clinical septic shock. Ann Surg. 1976 Sep;184(3):333-41. | PubMed | Slusher T, Gbadero D, Howard C, Lewison L, Giroir B, Toro L, et al. Randomized, placebo-controlled, double blinded trial of dexamethasone in African children with sepsis. Pediatr Infect Dis J. 1996 Jul;15(7):579-83. | PubMed |
Slusher T, Gbadero D, Howard C, Lewison L, Giroir B, Toro L, et al. Randomized, placebo-controlled, double blinded trial of dexamethasone in African children with sepsis. Pediatr Infect Dis J. 1996 Jul;15(7):579-83. | PubMed | Snijders D, Daniels JM, de Graaff CS, van der Werf TS, Boersma WG. Efficacy of corticosteroids in community-acquired pneumonia: a randomized double-blinded clinical trial. Am J Respir Crit Care Med. 2010 May 1;181(9):975-82. | CrossRef | PubMed |
Snijders D, Daniels JM, de Graaff CS, van der Werf TS, Boersma WG. Efficacy of corticosteroids in community-acquired pneumonia: a randomized double-blinded clinical trial. Am J Respir Crit Care Med. 2010 May 1;181(9):975-82. | CrossRef | PubMed | Sprung CL, Annane D, Keh D, Moreno R, Singer M, Freivogel K, et al. Hydrocortisone therapy for patients with septic shock. N Engl J Med. 2008 Jan 10;358(2):111-24. | CrossRef | PubMed |
Sprung CL, Annane D, Keh D, Moreno R, Singer M, Freivogel K, et al. Hydrocortisone therapy for patients with septic shock. N Engl J Med. 2008 Jan 10;358(2):111-24. | CrossRef | PubMed | Sprung CL, Annane D, Keh D, Moreno R, Singer M, Freivogel K, et al. Hydrocortisone therapy for patients with septic shock. N Engl J Med. 2008 Jan 10;358(2):111-24. | CrossRef | PubMed |
Sprung CL, Annane D, Keh D, Moreno R, Singer M, Freivogel K, et al. Hydrocortisone therapy for patients with septic shock. N Engl J Med. 2008 Jan 10;358(2):111-24. | CrossRef | PubMed | Tandan, SM, Guleria, R, Gupta, N. Low dose steroids and adrenocortical insufficiency in septic shock: a double-blind randomised controlled trial from India. Am J Respir Crit Care Med. 2005;171:A43. | Link |
Tandan, SM, Guleria, R, Gupta, N. Low dose steroids and adrenocortical insufficiency in septic shock: a double-blind randomised controlled trial from India. Am J Respir Crit Care Med. 2005;171:A43. | Link | Veterans Administration Systemic Sepsis Cooperative Study Group. Effect of high-dose glucocorticoid therapy on mortality in patients with clinical signs of systemic sepsis. N Engl J Med. 1987 Sep 10;317(11):659-65. | PubMed |
Veterans Administration Systemic Sepsis Cooperative Study Group. Effect of high-dose glucocorticoid therapy on mortality in patients with clinical signs of systemic sepsis. N Engl J Med. 1987 Sep 10;317(11):659-65. | PubMed | Thompson, WL, Gurley, HT, Lutz, BA, Jackson, DL, Kvols, LK, Morris, IA. Inefficacy of glucocorticoids in shock (double-blind-study). CLINICAL RESEARCH. 1976;24(3):A258-A258. | Link |
Thompson, WL, Gurley, HT, Lutz, BA, Jackson, DL, Kvols, LK, Morris, IA. Inefficacy of glucocorticoids in shock (double-blind-study). CLINICAL RESEARCH. 1976;24(3):A258-A258. | Link | Thwaites GE, Nguyen DB, Nguyen HD, Hoang TQ, Do TT, Nguyen TC, et al. Dexamethasone for the treatment of tuberculous meningitis in adolescents and adults. N Engl J Med. 2004 Oct 21;351(17):1741-51. | PubMed |
Thwaites GE, Nguyen DB, Nguyen HD, Hoang TQ, Do TT, Nguyen TC, et al. Dexamethasone for the treatment of tuberculous meningitis in adolescents and adults. N Engl J Med. 2004 Oct 21;351(17):1741-51. | PubMed | Torres A, Sibila O, Ferrer M, Polverino E, Menendez R, Mensa J, et al. Effect of corticosteroids on treatment failure among hospitalized patients with severe community-acquired pneumonia and high inflammatory response: a randomized clinical trial. JAMA. 2015 Feb 17;313(7):677-86. | CrossRef | PubMed |
Torres A, Sibila O, Ferrer M, Polverino E, Menendez R, Mensa J, et al. Effect of corticosteroids on treatment failure among hospitalized patients with severe community-acquired pneumonia and high inflammatory response: a randomized clinical trial. JAMA. 2015 Feb 17;313(7):677-86. | CrossRef | PubMed | Wagner HN Jr, Bennett IL Jr, Lasagna L, Cluff LE, Rosenthal MB, Mirick GS. The effect of hydrocortisone upon the course of pneumococcal pneumonia treated with penicillin. Bull Johns Hopkins Hosp. 1956 Mar;98(3):197-215. | PubMed |
Wagner HN Jr, Bennett IL Jr, Lasagna L, Cluff LE, Rosenthal MB, Mirick GS. The effect of hydrocortisone upon the course of pneumococcal pneumonia treated with penicillin. Bull Johns Hopkins Hosp. 1956 Mar;98(3):197-215. | PubMed | Yildiz O, Doganay M, Aygen B, G³ven M, Keleştimur F, Tutu¹ A. Physiological-dose steroid therapy in sepsis [ISRCTN36253388]. Crit Care. 2002 Jun;6(3):251-9. | PubMed |
Yildiz O, Doganay M, Aygen B, G³ven M, Keleştimur F, Tutu¹ A. Physiological-dose steroid therapy in sepsis [ISRCTN36253388]. Crit Care. 2002 Jun;6(3):251-9. | PubMed | Yildiz O, Tanriverdi F, Simsek S, Aygen B, Kelestimur F. The effects of moderate-dose steroid therapy in sepsis: A placebo-controlled, randomized study. J Res Med Sci. 2011 Nov;16(11):1410-21. | PubMed |
Yildiz O, Tanriverdi F, Simsek S, Aygen B, Kelestimur F. The effects of moderate-dose steroid therapy in sepsis: A placebo-controlled, randomized study. J Res Med Sci. 2011 Nov;16(11):1410-21. | PubMed | Bone RC, Sibbald WJ, Sprung CL. The ACCP-SCCM consensus conference on sepsis and organ failure. Chest. 1992 Jun;101(6):1481-3. | PubMed |
Bone RC, Sibbald WJ, Sprung CL. The ACCP-SCCM consensus conference on sepsis and organ failure. Chest. 1992 Jun;101(6):1481-3. | PubMed | Singer, Mervyn, et al. "The third international consensus definitions for sepsis and septic shock (sepsis-3). Jama (2016): 801-810. | Link |
Singer, Mervyn, et al. "The third international consensus definitions for sepsis and septic shock (sepsis-3). Jama (2016): 801-810. | Link | Dellinger RP, Levy MM, Rhodes A, Annane D, Gerlach H, Opal SM, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Crit care med. 2013;41(2):580-637. | Link |
Dellinger RP, Levy MM, Rhodes A, Annane D, Gerlach H, Opal SM, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Crit care med. 2013;41(2):580-637. | Link |