 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
La neutropenia febril prolongada conlleva un alto riesgo de desarrollar infecciones fúngicas invasoras, por lo que habitualmente se administra terapia antifúngica empírica en estos casos. Sin embargo, esta se asocia a importantes efectos adversos, por lo que se ha propuesto como alternativa la estrategia "preemptive" o anticipada, es decir, la indicación de antifúngicos sólo ante la evidencia indirecta de infección fúngica invasora. Utilizando la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en 30 bases de datos, identificamos tres revisiones sistemáticas que en conjunto incluyen doce estudios. Cuatro estudios aleatorizados evaluaron la pregunta abordada en este artículo. Realizamos un metanálisis y tablas de resumen de los resultados utilizando el método GRADE. Concluimos que no está claro si la estrategia "preemptive" tiene algún efecto sobre la mortalidad porque la certeza de la evidencia es muy baja, pero podría disminuir levemente el uso de antifúngicos en pacientes con neutropenia febril prolongada.
La fiebre ocurre con frecuencia en pacientes con neutropenia inducida por quimioterapia, pero la infección es clínicamente documentada sólo en un 20 a 30% de los casos [1]. Las infecciones fúngicas invasoras suelen aparecer después de la primera semana de neutropenia febril con tratamiento antibiótico empírico y conllevan alta morbimortalidad, en especial en pacientes sometidos a trasplante alogénico de médula ósea [2]. Es por esto que ha sido práctica habitual el inicio empírico de antifúngicos en pacientes con neutropenia febril prolongada, y así es recomendado en varias guías clínicas. Con esta estrategia un 40 a 50% de pacientes son tratados con terapia antifúngica empírica, mientras que la incidencia estimada de infecciones fúngicas invasoras es sólo 10 a 15% [3]. Esto implica que una importante proporción de los pacientes son sometidos a un tratamiento innecesario, con potencial toxicidad y alto costo. Se ha planteado como alternativa la estrategia preemptive o anticipada, basada en la indicación de antifúngicos sólo ante la evidencia indirecta de infección fúngica invasora (ya sea test serológico positivo o imagen sugerente).
Utilizamos la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en 30 bases de datos, para identificar revisiones sistemáticas y sus estudios primarios incluidos. Con esta información generamos un resumen estructurado, siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios, tablas de resumen de resultados con el método GRADE, y tabla de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia. |
Encontramos tres revisiones sistemáticas [4],[5],[6] que incluyen en total doce estudios primarios [7],[8],[9],[10], [11],[12],[13],[14],[15],[16],[17],[18] entre ellos cinco estudios controlados aleatorizados [9],[10],[13],[15],[18]. Uno de los estudios controlados aleatorizados fue excluido de este resumen por no presentar tratamiento empírico como comparación [9]. Esta tabla y el resumen en general se basan en los cuatro estudios aleatorizados pertinentes a la pregunta [10],[13],[15],[18]. |
|
Qué tipo de pacientes incluyeron los estudios |
Dos estudios incluyeron pacientes adultos [10],[15], un estudio incluyó adultos y niños [18] y un estudio no especificó si incluía adultos o niños [13]. Los cuatro estudios incluyeron únicamente neoplasias hematológicas; de estos, un estudio incluyó sólo pacientes con transplante de médula ósea [13], y el resto de los estudios incluyó pacientes en quimioterapia o con transplante de médula ósea [10],[15],[18]. |
|
Qué tipo de intervenciones incluyeron los estudios |
Los estudios utilizaron criterios distintos para iniciar antifúngicos en la estrategia preemptive. Respecto a los test diagnósticos usados para definir inicio de antifúngicos: tres estudios midieron galactomanana dos veces a la semana [10],[15],[18]; dos estudios usaron PCR, un estudio nested PCR para Aspergillus [15] y un estudio non-nested PCR para Aspergillus y Candida [13]; sólo un estudio realizó hemocultivos [13]; todos los estudios emplearon imágenes; dos estudios realizaron tomografía computada de tórax si existían criterios diagnósticos de laboratorio positivos [15],[18], un estudio tomografía computada de tórax y abdomen a todos los pacientes [13], y un estudio radiografía de tórax seguida de tomografía computada de tórax [10]. |
|
Qué tipo de desenlaces midieron |
Las distintas revisiones sistemáticas realizaron metanálisis de los siguientes desenlaces:
|
La información sobre los efectos de la estrategia preemptive está basada en cuatro estudios aleatorizados que incluyen 988 pacientes [10],[13],[15],[18]. Tres estudios reportaron mortalidad total [10],[13],[15] y los cuatro reportaron el uso de antifúngicos. El resumen de los resultados es el siguiente:
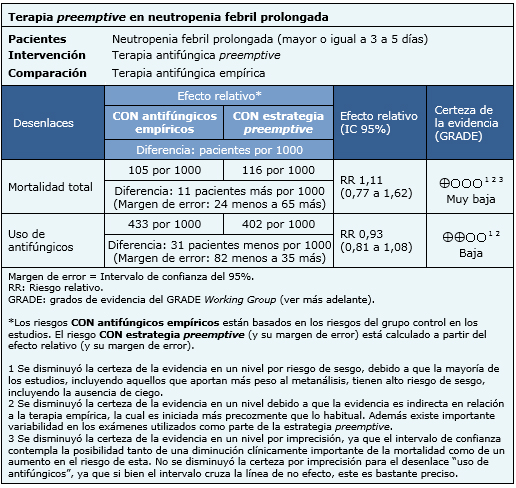

|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Qué piensan los pacientes y sus tratantes |
|
| Consideraciones de recursos |
|
|
Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
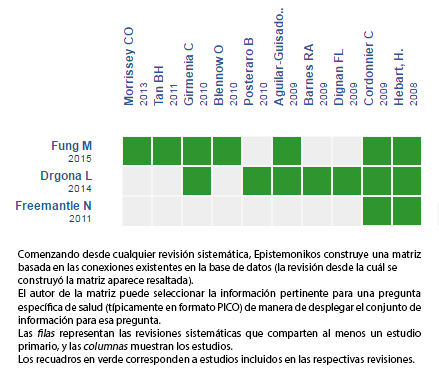
Siga el enlace para acceder a la versión interactiva: Estrategia anticipada (preemptive) en neutropenia febril
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más rápida.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta. El detalle de los métodos para elaborar este resumen están descritos aquí: http://dx.doi.org/10.5867/medwave.2014.06.5997.
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Los resúmenes de evidencia siguen un riguroso proceso de revisión por pares interno.
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Patients with prolonged febrile neutropenia are at high risk of invasive fungal infection, so it has been standard practice to initiate empirical antifungal therapy in these cases. However, this strategy is associated with important toxicity, so diagnostic test-guided preemptive antifungal therapy has been proposed as an alternative. Searching in Epistemonikos database, which is maintained by screening 30 databases, we identified three systematic reviews including twelve studies overall. Four randomized controlled trials addressed the question of this article. We combined the evidence using meta-analysis and generated a summary of findings following the GRADE approach. We concluded it is not clear whether preemptive strategy affects mortality because the certainty of the evidence is very low, but it might slightly decrease the use of antifungal agents in patients with prolonged febrile neutropenia.
 Autores:
Erica Koch[1,2], Gabriel Rada[1,2,3,4,5]
Autores:
Erica Koch[1,2], Gabriel Rada[1,2,3,4,5]

Citación: Koch E, Rada G. Is preemptive antifungal therapy a good alternative to empirical treatment in prolonged febrile neutropenia?. Medwave 2016;16(Suppl 2):36463 doi: 10.5867/medwave.2016.6463
Fecha de publicación: 9/6/2016

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Freifeld AG, Bow EJ, Sepkowitz KA, Boeckh MJ, Ito JI, Mullen CA, et al. Clinical practice guideline for the use of antimicrobial agents in neutropenic patients with cancer: 2010 update by the infectious diseases society of america. Clin Infect Dis. 2011 Feb 15;52(4):e56-93.
| CrossRef | PubMed |
Freifeld AG, Bow EJ, Sepkowitz KA, Boeckh MJ, Ito JI, Mullen CA, et al. Clinical practice guideline for the use of antimicrobial agents in neutropenic patients with cancer: 2010 update by the infectious diseases society of america. Clin Infect Dis. 2011 Feb 15;52(4):e56-93.
| CrossRef | PubMed | Dignan FL, Evans SO, Ethell ME, Shaw BE, Davies FE, Dearden CE, et al. An early CT-diagnosis-based treatment strategy for invasive fungal infection in allogeneic transplant recipients using caspofungin first line: an effective strategy with low mortality. Bone Marrow Transplant. 2009 Jul;44(1):51-6. | CrossRef | PubMed |
Dignan FL, Evans SO, Ethell ME, Shaw BE, Davies FE, Dearden CE, et al. An early CT-diagnosis-based treatment strategy for invasive fungal infection in allogeneic transplant recipients using caspofungin first line: an effective strategy with low mortality. Bone Marrow Transplant. 2009 Jul;44(1):51-6. | CrossRef | PubMed | Mahfouz T, Anaissie E.Prevention of fungal infections in the immunocompromised host. Curr Opin Investig Drugs. 2003 Aug;4(8):974-90. | PubMed |
Mahfouz T, Anaissie E.Prevention of fungal infections in the immunocompromised host. Curr Opin Investig Drugs. 2003 Aug;4(8):974-90. | PubMed | Freemantle N, Tharmanathan P, Herbrecht R. Systematic review and mixed treatment comparison of randomized evidence for empirical, pre-emptive and directed treatment strategies for invasive mould disease. J Antimicrob Chemother. 2011 Jan;66 Suppl 1:i25-35. | CrossRef | PubMed |
Freemantle N, Tharmanathan P, Herbrecht R. Systematic review and mixed treatment comparison of randomized evidence for empirical, pre-emptive and directed treatment strategies for invasive mould disease. J Antimicrob Chemother. 2011 Jan;66 Suppl 1:i25-35. | CrossRef | PubMed | Drgona L, Khachatryan A, Stephens J, Charbonneau C, Kantecki M, Haider S, et al. Clinical and economic burden of invasive fungal diseases in Europe: focus on pre-emptive and empirical treatment of Aspergillus and Candida species. Eur J Clin Microbiol Infect Dis. 2014 Jan;33(1):7-21. | CrossRef | PubMed |
Drgona L, Khachatryan A, Stephens J, Charbonneau C, Kantecki M, Haider S, et al. Clinical and economic burden of invasive fungal diseases in Europe: focus on pre-emptive and empirical treatment of Aspergillus and Candida species. Eur J Clin Microbiol Infect Dis. 2014 Jan;33(1):7-21. | CrossRef | PubMed | Fung M, Kim J, Marty FM, Schwarzinger M, Koo S. Meta-Analysis and Cost Comparison of Empirical versus Pre-Emptive Antifungal Strategies in Hematologic Malignancy Patients with High-Risk Febrile Neutropenia. PLoS One. 2015 Nov 10;10(11):e0140930. | CrossRef | PubMed |
Fung M, Kim J, Marty FM, Schwarzinger M, Koo S. Meta-Analysis and Cost Comparison of Empirical versus Pre-Emptive Antifungal Strategies in Hematologic Malignancy Patients with High-Risk Febrile Neutropenia. PLoS One. 2015 Nov 10;10(11):e0140930. | CrossRef | PubMed | Aguilar-Guisado M, Espigado I, Cordero E, Noguer M, Parody R, Pachón J, et al. Empirical antifungal therapy in selected patients with persistent febrile neutropenia. Bone Marrow Transplant. 2010 Jan;45(1):159-64.
| CrossRef | PubMed |
Aguilar-Guisado M, Espigado I, Cordero E, Noguer M, Parody R, Pachón J, et al. Empirical antifungal therapy in selected patients with persistent febrile neutropenia. Bone Marrow Transplant. 2010 Jan;45(1):159-64.
| CrossRef | PubMed | Barnes RA, White PL, Bygrave C, Evans N, Healy B, Kell J. Clinical impact of enhanced diagnosis of invasive fungal disease in high-risk haematology and stem cell transplant patients. J Clin Pathol. 2009 Jan;62(1):64-9. | CrossRef | PubMed |
Barnes RA, White PL, Bygrave C, Evans N, Healy B, Kell J. Clinical impact of enhanced diagnosis of invasive fungal disease in high-risk haematology and stem cell transplant patients. J Clin Pathol. 2009 Jan;62(1):64-9. | CrossRef | PubMed | Blennow O, Remberger M, Klingspor L, Omazic B, Fransson K, Ljungman P, et al. Randomized PCR-based therapy and risk factors for invasive fungal infection following reduced-intensity conditioning and hematopoietic SCT. Bone Marrow Transplant. 2010 Dec;45(12):1710-8. | CrossRef | PubMed |
Blennow O, Remberger M, Klingspor L, Omazic B, Fransson K, Ljungman P, et al. Randomized PCR-based therapy and risk factors for invasive fungal infection following reduced-intensity conditioning and hematopoietic SCT. Bone Marrow Transplant. 2010 Dec;45(12):1710-8. | CrossRef | PubMed | Cordonnier C, Pautas C, Maury S, Vekhoff A, Farhat H, Suarez F, et al. Empirical versus preemptive antifungal therapy for high-risk, febrile, neutropenic patients: a randomized, controlled trial. Clin Infect Dis. 2009 Apr 15;48(8):1042-51. | CrossRef | PubMed |
Cordonnier C, Pautas C, Maury S, Vekhoff A, Farhat H, Suarez F, et al. Empirical versus preemptive antifungal therapy for high-risk, febrile, neutropenic patients: a randomized, controlled trial. Clin Infect Dis. 2009 Apr 15;48(8):1042-51. | CrossRef | PubMed | Dignan FL, Evans SO, Ethell ME, Shaw BE, Davies FE, Dearden CE, et al. An early CT-diagnosis-based treatment strategy for invasive fungal infection in allogeneic transplant recipients using caspofungin first line: an effective strategy with low mortality. Bone Marrow Transplant. 2009 Jul;44(1):51-6. | CrossRef | PubMed |
Dignan FL, Evans SO, Ethell ME, Shaw BE, Davies FE, Dearden CE, et al. An early CT-diagnosis-based treatment strategy for invasive fungal infection in allogeneic transplant recipients using caspofungin first line: an effective strategy with low mortality. Bone Marrow Transplant. 2009 Jul;44(1):51-6. | CrossRef | PubMed | Girmenia C, Micozzi A, Gentile G, Santilli S, Arleo E, Cardarelli L, et al. Clinically driven diagnostic antifungal approach in neutropenic patients: a prospective feasibility study. J Clin Oncol. 2010 Feb 1;28(4):667-74. | CrossRef | PubMed |
Girmenia C, Micozzi A, Gentile G, Santilli S, Arleo E, Cardarelli L, et al. Clinically driven diagnostic antifungal approach in neutropenic patients: a prospective feasibility study. J Clin Oncol. 2010 Feb 1;28(4):667-74. | CrossRef | PubMed | Hebart H, Klingspor L, Klingebiel T, Loeffler J, Tollemar J, Ljungman P, et al. A prospective randomized controlled trial comparing PCR-based and empirical treatment with liposomal amphotericin B in patients after allo-SCT. Bone Marrow Transplant. 2009 Apr;43(7):553-61. | CrossRef | PubMed |
Hebart H, Klingspor L, Klingebiel T, Loeffler J, Tollemar J, Ljungman P, et al. A prospective randomized controlled trial comparing PCR-based and empirical treatment with liposomal amphotericin B in patients after allo-SCT. Bone Marrow Transplant. 2009 Apr;43(7):553-61. | CrossRef | PubMed | Maertens J, Theunissen K, Verhoef G, Verschakelen J, Lagrou K, Verbeken E, et al. Galactomannan and computed tomography-based preemptive antifungal therapy in neutropenic patients at high risk for invasive fungal infection: a prospective feasibility study. Clin Infect Dis. 2005 Nov 1;41(9):1242-50. | PubMed |
Maertens J, Theunissen K, Verhoef G, Verschakelen J, Lagrou K, Verbeken E, et al. Galactomannan and computed tomography-based preemptive antifungal therapy in neutropenic patients at high risk for invasive fungal infection: a prospective feasibility study. Clin Infect Dis. 2005 Nov 1;41(9):1242-50. | PubMed | Morrissey CO, Chen SC, Sorrell TC, Milliken S, Bardy PG, Bradstock KF, et al. Galactomannan and PCR versus culture and histology for directing use of antifungal treatment for invasive aspergillosis in high-risk haematology patients: a randomised controlled trial. Lancet Infect Dis. 2013 Jun;13(6):519-28. | CrossRef | PubMed |
Morrissey CO, Chen SC, Sorrell TC, Milliken S, Bardy PG, Bradstock KF, et al. Galactomannan and PCR versus culture and histology for directing use of antifungal treatment for invasive aspergillosis in high-risk haematology patients: a randomised controlled trial. Lancet Infect Dis. 2013 Jun;13(6):519-28. | CrossRef | PubMed | Oshima K, Kanda Y, Asano-Mori Y, Nishimoto N, Arai S, Nagai S, et al. Presumptive treatment strategy for aspergillosis in allogeneic haematopoietic stem cell transplant recipients. J Antimicrob Chemother. 2007 Aug;60(2):350-5. | PubMed |
Oshima K, Kanda Y, Asano-Mori Y, Nishimoto N, Arai S, Nagai S, et al. Presumptive treatment strategy for aspergillosis in allogeneic haematopoietic stem cell transplant recipients. J Antimicrob Chemother. 2007 Aug;60(2):350-5. | PubMed | Posteraro B, Sanguinetti M, Boccia S, De Feo E, La Sorda M, Tana M, et al. Early mannan detection in bronchoalveolar lavage fluid with preemptive treatment reduces the incidence of invasive Candida infections in preterm infants. Pediatr Infect Dis J. 2010 Sep;29(9):844-8. | CrossRef | PubMed |
Posteraro B, Sanguinetti M, Boccia S, De Feo E, La Sorda M, Tana M, et al. Early mannan detection in bronchoalveolar lavage fluid with preemptive treatment reduces the incidence of invasive Candida infections in preterm infants. Pediatr Infect Dis J. 2010 Sep;29(9):844-8. | CrossRef | PubMed |