 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: herbal highs, psychoactive drugs, salvia, ayahuasca
Existe un interés creciente en los vegetales con efectos psicoactivos por parte de consumidores, con diferentes niveles de experiencia. Esto ha generado una necesidad de actualización de conocimientos del lado de los profesionales médicos y de otros responsables de la salud pública. Se trata, por lo general, de plantas de uso en ceremonias chamánicas con intención curativa, en rituales o simplemente de uso tradicional que han dado el salto al mundo occidental como nuevas drogas psicoactivas, en gran medida gracias a la facilidad de compra, venta, cultivo e intercambio de información que ofrece Internet. Recopilamos en este texto los vegetales con propiedades psicoactivas más relevantes, tanto por su frecuente mención en foros de usuarios o en portales destinados a la reducción de dańos en el consumo de drogas, como por su aparición en textos científicos.
Desde tiempos inmemoriales, el ser humano y muchos otros animales hemos utilizado las plantas con fines no meramente alimenticios. De hecho, las propiedades medicinales de los vegetales están en el origen mismo del desarrollo farmacéutico. Entre estas propiedades, la psicoactividad ha demostrado ser de una notable importancia antropológica, pues la búsqueda de estados alterados de conciencia se puede rastrear en todas las épocas y culturas [1].
El uso no tradicional de hierbas, árboles y arbustos ha ido introduciéndose en el mundo occidental, en círculos progresistas o marginales inicialmente, para luego experimentar toda una expansión poblacional, acrecentada con la llegada de Internet [2],[3]. Algunos de estos vegetales pertenecen al conjunto denominado nuevas drogas psicoactivas. Las nuevas drogas psicoactivas se definen como aquellas sustancias que no están fiscalizadas aún a nivel internacional, pero que suponen un riesgo potencial para la salud pública. En el concepto caben, asimismo, las nuevas formas y contextos de uso o los nuevos medios de distribución de drogas ya ilegalizadas [4].
De la importancia epidemiológica de las nuevas drogas psicoactivas en general, y de los coloquialmente conocidos como herbal highs en particular, dan cuenta multitud de trabajos científicos, así como informes de organismos internacionales que apuntan hacia los vegetales como una fuente en auge de nuevas drogas psicoactivas entre la población joven [5],[6],[7],[8].
Ayahuasca y sus constituyentes
Se trata de un preparado vegetal cocido a fuego, originario de poblaciones indígenas amazónicas, que ha sido utilizada tradicionalmente en rituales espirituales, de premonición y de sanación [1]. Desde principios del siglo XX su consumo forma parte también de las ceremonias de congregaciones religiosas como la União do Vegetal o el Santo Daime en Brasil, si bien en las últimas décadas se han ido conformando grupos adscritos a estos rituales por todo el mundo. La ayahuasca se consume también dentro de colectivos urbanos, con objetivos artísticos y de crecimiento personal, cercanos a la filosofía New Age [4]. La ingestión como sacramento religioso está contemplada en países que disfrutan de un cierto grado de libertad de culto. Sin embargo, el consumo y la distribución de plantas fuera de este contexto particular están penados por la ley a nivel internacional.
La ayahuasca se cocina a partir de al menos dos plantas diferentes, que habitualmente son la liana Banisteriopsis caapi y el arbusto Psychotria viridis. Con frecuencia se añaden otros vegetales, como Diplopterys cabrerana, de la misma familia que la primera [9]. Banisteriopsis caapi contiene β-carbolinas (harmina, harmalina y tetrahidroharmina), con propiedad inhibidora de la monoaminooxidasa, mientras que las hojas de Psychotria y la liana Diplopterys contienen N,N-dimetiltriptamina, un alucinógeno serotoninérgico de corta duración, aislado por vez primera en los años cincuenta del siglo pasado en las semillas de plantas del género Piptadenia [1]. Es inactivo si se ingiere por vía oral, a causa de la degradación intestinal y hepática de la monoaminooxidasa. No obstante, cuando se mezcla la N,N-dimetiltriptamina con inhibidores de esta enzima, como las β-carbolinas, logra alcanzar el sistema nervioso central y producir sus efectos, particularmente a través de los receptores 5-HT2A [9]. Más detalles sobre la farmacología de la N,N-dimetiltriptamina se puede consultar en la Tabla 1.
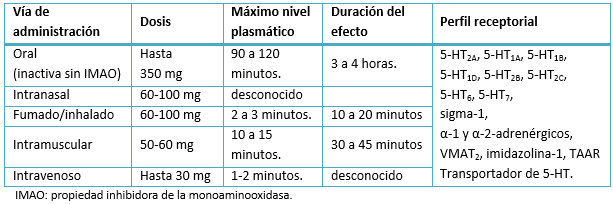
Tabla 1. Aspectos farmacológicos de la N,N-dimetiltriptamina .
Se denomina anahuasca (análogos de la ayahuasca) al brebaje resultante de la combinación entre plantas como diversas partes de Passiflora incarnata o las semillas de Peganum harmala, que contienen carbolinas, y los hongos Psilocybe, las raíces de Desmanthus illinoensis (mimosa de las praderas), los frutos de los árboles del género Virola o las hojas de Acacia phlebophylla como fuentes de triptaminas [1],[10]. En la Tabla 2 se recogen otras fuentes vegetales de triptaminas. Por su parte, se conoce popularmente como farmahuasca al uso concomitante de un inhibidor de la monoaminooxidasa sintético junto con una triptamina, sintética o natural [11].
Los primeros síntomas tras la ingestión de la pócima, de potente sabor amargo, son las náuseas y los vómitos cerca de una hora después de la toma. De forma progresiva, aparecen visiones, de colores y de formas geométricas. El individuo puede experimentar una desconexión total con el medio, con vivencias de distorsión del espacio, del tiempo, de la identidad, así como de los significados de los recuerdos [10]. La intoxicación ha sido definida como una experiencia onírica de plena conciencia. El aspecto afectivo es muy notable: puede ocasionar desde euforia a intensa angustia. En ocasiones, el sujeto disfruta de “experiencias cumbre”, con un profundo sentido de trascendencia [11]. En cualquier caso, como sucede con otros enteógenos, la vivencia depende de las características del entorno, de la preparación y las expectativas del sujeto, de la compañía o de la actuación del guía.
Aunque sin duda es el efecto visionario de las triptaminas el más buscado por los que consumen ayahuasca, las carbolinas con actividad inhibidora de la monoaminooxidasa, son también psicoactivas, pues tanto Peganum harmala como Passiflora incarnata se han utilizado en etnomedicina como tranquilizantes [10]. En los foros de usuarios psiconáuticos, Peganum harmala (conocida popularmente como Ruda Siria o Harmel) también se consume en solitario, buscando el efecto de “borrachera” que induce [12].
La ayahuasca es considerada una pócima segura, como la mayor parte de las triptaminas presentes de forma natural en plantas, hongos y animales. Las complicaciones del consumo se relacionan con la activación del sistema nervioso vegetativo simpático. Han sido descritos casos aislados de fallo renal agudo y de rabdomiolisis [13].
No obstante, a pesar de la seguridad reportada del uso de ayahuasca de manera tradicional, hay que prestar atención a algunas particularidades:

Tabla 2. Fuentes vegetales de triptaminas simples
La ayahuasca ha sido estudiada por sus efectos beneficiosos sobre el sueño REM y de ondas lentas, así como en la terapia del párkinson e incluso como protector frente a neoplasias [4],[14]. No obstante, es en el tratamiento de adicciones a sustancias donde ha acumulado mayor evidencia clínica terapéutica.
El programa del centro Takiwasi, en la amazonia peruana, ha aportado durante más de dos décadas numerosos casos de éxito en el tratamiento de adictos a cocaína y otras drogas. En dicho programa se reconoce el valor sanador, no sólo del ritual tradicional de toma de ayahuasca, sino también del entorno, la convivencia y las diversas interacciones con un equipo multidisciplinar durante varios meses. Otro grupo que ha incluido la perspectiva chamánica del uso de ayahuasca en la terapia de las adicciones es el Instituto de Etnopsicología Amazónica Aplicada (IDEAA, de sus siglas en inglés Institute of Applied Amazonian Ethnopsychology), cuyo programa se caracteriza por la integración de técnicas occidentales de meditación o de psicología transpersonal con los rituales sincretistas de la iglesia del Santo Daime y ciertas prácticas tradicionales. Por otro lado, la participación en las ceremonias religiosas de la União do Vegetal ha señalado la capacidad de la ayahuasca en estos contextos para la prevención del consumo de alcohol y de la aparición de psicopatología, entre otras virtudes [15].
Ololiuqui. Vegetales que contienen lisergamidas
El término ololiuqui (literalmente, cosa redonda) se refiere a las semillas de Rivea corymbosa, una enredadera leñosa, natural del continente americano. Sus raíces son fibrosas y delgadas, y sus semillas redondas y de color café [1]. Ampliamente utilizada en Oaxaca (México), se le atribuyen múltiples capacidades medicinales.
Por su parte, Ipomoea violacea, conocida como gloria de la mañana, dondiego de día, matacabras o badoh negro, es otra planta herbácea de la familia de las convolvuláceas, natural de Centroamérica, extendida por los países tropicales e introducida en Europa como ornamental. Sus semillas son negras y angulosas [4].
Argyreia nervosa, conocida popularmente como Rosa de Madera Hawaiana (Hawaiian Baby Woodrose), es una trepadora originaria del subcontinente indio y cuyas hojas se utilizan como antiséptico y antiinflamatorio en medicina ayurvédica. En Occidente es cultivada con fines ornamentales [4]. Son, sin embargo, sus semillas las que cuentan con un poder psicoactivo muy popular entre los consumidores. De hecho, se trata del tercer producto legal más solicitado en Reino Unido a través de Internet con intención de su consumo psicodélico [16].

"Arygeria" by Koń - from pl-wiki. Licensed under CC BY-SA 3.0 via Commons – Disponible en:
https://commons.wikimedia.org/wiki/File:Arygeria.JPG#/media/File:Arygeria.JPG
Figura 1. Semillas de Argyreia nervosa
Si las semillas de estos vegetales se ingieren enteras o incluso partidas, no ocasionan ningún efecto. Es necesario molerlas finamente. Efectos suaves y moderados comienzan a aparecer con unas cinco semillas de Argyreia nervosa o con unas veinte de Ipomoea. Las semillas de Rivea corymbosa tienen una potencia considerablemente menor que las de Ipomea [10]. Los principios activos son lisergamidas (triptaminas complejas, estructuralmente relacionadas con la dietilamida de ácido lisérgico o LSD), como la ergina (amida del ácido lisérgico, LSA o LA-111), la isoergina o la ergonovina. Su acción está mediada por receptores serotoninérgicos (tipo 2A y 1) en el sistema nervioso central, así como dopaminérgicos y adrenérgicos, también a nivel periférico.
La intoxicación por lisergamidas provoca alucinaciones visuales, táctiles, somáticas y, de manera característica, sinestesias. Se distorsiona la vivencia de tiempo y espacio. En altas dosis se pierde la conciencia de sí mismo. Se pueden dar desde estados de angustia psicótica a otros de felicidad extática [4]. Con respecto al consumo particular de Argyreia nervosa, los usuarios suelen relatar una experiencia más confusional con respecto a la producida por la dietilamida de ácido lisérgico [12]. No es de extrañar, pues las semillas de esta planta contienen también alcaloides tropanos de efecto anticolinérgico [4].
Las complicaciones de la intoxicación aguda se relacionan con los estados de angustia, paranoides o con las conductas de riesgo en situaciones de pérdida del contacto con la realidad. Muy raramente se vinculan con la toxicidad intrínseca de la sustancia [1]. No obstante, también han sido relacionadas con trastornos afectivos, trastornos psicóticos mantenidos y con comportamientos suicidas en población susceptible [4].
Amapola
Entre las plantas mesegueras más extendidas se encuentra el ababol, amapola silvestre o simplemente amapola, Papaver rhoeas, una especie de la familia Papaveraceae –de la raíz pap, “hinchado”, alusión a la forma globosa del fruto [17] - de amplia distribución y fáciles reconocimiento y adquisición. Acompañante del ser humano “en su conquista del mundo, mezclando sus semillas a las de los cereales” [18], ha sido utilizada desde hace más de 2000 años por sus supuestas acciones béquica, emoliente y ligeramente narcótica [19].
Su uso se mantiene vivo a lo largo del tiempo, si bien con un giro en sus tendencias de consumo. La intoxicación ha sido descrita tras un consumo gastronómico elevado, de entre 250 y 500 gramos de planta cocinada, como un cuadro de molestias gastrointestinales (náuseas y vómitos), ligera sensación disneica, miosis y leve toxicidad neurológica (inquietud, confusión, somnolencia, sacudidas y entumecimiento de extremidades) [19]. Ocasionalmente se ha comunicado algún óbito por un consumo excesivo no intencional [20], así como el potencial hepatotóxico de la planta [21]. No obstante, la principal causa de intoxicación mortal radica en la confusión con la amapola pluricolorida o adormidera (Papaver somniferum), fuente original de los alcaloides opiáceos, potencialmente mortales, como morfina, codeína, tebaína o noscapina, no presentes en la amapola (Papaver rhoeas) [18].
La búsqueda de sus efectos psicotrópicos la ha situado en el punto de mira del refinamiento psiconáutico experimental, difundido a través de la Web en los foros de reducción del daño asociado a consumo de drogas, en los que informan que la planta puede ser consumida en forma de infusión, hojas y flores secas desmenuzadas para ser fumadas, o la concentrada decocción de partes secas del vegetal entero en una suerte de “rachacha” desprovista de morfina, aunque con suficientes cualidades narcotizantes para considerarlo un producto opiáceo [22],[23]]. El principal compuesto al que se atribuye dicha sintomatología es la readina, alcaloide particularmente común en las especies rhoeas del género Papaver [24], identificándose en menor medida otros compuestos nitrogenados como reagenina o rearrubina. Similares composición y usos se aplican a las americanas california poppy (Eschscholzia californica) y al cardosanto o chicalote (Argemone mexicana) [25].

"Poster papaver 3a" by Alvesgaspar - Own work. Licensed under CC BY-SA 3.0 via Wikimedia Commons – disponible en:
https://commons.wikimedia.org/wiki/File:Poster_papaver_3a.jpg#/media/File:Poster_papaver_3a.jpg
Figura 2. Fruto y flor de la amapola.
Ephedra spp
La efedrina es el protoalcaloide fundamental de arbustos del género Ephedra, llegando al 90% del total de principios activos en las especies asiáticas, por ejemplo Ephedra sinica (má huáng), no así en las europeas y americanas, cuya proporción puede ser nula. Es debido a este alto contenido farmacológico en las variedades orientales, por lo que la medicina tradicional china se ha valido del matorral desde hace milenios para paliar la constricción bronquial, cuadros alérgicos y, lo mismo que el café, el khat, el betel o la coca en otros lugares del planeta, como estimulante para mitigar el hambre y combatir la fatiga laboral.
La molécula precedente natural de las anfetaminas, cuya producción industrial comenzó en Estados Unidos hacia 1930 [25], el má huáng –efedrina- bien puede haber sido el primero de los remedios herbales chinos en utilizarse en medicina occidental, si bien la mayor parte de la efedrina consumida hoy día es un fármaco de síntesis [26]. Químicamente se trata de una anfetamina sustituida, actualmente incluida en la Tabla I de la Lista Roja de la Junta Internacional de Fiscalización de Estupefacientes como precursor de sustancias ilícitas, por su vasta utilización en la elaboración de metanfetamina (también de metcatinona) [27].
En Occidente, los derivados de la efedrina fueron –y son todavía, en menor medida- extensamente consumidos sobre todo por el colectivo de deportistas, como suplementos dietéticos para bajar peso y mejorar el rendimiento atlético [28]. Desde hace años, efedrina y pseudoefedrina forman parte también de otra lista, la de sustancias y métodos prohibidos por la Agencia Mundial Antidopaje [29]. En todo caso, su eficacia como adelgazante y potenciador muscular es muy moderada, y los largos períodos de tratamiento necesarios a tal fin han mostrado una toxicidad no admisible [30].
En diciembre de 2003, la Food and Drug Administration (FDA) declaró prohibidos todos los suplementos dietéticos que contengan efedrina. Según un reciente comunicado referido a Estados Unidos, desde 2002 hasta 2013 se ha producido un descenso del 98% en el número de intoxicaciones mayores o letales por consumo de efedrina [31].
Su mecanismo de acción como amina simpaticomimética es bien conocido: tiene efecto estimulante directo y básicamente indirecto α y β-adrenérgico, debido a la liberación de noradrenalina. Actúa como excitante del sistema nervioso central, vasoconstrictor periférico, hipertensivo, broncodilatador e impelente del centro respiratorio [28].
Existen numerosos preparados comercializados a base de hidrocloruro de efedrina, pseudoefedrina hidrocloruro y pseudoefedrina sulfato, con indicaciones terapéuticas derivadas de su acción simpaticotónica. Su estrecho margen terapéutico puede causar síntomas de intoxicación con sólo doblar o triplicar la dosis terapéutica recomendada (25 a 50 miligramos por toma, máximo 150 al día) [28].
Kanna
Sceletium tortuosum L. o Mesembryanthemum tortuosum N.E.Br., nombre binomial de la popular kanna, es la especie más conocida del género Sceletium, planta consumida tradicionalmente en el África subsahariana por los Khoisan -término colectivo que designa a hotentotes y bosquimanos-. Al parecer estos grupos humanos ancestrales viajaban grandes distancias e incluso comerciaban con la planta, buscando sus efectos embriagantes, fundamentalmente sedorrelajación, euforia suave, analgesia, supresión de la sed y el apetito [32],[33]. Hoy día es un producto disponible –tintura, tabletas, cápsulas, pulverizado- a precios asequibles en tiendas virtuales de la Web o en coffeeshops de la capital holandesa.
Una vasta y poco conocida cantidad de alcaloides se han identificado en las especies de Sceletium, en diferentes proporciones según la variedad, edad y estado orgánico de la planta y la época del año, siendo la mesembrina el principal de todos ellos y responsable en gran parte de los efectos sedantes [32],[33]. La kanna se puede aspirar, fumar, tomar en infusión, masticar o tragar, dosificando, conforme a la vía de administración y la calidad del producto, en rangos que oscilan entre 20 miligramos de rapé y 5 gramos de los elaborados orales. Según informes de usuarios, se da una potenciación mutua al consumir kanna con alcohol y/o cannabis [12].
A las dosis habituales recomendadas no parecen producirse efectos secundarios graves, tanto en consumos agudos como crónicos, ni dependencia, considerándose la kanna un vegetal psicoactivo seguro. Es aconsejable no consumirlo a la vez con fármacos serotoninérgicos. Los efectos secundarios incluyen dolores de cabeza, apatía, hiporexia, depresión.
Se ha atribuido la actividad ansiolítica del extracto estandarizado de la planta, comercializado bajo el nombre de Zembrin ®, a su acción dual como inhibidor de la fosfodiesterasa 4 y de la recaptación de serotonina [33],[34].
Khat
Se conoce bajo el nombre de khat (qat, tschat, miraa) a las hojas frescas del arbusto Catha edulis, cuyo consumo como estimulante es conocido desde hace siglos, principalmente en zonas del Cuerno de África y de la Península Arábiga (Etiopía, Somalia, Yemen). En el caso de este último país es donde se han registrado prevalencias de consumo más altas, hasta de un 90% en ciertas regiones en varones adultos [35],[36].
A pesar del carácter tradicional inherente al consumo de khat, en Occidente su uso como psicoestimulante podría incluirse dentro del ámbito de las nuevas drogas, puesto que no ha sido hasta las últimas décadas en que se ha observado un incremento del uso de khat asociado a la inmigración desde países donde su consumo es habitual. Además, se han empezado a observar patrones de consumo atípicos en personas más jóvenes y con cierto desarraigo de su cultura de origen [37],[38]. Por otra parte, la reciente aparición de las catinonas sintéticas como drogas de abuso ha hecho resurgir el interés de la comunidad científica por el khat, tanto por las similitudes a nivel psicofarmacológico, como por las pistas sobre efectos clínicos y complicaciones que podría aportar el “viejo” khat al estudio de las novedosas catinonas [4].
Las principales moléculas psicoactivas presentes en las hojas de Catha edulis son la catinona y, en menor medida, la catina, que es derivada de la anterior y menos activa a nivel farmacológico. De manera similar a las ya mencionadas catinonas sintéticas (mefedrona, flefedrona) o a la anfetamina, la catinona actúa inhibiendo la recaptación de dopamina y noradrenalina, dando lugar a una estimulación simpaticomimética tanto central como periférica. Sin embargo, sus efectos sobre el sistema serotoninérgico son escasos o inexistentes [39].

«Catha edulis» de User:Katpatuka - With kind permission of / Mit freundlicher Erlaubnis vom Botanischen Garten Ruhr-Universität Bochum. Disponible en:
https://commons.wikimedia.org/wiki/File:Catha_edulis.jpg#/media/File:Catha_edulis.jpg
Figura 3. Hojas de Catha edulis.
Los efectos clínicos del khat se han comparado a los de altas dosis de cafeína. Los primeros efectos aparecen a los minutos de iniciar el consumo e incluyen cierta sensación de bienestar, locuacidad, aumento de la sociabilidad e incremento de la capacidad de concentración. Cuando el consumo se prolonga, puede provocar irritabilidad y anorexia [40]. A nivel físico, los síntomas son similares a los provocados por otros simpaticomiméticos: incremento de la presión arterial, estreñimiento o retención urinaria [37]. El consumo crónico de khat se asocia a un aumento de morbimortalidad documentado en la literatura, aumento de la mortalidad cardiovascular, gastritis crónica, hepatopatía, displasias y cánceres orales, disfunción sexual e incremento del riesgo de aborto [39],[41]. Además, a nivel psicopatológico, el consumo de khat podría empeorar el curso de una psicosis previamente diagnosticada o dar lugar, de manera aguda, a reacciones paranoides [42]. Por último, se ha sugerido que el consumo crónico de khat puede provocar fenómenos de tolerancia y dependencia, así como conducir a un deterioro en los ámbitos social y laboral [43].
Kratom
El término kratom (o ketum) engloba una serie de productos de origen vegetal, derivados de las hojas del arbusto Mytragina speciosa, endémico del Sudeste Asiático. Se trata de una planta utilizada desde hace siglos en la medicina tradicional de Tailandia y Malasia y que aún a día de hoy se consume en regiones rurales de estos países como remedio vigorizante, afrodisíaco y analgésico [44],[45]. El consumo del kratom se realiza fundamentalmente por vía oral, infundiendo las hojas en agua hervida. Existen informes, no obstante, de consumo inhalado, fumando los extractos secos de kratom [46]. Durante los últimos 10 años, se ha observado una expansión espectacular del consumo de kratom en Occidente, facilitado por el comercio en línea, hasta situarse como una de las sustancias psicoactivas más presentes en Internet. [16].
Las hojas de Mytragina speciosa contienen numerosas sustancias con potencial psicoactividad. La más conocida es la mitraginina, que actúa como un agonista de receptores delta y mu opioides. En menor proporción también se encuentra la 7-hidroximitraginina, de la que se ha descrito una actividad agonista opiode unas 40 veces más potente que la de la morfina. Además, se ha sugerido que el kratom también podría tener efectos serotoninérgicos y dopaminérgicos [47].
Se han identificado dos tipos de consumidores de kratom. Por un lado, aquellos que lo utilizan para aliviar síntomas de dolor crónico. Por otro, pacientes con dependencia a otros opiáceos que, al no poder acceder a los mismos, utilizan el kratom para paliar los síntomas abstinenciales. Así, el kratom podría estar remplazando a fármacos opiáceos que se adquirían por Internet sin prescripción médica [48]. Los usuarios del kratom describen, con la intoxicación, una relajación placentera, similar a la que se obtiene con opiáceos clásicos como la morfina [46]. Se ha sugerido, no obstante, que a dosis bajas o al inicio de la intoxicación, los efectos estimulantes podrían predominar sobre los sedativos [49]. Además, la intoxicación puede acompañarse de vómitos y náuseas, sudoración o miosis. Como posibles complicaciones, se han reseñado las convulsiones y la colestasis intrahepática [50].
Aunque no se han descrito muertes asociadas al uso exclusivo de kratom, sí se han observado intoxicaciones letales cuando se combinaba con otras sustancias depresoras del sistema nervioso central, como benzodiacepinas u opiáceos sintéticos [51]. El consumo de kratom continuado en el tiempo puede dar lugar a fenómenos de tolerancia y dependencia. Asimismo, su interrupción brusca produciría síntomas de abstinencia similares a los provocados por otros opiáceos (ansiedad, mialgias, diarrea, rinorrea, etcétera) [52].
Salvia divinorum
Salvia divinorum es una hierba que crece en regiones reducidas del interior de México. Relativamente desconocida hasta mediados del siglo XX, su uso tradicional se limitaba a ceremonias de adivinación o sanación llevadas a cabo por pueblos de la etnia mazateca [53]. No obstante, en las últimas décadas ha tenido lugar una importante expansión de su uso en todo el mundo, probablemente asociado a la venta por Internet desprovista de significados rituales [54]. Aunque el consumo tradicional se realizaba mascando hojas frescas, actualmente Salvia divinorum se consume fumando extractos secos de la planta, de potencia variable [4].

"Salvia divinorum - Herba de Maria". Licensed under CC BY-SA 3.0 via Wikimedia Commons – Disponible en:
https://commons.wikimedia.org/wiki/File:Salvia_divinorum_-Herba_de_Maria.jpg#/media/File:Salvia_divinorum_-_Herba_de_Maria.jpg.
Figura 4. Hojas de Salvia divinorum.
Se trata de una planta de fácil acceso a través de Internet y popular, debido a la baja percepción de riesgo por parte de sus consumidores [16]. Esto probablemente haya facilitado que su uso se extienda entre adultos jóvenes e incluso adolescentes o estudiantes, generando cierta alarma social [55],[56].
La salvinorina A, un agonista kappa-opioide intensamente selectivo, es la principal sustancia activa de la planta [57]. Salvia divinorum presenta por tanto una farmacología única, que contrasta con las de otras sustancias psicodélicas conocidas, en las que predomina el efecto serotoninérgico. Se ha sugerido que la diana principal de la salvinorina A sería el claustrum, lo que explicaría sus efectos predominantemente disociativos [58].
La Salvia divinorum se puede clasificar entre las sustancias psicodélicas. Aunque a dosis bajas o al inicio de la intoxicación predomina la ansiólisis, así como cierta desinhibición, posteriormente van surgiendo cambios senso-perceptivos, tanto de tipo propioceptivo o vestibular como visual. A dosis muy altas, aparece un efecto disociativo más evidente [4],[59]. El cuadro tiende a ceder al cabo de unos 20 minutos de la última inhalación y no asocia signos físicos evidentes más allá de una dudosa aceleración del ritmo cardíaco [60]. Por otra parte, no hay datos de muertes o complicaciones graves relacionadas con el consumo agudo o crónico de Salvia divinorum.
Tabernanthe iboga
Las raíces del arbusto africano Tabernanthe iboga se han consumido tradicionalmente en zonas de África occidental como vigorizante o, a dosis mayores, como alucinógeno en ritos iniciáticos [3]. En Europa y América su uso fue incrementándose a partir de los años 80 a raíz de la observación, por parte de grupos de autoayuda, de que su consumo podría reducir los síntomas de abstinencia y craving a cocaína y heroína [60]. Así, la ibogaína, principal alcaloide presente en las raíces de Tabernanthe iboga, se ha encuadrado como sustancia dirigida al tratamiento de adicciones, tanto en contextos alternativos como en estudios científicos renombrados. A pesar de que su efectividad sigue siendo debatida al día de hoy [62],[63], algunos estudios sugieren que la ibogaína reduce el craving a opiáceos [64] y prolonga los periodos sin consumo en dependientes a sustancias estimulantes como cocaína o crack [65], lo que la podría colocar como una posible herramienta terapéutica en este campo [64]. El consumo habitual es oral; mientras que los usuarios tradicionales ingerían un preparado a base de raíces de Tabernanthe iboga, para sus aplicaciones modernas es más fácil encontrar polvo de clorhidrato de ibogaína [66].
La ibogaína actúa fundamentalmente a través de su metabolito noribogaína, de mayor vida media. Sendas sustancias poseen efectos antagonistas del receptor glutamatérgico NMDA y del receptor nicotínico α3β4 de acetilcolina [66].
La intoxicación da lugar a un estado oneroide, que se asemeja a un “sueño vívido” y en el que pueden ocurrir alteraciones sensoperceptivas auditivas y visuales [66]. Además, la experiencia del paciente bajo los efectos de ibogaína suele incluir visiones que promueven la introspección psicológica respecto a su adicción. Esta sustancia facilita un estado de “consciencia cósmica” que podría subyacer en su posible eficacia en el tratamiento de adicciones [15]. El consumo de ibogaína, incluso puntual, no está exento de riesgo, puesto que se han reportado varias decenas de muertes asociadas al mismo [67]. El mecanismo de producción podría ser una prolongación del intervalo QT que conduciría a una taquiarritmia ventricular intermitente en Torsade de pointes [68],[69]. Otra complicación descrita recientemente es la aparición de síntomas de manía tras el consumo de ibogaína [70].
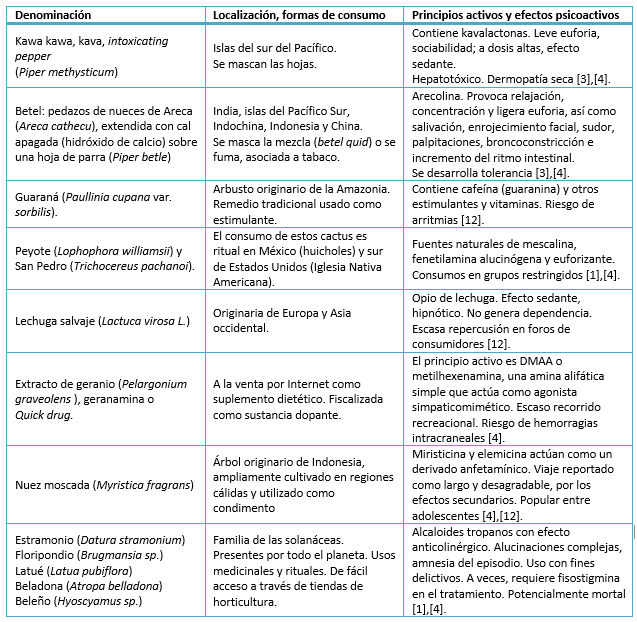
Tabla 3. Otros vegetales psicoactivos usados como nuevas drogas psicoactivas.
Coincidiendo con la constante reinvención del uso global de nuevas drogas psicoactivas, la comunidad de e-psiconautas ha mostrado su interés tanto en especies psicótropas africanas [71], como en vegetales psicoactivos menos conocidos en el resto de los continentes, tratando de seguir la estela de “redescubrimientos” como la kanna o las catinonas sintéticas derivadas de Catha edulis [4].
Sin embargo, hemos podido constatar que algunas recientes incorporaciones de estos vegetales al acervo de conocimiento médico-psiconáutico se basan en tibias opiniones personales de consumidores sobre experiencias aisladas, de escaso valor científico, o bien en informes obtenidos a su vez en comunicaciones de campo, de validez semejante. Ejemplos de ello encontramos tanto en comunidades cibernéticas dedicadas a compartir información sobre drogas [46], como en reciente literatura científica especializada [72] que se ha hecho eco de este movimiento consumista. Entre éstos se cuentan la amerindia “sinicuichi” (Heimia salicifolia), arbusto utilizado tradicionalmente en etnomedicina como antiinflamatorio, publicitado por la comunidad e-psiconáutica tras sesgadas experiencias sobre su supuesta psicoactividad [12],[46]; la hortensia (Hydrangea sp), cuyo consumo fumado con intención expansiva de la conciencia ha sido notificado en Francia y Alemania, informando igualmente del riesgo de producción de cianuro de hidrógeno (ácido cianhídrico) en la combustión de las hojas, situando a esta planta ornamental en la lista de tóxicos vegetales potencialmente letales más que en la de psicótropos [73],[74]; la corteza del arbusto oriundo de China, Magnolia officinalis, con actividad científicamente reconocida como antiestresante y como antioxidante, cuyos principios activos interesan a receptores cannabinoides y GABAérgicos [75], lo que puede haber servido de reclamo para un consumo recreacional de escasa relevancia [12]; y por último el vegetal prototipo de este controvertido grupo, african peach (Nauclea latifolia), informado inicialmente como fuente del principio activo tramadol, analgésico de síntesis utilizado en la farmacopea occidental desde su descubrimiento y salida al mercado en los años 70.
Efectivamente, en 2013 se encontró que cierta cantidad de la droga estaba presente de forma natural en la raíz del “melocotón africano”, árbol utilizado por indígenas cameruneses debido a sus propiedades analgésicas [76]. Sin embargo, en septiembre de 2014, nuevas investigaciones postularon que se trataba de una contaminación cruzada antropogénica. Es decir, los granjeros de una zona de Camerún consumían diariamente tramadol para aumentar su resistencia durante la jornada laboral, práctica que hicieron extensiva a sus animales de tiro y ganado. Después, las deyecciones de hombres y sobre todo de animales, pasarían no sólo a las raíces de las plantas cercanas –entre las que encontraron Nauclea latifolia-, sino al agua de las acequias y a la de pozos que bebe la gente del lugar [77].
Estos son algunos ejemplos de plantas a las que medios de comunicación de diferente naturaleza les han otorgado una publicidad equívoca respecto de su psicoactividad y, por extensión, de sus riesgos potenciales.
Existe un interés creciente en los vegetales psicoactivos, ilustrado por la proliferación de publicaciones científicas, de reportes de organismos oficiales internacionales y de información polifacética en la red. A pesar de que muchas plantas son utilizadas desde hace milenios, el mundo occidental se hace eco de intoxicaciones y novedosos patrones de consumo, en el contexto de las nuevas drogas psicoactivas.
Algunos vegetales, como la pócima ayahuasca, resultante de varias plantas, o el arbusto Tabernanthe iboga han demostrado eficacia en el tratamiento de adicciones a sustancias. Otros, como Ephedra spp. o Catha edulis han servido de inspiración para la síntesis tanto de nuevas drogas como de sustancias ilegales. Ciertos vegetales, como kratom, Salvia divinorum o las semillas de Rosa de Madera Hawaiana son productos muy demandados por Internet.
Dado que muchas de estas plantas se han utilizado de forma tradicional, existe un cierto grado de evidencia a favor de su escasa capacidad adictiva, en general. Aunque se van reportando casos clínicos de complicaciones médicas asociadas a las intoxicaciones, algunas de ellas letales, el conocimiento sobre el perfil de seguridad de estos vegetales es escaso. De hecho, artículos científicos señalan plantas con riesgo de abuso, al menos, controvertido. Son necesarios más estudios farmacológicos para poder determinar el rango de seguridad de cada una de estas plantas, así como sus posibles cualidades terapéuticas.
Conflictos de intereses
Los autores han completado el formulario de declaración de conflictos de intereses del ICMJE, y declaran no haber recibido financiamiento para la realización del artículo, la autora Helen Dolengevich Segal declara tener derechos de autor sobre el libro Nuevas Drogas Psicoactivas, Entheos, 2015. Los formularios pueden solicitarse al autor o la Revista.
Financiamiento
Los autores declaran que no hubo fuentes de financiación externas.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

There is growing interest in plants with psychoactive effects among consumers with different levels of experience. This has generated a need for updated knowledge among medical professionals and other health workers. These plants, which may be used in shamanic healing ceremonies or rituals or just for traditional purposes, have emerged in the Western world as new psychoactive drugs; largely thanks to the ease of purchase, sale, cultivation and exchange of information that the Internet offers. This review summarizes the current knowledge about the most important psychoactive plants, either by their mention in Internet forums or harm-reduction portals or by their allusion in scientific texts.
 Autores:
Beatriz Rodríguez Salgado[1], Jorge Gómez-Arnau Ramírez[2], Daniel Sánchez Mateos[3], Helen Dolengevich Segal[2]
Autores:
Beatriz Rodríguez Salgado[1], Jorge Gómez-Arnau Ramírez[2], Daniel Sánchez Mateos[3], Helen Dolengevich Segal[2]

Citación: Rodríguez Salgado B, Gómez-Arnau Ramírez J, Sánchez Mateos D, Dolengevich Segal H. Vegetables as new psychoactive drugs: a narrative review. Medwave 2016 Ene;16(1):e6372 doi: 10.5867/medwave.2016.01.6372
Fecha de envío: 1/11/2015
Fecha de aceptación: 2/1/2016
Fecha de publicación: 21/1/2016
Origen: no solicitado
Tipo de revisión: con revisión por dos pares revisores externos, a doble ciego

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Schultes RE, Hofmann A. Plantas de los Dioses. México, Fondo de Cultura Económica, 2000.
Schultes RE, Hofmann A. Plantas de los Dioses. México, Fondo de Cultura Económica, 2000.  Dolengevich-Segal H, Rodríguez Salgado B, Gómez-Arnau Ramírez J, Sánchez-Mateos D. New Psychoactive Drugs. Adicciones. 2015 Sep 15;27(3):231-232.
| PubMed |
Dolengevich-Segal H, Rodríguez Salgado B, Gómez-Arnau Ramírez J, Sánchez-Mateos D. New Psychoactive Drugs. Adicciones. 2015 Sep 15;27(3):231-232.
| PubMed | Ujváry I. Psychoactive natural products: overview of recent developments. Ann Ist Super Sanita. 2014; 50(1):12-27. | CrossRef | PubMed |
Ujváry I. Psychoactive natural products: overview of recent developments. Ann Ist Super Sanita. 2014; 50(1):12-27. | CrossRef | PubMed | Dolengevich Segal H, Gómez-Arnau Ramírez J, Rodríguez Salgado B, Sánchez-Mateos D (editores). Nuevas Drogas Psicoactivas. Espańa: Entheos; 2015.
Dolengevich Segal H, Gómez-Arnau Ramírez J, Rodríguez Salgado B, Sánchez-Mateos D (editores). Nuevas Drogas Psicoactivas. Espańa: Entheos; 2015.  Nelson ME, Bryant SM, Aks SE. Emerging drugs of abuse. Emerg Med Clin North Am. 2014 Feb;32(1):1-28. | CrossRef | PubMed |
Nelson ME, Bryant SM, Aks SE. Emerging drugs of abuse. Emerg Med Clin North Am. 2014 Feb;32(1):1-28. | CrossRef | PubMed | United Nations Office on Drugs and Crime. The Challenge of New Psychoactive Substances. 2013, unodc.org [on line]. | Link |
United Nations Office on Drugs and Crime. The Challenge of New Psychoactive Substances. 2013, unodc.org [on line]. | Link | Kikura-Hanajiri R, Uchiyama N, Goda Y. Survey of current trends in the abuse of psychotropic substances and plants in Japan. Leg Med (Tokyo). 2011 May; 13(3):109-15. | CrossRef | PubMed |
Kikura-Hanajiri R, Uchiyama N, Goda Y. Survey of current trends in the abuse of psychotropic substances and plants in Japan. Leg Med (Tokyo). 2011 May; 13(3):109-15. | CrossRef | PubMed | Burns L, Roxburgh A, Matthews A, Bruno R, Lenton S, Van Buskirk J. The rise of new psychoactive substance use in Australia. Drug Test Anal. 2014 Jul-Aug; 6(7-8):846-9. | CrossRef | PubMed |
Burns L, Roxburgh A, Matthews A, Bruno R, Lenton S, Van Buskirk J. The rise of new psychoactive substance use in Australia. Drug Test Anal. 2014 Jul-Aug; 6(7-8):846-9. | CrossRef | PubMed | Riba J, Valle M, Urbano G, Yritia M, Morte A, Barbanoj MJ. Human pharmacology of ayahuasca: subjective and cardiovascular effects, monoamine metabolite excretion, and pharmacokinetics. J Pharmacol Exp Ther. 2003; 306(1):73-83. | PubMed |
Riba J, Valle M, Urbano G, Yritia M, Morte A, Barbanoj MJ. Human pharmacology of ayahuasca: subjective and cardiovascular effects, monoamine metabolite excretion, and pharmacokinetics. J Pharmacol Exp Ther. 2003; 306(1):73-83. | PubMed | Ott J. Pharmacotheon. Espańa: Los Libros de la Liebre de Marzo; 2000.
Ott J. Pharmacotheon. Espańa: Los Libros de la Liebre de Marzo; 2000.  Majić T, Schmidt TT, Gallinat J. Peak experiences and the afterglow phenomenon: when and how do therapeutic effects of hallucinogens depend on psychedelic experiences? J Psychopharmacol. 2015; 29(3):241-53. | CrossRef | PubMed |
Majić T, Schmidt TT, Gallinat J. Peak experiences and the afterglow phenomenon: when and how do therapeutic effects of hallucinogens depend on psychedelic experiences? J Psychopharmacol. 2015; 29(3):241-53. | CrossRef | PubMed | Araújo AM, Carvalho F, Bastos Mde L, Guedes de Pinho P, Carvalho M. The hallucinogenic world of tryptamines: an updated review. Arch Toxicol. 2015; 89(8):1151-73. | CrossRef | PubMed |
Araújo AM, Carvalho F, Bastos Mde L, Guedes de Pinho P, Carvalho M. The hallucinogenic world of tryptamines: an updated review. Arch Toxicol. 2015; 89(8):1151-73. | CrossRef | PubMed | Barbanoj MJ, Riba J, Clos S, Giménez S, Grasa E, Romero S. Daytime Ayahuasca administration modulates REM and slow-wave sleep in healthy volunteers. Psychopharmacology (Berl). 2008 Feb;196(2):315-26. | PubMed |
Barbanoj MJ, Riba J, Clos S, Giménez S, Grasa E, Romero S. Daytime Ayahuasca administration modulates REM and slow-wave sleep in healthy volunteers. Psychopharmacology (Berl). 2008 Feb;196(2):315-26. | PubMed | Winkelman M. Psychedelics as medicines for substance abuse rehabilitation: evaluating treatments with LSD, Peyote, Ibogaine and Ayahuasca. Curr Drug Abuse Rev. 2014;7(2):101-16. | PubMed |
Winkelman M. Psychedelics as medicines for substance abuse rehabilitation: evaluating treatments with LSD, Peyote, Ibogaine and Ayahuasca. Curr Drug Abuse Rev. 2014;7(2):101-16. | PubMed | Schmidt MM, Sharma A, Schifano F, Feinmann C. "Legal highs" on the net-Evaluation of UK-based Websites, products and product information. Forensic Sci Int. 2011 Mar 20; 206(1-3):92-7. | CrossRef | PubMed |
Schmidt MM, Sharma A, Schifano F, Feinmann C. "Legal highs" on the net-Evaluation of UK-based Websites, products and product information. Forensic Sci Int. 2011 Mar 20; 206(1-3):92-7. | CrossRef | PubMed | Font Quer P. Antófitos, Papaveráceas. En: Plantas Medicinales. El Dioscórides renovado, Espańa: Editorial Península; 2005:242-4.
Font Quer P. Antófitos, Papaveráceas. En: Plantas Medicinales. El Dioscórides renovado, Espańa: Editorial Península; 2005:242-4.  Mességué M. Amapola. En: Mi herbario de salud. Espańa: Plaza & Janes;1975: 64-6.
Mességué M. Amapola. En: Mi herbario de salud. Espańa: Plaza & Janes;1975: 64-6.  Günaydın YK, Dündar ZD, Çekmen B, Akıllı NB, Köylü R, Cander B. Intoxication due to Papaver rhoeas (Corn Poppy): Five Case Reports. Case Rep Med. 2015;2015:321360. | CrossRef | PubMed |
Günaydın YK, Dündar ZD, Çekmen B, Akıllı NB, Köylü R, Cander B. Intoxication due to Papaver rhoeas (Corn Poppy): Five Case Reports. Case Rep Med. 2015;2015:321360. | CrossRef | PubMed | El País, 14/06/1995, Martínez A. Un hombre muere tras beber una tisana de amapolas. El País. 14/06/1995; Archivo [on line]. | Link |
El País, 14/06/1995, Martínez A. Un hombre muere tras beber una tisana de amapolas. El País. 14/06/1995; Archivo [on line]. | Link | Gonullu H, Karadas S, Dulger AC, Ebinc S. Hepatotoxicity associated with the ingestion of Papaver Rhoease. J Pak Med Assoc. 2014;64(10):1189-90. | PubMed |
Gonullu H, Karadas S, Dulger AC, Ebinc S. Hepatotoxicity associated with the ingestion of Papaver Rhoease. J Pak Med Assoc. 2014;64(10):1189-90. | PubMed | Azerty. "Concentrated Decoction: An Experience with Poppies - California (ID 63290)". Erowid.org. Jan 21, 2010. erowid.org [on line]. | Link |
Azerty. "Concentrated Decoction: An Experience with Poppies - California (ID 63290)". Erowid.org. Jan 21, 2010. erowid.org [on line]. | Link | TEK. “Guide To Making (a Sort Of) Laudanum, (A step by step pictorial)”. Drugs-forum.org. April 4, 2008 [on line]. | Link |
TEK. “Guide To Making (a Sort Of) Laudanum, (A step by step pictorial)”. Drugs-forum.org. April 4, 2008 [on line]. | Link | Escohotado A. Sección primera. La Era Pagana. 4. La Ebriedad Sagrada. III. La América Precolombina. 2. La civilización andina. b. Otros estimulantes americanos. En: Historia General de las Drogas. Espańa, Espasa Calpe; 1998.
Escohotado A. Sección primera. La Era Pagana. 4. La Ebriedad Sagrada. III. La América Precolombina. 2. La civilización andina. b. Otros estimulantes americanos. En: Historia General de las Drogas. Espańa, Espasa Calpe; 1998.  The Ephedra site. Clinical Toxicology Review, Vol. 18, No. 10 July 1996. EPHEDRA ('MA HUANG') [on line]. | Link |
The Ephedra site. Clinical Toxicology Review, Vol. 18, No. 10 July 1996. EPHEDRA ('MA HUANG') [on line]. | Link | JIFE (Junta Internacional de Fiscalización de Estupefacientes). Decimocuarta edición, enero de 2015. Lista Roja. Lista de precursores y sustancias químicas utilizados frecuentemente en la fabricación ilícita de estupefacientes y sustancias sicotrópicas sometidos a fiscalización internacional. [on line]. | Link |
JIFE (Junta Internacional de Fiscalización de Estupefacientes). Decimocuarta edición, enero de 2015. Lista Roja. Lista de precursores y sustancias químicas utilizados frecuentemente en la fabricación ilícita de estupefacientes y sustancias sicotrópicas sometidos a fiscalización internacional. [on line]. | Link | Avois L, Robinson N, Saudan C, Baume N, Mangin P, Saugy M. Central nervous system stimulants and sport practice. Br J Sports Med. 2006;40 Suppl 1:i16-20. | PubMed |
Avois L, Robinson N, Saudan C, Baume N, Mangin P, Saugy M. Central nervous system stimulants and sport practice. Br J Sports Med. 2006;40 Suppl 1:i16-20. | PubMed | Agencia Mundial Antidopaje, 20 de septiembre de 2014. El Código Mundial Antidopaje. La lista de prohibiciones 2015. Estándar internacional [on line]. | Link |
Agencia Mundial Antidopaje, 20 de septiembre de 2014. El Código Mundial Antidopaje. La lista de prohibiciones 2015. Estándar internacional [on line]. | Link | Shekelle PG, Hardy ML, Morton SC, Maglione M, Mojica WA, Suttorp MJ, et al. Efficacy and safety of ephedra and ephedrine for weight loss and athletic performance: a meta-analysis. JAMA. 2003 Mar 26;289(12):1537-45. | PubMed |
Shekelle PG, Hardy ML, Morton SC, Maglione M, Mojica WA, Suttorp MJ, et al. Efficacy and safety of ephedra and ephedrine for weight loss and athletic performance: a meta-analysis. JAMA. 2003 Mar 26;289(12):1537-45. | PubMed | Zell-Kanter M, Quigley MA, Leikin JB. Reduction in ephedra poisonings after FDA ban. N Engl J Med. 2015 May 28;372(22):2172-4. | CrossRef | PubMed |
Zell-Kanter M, Quigley MA, Leikin JB. Reduction in ephedra poisonings after FDA ban. N Engl J Med. 2015 May 28;372(22):2172-4. | CrossRef | PubMed | Smith MT, Crouch NR, Gericke N, Hirst M. Psychoactive constituents of the genus Sceletium N.E.Br. and other Mesembryanthemaceae: a review. J Ethnopharmacol. 1996;50(3):119-30. | PubMed |
Smith MT, Crouch NR, Gericke N, Hirst M. Psychoactive constituents of the genus Sceletium N.E.Br. and other Mesembryanthemaceae: a review. J Ethnopharmacol. 1996;50(3):119-30. | PubMed | Harvey AL, Young LC, Viljoen AM, Gericke NP. Pharmacological actions of the South African medicinal and functional food plant Sceletium tortuosum and its principal alkaloids. J Ethnopharmacol. 2011 Oct 11;137(3):1124-9. | CrossRef | PubMed |
Harvey AL, Young LC, Viljoen AM, Gericke NP. Pharmacological actions of the South African medicinal and functional food plant Sceletium tortuosum and its principal alkaloids. J Ethnopharmacol. 2011 Oct 11;137(3):1124-9. | CrossRef | PubMed | Terburg D, Syal S, Rosenberger LA, Heany S, Phillips N, Gericke N, Stein DJ, van Honk J. Acute effects of Sceletium tortuosum (Zembrin), a dual 5-HT reuptake and PDE4 inhibitor, in the human amygdala and its connection to the hypothalamus. Neuropsychopharmacology. 2013;38(13):2708-16. | CrossRef | PubMed |
Terburg D, Syal S, Rosenberger LA, Heany S, Phillips N, Gericke N, Stein DJ, van Honk J. Acute effects of Sceletium tortuosum (Zembrin), a dual 5-HT reuptake and PDE4 inhibitor, in the human amygdala and its connection to the hypothalamus. Neuropsychopharmacology. 2013;38(13):2708-16. | CrossRef | PubMed | Al-Mugahed L. Khat chewing in Yemen: turning over a new leaf. Bull World Health Organ. 2008;86(10):741-2.
| PubMed |
Al-Mugahed L. Khat chewing in Yemen: turning over a new leaf. Bull World Health Organ. 2008;86(10):741-2.
| PubMed | Gebissa E. Khat in the Horn of Africa: historical perspectives and current trends. J Ethnopharmacol. 2010 Dec 1;132(3):607-14. | CrossRef | PubMed |
Gebissa E. Khat in the Horn of Africa: historical perspectives and current trends. J Ethnopharmacol. 2010 Dec 1;132(3):607-14. | CrossRef | PubMed | Wabe NT. Chemistry, pharmacology, and toxicology of khat (catha edulis forsk): a review. Addict Health. 2011;3(3-4):137-49. | PubMed |
Wabe NT. Chemistry, pharmacology, and toxicology of khat (catha edulis forsk): a review. Addict Health. 2011;3(3-4):137-49. | PubMed | Griffiths P, Lopez D, Sedefov R, Gallegos A, Hughes B, Noor A, et al. Khat use and monitoring drug use in Europe: the current situation and issues for the future. J Ethnopharmacol. 2010 Dec 1;132(3):578-83. | CrossRef | PubMed |
Griffiths P, Lopez D, Sedefov R, Gallegos A, Hughes B, Noor A, et al. Khat use and monitoring drug use in Europe: the current situation and issues for the future. J Ethnopharmacol. 2010 Dec 1;132(3):578-83. | CrossRef | PubMed | Nencini P, Ahmed AM. Khat consumption: a pharmacological review. Drug Alcohol Depend. 1989 Jan;23(1):19-29. | PubMed |
Nencini P, Ahmed AM. Khat consumption: a pharmacological review. Drug Alcohol Depend. 1989 Jan;23(1):19-29. | PubMed | Corkery JM, Schifano F, Oyefeso A, Ghodse AH, Tonia T, Naidoo V, et al. Overview of literature and information on "khat-related" mortality: a call for recognition of the issue and further research. Ann Ist Super Sanita. 2011;47(4):445-64. | CrossRef | PubMed |
Corkery JM, Schifano F, Oyefeso A, Ghodse AH, Tonia T, Naidoo V, et al. Overview of literature and information on "khat-related" mortality: a call for recognition of the issue and further research. Ann Ist Super Sanita. 2011;47(4):445-64. | CrossRef | PubMed | Odenwald M, Neuner F, Schauer M, Elbert T, Catani C, Lingenfelder B, Hinkel H, Häfner H, Rockstroh B. Khat use as risk factor for psychotic disorders: a cross-sectional and case-control study in Somalia. BMC Med. 2005 Feb 12;3:5. | PubMed |
Odenwald M, Neuner F, Schauer M, Elbert T, Catani C, Lingenfelder B, Hinkel H, Häfner H, Rockstroh B. Khat use as risk factor for psychotic disorders: a cross-sectional and case-control study in Somalia. BMC Med. 2005 Feb 12;3:5. | PubMed | Kassim S, Croucher R, al'Absi M. Khat dependence syndrome: a cross sectional preliminary evaluation amongst UK-resident Yemeni khat chewers. J Ethnopharmacol. 2013 Apr 19;146(3):835-41. | CrossRef | PubMed |
Kassim S, Croucher R, al'Absi M. Khat dependence syndrome: a cross sectional preliminary evaluation amongst UK-resident Yemeni khat chewers. J Ethnopharmacol. 2013 Apr 19;146(3):835-41. | CrossRef | PubMed | Jansen KL, Prast CJ. Ethnopharmacology of kratom and the Mitragyna alkaloids. J Ethnopharmacol. 1988;23(1):115-9. | PubMed |
Jansen KL, Prast CJ. Ethnopharmacology of kratom and the Mitragyna alkaloids. J Ethnopharmacol. 1988;23(1):115-9. | PubMed | Ahmad K, Aziz Z. Mitragyna speciosa use in the northern states of Malaysia: a cross-sectional study. J Ethnopharmacol. 2012 May 7;141(1):446-50. | CrossRef | PubMed |
Ahmad K, Aziz Z. Mitragyna speciosa use in the northern states of Malaysia: a cross-sectional study. J Ethnopharmacol. 2012 May 7;141(1):446-50. | CrossRef | PubMed | Stolt AC, Schröder H, Neurath H, Grecksch G, Höllt V, Meyer MR, et al. Behavioral and neurochemical characterization of kratom (Mitragyna speciosa) extract. Psychopharmacology (Berl). 2014;231(1):13-25. | CrossRef | PubMed |
Stolt AC, Schröder H, Neurath H, Grecksch G, Höllt V, Meyer MR, et al. Behavioral and neurochemical characterization of kratom (Mitragyna speciosa) extract. Psychopharmacology (Berl). 2014;231(1):13-25. | CrossRef | PubMed | Boyer EW, Babu KM, Macalino GE. Self-treatment of opioid withdrawal with a dietary supplement, Kratom. Am J Addict. 2007;16(5):352-6. | PubMed |
Boyer EW, Babu KM, Macalino GE. Self-treatment of opioid withdrawal with a dietary supplement, Kratom. Am J Addict. 2007;16(5):352-6. | PubMed | Babu KM, McCurdy CR, Boyer EW. Opioid receptors and legal highs: Salvia divinorum and Kratom. Clin Toxicol (Phila). 2008;46(2):146-52. | CrossRef | PubMed |
Babu KM, McCurdy CR, Boyer EW. Opioid receptors and legal highs: Salvia divinorum and Kratom. Clin Toxicol (Phila). 2008;46(2):146-52. | CrossRef | PubMed | Dorman C, Wong M, Khan A. Cholestatic hepatitis from prolonged kratom use: a case report. Hepatology. 2015;61(3):1086-7. | CrossRef | PubMed |
Dorman C, Wong M, Khan A. Cholestatic hepatitis from prolonged kratom use: a case report. Hepatology. 2015;61(3):1086-7. | CrossRef | PubMed | Kronstrand R, Roman M, Thelander G, Eriksson A. Unintentional fatal intoxications with mitragynine and O-desmethyltramadol from the herbal blend Krypton. J Anal Toxicol. 2011;35(4):242-7. | PubMed |
Kronstrand R, Roman M, Thelander G, Eriksson A. Unintentional fatal intoxications with mitragynine and O-desmethyltramadol from the herbal blend Krypton. J Anal Toxicol. 2011;35(4):242-7. | PubMed | Singh D, Müller CP, Vicknasingam BK. Kratom (Mitragyna speciosa) dependence, withdrawal symptoms and craving in regular users. Drug Alcohol Depend. 2014 1;139:132-7. | CrossRef | PubMed |
Singh D, Müller CP, Vicknasingam BK. Kratom (Mitragyna speciosa) dependence, withdrawal symptoms and craving in regular users. Drug Alcohol Depend. 2014 1;139:132-7. | CrossRef | PubMed | Valdés LJ 3rd, Díaz JL, Paul AG. Ethnopharmacology of ska María Pastora (Salvia divinorum, Epling and Játiva-M.). J Ethnopharmacol. 1983;7(3):287-312. | PubMed |
Valdés LJ 3rd, Díaz JL, Paul AG. Ethnopharmacology of ska María Pastora (Salvia divinorum, Epling and Játiva-M.). J Ethnopharmacol. 1983;7(3):287-312. | PubMed | Hoover V, Marlowe DB, Patapis NS, Festinger DS, Forman RF. Internet access to Salvia divinorum: implications for policy, prevention, and treatment. J Subst Abuse Treat. 2008;35(1):22-7. | PubMed |
Hoover V, Marlowe DB, Patapis NS, Festinger DS, Forman RF. Internet access to Salvia divinorum: implications for policy, prevention, and treatment. J Subst Abuse Treat. 2008;35(1):22-7. | PubMed | Nyi PP, Lai EP, Lee DY, Biglete SA, Torrecer GI, Anderson IB. Influence of age on Salvia divinorum use: results of an Internet survey. J Psychoactive Drugs. 2010;42(3):385-92.
| PubMed |
Nyi PP, Lai EP, Lee DY, Biglete SA, Torrecer GI, Anderson IB. Influence of age on Salvia divinorum use: results of an Internet survey. J Psychoactive Drugs. 2010;42(3):385-92.
| PubMed | Currie CL. Epidemiology of adolescent Salvia divinorum use in Canada. Drug Alcohol Depend. 2013 1;128(1-2):166-70. | CrossRef | PubMed |
Currie CL. Epidemiology of adolescent Salvia divinorum use in Canada. Drug Alcohol Depend. 2013 1;128(1-2):166-70. | CrossRef | PubMed | Cunningham CW, Rothman RB, Prisinzano TE. Neuropharmacology of the naturally occurring kappa-opioid hallucinogen salvinorin A. Pharmacol Rev. 2011;63(2):316-47. | CrossRef | PubMed |
Cunningham CW, Rothman RB, Prisinzano TE. Neuropharmacology of the naturally occurring kappa-opioid hallucinogen salvinorin A. Pharmacol Rev. 2011;63(2):316-47. | CrossRef | PubMed | Stiefel KM, Merrifield A, Holcombe AO. The claustrum's proposed role in consciousness is supported by the effect and target localization of Salvia divinorum. Front Integr Neurosci. 2014 Feb 26;8:20. | CrossRef | PubMed |
Stiefel KM, Merrifield A, Holcombe AO. The claustrum's proposed role in consciousness is supported by the effect and target localization of Salvia divinorum. Front Integr Neurosci. 2014 Feb 26;8:20. | CrossRef | PubMed | Johnson MW, MacLean KA, Reissig CJ, Prisinzano TE, Griffiths RR. Human psychopharmacology and dose-effects of salvinorin A, a kappa opioid agonist hallucinogen present in the plant Salvia divinorum. Drug Alcohol Depend. 2011 1;115(1-2):150-5. | CrossRef | PubMed |
Johnson MW, MacLean KA, Reissig CJ, Prisinzano TE, Griffiths RR. Human psychopharmacology and dose-effects of salvinorin A, a kappa opioid agonist hallucinogen present in the plant Salvia divinorum. Drug Alcohol Depend. 2011 1;115(1-2):150-5. | CrossRef | PubMed | Dueweke JR. Towards evidence-based emergency medicine: best BETs from the Manchester Royal Infirmary. BET 3: what are the clinical features of Salvia divinorum toxicity? Emerg Med J. 2013;30(4):341-2. | CrossRef | PubMed |
Dueweke JR. Towards evidence-based emergency medicine: best BETs from the Manchester Royal Infirmary. BET 3: what are the clinical features of Salvia divinorum toxicity? Emerg Med J. 2013;30(4):341-2. | CrossRef | PubMed | Sheppard SG. A preliminary investigation of ibogaine: case reports and recommendations for further study. J Subst Abuse Treat. 1994;11(4):379-85. | PubMed |
Sheppard SG. A preliminary investigation of ibogaine: case reports and recommendations for further study. J Subst Abuse Treat. 1994;11(4):379-85. | PubMed | Vastag B. Addiction research. Ibogaine therapy: a 'vast, uncontrolled experiment'. Science. 2005 Apr 15;308(5720):345-6. | PubMed |
Vastag B. Addiction research. Ibogaine therapy: a 'vast, uncontrolled experiment'. Science. 2005 Apr 15;308(5720):345-6. | PubMed | Schenberg EE, de Castro Comis MA, Chaves BR, da Silveira DX. Treating drug dependence with the aid of ibogaine: a retrospective study. J Psychopharmacol. 2014;28(11):993-1000. | CrossRef | PubMed |
Schenberg EE, de Castro Comis MA, Chaves BR, da Silveira DX. Treating drug dependence with the aid of ibogaine: a retrospective study. J Psychopharmacol. 2014;28(11):993-1000. | CrossRef | PubMed | Alper K, Bouso JC. Ibogaine: a review. En: Alper KR, Glick SD, Cordell GA (editores). Ibogaine: Proceedings of the First International Conference (Also published as Volume 56 of The Alkaloids Chemistry and Biology). EEUU, San Diego: Academic Press; 2001. | Link |
Alper K, Bouso JC. Ibogaine: a review. En: Alper KR, Glick SD, Cordell GA (editores). Ibogaine: Proceedings of the First International Conference (Also published as Volume 56 of The Alkaloids Chemistry and Biology). EEUU, San Diego: Academic Press; 2001. | Link | Schenberg EE, de Castro Comis MA, Chaves BR, da Silveira DX. Treating drug dependence with the aid of ibogaine: a retrospective study. J Psychopharmacol. 2014 Nov;28(11):993-1000.
| CrossRef | PubMed |
Schenberg EE, de Castro Comis MA, Chaves BR, da Silveira DX. Treating drug dependence with the aid of ibogaine: a retrospective study. J Psychopharmacol. 2014 Nov;28(11):993-1000.
| CrossRef | PubMed | Alper KR, Lotsof HS, Kaplan CD. The ibogaine medical subculture. J Ethnopharmacol. 2008 4;115(1):9-24. | PubMed |
Alper KR, Lotsof HS, Kaplan CD. The ibogaine medical subculture. J Ethnopharmacol. 2008 4;115(1):9-24. | PubMed | Alper KR, Stajić M, Gill JR. Fatalities temporally associated with the ingestion of ibogaine. J Forensic Sci. 2012;57(2):398-412. | CrossRef | PubMed |
Alper KR, Stajić M, Gill JR. Fatalities temporally associated with the ingestion of ibogaine. J Forensic Sci. 2012;57(2):398-412. | CrossRef | PubMed | Paling FP, Andrews LM, Valk GD, Blom HJ. Life-threatening complications of ibogaine: three case reports. Neth J Med. 2012;70(9):422-4. | PubMed |
Paling FP, Andrews LM, Valk GD, Blom HJ. Life-threatening complications of ibogaine: three case reports. Neth J Med. 2012;70(9):422-4. | PubMed | Hildyard C, Macklin P, Prendergast B, Bashir Y. A Case of QT Prolongation and Torsades de Pointes Caused by Ibogaine Toxicity. J Emerg Med. 2015 Aug 29. pii:S0736-4679(15)00673-3. | CrossRef | PubMed |
Hildyard C, Macklin P, Prendergast B, Bashir Y. A Case of QT Prolongation and Torsades de Pointes Caused by Ibogaine Toxicity. J Emerg Med. 2015 Aug 29. pii:S0736-4679(15)00673-3. | CrossRef | PubMed | Marta CJ, Ryan WC, Kopelowicz A, Koek RJ. Mania following use of ibogaine: A case series. Am J Addict. 2015;24(3):203-5. | CrossRef | PubMed |
Marta CJ, Ryan WC, Kopelowicz A, Koek RJ. Mania following use of ibogaine: A case series. Am J Addict. 2015;24(3):203-5. | CrossRef | PubMed | Orsolini L, Papanti GD, Francesconi G, Schifano F. Mind navigators of chemicals' experimenters? A web-based description of e-psychonauts. Cyberpsychol Behav Soc Netw. 2015;18(5):296-300.
| CrossRef | PubMed |
Orsolini L, Papanti GD, Francesconi G, Schifano F. Mind navigators of chemicals' experimenters? A web-based description of e-psychonauts. Cyberpsychol Behav Soc Netw. 2015;18(5):296-300.
| CrossRef | PubMed | Schifano F, Orsolini L, Duccio Papanti G, Corkery JM. Novel psychoactive substances of interest for psychiatry. World Psychiatry. 2015;14(1):15-26. | CrossRef | PubMed |
Schifano F, Orsolini L, Duccio Papanti G, Corkery JM. Novel psychoactive substances of interest for psychiatry. World Psychiatry. 2015;14(1):15-26. | CrossRef | PubMed | High danger hydrangea? French police hunt gang peddling 'cheaper weed'. The Guardian. 6/02/2014 [on line]. | Link |
High danger hydrangea? French police hunt gang peddling 'cheaper weed'. The Guardian. 6/02/2014 [on line]. | Link | Rempel V, Fuchs A, Hinz S, Karcz T, Lehr M, Koetter U, Müller CE. Magnolia Extract, Magnolol, and Metabolites: Activation of Cannabinoid CB2 Receptors and Blockade of the Related GPR55. ACS Med Chem Lett. 2012 Nov 14;4(1):41-5. | CrossRef | PubMed |
Rempel V, Fuchs A, Hinz S, Karcz T, Lehr M, Koetter U, Müller CE. Magnolia Extract, Magnolol, and Metabolites: Activation of Cannabinoid CB2 Receptors and Blockade of the Related GPR55. ACS Med Chem Lett. 2012 Nov 14;4(1):41-5. | CrossRef | PubMed |