 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: Hashimoto’s encephalopathy, Steroid-responsive encephalopathy associated with autoimmune thyroiditis, Hashimoto's encephalitis
La encefalopatía de Hashimoto es una enfermedad rara. Se reporta una prevalencia de 2,1 por cada 100 000 habitantes. Entre las manifestaciones clínicas se describen confusión, disminución del estado de consciencia, déficit cognitivo, convulsiones, mioclonus, ataxia y/o déficits neurológicos focales. Debido a la amplia variedad de signos y síntomas, la sospecha clínica diagnóstica es fundamental. El diagnóstico se basa en tres pilares: la presencia de manifestaciones clínicas neurológicas, con la exclusión de otras causas de encefalopatía; presencia de anticuerpos antitiroideos aumentados; una mejoría clínica notable luego de la administración de inmunomoduladores. El tratamiento de la encefalopatía de Hashimoto tiene dos objetivos: controlar el proceso autoinmune y controlar las complicaciones de la enfermedad. Aunque en la mayoría de los casos la recuperación es completa con el tratamiento, el riesgo de recaídas puede oscilar entre 12,5 a 40% en seguimientos a dos ańos.
|
Ideas clave
|
La encefalopatía de Hashimoto es una patología que fue originalmente descrita por Brain en 1966[1], quien sospechaba una base autoinmune[2]. Es una rara enfermedad caracterizada por un cuadro de encefalopatía asociado a una variedad de síntomas neuropsiquiátricos con anticuerpos antitiroideos positivos[3]. Este trastorno debe ser considerado en pacientes que no tengan patología neurológica previa[4] y luego de descartar la causa infecciosa[5]. La función tiroidea en la mayoría de los casos es normal y llama la atención la excelente respuesta a corticoides[6].
Por lo inusual de su presentación, es importante el conocimiento de las características asociadas a esta patología para su correcto diagnóstico y óptimo tratamiento puesto que, dependiendo de la severidad de la presentación, podría llegar a ser mortal.
El objetivo de esta revisión es dar un alcance del conocimiento actual de los mecanismos fisiopatológicos de esta enfermedad, así como su diagnóstico y manejo; siendo estos conocimientos de vital importancia para el médico especialista.
El artículo se sustenta en la revisión sistemática de diversas bases de datos, para luego someter a un análisis crítico la bibliografía encontrada. Debido a lo controversial de esta patología, la evidencia disponible está principalmente basada en estudios observacionales. Por este motivo, los artículos incluidos fueron mayoritariamente del tipo series y reporte de casos, así como revisiones narrativas.
Criterios de inclusión
En una primera selección se incluyeron todas las publicaciones en los idiomas español e inglés de los últimos cinco años. También se incluyó la bibliografía relevante anterior a la búsqueda, cuyo contenido fue importante para la discusión. Se excluyeron los casos descritos sólo como resúmenes de congresos y/o cartas al editor debido a lo sucinto de la información. Posterior a ello, se evaluó cada caso clínico y series de casos individualmente. También se excluyeron aquellos donde no se hubieran detallado los valores específicos de los anticuerpos antitiroideos (no se consideraron frases como “anticuerpos altos” o “anticuerpos fuera del rango normal”) o si el valor de los anticuerpos no fue lo suficientemente alto para ser parte del diagnóstico (todo reporte de caso en el que al menos un anticuerpo antitiroideo sobrepasó el punto de corte mínimo de 100 micro unidades internacionales por mililitro fue incluido) (Figura 1).
Figura 1. Flujo en la selección de artículos.
Estrategia de búsqueda
Se evaluaron las publicaciones disponibles en las principales bases de datos: MEDLINE/PubMed, ScienceDirect, ProQuest, EBSCO, LILACS , SciELO y otros motores de búsqueda como Google Scholar. Se efectuaron búsquedas con las palabras clave (en inglés y español) en título o abstract “Hashimoto’s encephalopathy”, “Steroid-responsive encephalopathy associated with autoinmune thyroiditis” o “Hashimoto's encephalitis” como concepto suplementario. Se usaron los términos booleanos “AND” y “OR”. Este proceso fue realizado independientemente por ambos investigadores.
Prevalencia
La encefalopatía de Hashimoto es una enfermedad rara. Se reporta una prevalencia de 2,1 por cada 100 000 habitantes, se presenta principalmente en la población adulta con una edad de inicio de 50 años y predominantemente en el sexo femenino en una proporción de cinco a uno[7]. En la población pediátrica existen reportes de presentación desde los 14 meses[8], aunque la mayor frecuencia se encuentra en la adolescencia[9] con un máximo de edad a los 14 años.
Etiología
La etiología de la encefalopatía de Hashimoto es de carácter autoinmune. La forma de presentación como su preponderancia en el sexo femenino, la coexistencia con otras enfermedades autoinmunes hasta en el 30% de los casos[10] (lupus eritematoso sistémico, miastenia gravis, desórdenes del colágeno, entre otras), colocan a esta patología dentro del grupo de las enfermedades inmunológicas.
Recientemente, debido a su naturaleza autoinmune, algunos autores han creído conveniente renombrarla como encefalopatía asociada a enfermedad tiroidea autoinmune[11]. Ello explicaría mejor su etiología y nos da opción de vincularla con toda la variedad de anticuerpos presentes en la autoinmunidad tiroidea y no sólo a los estrechamente relacionados con la tiroiditis de Hashimoto (anti –TPO). La decisión de conservar el nombre tradicional de encefalopatía de Hashimoto en esta revisión, tiene como finalidad el facilitar la búsqueda bibliográfica.
En cuanto a la fisiopatología, son dos las explicaciones vigentes. La primera que es la más extendida, plantea que los anticuerpos antitiroideos anti-tiroglobulina (Anti-Tg), anti-peroxidasa tiroidea (Anti-TPO) o Anti receptor de TSH (anti-TSHR/TRAb), iniciarían la cascada fisiopatológica en esta enfermedad. Esto se debería a que existe evidencia de que los anticuerpos Anti-TPO se unen a los astrocitos y perturbarían la función del sistema nervioso central[3].
La segunda explicación va en búsqueda de otros anticuerpos contra autoantígenos del endotelio vascular cerebral, relacionándolos con daño en el tejido neuronal[12]. Se encontró altos títulos de anticuerpos anti α-enolasa (proteína citosólica de la vía glucolítica de 34 Kilodaltons[13]) común para tejido tiroideo y cerebral[5], en pacientes con encefalopatía de Hashimoto que tuvieron excelente respuesta a los corticoides[14]. Estos anticuerpos atacarían sólo el extremo N-amino terminal de la α-enolasa[15] y podrían ser usados como prueba confirmatoria[16].
Otros anticuerpos propuestos serian anticuerpos Ig G para una proteína neuronal de 36 Kilodaltons, la dimetilargininasa I (presente en células del endotelio) y la aldehído reductasa I (presente en células vasculares y neuronales)[11],[17]. Todas estas proteínas aún están en estudio. De manera menos clara, también se ha vinculado a los anticuerpos contra la célula parietal o el factor intrínseco[18]. Como vemos, existe aún mucha controversia en la etiopatogenia de esta patología.
La literatura sugiere dos formas de presentación. Una de tipo vasculítico recurrente con edema cerebral y reducción del flujo sanguíneo cerebral por lesiones de la microvasculatura que se presenta de manera insidiosa, donde además de la disminución del nivel de conciencia existen alteraciones similares a stroke. Una segunda forma progresiva se expresa como encefalopatía (confusión, psicosis, coma), donde se postula que los anticuerpos antitiroideos cruzarían la barrera hematoencefálica produciendo lesión cerebral[19].
Manifestaciones clínicas
Aunque clásicamente la encefalopatía de Hashimoto se define como un síndrome de características neuropsiquiátricas que producen la desconexión del paciente con su entorno en diverso grado de severidad, que incluso puede llegar hasta el coma[20]. El espectro neurológico de manifestaciones es bien amplio y pueden preceder con bastante anticipación (de días a meses) a la encefalopatía en sí.
Es así, que podemos distinguir las siguientes etapas:
Periodo pre-encefalópatico: las manifestaciones neurológicas son diversas, pudiendo simular cualquier patología del sistema nervioso central. En una serie estudiada de 13 pacientes, se encontró que las manifestaciones más frecuentes asociadas fueron deterioro cognitivo y cambios de comportamiento en 10 pacientes con predominio de compromiso frontal y temporal en la evaluación neuropsicológica, convulsiones en seis, trastornos del sueño en nueve en forma de hipersomnia en seis y reducción del sueño en tres y cefalea en cuatro pacientes4. También se ha asociado a narcolepsia de inicio súbito con cataplexia[21].
Existen casos reportados mucho más complejos, donde la alteración neurológica predominante ha sido de características psiquiátricas como catatonía[22], alucinaciones auditivas, psicosis[23], delirio de persecución y cambios en el estado de ánimo, llegando a ser mal diagnosticado como demencia senil[24], o enmascarado por depresión en el anciano[25]. No todos los pacientes presentan esta etapa.
Encefalopatía propiamente dicha: desconexión gradual o abrupta con el entorno que se puede presentar de manera aislada o antecedida por el periodo antes mencionado.
En ambos casos, la base del diagnóstico es la presencia de anticuerpos antitiroideos elevados y la mejoría casi inmediata luego del inicio de inmunomoduladores[26].
Además, con fines didácticos también podemos clasificar a la encefalopatía de Hashimoto por la manifestación del sistema nervioso central que más predomina en el paciente, sea esta presentación en la etapa pre-encefalópatica o como parte de la encefalopatía (Tabla 1).
Los disturbios autonómicos como hipotensión, bradicardia e hipotermia se relacionan con la afectación hipotalámica y de centros neurovegetativos[2]. En estos casos, es importante descartar la afectación de eje hipotálamo – hipófisis – suprarrenal. La afectación del cerebelo asociada o no a encefalopatía se manifiesta como hipotonía, opsoclonus, dismetría y disdiadococinesia[1]. En ambos casos, la forma de presentación es la manifestación de una vasculitis cerebral generalizada.
El tiempo de duración de las manifestaciones clínicas es variable. Se reporta entre dos días hasta ocho meses[18]; esto depende del momento de inicio del tratamiento, aunque la presentación más frecuente es un inicio súbito con una mejoría clínica rápida luego del inicio de corticoides.
La propia alteración de la función tiroidea puede traer confusión al momento del diagnóstico. El hipotiroidismo descompensado puede presentar complicaciones neurológicas como convulsiones, demencia o psicosis; pero se diferencia de la encefalopatía de Hashimoto en que estas mejoran cuando se reemplaza la tiroxina. Menos frecuentemente se asocia a estados de hipertiroidismo[27], haciéndose necesario el diagnóstico diferencial de psicosis por tirotoxicosis. En cualquier caso, la sospecha clínica es la que lleva al diagnóstico.
Algunos desordenes metabólicos pueden coexistir con la presentación de la encefalopatía[28] como hiponatremia, hiperglicemia, uremia, entre otros; lo que hace más difícil el diagnóstico. En todo caso, el diagnóstico diferencial se hace cuando el manejo específico para cada uno de estos disturbios metabólicos no se plasma en una mejoría del estado del paciente.
Diagnóstico
El diagnóstico de encefalopatía de Hashimoto se basa en un diagnóstico de exclusión. Se debe primeramente agotar todas las posibilidades de patologías propias del sistema nervioso central (tumorales, infecciosa, autoinmunes), así como patologías metabólicas y síndromes paraneoplásicos.
Aunque aún no hay criterios diagnósticos mundialmente aceptados para la encefalopatía de Hashimoto, el diagnóstico se basa en la presencia de manifestaciones clínicas a nivel de sistema nervioso central como confusión, disminución del estado de consciencia, déficit cognitivo, convulsiones, mioclonus, ataxia y/o déficits neurológicos focales[29], entre otros; con la exclusión de otras causas de encefalopatía[9].
Sumado a lo anterior, es criterio fundamental encontrar al menos a un anticuerpo antitiroideo francamente elevado. La literatura señala que el anti-TPO tendría que ser mayor de 200 micro unidades internacionales por mililitro (más de cinco veces el valor normal) e inclusive algunos autores colocan como umbral un punto de corte 500 micro unidades internacionales por mililitro[17]. A pesar de esto, son muchos los casos que se encuentran publicados que no siguen este patrón y hacen el diagnóstico con valores mucho más bajos (Tabla 1), lo que deja en duda un adecuado diagnóstico. Debido a que la presencia de anticuerpos anti-tiroideos es bastante prevalente en la población sana y los síntomas son diversos, el diagnóstico de encefalopatía de Hashimoto se hace difícil[30] y es ahí donde surge la pregunta ¿realmente existe esta enfermedad? ¿O solo estamos viendo las manifestaciones de una patología autoinmune, netamente cerebral que aún desconocemos?
Nosotros sugerimos utilizar como punto de corte, el valor de cualquier anticuerpo antitiroideos mayor o igual de 100 micro unidades internacionales por mililitro para avalar la sospecha diagnóstica. Pero un valor mayor o igual a 200 micro unidades internacionales por mililitro en por lo menos uno de los tres tipos de anticuerpos antitiroideos (anti peroxidasa tiroidea, anti – tiroglobulina y/o anti receptor de TSH), deja mucho más claro el diagnóstico. En ambos casos, luego de excluir otras patologías del sistema nervioso central, el diagnóstico quedaría corroborado con una mejoría notoria con corticoterapia.
Los anticuerpos anti-tiroideos son necesarios pero no suficientes para el diagnóstico, y el título no se correlaciona directamente con la severidad de la enfermedad[84],[85]. En cuanto a la función tiroidea, la mayor parte de los pacientes son eutiroideos al momento de la presentación de la encefalopatía.
El análisis del líquido cefalorraquídeo puede presentar parámetros inflamatorios como la elevación del nivel de proteínas cuyo valor también mejora luego del tratamiento[84], aunque hasta en el 80% de los pacientes tiene características normales[19]. Ocasionalmente, también se puede aislar los anticuerpos antitiroideos y se mantienen elevados posterior a la recuperación del paciente[33]. Es importante resaltar que los anticuerpos antitiroideos en líquido cefalorraquídeo, se pueden encontrar también en pacientes con enfermedades tiroideas diversas u otras patologías de sistema nervioso central como la neurosífilis[86] sin necesidad de estar presentando encefalopatía de Hashimoto en el momento del dosaje.
El electroencefalograma tiene hallazgos inespecíficos que pueden variar dependiendo de las manifestaciones neurológicas que presente el paciente. La alteración que se encuentra con más frecuencia es la aparición de ondas lentas en relación a la encefalopatía[82] y en caso de la presentación asociada a crisis convulsiva se pueden observar focos epileptógeno.
En los exámenes de imágenes (tomografía y/o resonancia magnética cerebral) son en la mayoría de los casos normales o inespecíficos, pero son cruciales para descartar otras etiologías. Entre 49 y 50% de los pacientes pueden presentar atrofia cerebral difusa en localización cortical o subcortical[19], infartos y/o anormalidades focales corticales87. De los casos evaluados, dos de ellos reportaron alteraciones similares a lesiones en región de silla turca.
Tratamiento
El tratamiento de la encefalopatía de Hashimoto tiene dos objetivos. El primero es controlar el proceso autoinmune con la administración de inmunomodulares o recambio plasmático. Lo segundo es controlar las complicaciones de la enfermedad: en el caso de convulsiones agregar antiepilépticos y en el caso de edema cerebral usar manitol[38].
Dentro de los inmunomoduladores la primera línea de tratamiento son los corticoides. El tratamiento se inicia con la administración de metilprednisolona endovenosa de tres a siete días (adultos: un gramo al día, niños: 20 a 30 milígramos por kilogramo al día)[33] seguido de altas dosis de prednisona oral (dosis de uno a dos milígramos por kilogramo al día), que van a ser descontinuadas lentamente conforme se vea la mejoría de los síntomas[29],[88]. La dosis de mantenimiento puede durar desde meses hasta uno o dos años[15].
Otras inmunomoduladores son la inmunoglobulina intravenosa, los anticuerpos monoclonales, azatioprina y el metotrexate. La inmunoglobulina intravenosa es de utilidad cuando los pacientes tienen una respuesta incompleta a esteroides[9], o cuando se presentan recaídas al momento de desescalar. En el caso de anticuerpos monoclonales, la dosis sugerida de rituximab es de 1000 milígramos por vía endovenosa el día uno y 14; y luego una vez cada seis a nueve meses, dependiendo del recuento de leucocitos[89]. Este medicamento es bien tolerado y produce una remisión sostenida, sin necesidad de asociarlo a corticoides[90].
La inclusión de la plasmaféresis en la terapia tenía como objetivo la remoción de los anticuerpos antitiroideos circulantes, pero como se ha demostrado que la severidad de la enfermedad no se relaciona con el título de anticuerpos, se piensa que en la plasmaféresis también se remueven otros anticuerpos desconocidos para encefalopatía de Hashimoto. También se removeríancomplejos autoinmunes, citoquinas y/u otros mediadores inflamatorios[62], siendo esto último lo que da la mejoría clínica al paciente. La cantidad de sesiones pueden variar entre tres a 10[36].
Pronóstico
La mayoría de los pacientes cursan con mejoría completa luego del inicio de la corticoterapia. Pero el riesgo de recaída puede llegar entre el 12,5 al 40% en el seguimiento a dos años[29]. Un 12,5% no responde a los esteroides, por lo que ameritan inmunosupresores[84]. La frecuencia de presentación de secuelas neurológicas en adultos no ha sido reportada. En niños fueron identificados déficits neurológicos persistentes en más del 20%, luego de un seguimiento de cuatro años[91].
Los casos clínicos revisados hacen pensar que probablemente esta enfermedad es subdiagnosticada. Por lo que es razonable sugerir que todo paciente con una encefalopatía inexplicable, particularmente en mujeres, debe pensarse en descartar la encefalopatía de Hashimoto. Por esta razón, es necesario solicitarles los anticuerpos antitiroideos.
En este contexto, hacen el diagnóstico la positividad de los referidos anticuerpos, un electroencefalograma con ondas lentas y foco de actividad que sugiera la presencia de foco epileptógeno, una resonancia magnética cerebral normal o con hallazgos de vasculitis o lesiones isquémicas difusas, así como una mejoría clínica a la inmunoterapia (corticoterapia, inmunoglobulinas o plasmaféresis).
Roles de autoría
IP: conceptualización, investigación, metodología, administración del proyecto, supervisión, visualización, escritura-revisión original, escritura revisión y edición.
JP: conceptualización, investigación, metodología, supervisión, escritura-revisión original, escritura revisión y edición.
Agradecimientos
Los autores agradecen la colaboración y excelente disposición del Dr. Jorge Benavides Vásquez, asistente de investigación, División de Endocrinología Pediátrica, Penn State College of Medicine, Hershey, Pennsylvania, Estados Unidos, por la traducción de la versión original al inglés.
Conflictos de intereses
Los autores han completado el formulario de declaración de conflictos de intereses del ICMJE, y declaran no haber recibido financiamiento para la realización del reporte; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado, en los últimos tres años; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. Los formularios pueden ser solicitados contactando a la autora responsable o a la dirección editorial de la Revista.
Financiamiento
Los autores declaran que no hubo fuentes de financiación externas.

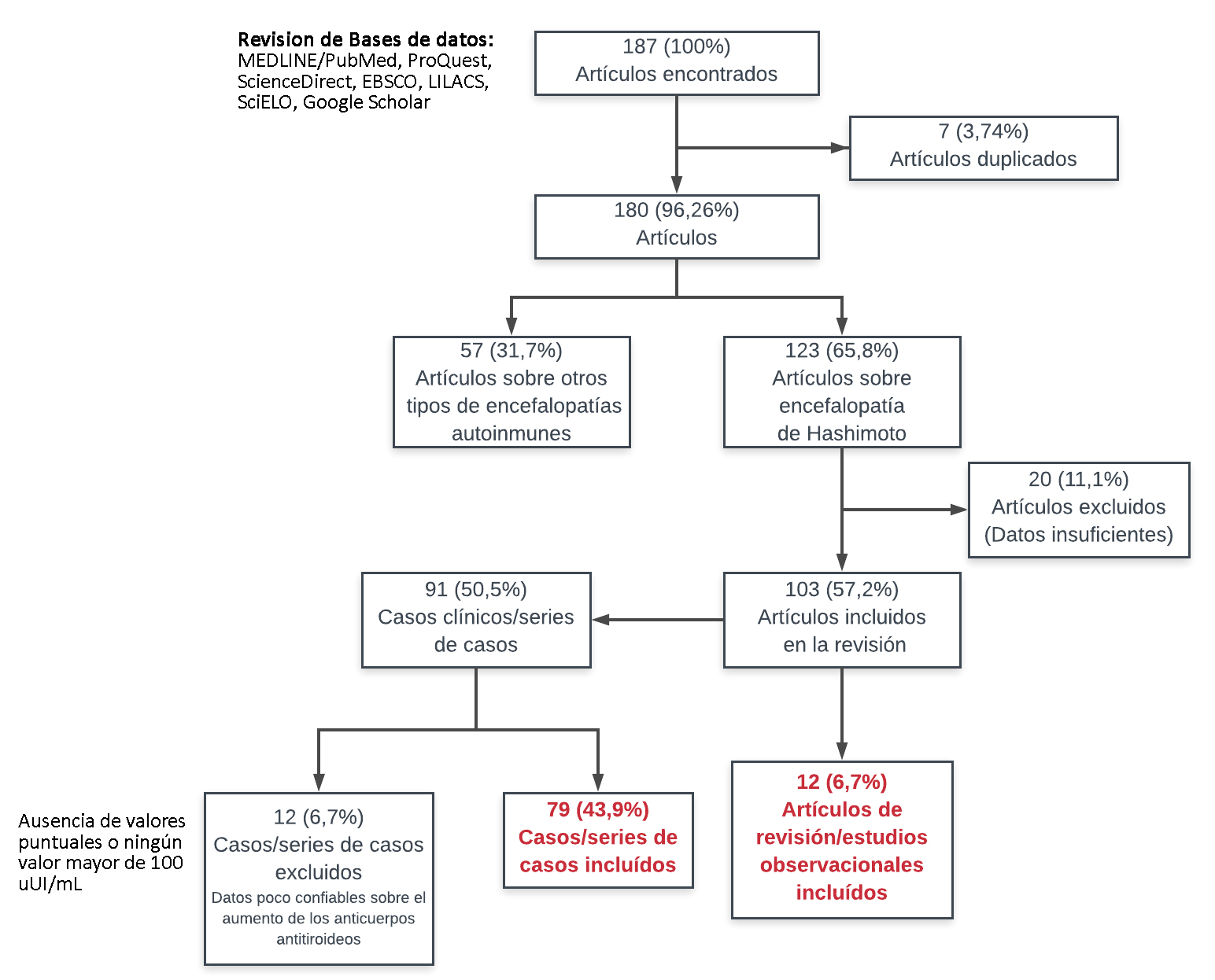 Figura 1. Flujo en la selección de artículos.
Figura 1. Flujo en la selección de artículos.

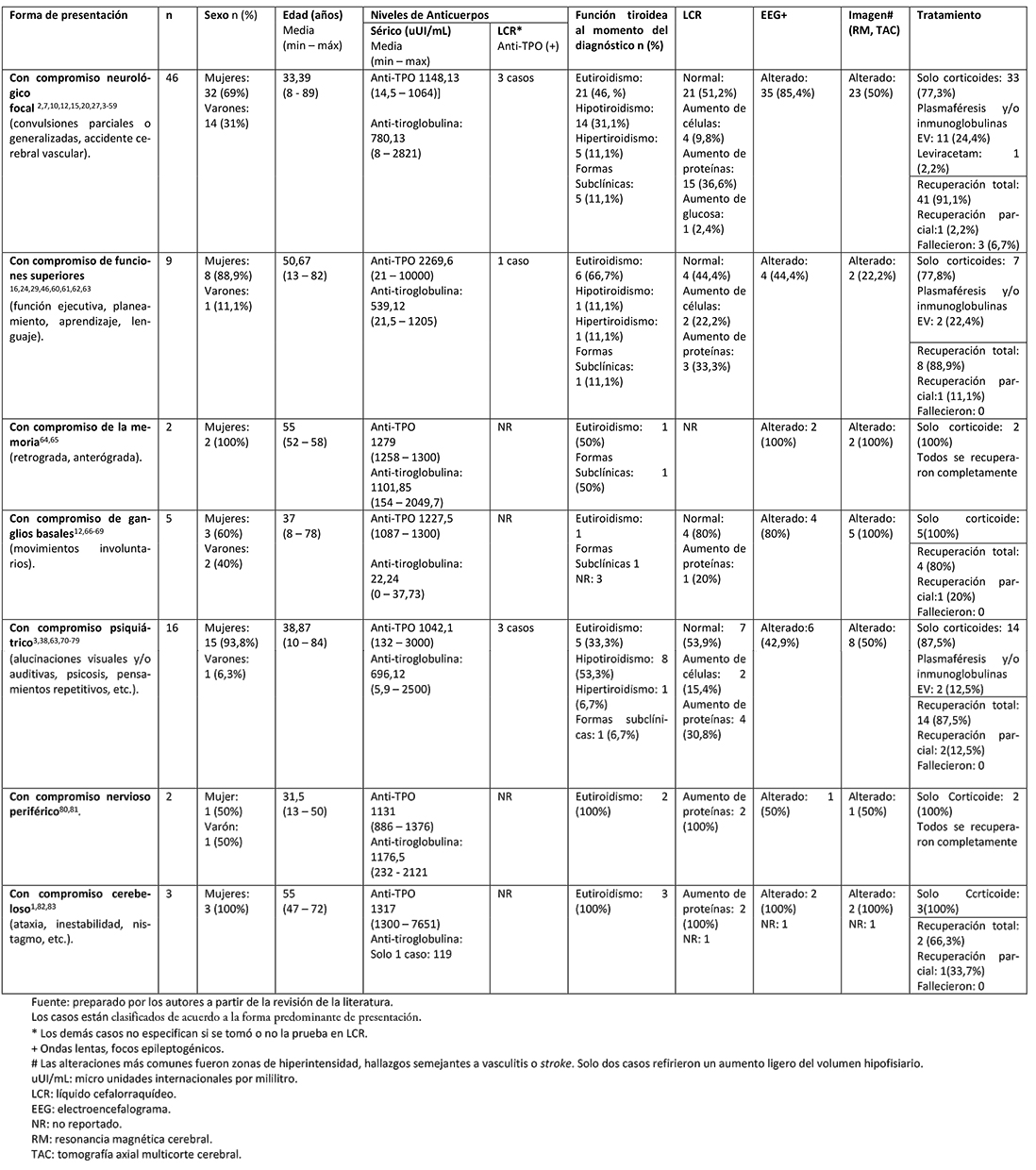 Tabla 1. Características clínicas, de laboratorio, imágenes y tratamiento de casos y series de casos publicados.
Tabla 1. Características clínicas, de laboratorio, imágenes y tratamiento de casos y series de casos publicados.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Hashimoto's encephalopathy is a rare disease, with a reported prevalence of 2.1 per 100 000. Clinical manifestations include confusion, decreased state of consciousness, cognitive deficit, seizures, myoclonus, ataxia, and focal neurological deficits. Due to the wide variety of signs and symptoms, clinical diagnostic suspicion is essential. Diagnosis is based on three pillars: the presence of neurological clinical manifestations after ruling out other causes of encephalopathy. 2) Presence of increased antithyroid antibodies. 3) Significant clinical improvement after the administration of immunomodulation. The treatment of Hashimoto's encephalopathy pursues two objectives: to control the autoimmune process and to control the complications of the disease. Although in most cases recovery is complete with treatment, the risk of relapse can range from 12.5 to 40% in follow-ups to 2 years.
 Autores:
Isabel Pinedo-Torres[1], José Luis Paz-Ibarra[2]
Autores:
Isabel Pinedo-Torres[1], José Luis Paz-Ibarra[2]

Citación: Pinedo-Torres I, Paz-Ibarra JL. Current knowledge on Hashimoto's encephalopathy: a literature review. Medwave 2018;18(6):e7298 doi: 10.5867/medwave.2018.06.7298
Fecha de envío: 4/7/2018
Fecha de aceptación: 21/9/2018
Fecha de publicación: 22/10/2018
Origen: no solicitado
Tipo de revisión: con revisión por cinco pares revisores externos, a doble ciego

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Álvarez Bravo G, Yusta Izquierdo A, Carvalho Monteiro G, Sánchez I. Cerebellopathy secondary to anti-peroxidase antibody-mediated toxicity. A special case of Hashimoto encephalopathy. J Neuroimmunol. 2017 Nov 15;312:1-3. | CrossRef | PubMed |
Álvarez Bravo G, Yusta Izquierdo A, Carvalho Monteiro G, Sánchez I. Cerebellopathy secondary to anti-peroxidase antibody-mediated toxicity. A special case of Hashimoto encephalopathy. J Neuroimmunol. 2017 Nov 15;312:1-3. | CrossRef | PubMed | Chen KA, Brilot F, Dale RC, Lafferty AR, Andrews PI. Hashimoto's encephalopathy and anti-MOG antibody encephalitis: 50 years after Lord Brain's description. Eur J Paediatr Neurol. 2017 Nov;21(6):898-901. | CrossRef | PubMed |
Chen KA, Brilot F, Dale RC, Lafferty AR, Andrews PI. Hashimoto's encephalopathy and anti-MOG antibody encephalitis: 50 years after Lord Brain's description. Eur J Paediatr Neurol. 2017 Nov;21(6):898-901. | CrossRef | PubMed | Bonnet U, Selle C, Kuhlmann R. Delirious Mania Associated with Autoimmune Gastrothyroidal Syndrome of a Mid-Life Female: The Role of Hashimoto Encephalopathy and a 3-Year Follow-Up including Serum Autoantibody Levels. Case Rep Psychiatry. 2016;2016:4168050. | CrossRef | PubMed |
Bonnet U, Selle C, Kuhlmann R. Delirious Mania Associated with Autoimmune Gastrothyroidal Syndrome of a Mid-Life Female: The Role of Hashimoto Encephalopathy and a 3-Year Follow-Up including Serum Autoantibody Levels. Case Rep Psychiatry. 2016;2016:4168050. | CrossRef | PubMed | Sharma PM, Javali M, Mahale R, Madhusudhan BK, Majeed AA, Srinivasa R. Hashimoto encephalopathy: A study of the clinical profile, radiological and electrophysiological correlation in a Tertiary Care Center in South India. J Neurosci Rural Pract. 2015 Jul-Sep;6(3):309-14. | CrossRef | PubMed |
Sharma PM, Javali M, Mahale R, Madhusudhan BK, Majeed AA, Srinivasa R. Hashimoto encephalopathy: A study of the clinical profile, radiological and electrophysiological correlation in a Tertiary Care Center in South India. J Neurosci Rural Pract. 2015 Jul-Sep;6(3):309-14. | CrossRef | PubMed | Yu HJ, Lee J, Seo DW, Lee M. Clinical manifestations and treatment response of steroid in pediatric Hashimoto encephalopathy. J Child Neurol. 2014 Jul;29(7):938-42.
| CrossRef | PubMed |
Yu HJ, Lee J, Seo DW, Lee M. Clinical manifestations and treatment response of steroid in pediatric Hashimoto encephalopathy. J Child Neurol. 2014 Jul;29(7):938-42.
| CrossRef | PubMed | Aleksic S, Oh H, Patel KG, Roy R, Raghuwanshi MP, Kaplan JM. An unusual patient with hashimoto thyroiditis, features of steroid-responsive encephalopathy associated with autoimmune thyroiditis, and concurrent minimal change renal disease. AACE Clinical Case Reports. 2017;3(4):299-302. | CrossRef |
Aleksic S, Oh H, Patel KG, Roy R, Raghuwanshi MP, Kaplan JM. An unusual patient with hashimoto thyroiditis, features of steroid-responsive encephalopathy associated with autoimmune thyroiditis, and concurrent minimal change renal disease. AACE Clinical Case Reports. 2017;3(4):299-302. | CrossRef | Yu HJ, Lee J, Seo DW, Lee M. Clinical manifestations and treatment response of steroid in pediatric hashimoto encephalopathy. J Child Neurol. 2014;29(7):938–42. | CrossRef |
Yu HJ, Lee J, Seo DW, Lee M. Clinical manifestations and treatment response of steroid in pediatric hashimoto encephalopathy. J Child Neurol. 2014;29(7):938–42. | CrossRef | Ergul AB, Altuner Torun Y, Altug U, Mutlu FT, Celik SF, Guven AS. Congenital Hemophilia A Presenting With Hashimoto's Encephalopathy and Myocarditis: The First Reported Case. J Pediatr Hematol Oncol. 2018 Oct;40(7):e435-e438. | CrossRef | PubMed |
Ergul AB, Altuner Torun Y, Altug U, Mutlu FT, Celik SF, Guven AS. Congenital Hemophilia A Presenting With Hashimoto's Encephalopathy and Myocarditis: The First Reported Case. J Pediatr Hematol Oncol. 2018 Oct;40(7):e435-e438. | CrossRef | PubMed | Lee J, Yu HJ, Lee J. Hashimoto encephalopathy in pediatric patients: Homogeneity in clinical presentation and heterogeneity in antibody titers. Brain Dev.2017;40(1):42-48. | CrossRef |
Lee J, Yu HJ, Lee J. Hashimoto encephalopathy in pediatric patients: Homogeneity in clinical presentation and heterogeneity in antibody titers. Brain Dev.2017;40(1):42-48. | CrossRef | Zhu Y, Yang H, Xiao F. Hashimoto's encephalopathy: a report of three cases and relevant literature reviews. Int J Clin Exp Med. 2015 Sep 15;8(9):16817-26. | PubMed |
Zhu Y, Yang H, Xiao F. Hashimoto's encephalopathy: a report of three cases and relevant literature reviews. Int J Clin Exp Med. 2015 Sep 15;8(9):16817-26. | PubMed | Singh D, Dyer A, Gu S, McCarville P, Hess A, Akingbola O, et al. An Unusual Cause of Frequent, Sudden, Transient, Unexplained Falls and New-Onset Status Epilepticus: Case Report and Mini-Review. Clin Pediatr (Phila). 2018 Feb;57(2):173-179. | CrossRef | PubMed |
Singh D, Dyer A, Gu S, McCarville P, Hess A, Akingbola O, et al. An Unusual Cause of Frequent, Sudden, Transient, Unexplained Falls and New-Onset Status Epilepticus: Case Report and Mini-Review. Clin Pediatr (Phila). 2018 Feb;57(2):173-179. | CrossRef | PubMed | Carolina Mendoza F.1 y Hernán García B. Encefalopatía respondedora a corticoide asociada a tiroiditis autoinmune (SREAT): una causa no habitual de compromiso de conciencia en pediatría, reporte de 2 casos. Rev Chil Endocrinol Diabetes. 2015;8(3):98-101. | Link |
Carolina Mendoza F.1 y Hernán García B. Encefalopatía respondedora a corticoide asociada a tiroiditis autoinmune (SREAT): una causa no habitual de compromiso de conciencia en pediatría, reporte de 2 casos. Rev Chil Endocrinol Diabetes. 2015;8(3):98-101. | Link | Fujii A, Yoneda M, Ito T, Yamamura O, Satomi S, Higa H, et al. Autoantibodies against the amino terminal of alpha-enolase are a useful diagnostic marker of Hashimoto's encephalopathy. J Neuroimmunol. 2005 May;162(1-2):130-6. | PubMed |
Fujii A, Yoneda M, Ito T, Yamamura O, Satomi S, Higa H, et al. Autoantibodies against the amino terminal of alpha-enolase are a useful diagnostic marker of Hashimoto's encephalopathy. J Neuroimmunol. 2005 May;162(1-2):130-6. | PubMed | Sapkota SK, Sapkota BL, Pitiyanuvath N. Hashimoto encephalopathy or neurosarcoidosis? A case report. Neurohospitalist. 2015 Apr;5(2):70-3. | CrossRef | PubMed |
Sapkota SK, Sapkota BL, Pitiyanuvath N. Hashimoto encephalopathy or neurosarcoidosis? A case report. Neurohospitalist. 2015 Apr;5(2):70-3. | CrossRef | PubMed | Gul Mert G, Horoz OO, Herguner MO, Incecik F, Yildizdas RD, Onenli Mungan N, et al. Hashimoto's encephalopathy: four cases and review of literature. Int J Neurosci. 2014 Apr;124(4):302-6. | CrossRef | PubMed |
Gul Mert G, Horoz OO, Herguner MO, Incecik F, Yildizdas RD, Onenli Mungan N, et al. Hashimoto's encephalopathy: four cases and review of literature. Int J Neurosci. 2014 Apr;124(4):302-6. | CrossRef | PubMed | Alazzeh A, Jaroudi S, Gooch M, Peiris AN. Focal neurological presentation in Hashimoto's encephalopathy mimicking a vascular occlusion of the middle cerebral artery. BMJ Case Rep. 2017 Jul 14;2017. pii: bcr-2017-219933. | CrossRef | PubMed |
Alazzeh A, Jaroudi S, Gooch M, Peiris AN. Focal neurological presentation in Hashimoto's encephalopathy mimicking a vascular occlusion of the middle cerebral artery. BMJ Case Rep. 2017 Jul 14;2017. pii: bcr-2017-219933. | CrossRef | PubMed | Laycock K, Chaudhuri A, Fuller C, Khatami Z, Nkonge F, Stojanovic N. A novel assessment and treatment approach to patients with Hashimoto's encephalopathy. Endocrinol Diabetes Metab Case Rep. 2018 Apr 27;2018. pii: 17-0117. | CrossRef | PubMed |
Laycock K, Chaudhuri A, Fuller C, Khatami Z, Nkonge F, Stojanovic N. A novel assessment and treatment approach to patients with Hashimoto's encephalopathy. Endocrinol Diabetes Metab Case Rep. 2018 Apr 27;2018. pii: 17-0117. | CrossRef | PubMed | Bhoi SK, Kalita J, Misra UK. Clinical spectrum of Hashimoto encephalopathy: report of 5 cases. Acta Neurol Belg. 2016 Mar;116(1):101-4. | CrossRef | PubMed |
Bhoi SK, Kalita J, Misra UK. Clinical spectrum of Hashimoto encephalopathy: report of 5 cases. Acta Neurol Belg. 2016 Mar;116(1):101-4. | CrossRef | PubMed | Barseem NF, Helwa MA. Hashimoto’s encephalopathy presenting with acute confusional state in a patient with hypothyroidism. Egypt Pediatr Assoc Gaz. 2015;63(2):69-73. | CrossRef |
Barseem NF, Helwa MA. Hashimoto’s encephalopathy presenting with acute confusional state in a patient with hypothyroidism. Egypt Pediatr Assoc Gaz. 2015;63(2):69-73. | CrossRef | Hilberath JM, Schmidt H, Wolf GK. Steroid-responsive encephalopathy associated with autoimmune thyroiditis (SREAT): case report of reversible coma and status epilepticus in an adolescent patient and review of the literature. Eur J Pediatr. 2014 Oct;173(10):1263-73. | CrossRef | PubMed |
Hilberath JM, Schmidt H, Wolf GK. Steroid-responsive encephalopathy associated with autoimmune thyroiditis (SREAT): case report of reversible coma and status epilepticus in an adolescent patient and review of the literature. Eur J Pediatr. 2014 Oct;173(10):1263-73. | CrossRef | PubMed | Georgiev D, Kojović M, Klanjšček G, Dolenc-Grošelj L. Hashimoto encephalopathy associated rapid onset narcolepsy type 1. Sleep Med. 2017 Jan;29:94-95. | CrossRef | PubMed |
Georgiev D, Kojović M, Klanjšček G, Dolenc-Grošelj L. Hashimoto encephalopathy associated rapid onset narcolepsy type 1. Sleep Med. 2017 Jan;29:94-95. | CrossRef | PubMed | Lalanne L, Meriot ME, Ruppert E, Zimmermann MA, Danion JM, Vidailhet P. Attempted infanticide and suicide inaugurating catatonia associated with Hashimoto's encephalopathy: a case report. BMC Psychiatry. 2016 Jan 19;16:13. | CrossRef | PubMed |
Lalanne L, Meriot ME, Ruppert E, Zimmermann MA, Danion JM, Vidailhet P. Attempted infanticide and suicide inaugurating catatonia associated with Hashimoto's encephalopathy: a case report. BMC Psychiatry. 2016 Jan 19;16:13. | CrossRef | PubMed | Haider AS, Alam M, Adetutu E, Thakur R, Gottlich C, DeBacker DL, et al. Autoimmune Schizophrenia? Psychiatric Manifestations of Hashimoto's Encephalitis. Cureus. 2016 Jul 5;8(7):e672. | CrossRef | PubMed |
Haider AS, Alam M, Adetutu E, Thakur R, Gottlich C, DeBacker DL, et al. Autoimmune Schizophrenia? Psychiatric Manifestations of Hashimoto's Encephalitis. Cureus. 2016 Jul 5;8(7):e672. | CrossRef | PubMed | Goh KK, Chiu YH, Shen WW. Hashimoto's encephalopathy mimicking presenile dementia. Gen Hosp Psychiatry. 2014 May-Jun;36(3):360.e9-11. | CrossRef | PubMed |
Goh KK, Chiu YH, Shen WW. Hashimoto's encephalopathy mimicking presenile dementia. Gen Hosp Psychiatry. 2014 May-Jun;36(3):360.e9-11. | CrossRef | PubMed | Chang Y, Kuo YH, Wu PC, Yeh YC, Chen HC. The misdiagnosis of steroid-responsive encephalopathy associated with autoimmune thyroiditis as masked depression in an elderly euthyroid woman. Psychosomatics. 2013 Nov-Dec;54(6):599-603. | CrossRef | PubMed |
Chang Y, Kuo YH, Wu PC, Yeh YC, Chen HC. The misdiagnosis of steroid-responsive encephalopathy associated with autoimmune thyroiditis as masked depression in an elderly euthyroid woman. Psychosomatics. 2013 Nov-Dec;54(6):599-603. | CrossRef | PubMed | Vivek AK, Arun AB, Menon V, Kandasamy P. Acute polymorphic psychosis as a presenting feature of Hashimoto's encephalopathy. Asian J Psychiatr. 2016 Feb;19:19-20. | CrossRef | PubMed |
Vivek AK, Arun AB, Menon V, Kandasamy P. Acute polymorphic psychosis as a presenting feature of Hashimoto's encephalopathy. Asian J Psychiatr. 2016 Feb;19:19-20. | CrossRef | PubMed | Huang X, Yu Y, Zhang H, Liu J, Sun Y, Chang M, Cui C. Hashimoto encephalopathy associated with hyperthyroidism: A case report. Exp Ther Med. 2014 Aug;8(2):515-518. | CrossRef |
Huang X, Yu Y, Zhang H, Liu J, Sun Y, Chang M, Cui C. Hashimoto encephalopathy associated with hyperthyroidism: A case report. Exp Ther Med. 2014 Aug;8(2):515-518. | CrossRef | Kim J, Shin H, Kang K, Kwon O, Park JM, Kim BK, Lee JJ. Hashimoto's encephalopathy: South Korean experiences. Acta Neurol Belg. 2014 Sep;114(3):209-16. | CrossRef | PubMed |
Kim J, Shin H, Kang K, Kwon O, Park JM, Kim BK, Lee JJ. Hashimoto's encephalopathy: South Korean experiences. Acta Neurol Belg. 2014 Sep;114(3):209-16. | CrossRef | PubMed | Gauthier AC, Baehring JM. Hashimoto’s encephalopathy mimicking Creutzfeldt-Jakob disease. J Clin Neurosci. 2017;35:72-3. | CrossRef |
Gauthier AC, Baehring JM. Hashimoto’s encephalopathy mimicking Creutzfeldt-Jakob disease. J Clin Neurosci. 2017;35:72-3. | CrossRef | Kishitani T, Matsunaga A, Ikawa M, Hayashi K, Yamamura O, Hamano T, et al. Limbic encephalitis associated with anti-NH2-terminal of α-enolase antibodies: A clinical subtype of Hashimoto encephalopathy. Medicine (Baltimore). 2017 Mar;96(10):e6181. | CrossRef | PubMed |
Kishitani T, Matsunaga A, Ikawa M, Hayashi K, Yamamura O, Hamano T, et al. Limbic encephalitis associated with anti-NH2-terminal of α-enolase antibodies: A clinical subtype of Hashimoto encephalopathy. Medicine (Baltimore). 2017 Mar;96(10):e6181. | CrossRef | PubMed | Zhu M, Yu X, Liu C, Duan C, Li C, Zhu J, Zhang Y. Hashimoto's encephalitis associated with AMPAR2 antibodies: a case report. BMC Neurol. 2017 Feb 21;1(1):37. | CrossRef | PubMed |
Zhu M, Yu X, Liu C, Duan C, Li C, Zhu J, Zhang Y. Hashimoto's encephalitis associated with AMPAR2 antibodies: a case report. BMC Neurol. 2017 Feb 21;1(1):37. | CrossRef | PubMed | Farrell RM, Foster MB, Omoruyi AO, Kingery SE, Wintergerst KA. Hashimoto's encephalopathy: a rare pediatric brain disease. J Pediatr Endocrinol Metab. 2015
May;28(5-6):721-4. | CrossRef | PubMed |
Farrell RM, Foster MB, Omoruyi AO, Kingery SE, Wintergerst KA. Hashimoto's encephalopathy: a rare pediatric brain disease. J Pediatr Endocrinol Metab. 2015
May;28(5-6):721-4. | CrossRef | PubMed | Chandrasekaram S, Mudenha E, Mendis B, Szabo A, Fernando D. Hashimoto’s Encephalopathy: An Unusual Cause of Autoimmune Encephalopathy in a Clinically and Biochemically Euthyroid Patient. European Journal of Case Reports in Internal Medicine 2014: 1(1) | CrossRef |
Chandrasekaram S, Mudenha E, Mendis B, Szabo A, Fernando D. Hashimoto’s Encephalopathy: An Unusual Cause of Autoimmune Encephalopathy in a Clinically and Biochemically Euthyroid Patient. European Journal of Case Reports in Internal Medicine 2014: 1(1) | CrossRef | Zhao W, Li J, Wang J, Guo Y, Tuo H, Kang Z, et al. A case of Hashimoto encephalopathy: clinical manifestation, imaging, pathology, treatment, and prognosis. Neurologist. 2011 May;17(3):141-3. | CrossRef | PubMed |
Zhao W, Li J, Wang J, Guo Y, Tuo H, Kang Z, et al. A case of Hashimoto encephalopathy: clinical manifestation, imaging, pathology, treatment, and prognosis. Neurologist. 2011 May;17(3):141-3. | CrossRef | PubMed | Cook MK, Malkin M, Karafin MS. The use of plasma exchange in Hashimoto's encephalopathy: A case report and review of the literature. J Clin Apher. 2015 Jun;30(3):188-92. | CrossRef | PubMed |
Cook MK, Malkin M, Karafin MS. The use of plasma exchange in Hashimoto's encephalopathy: A case report and review of the literature. J Clin Apher. 2015 Jun;30(3):188-92. | CrossRef | PubMed | Maydell BV, Kopp M, v Komorowski G, Joe A, Juengling FD, Korinthenberg R. Hashimoto encephalopathy - is it underdiagnosed in pediatric patients? Neuropediatrics. 2002 Apr;33(2):86-9. | PubMed |
Maydell BV, Kopp M, v Komorowski G, Joe A, Juengling FD, Korinthenberg R. Hashimoto encephalopathy - is it underdiagnosed in pediatric patients? Neuropediatrics. 2002 Apr;33(2):86-9. | PubMed | Chang JS, Chang TC. Hashimoto's encephalopathy: report of three cases. J Formos Med Assoc. 2014 Nov;113(11):862-6. | CrossRef | PubMed |
Chang JS, Chang TC. Hashimoto's encephalopathy: report of three cases. J Formos Med Assoc. 2014 Nov;113(11):862-6. | CrossRef | PubMed | Nelson SE, Jassam YN, Taylor LP. A case of refractory hashimoto’s encephalopathy demonstrating improvement with plasmapheresis. Case Reports Intern Med [Internet]. 2014;1(2):83-8.
| CrossRef |
Nelson SE, Jassam YN, Taylor LP. A case of refractory hashimoto’s encephalopathy demonstrating improvement with plasmapheresis. Case Reports Intern Med [Internet]. 2014;1(2):83-8.
| CrossRef | Duffey P, Yee S, Reid IN, Bridges LR. Hashimoto's encephalopathy: postmortem findings after fatal status epilepticus. Neurology. 2003 Oct 28;61(8):1124-6. | PubMed |
Duffey P, Yee S, Reid IN, Bridges LR. Hashimoto's encephalopathy: postmortem findings after fatal status epilepticus. Neurology. 2003 Oct 28;61(8):1124-6. | PubMed | Saygi S, Ozkale Y, Erol I. Tic disorder probably associated with steroid responsive encephalopathy with autoimmune thyroiditis (SREAT). Indian J Pediatr. 2014 Oct;81(10):1105-7. | CrossRef | PubMed |
Saygi S, Ozkale Y, Erol I. Tic disorder probably associated with steroid responsive encephalopathy with autoimmune thyroiditis (SREAT). Indian J Pediatr. 2014 Oct;81(10):1105-7. | CrossRef | PubMed | Wong LC, Freeburg JD, Montouris GD, Hohler AD. Two patients with Hashimoto's encephalopathy and uncontrolled diabetes successfully treated with levetiracetam. J Neurol Sci. 2015 Jan 15;348(1-2):251-2. | CrossRef | PubMed |
Wong LC, Freeburg JD, Montouris GD, Hohler AD. Two patients with Hashimoto's encephalopathy and uncontrolled diabetes successfully treated with levetiracetam. J Neurol Sci. 2015 Jan 15;348(1-2):251-2. | CrossRef | PubMed | Masuda H, Mori M, Ito S, Yagishita T, Kuwabara S. Steroid-Responsive Epilepsia Partialis Continua with Anti-Thyroid Antibodies: A Spectrum of Hashimoto's Encephalopathy? Case Rep Neurol. 2014 May 17;6(2):166-70. | CrossRef | PubMed |
Masuda H, Mori M, Ito S, Yagishita T, Kuwabara S. Steroid-Responsive Epilepsia Partialis Continua with Anti-Thyroid Antibodies: A Spectrum of Hashimoto's Encephalopathy? Case Rep Neurol. 2014 May 17;6(2):166-70. | CrossRef | PubMed | Tokareva YV, Kotov AS, Semenova EI, Eliseev YV, Romanova MV, Alakova MA, et al. Status of Acute Symptomatic Seizures in a Female Patient with Thyrotoxicosis: Hashimoto’s Encephalopathy. A Case Report. Hum Physiol. 2017;43(8):922-6. | CrossRef |
Tokareva YV, Kotov AS, Semenova EI, Eliseev YV, Romanova MV, Alakova MA, et al. Status of Acute Symptomatic Seizures in a Female Patient with Thyrotoxicosis: Hashimoto’s Encephalopathy. A Case Report. Hum Physiol. 2017;43(8):922-6. | CrossRef | Al-Busaidi M, Burad J, Al-Belushi A, Gujjar A. Super Refractory Status Epilepticus in Hashimoto's Encephalopathy. Oman Med J. 2017 May;32(3):247-250. | CrossRef | PubMed |
Al-Busaidi M, Burad J, Al-Belushi A, Gujjar A. Super Refractory Status Epilepticus in Hashimoto's Encephalopathy. Oman Med J. 2017 May;32(3):247-250. | CrossRef | PubMed | Dontje B, Van Santen HM, Niermeijer JM, Schonenberg-Meinema D, Van Trotsenburg ASP. Antithyroperoxidase Antibodies in Encephalopathy: Diagnostic Marker or Incidental Finding? J Pediatr Neurol. 2016;14(1):17-20. | CrossRef |
Dontje B, Van Santen HM, Niermeijer JM, Schonenberg-Meinema D, Van Trotsenburg ASP. Antithyroperoxidase Antibodies in Encephalopathy: Diagnostic Marker or Incidental Finding? J Pediatr Neurol. 2016;14(1):17-20. | CrossRef | Graham BR, Shiff N, Nour M, Hasal S, Huntsman R, Almubarak S. Hashimoto Encephalopathy Presenting With Stroke-Like Episodes in an Adolescent Female: A Case Report and Literature Review. Pediatr Neurol. 2016 Jun;59:62-70. | CrossRef | PubMed |
Graham BR, Shiff N, Nour M, Hasal S, Huntsman R, Almubarak S. Hashimoto Encephalopathy Presenting With Stroke-Like Episodes in an Adolescent Female: A Case Report and Literature Review. Pediatr Neurol. 2016 Jun;59:62-70. | CrossRef | PubMed | Sánchez Contreras A, Rojas SA, Manosalva A, Méndez Patarroyo PA, Lorenzana P, Restrepo JF, et al. Hashimoto encephalopathy (autoimmune encephalitis). J Clin Rheumatol. 2004 Dec;10(6):339-43. | PubMed |
Sánchez Contreras A, Rojas SA, Manosalva A, Méndez Patarroyo PA, Lorenzana P, Restrepo JF, et al. Hashimoto encephalopathy (autoimmune encephalitis). J Clin Rheumatol. 2004 Dec;10(6):339-43. | PubMed | Afshari M, Afshari ZS, Schuele SU. Pearls & oy-sters: Hashimoto encephalopathy. Neurology. 2012 May 29;78(22):e134-7. | CrossRef | PubMed |
Afshari M, Afshari ZS, Schuele SU. Pearls & oy-sters: Hashimoto encephalopathy. Neurology. 2012 May 29;78(22):e134-7. | CrossRef | PubMed | Gutch M, Bhattacharjee A, Kumar S, Pushkar D. Hashimoto's Encephalitis: Rare Manifestation of Hypothyroidism. Int J Appl Basic Med Res. 2017 Jul-Sep;7(3):193-195. | CrossRef | PubMed |
Gutch M, Bhattacharjee A, Kumar S, Pushkar D. Hashimoto's Encephalitis: Rare Manifestation of Hypothyroidism. Int J Appl Basic Med Res. 2017 Jul-Sep;7(3):193-195. | CrossRef | PubMed | Report C, Guardia CF, Bernat JL. Hashimoto’s Encephalopathy : Case Report and Literature Review. SOJ Neurol. 2014;1(1):1-2. | Link |
Report C, Guardia CF, Bernat JL. Hashimoto’s Encephalopathy : Case Report and Literature Review. SOJ Neurol. 2014;1(1):1-2. | Link | Montagna G, Imperiali M, Agazzi P, D'Aurizio F, Tozzoli R, Feldt-Rasmussen U, et al. Hashimoto's encephalopathy: A rare proteiform disorder. Autoimmun Rev. 2016 May;15(5):466-76. | CrossRef | PubMed |
Montagna G, Imperiali M, Agazzi P, D'Aurizio F, Tozzoli R, Feldt-Rasmussen U, et al. Hashimoto's encephalopathy: A rare proteiform disorder. Autoimmun Rev. 2016 May;15(5):466-76. | CrossRef | PubMed | Oz Tuncer G, Teber S, Kutluk MG, Albayrak P, Deda G. Hashimoto's encephalopathy presenting as pseudobulbar palsy. Childs Nerv Syst. 2018 Jun;34(6):1251-1254. | CrossRef | PubMed |
Oz Tuncer G, Teber S, Kutluk MG, Albayrak P, Deda G. Hashimoto's encephalopathy presenting as pseudobulbar palsy. Childs Nerv Syst. 2018 Jun;34(6):1251-1254. | CrossRef | PubMed | Hwang W, Jeong D. Hashimoto’s Encephalopathy with Reversible Diffuse Leukoencephalopathy. J Neurocrit Care. 2018;11(1):54-7. | CrossRef |
Hwang W, Jeong D. Hashimoto’s Encephalopathy with Reversible Diffuse Leukoencephalopathy. J Neurocrit Care. 2018;11(1):54-7. | CrossRef | Riangwiwat T, Sangtian J, Sriphrapradang C. Steroid-responsive encephalopathy: an under recognised aspect of Hashimoto's thyroiditis. BMJ Case Rep. 2015 Mar 12;2015. pii: bcr2014208969. | CrossRef | PubMed |
Riangwiwat T, Sangtian J, Sriphrapradang C. Steroid-responsive encephalopathy: an under recognised aspect of Hashimoto's thyroiditis. BMJ Case Rep. 2015 Mar 12;2015. pii: bcr2014208969. | CrossRef | PubMed | Gupta A, Shelton W, Singh R, Pandey A. Altered mental status: what is the diagnosis? Case Reports. BMJ Case Rep. 2015 Feb 12;2015. pii: bcr2014207533. | CrossRef | PubMed |
Gupta A, Shelton W, Singh R, Pandey A. Altered mental status: what is the diagnosis? Case Reports. BMJ Case Rep. 2015 Feb 12;2015. pii: bcr2014207533. | CrossRef | PubMed | Sato R, Takada T, Nasu M. Hashimoto Encephalopathy: A Case Report. Am J Med. 2016 Sep;129(9):e187. | CrossRef | PubMed |
Sato R, Takada T, Nasu M. Hashimoto Encephalopathy: A Case Report. Am J Med. 2016 Sep;129(9):e187. | CrossRef | PubMed | Varrasi C, Vecchio D, Magistrelli L, Strigaro G, Tassi L, Cantello R. Auditory seizures in autoimmune epilepsy: a case with anti-thyroid antibodies. Epileptic Disord. 2017 Mar 1;19(1):99-103. | CrossRef | PubMed |
Varrasi C, Vecchio D, Magistrelli L, Strigaro G, Tassi L, Cantello R. Auditory seizures in autoimmune epilepsy: a case with anti-thyroid antibodies. Epileptic Disord. 2017 Mar 1;19(1):99-103. | CrossRef | PubMed | Pari E, Rinaldi F, Premi E, Codella M, Rao R, Paghera B, et al. A follow-up ą⁸F-FDG brain PET study in a case of Hashimoto's encephalopathy causing drug-resistant status epilepticus treated with plasmapheresis. J Neurol. 2014 Apr;261(4):663-7. | CrossRef | PubMed |
Pari E, Rinaldi F, Premi E, Codella M, Rao R, Paghera B, et al. A follow-up ą⁸F-FDG brain PET study in a case of Hashimoto's encephalopathy causing drug-resistant status epilepticus treated with plasmapheresis. J Neurol. 2014 Apr;261(4):663-7. | CrossRef | PubMed | Wilcox RA, To T, Koukourou A, Frasca J. Hashimoto's encephalopathy masquerading as acute psychosis. J Clin Neurosci. 2008 Nov;15(11):1301-4. | CrossRef | PubMed |
Wilcox RA, To T, Koukourou A, Frasca J. Hashimoto's encephalopathy masquerading as acute psychosis. J Clin Neurosci. 2008 Nov;15(11):1301-4. | CrossRef | PubMed | Pathak LK, Vijayaraghavan V. Hashimoto ’s Encephalopathy : A Diagnosis in Disguise , Case Report and Review of Literature. J Med Cases. 2014;5(12):643-5. | CrossRef |
Pathak LK, Vijayaraghavan V. Hashimoto ’s Encephalopathy : A Diagnosis in Disguise , Case Report and Review of Literature. J Med Cases. 2014;5(12):643-5. | CrossRef | Endres D, Vry MS, Dykierek P, Riering AN, Lüngen E, Stich O, et al. Plasmapheresis Responsive Rapid Onset Dementia with Predominantly Frontal Dysfunction in the Context of Hashimoto's Encephalopathy. Front Psychiatry. 2017 Oct 26;8:212. | CrossRef | PubMed |
Endres D, Vry MS, Dykierek P, Riering AN, Lüngen E, Stich O, et al. Plasmapheresis Responsive Rapid Onset Dementia with Predominantly Frontal Dysfunction in the Context of Hashimoto's Encephalopathy. Front Psychiatry. 2017 Oct 26;8:212. | CrossRef | PubMed | Segers K, Braconnier P, Corazza F, Divano L, Mabrouk A, Robberecht J, et al. Subacute cognitive deterioration with high serum anti-thyroid peroxidase antibodies: two cases and a plea for pragmatism. Psychogeriatrics. 2013 Sep;13(3):175-9. | CrossRef | PubMed |
Segers K, Braconnier P, Corazza F, Divano L, Mabrouk A, Robberecht J, et al. Subacute cognitive deterioration with high serum anti-thyroid peroxidase antibodies: two cases and a plea for pragmatism. Psychogeriatrics. 2013 Sep;13(3):175-9. | CrossRef | PubMed | Nar Senol P, Bican Demir A, Bora I, Bakar M. Paroxysmal Amnesia Attacks due to Hashimoto's Encephalopathy. Case Rep Med. 2016;2016:1267192. | CrossRef | PubMed |
Nar Senol P, Bican Demir A, Bora I, Bakar M. Paroxysmal Amnesia Attacks due to Hashimoto's Encephalopathy. Case Rep Med. 2016;2016:1267192. | CrossRef | PubMed | Gutch M, Bhattacharjee A, Kumar S, Pushkar D. Hashimoto's Encephalitis: Rare Manifestation of Hypothyroidism. Int J Appl Basic Med Res. 2017 Jul-Sep;7(3):193-195. | CrossRef | PubMed |
Gutch M, Bhattacharjee A, Kumar S, Pushkar D. Hashimoto's Encephalitis: Rare Manifestation of Hypothyroidism. Int J Appl Basic Med Res. 2017 Jul-Sep;7(3):193-195. | CrossRef | PubMed | Philip R, Saran S, Gutch M, Gupta K. An unusual presentation of Hashimoto's encephalopathy. Indian J Endocrinol Metab. 2014 Jan;18(1):113-5. | CrossRef | PubMed |
Philip R, Saran S, Gutch M, Gupta K. An unusual presentation of Hashimoto's encephalopathy. Indian J Endocrinol Metab. 2014 Jan;18(1):113-5. | CrossRef | PubMed | Gutch M, Philip R, Saran S, Tungveersingh A. Steroid responsive myoclonus as a presentation of Hashimoto′s encephalopathy. Thyroid Res Pract. 2014;11(3):133-5. | CrossRef |
Gutch M, Philip R, Saran S, Tungveersingh A. Steroid responsive myoclonus as a presentation of Hashimoto′s encephalopathy. Thyroid Res Pract. 2014;11(3):133-5. | CrossRef | Kong FX, Lu QH, Guo ZK. Multiple intracranial lesions as the unusual imaging features of Hashimoto's encephalopathy: A case report. Medicine (Baltimore). 2018 May;97(21):e10814. | CrossRef | PubMed |
Kong FX, Lu QH, Guo ZK. Multiple intracranial lesions as the unusual imaging features of Hashimoto's encephalopathy: A case report. Medicine (Baltimore). 2018 May;97(21):e10814. | CrossRef | PubMed | Sharan A, Sengupta S, Mukhopadhyay S, Ghosh B. Hashimoto's Encephalopathy Presenting with Chorea. J Assoc Physicians India. 2015 Sep;63(9):83-4. | PubMed |
Sharan A, Sengupta S, Mukhopadhyay S, Ghosh B. Hashimoto's Encephalopathy Presenting with Chorea. J Assoc Physicians India. 2015 Sep;63(9):83-4. | PubMed | Endres D, Perlov E, Stich O, Tebartz van Elst L. Steroid responsive encephalopathy associated with autoimmune thyroiditis (SREAT) presenting as major depression. BMC Psychiatry. 2016 Jun 6;16:184. | CrossRef | PubMed |
Endres D, Perlov E, Stich O, Tebartz van Elst L. Steroid responsive encephalopathy associated with autoimmune thyroiditis (SREAT) presenting as major depression. BMC Psychiatry. 2016 Jun 6;16:184. | CrossRef | PubMed | Navin K, Kuppili PP, Bharadwaj B, Menon V. Is Depression with increased antithyroid autoantibodies a mere chance finding or Hashimoto's Encephalopathy? Asian J Psychiatr. 2018 Feb;32:112-113. | CrossRef | PubMed |
Navin K, Kuppili PP, Bharadwaj B, Menon V. Is Depression with increased antithyroid autoantibodies a mere chance finding or Hashimoto's Encephalopathy? Asian J Psychiatr. 2018 Feb;32:112-113. | CrossRef | PubMed | Kisabay A, Balikci K, Sari S, Selcuki D. Manifestation of Hashimoto’s encephalopathy with psychotic signs: a case presentation. Dasunem Adam J Psychiatry Neurol Sci. 2016;29(1):85-90. | CrossRef |
Kisabay A, Balikci K, Sari S, Selcuki D. Manifestation of Hashimoto’s encephalopathy with psychotic signs: a case presentation. Dasunem Adam J Psychiatry Neurol Sci. 2016;29(1):85-90. | CrossRef | Karthik MS, Nandhini K, Subashini V, Balakrishnan R. Hashimoto's Encephalopathy Presenting with Unusual Behavioural Disturbances in an Adolescent Girl. Case Rep Med. 2017;2017:3494310. | CrossRef | PubMed |
Karthik MS, Nandhini K, Subashini V, Balakrishnan R. Hashimoto's Encephalopathy Presenting with Unusual Behavioural Disturbances in an Adolescent Girl. Case Rep Med. 2017;2017:3494310. | CrossRef | PubMed | Brodtmann A. Hashimoto encephalopathy and Down syndrome. Arch Neurol. 2009 May;66(5):663-6. | CrossRef | PubMed |
Brodtmann A. Hashimoto encephalopathy and Down syndrome. Arch Neurol. 2009 May;66(5):663-6. | CrossRef | PubMed | Anandi VS, Bhattacharyya S, Banerjee B. Hashimoto's encephalopathy in a 10-year-old girl. Thyroid Res Pract 2017;14:89-91. | Link |
Anandi VS, Bhattacharyya S, Banerjee B. Hashimoto's encephalopathy in a 10-year-old girl. Thyroid Res Pract 2017;14:89-91. | Link | Ramdas Sarjerao Ransing, Kshirod Kumar Mishra 1 and Dipayan Sarkar. Neuropsychiatric Manifestation of Hashimoto’s Encephalopathy in an Adolescent and Treatment. Indian J Psychol Med. 2016;38(4):357-360. | CrossRef |
Ramdas Sarjerao Ransing, Kshirod Kumar Mishra 1 and Dipayan Sarkar. Neuropsychiatric Manifestation of Hashimoto’s Encephalopathy in an Adolescent and Treatment. Indian J Psychol Med. 2016;38(4):357-360. | CrossRef | Manappallil RG. Hashimoto’s Encephalopathy: Is it a Rare Condition or a Masquerading One ?
JCR.2015;5:490-493. | CrossRef |
Manappallil RG. Hashimoto’s Encephalopathy: Is it a Rare Condition or a Masquerading One ?
JCR.2015;5:490-493. | CrossRef | Shera IA, Vyas A, Bhat MS, Yousuf Q. Unusual case of Hashimoto's encephalopathy and pseudo-obstruction in a patient with undiagnosed hypothyroidism: a case report. J Med Case Rep. 2014 Sep 6;8:296. | CrossRef | PubMed |
Shera IA, Vyas A, Bhat MS, Yousuf Q. Unusual case of Hashimoto's encephalopathy and pseudo-obstruction in a patient with undiagnosed hypothyroidism: a case report. J Med Case Rep. 2014 Sep 6;8:296. | CrossRef | PubMed | Lee Y, House EM. Treatment of Steroid-Resistant Hashimoto Encephalopathy With Misidentification Delusions and Catatonia. Psychosomatics. 2017 May-Jun;58(3):322-327. | CrossRef | PubMed |
Lee Y, House EM. Treatment of Steroid-Resistant Hashimoto Encephalopathy With Misidentification Delusions and Catatonia. Psychosomatics. 2017 May-Jun;58(3):322-327. | CrossRef | PubMed | Report C, Mariotto S, Bonetti B, Donato F, Micheletti N, Zanoni T, et al. Ophthalmoparesis Mimicking Myasthenia Gravis as Acute Manifestation of Hashimoto ’ s Encephalopathy. J Mult Scler. 2015;2(2). | CrossRef |
Report C, Mariotto S, Bonetti B, Donato F, Micheletti N, Zanoni T, et al. Ophthalmoparesis Mimicking Myasthenia Gravis as Acute Manifestation of Hashimoto ’ s Encephalopathy. J Mult Scler. 2015;2(2). | CrossRef | Salpietro V, Mankad K, Polizzi A, Sugawara Y, Granata F, David E, et al. Pediatric Hashimoto's encephalopathy with peripheral nervous system involvement. Pediatr Int. 2014 Jun;56(3):413-6. | CrossRef | PubMed |
Salpietro V, Mankad K, Polizzi A, Sugawara Y, Granata F, David E, et al. Pediatric Hashimoto's encephalopathy with peripheral nervous system involvement. Pediatr Int. 2014 Jun;56(3):413-6. | CrossRef | PubMed | Zamora Elson M, Labarta Monzón L, Mallor Bonet T, Villacampa Clavér V, Avellanas Chavala M, Seron Arbeloa C. [Hashimoto's encephalitis, report of a case]. Med Intensiva. 2014 Nov;38(8):522-3. | CrossRef | PubMed |
Zamora Elson M, Labarta Monzón L, Mallor Bonet T, Villacampa Clavér V, Avellanas Chavala M, Seron Arbeloa C. [Hashimoto's encephalitis, report of a case]. Med Intensiva. 2014 Nov;38(8):522-3. | CrossRef | PubMed | Vikas Menon, Karthick Subramanian JST. Long-term plasma exchange as maintenance therapy for cerebellar-type Hashimoto’s encephalopathy, a case report. Transfus Apher Sci. 2018;57(3):418-20. | CrossRef |
Vikas Menon, Karthick Subramanian JST. Long-term plasma exchange as maintenance therapy for cerebellar-type Hashimoto’s encephalopathy, a case report. Transfus Apher Sci. 2018;57(3):418-20. | CrossRef | Zhou JY, Xu B, Lopes J, Blamoun J, Li L. Hashimoto encephalopathy: literature review. Acta Neurol Scand. 2017 Mar;135(3):285-290. | CrossRef | PubMed |
Zhou JY, Xu B, Lopes J, Blamoun J, Li L. Hashimoto encephalopathy: literature review. Acta Neurol Scand. 2017 Mar;135(3):285-290. | CrossRef | PubMed | Correia I, Marques IB, Ferreira R, Sousa L. Encephalopathy Associated with Autoimmune Thyroid Disease: A Potentially Reversible Condition. Case Rep Med. 2016;2016:9183979. | CrossRef | PubMed |
Correia I, Marques IB, Ferreira R, Sousa L. Encephalopathy Associated with Autoimmune Thyroid Disease: A Potentially Reversible Condition. Case Rep Med. 2016;2016:9183979. | CrossRef | PubMed | Ilias I, Karagiorga V, Paraskevas G, Bougea A, Bourbouli M, Pappa A, et al. Thyroid Autoantibodies in the Cerebrospinal Fluid of Subjects with and without Thyroid Disease: Implications for Hashimoto's Encephalopathy. J Thyroid Res. 2015;2015:819072. | CrossRef | PubMed |
Ilias I, Karagiorga V, Paraskevas G, Bougea A, Bourbouli M, Pappa A, et al. Thyroid Autoantibodies in the Cerebrospinal Fluid of Subjects with and without Thyroid Disease: Implications for Hashimoto's Encephalopathy. J Thyroid Res. 2015;2015:819072. | CrossRef | PubMed | Tomkins M, Cavalcoli F, Stanley E, O'Rourke K, Murphy S, Lynch T, Tamagno G. Autonomic alterations as a clinical manifestation of encephalopathy associated with autoimmune thyroid disease. Endocr J. 2018 Aug 27;65(8):869-875. | CrossRef | PubMed |
Tomkins M, Cavalcoli F, Stanley E, O'Rourke K, Murphy S, Lynch T, Tamagno G. Autonomic alterations as a clinical manifestation of encephalopathy associated with autoimmune thyroid disease. Endocr J. 2018 Aug 27;65(8):869-875. | CrossRef | PubMed | Cooper BL, et al. A young female with urinary retention – A case report of Hashimoto's Encephalopathy. American Journal of Emergency Medicine.2017;35(6):943.e1-943.e2. | CrossRef |
Cooper BL, et al. A young female with urinary retention – A case report of Hashimoto's Encephalopathy. American Journal of Emergency Medicine.2017;35(6):943.e1-943.e2. | CrossRef | Olmez I, Moses H, Sriram S, Kirshner H, Lagrange AH, Pawate S. Diagnostic and therapeutic aspects of Hashimoto's encephalopathy. J Neurol Sci. 2013 Aug 15;331(1-2):67-71. | CrossRef | PubMed |
Olmez I, Moses H, Sriram S, Kirshner H, Lagrange AH, Pawate S. Diagnostic and therapeutic aspects of Hashimoto's encephalopathy. J Neurol Sci. 2013 Aug 15;331(1-2):67-71. | CrossRef | PubMed |