 Para Descargar PDF debe Abrir sesiˇn.
Para Descargar PDF debe Abrir sesiˇn.
Palabras clave: fertility preservation, neoplasms, infertility, female
En los ˙ltimos a˝os, los avances mÚdicos han mejorado sustancialmente la sobrevida de los pacientes con cßncer, generando una mayor preocupaciˇn por la calidad de vida de los sobrevivientes. En particular, se ha prestado una creciente atenciˇn a los problemas reproductivos posteriores a los tratamientos oncolˇgicos. Las pautas internacionales sobre la preservaciˇn de la fertilidad en pacientes con cßncer, recomiendan que los equipos de salud debatan lo mßs pronto posible con todos los pacientes en edad reproductiva el impacto de la terapia sobre el sistema reproductor. TambiÚn insta a que se disponga y facilite el acceso oportuno a tÚcnicas de preservaciˇn de la fertilidad. El desarrollo de estas tÚcnicas en mujeres pre y post puberales son un esfuerzo reciente, y muchos pacientes y proveedores de la salud no estßn familiarizados con el rßpido avance en su investigaciˇn. En la presente revisiˇn se exponen las indicaciones, resultados y riesgos de las diferentes opciones disponibles en la actualidad.
Cada año, en el mundo se le diagnostica cáncer a más de 14 millones de personas y 8,2 millones fallecen por esta enfermedad [1]. Según la Organización Mundial de la Salud, más de la mitad de los diagnósticos y 65% de las muertes ocurre en los países en desarrollo [2]. En Chile cada año son diagnosticadas cerca de 40 mil personas con cáncer, constituyendo la segunda causa de muerte [3].
Uno de cada dos hombres y una de cada tres mujeres desarrollará cáncer en su vida. En Estados Unidos se diagnostica un cáncer cada 23 segundos y hay más de 10 millones de supervivientes de esta enfermedad, lo que supone aproximadamente 4% del total de la población de ese país [4]. La mayoría de las neoplasias aparecen en etapas avanzadas de la vida, sin embargo, 10% de estos casos ocurre en menores de 45 años de edad [5]. Los avances en la detección, diagnóstico y tratamiento del cáncer han elevado el índice de supervivencia, observándose en la última década una disminución de las tasas globales de mortalidad atribuibles al cáncer en mujeres de 1,6% por año [6]. Estudios estiman que cerca de 68% de los pacientes diagnosticados con cáncer están vivos a cinco años de tratamiento, y que para 2016 una de cada 21 personas fue una sobreviviente de algún cáncer [7],[8].
A medida que las tasas de curación y supervivencia aumentan, las consecuencias de los tratamientos cobran mayor relevancia. Una de las principales secuelas que surge como consecuencia de terapia oncológica es la pérdida parcial o definitiva de su capacidad reproductiva, impactando negativamente la salud y la calidad de vida de las mujeres. En vista de ello, existe un creciente interés entre los oncólogos y los especialistas en reproducción, por considerar la preservación de la fertilidad como un componente esencial en el enfoque integral del tratamiento del cáncer [9]. A pesar de lo anterior, la literatura científica sobre la materia es aún limitada, particularmente, para los hispanoparlantes. El presente artículo, describe y discute las opciones actuales para la preservación de la fertilidad en niñas y mujeres con cáncer, destacando los conocimientos vigentes sobre la seguridad, el acceso y el éxito de cada opción.
Se realizó una búsqueda de artículos en la base de datos de MEDLINE/PubMed. Se eligieron artículos indexados desde el año 1990 al año 2016. Se incluyeron artículos de revisión, ensayos clínicos y experimentales en modelos animales. Para la búsqueda se emplearon los términos MeSH: Fertility Preservation, Neoplasms e Infertility, Female. Se identificaron 176 artículos, correspondiendo 95 a revisiones de la literatura, cinco de ellos a metanálisis y dos ensayos clínicos controlados, a partir de los cuales se realizó una revisión narrativa o no sistemática. La información extraída de cada artículo fue incluida de acuerdo al consenso de los autores del manuscrito.
a. Foliculogénesis y el impacto de la radio y quimioterapia sobre la fertilidad
La ovogénesis comienza cuando las células germinales primordiales migran hacia la gónada embrionaria. El número máximo de ovocitos se alcanza a las 20 semanas de gestación, donde entre seis y siete millones de células germinales pueden ser identificadas en la gónada femenina. Desde entonces, se observa una pérdida progresiva de la reserva folicular por atresia, que termina en la menopausia [10].
La quimioterapia y la radioterapia afectan el número total de ovocitos, cuyo efecto secundario frecuente es la infertilidad, la insuficiencia ovárica primaria y/o la menopausia anticipada (Figura 1) [11]. Este efecto puede ser por daño directo sobre los ovocitos primordiales, los folículos en desarrollo, las células de la granulosa, el estroma y/o por daño vascular [12]. Dentro de los agentes quimioterapéuticos, la ciclofosfamida es el agente alquilante que causa el mayor daño a la reserva ovárica activando los folículos primordiales en un mecanismo que se ha descrito como de burnout [13]. Otros agentes como el cisplatino y la doxirubicina afectan directamente a los ovocitos y las células de la granulosa [14]. Por otro lado, la irradiación causa un daño permanente mediante la destrucción de los folículos pequeños y en desarrollo, junto con un daño acumulativo sobre el útero y vagina [15],[16]. Todo ello genera incapacidad o discapacidad para reproducirse, osteoporosis, enfermedad cardiovascular y/o trastornos psicosociales como la depresión, lo que repercute en la calidad de vida de la paciente [17],[18].
Figura 1. PÚrdida folicular normal y acelerada por la injuria gonadal.
El grado en que las noxas afectan la reserva ovárica depende de una serie de factores, incluyendo la edad de la paciente, los agentes gonadotóxicos utilizados, la dosis y la duración del tratamiento (Figura 1) [19].
Algunos agentes se asocian con mayor frecuencia con el daño gonadal (Tabla 1). La depleción folicular alcanza casi a > 80% de las mujeres que reciben agentes alquilantes en altas dosis (por ejemplo la ciclofosfamida), irradiación total del cuerpo antes del trasplante de células madre hematopoyéticas y/o irradiación directa de los ovarios; mientras que otras terapias han demostrado ser menos deletéreas [11], [20].
Se ha observado una amplia variabilidad en el impacto sobre la reserva ovárica para los diferentes agentes gonadotóxicos. Hasta la fecha, no existen herramientas precisas que permitan dar una adecuada consejería a los pacientes o familiares que se someten a un tratamiento de radio/quimioterapia. Más aún, cabe destacar que la reserva ovárica varía enormemente de una mujer a otra [21]. En ese contexto, el asesoramiento sobre las técnicas de preservación de fertilidad debe ser ofrecido a todas las niñas y mujeres antes de ser sometidas a agentes gonadotóxicos [6],[18],[22].
Tabla 1. Riesgo de falla ovßrica seg˙n tratamiento [23].
b. El rol del equipo multidisciplinario
El manejo clásico del paciente con cáncer está orientado a un rápido y oportuno acceso a los tratamientos, lo que ocasionalmente dificulta una adecuada consejería sobre las opciones para preservar la fertilidad. Más aún, en la mujer, el desarrollo de las técnicas de preservación de fertilidad es un esfuerzo reciente y muchas pacientes y proveedores de la salud no están familiarizados con el rápido avance en el desarrollo de las técnicas. Esto se traduce en una baja consejería y acceso a las técnicas disponibles hoy. En países desarrollados, entre 30 y 50% de las mujeres en edad reproductiva no reciben tales técnicas al iniciar radio o quimioterapia [24]. En Chile, en un estudio aún no publicado de 153 pacientes entre 19 y 35 años sometidas a quimioterapia en el hospital Carlos van Büren de Valparaíso entre los años 2011 y 2012, mostró que 26% de las pacientes recibió una consejería adecuada y sólo 9% fue derivada a un especialista en medicina reproductiva. Estas cifras contrastan con lo recomendado por la Sociedad Americana de Oncología Clínica (ASCO) y la Sociedad Europea de Oncología Médica (ESMO), quienes señalan que todos los pacientes debieran acceder a tratamientos de preservación de fertilidad previo al inicio de su tratamiento oncológico [18],[25].
La evaluación del riesgo de la fertilidad y la selección de una estrategia individualizada para optimizar la fertilidad después del tratamiento del cáncer, son enormes retos y requieren una intensa cooperación entre el equipo médico y las pacientes [20],[26]. En este contexto, los profesionales de la salud que tratan a pacientes jóvenes contra el cáncer o patologías benignas gonadotóxicas, deben ser conscientes de los efectos adversos del tratamiento sobre la fertilidad, de las estrategias para minimizar estos efectos y de las técnicas actualmente disponibles. Esto implica informar adecuadamente a las pacientes y sus familias, facilitar la oportuna referencia a un especialista en fertilidad y adaptar los tratamientos oncológicos a los requerimientos de las pacientes en relación a sus deseos reproductivos futuros.
Por su parte, los especialistas en fertilidad deben establecer tratamientos seguros, oportunos, asequibles y a un costo racional [22]. De igual modo, una vez superado el cáncer, el equipo de salud debe considerar la consejería, supervisión y ayuda reproductiva. Por último, se debe evaluar el mejor momento para concebir, considerando los deseos de las pacientes, el riesgo de recurrencia de la enfermedad, la sobrevida teórica y el daño potencial a la descendencia producto de enfermedades genéticas transmisibles o por la propia terapia oncológica [22]. El trabajo colaborativo y multidisciplinario aquí descrito se agrupa en una naciente disciplina llamada oncofertilidad [19],[26].
c. Estrategia de preservación de fertilidad
Las alternativas disponibles en la actualidad son elaboradas sobre evidencia médica del mejor nivel disponible, permiten recomendar diferentes métodos considerando la edad de la paciente, el tipo de cáncer, el tipo de tratamiento, la presencia de una pareja masculina, el tiempo disponible para antes del tratamiento gonadotóxico y la probabilidad de metástasis ovárica [18],[22] (Tabla 2 y Figura 2).
Tabla 2. Ventajas y desventajas de las estrategias de preservaciˇn de fertilidad.
1. Criopreservación de ovocitos o embriones: son técnicas establecidas, efectivas y probadas para preservar la capacidad reproductiva. Se consideran técnicas convencionales dentro de la medicina reproductiva [22]. Ambas incorporan un periodo de hiperestimulación ovárica controlada de 9 a 14 días, cuyo objetivo es aumentar el número de ovocitos para que una vez extraídos puedan ser criopreservados o inseminados, aumentando la probabilidad futura de lograr un embarazo. La dosificación y el protocolo seleccionado se determina considerando la reserva ovárica y la sensibilidad tumoral a las hormonas femeninas [9]. Aunque hay datos contradictorios, el diagnóstico del cáncer pareciera no afectar a la reserva ovárica o la capacidad de respuesta a las gonadotropinas antes de exponerse al tratamiento gonadotóxico [27],[28].
En condiciones que apremian el inicio del tratamiento oncológico, la implementación de nuevos protocolos permite el inicio de la estimulación sin esperar la menstruación de la paciente, reduciendo el periodo de latencia desde la derivación a la recolección de los ovocitos de cuatro a dos semanas [29],[30]. Más aún, una precoz derivación sumada a la aplicación de tales protocolos ha demostrado no modificar el inicio de la quimioterapia e incluso proporcionar la oportunidad de más de un ciclo de criopreservación [31],[32],[33].
Otras modificaciones a los protocolos de estimulación han permitido reducir los niveles suprafisiológicos de esteroides sexuales observados en la estimulación convencional, aumentando la seguridad teórica de la técnica en pacientes con cáncer hormonodependientes, sin comprometer los resultados observados [34]. Estudios prospectivos con estos protocolos han demostrado, con un seguimiento de hasta cinco años, que las tasas de recurrencia y supervivencia al cáncer son similares a quienes no recibieron tratamiento de preservación de fertilidad [35],[36].
Durante décadas, la criopreservación de embriones fue el único método de preservación de fertilidad considerado no experimental por la Sociedad Americana de Reproducción (ASRM) [22]. Su seguridad y eficacia se extrapola de los tratamientos convencionales de reproducción asistida, donde se reportan miles de nacidos cada año a partir de embriones congelados. Los embriones humanos son altamente resistentes al daño por congelación, con una tasa de supervivencia e implantación de más de 90 y 30% respectivamente [9],[37]. No obstante, la criopreservación de ovocitos se considera una mejor opción, al ser aplicable en mujeres jóvenes o adolescentes, mujeres sin pareja o para quienes desean una mayor flexibilidad reproductiva. De igual modo, es de elección en quienes tienen una preocupación ética o religiosa relacionada con la disposición futura del embrión [9].
Durante la última década, se han observado importantes avances en las técnicas de vitrificación que minimizan el daño a la estructura celular por la formación de cristales de agua observado con las técnicas de congelación lenta [38]. La creciente experiencia y los avances logrados en la criopreservación permiten que los resultados reproductivos con ovocitos criopreservados/descongelados sean comparables con las tasas de ovocitos frescos sometidos a técnicas de reproducción asistida [39],[40]. En consecuencia, desde el año 2013 que esta técnica se considera estándar por las sociedades Americana y Europea de Reproducción [41],[42]. Las tasas estimadas de embarazo, una vez descongelados los ovocitos, varía según el número de gametos criopreservados y la edad de la paciente, de tal modo que cada ovocito aporta una tasa de embarazo entre 4 y 8%, reportándose tasas de embarazo promedio entre 30 y 50% [43],[44]. Existen herramientas digitales que entregan tasas de embarazo según las principales variables relacionadas (http://fertilitypreservation.org/advanced-treatments/fertility-preservation)
La criopreservación de ovocitos/embriones se desaconseja una vez iniciada la quimioterapia, debido a que la respuesta del ovario a la estimulación y la calidad de los ovocitos recuperados disminuyen tras el inicio de la quimioterapia [45]. Es conocido que la quimioterapia induce a la ruptura del ADN en los ovocitos humanos, haciendo recomendable esperar al menos seis meses antes de intentar concebir [45].
2. Criopreservación de tejido ovárico: es la única opción para preservación de la fertilidad disponible en niñas prepúberes y para mujeres que no pueden retrasar el inicio de la quimioterapia [6].
Se basa en el principio que la corteza ovárica es el reservorio de los folículos primordiales, por tanto su remoción quirúrgica, la criopreservación y posterior reimplante, permite la preservación de la función reproductiva y hormonal de las pacientes sometidas a la técnica. Desde el primer nacimiento reportado con esta técnica por Donnez en el año 2004 [46], la criopreservación de tejido ovárico se ha convertido en una técnica cada vez más utilizada para la preservación de fertilidad, reportando a la fecha al menos 60 niños nacidos vivos [47]. En Europa se realizan entre 2500 y 6500 extracciones de corteza por año [48], y su tasa de éxito reportada es de 29% por paciente reimplantada, lo que ha impulsado a líderes de opinión a considerar esta técnica no experimental [49].
En las pacientes auto-trasplantadas, se ha reportado la restauración de la actividad ovárica en el 100% de ellas, con una duración media de la función ovárica de cinco años en los casos con alta densidad folicular [47]. La seguridad de la técnica sobre la descendencia se ha demostrado en series de casos con nacidos vivos sin defectos congénitos [50]. No obstante estos avances, su uso es aún restringido al ser un procedimiento invasivo y con relativamente pocos centros médicos con experiencia en esta técnica. Los principales desafíos de la técnica incluyen el daño al tejido por isquemia, la posterior revascularización y la posibilidad teórica de la reintroducción de las células tumorales malignas [22].
Se han desarrollado guías para la correcta selección de las pacientes tributarias a esta técnica, restringiendo su uso a niñas prepúberes y mujeres:
a. Menores de 35 o 39 años.
b. Sin tratamiento gonadotóxico previo.
c. Con una oportunidad realista de supervivencia a cinco años.
d. Con riesgo de pérdida de la capacidad de reproducción por tratamiento oncológico superior al 50%.
e. Con bajo o sin riesgo de reintroducir células malignas con el reimplante.
f. Con serología negativa para infecciones de transmisión sexual.
g. Con el consentimiento informado de los padres o representantes legales [51],[52].
3. Protección de la función ovárica nativa: existen técnicas de menor efectividad que pueden ser utilizadas en forma complementaria con las ya desarrolladas. Estás técnicas se pueden diferenciar según el tipo de gonadotóxico utilizado:
i. Radioterapia. La transposición de ovario es una técnica quirúrgica en que los ovarios se mueven para distanciarse del campo de radiación. Se utiliza frecuentemente cuando se indica radiación pélvica, tal como para el cáncer cervical o de vagina. Involucra la movilización del pedículo vascular y la fijación del ovario fuera de la pelvis. La ubicación exacta para la transposición depende del tratamiento planificado y la anatomía de la paciente [9],[53]. Los resultados de la técnica son inconsistentes (entre 16 y 90% de éxito) [11], demostrándose que los ovarios reciben hasta 15% de la dosis total pélvica [15]. La técnica se asocia a complicaciones y requiere del reposicionamiento de los ovarios en la pelvis post radioterapia, a fin de facilitar el embarazo espontáneo [11]. Para mejorar las posibilidades de embarazo, se ha postulado un abordaje combinado, criopreservando la corteza de un ovario y realizando la transposición del contralateral en el mismo acto quirúrgico [54].
ii. Quimioterapia. Recientemente se ha utilizado la hormona liberadora de gonadotropina (GnRH) en forma previa o durante la quimioterapia, como una forma de reducir los efectos gonadotóxicos del tratamiento del cáncer. Los agonistas de hormona liberadora de gonadotropina bloquean la actividad del eje hipotálamo-hipofisario-gonadal, suprimiendo los niveles de gonadotropina a niveles prepuberales. A pesar de que algunos estudios recientes han demostrado cierto grado de protección gonadal mediante la medición de resultado intermedios como la tasa de amenorrea, las medidas del efecto no han tenido impacto sobre el test de reserva ovárica fidedignos como la hormona antimülleriana (AMH) o el conteo de folículos antrales, ni han demostrado mejorar las tasas de embarazo [55],[56],[57],[58]. El comité de la Sociedad Americana de Reproducción, la Sociedad Americana de Oncología Clínica y numerosos autores, desaconsejan el uso de análogos de la hormona liberadora de gonadotropina como protección gonadal en pacientes con cáncer. Su uso debe considerarse sólo como una alternativa complementaria a tratamientos con efectos reproductivos probados [18], [22],[49].
d. Otras técnicas emergentes:
i. Criopreservación de ovocitos tras maduración in vitro. En cualquier etapa del ciclo menstrual se puede observar una cohorte de folículos antrales pequeños [10]. Estos folículos se pueden recuperar a través de una aspiración transvaginal, en un ciclo natural o tras una breve estimulación ovárica para ser congelados¸ habitualmente después de la maduración in vitro [19]. De esta manera, esta técnica es una opción para las mujeres que no tienen suficiente tiempo o presentan una contraindicación para completar un ciclo de estimulación ovárica. A pesar de que más de 2000 niños han nacido gracias al uso de ovocitos frescos madurados in vitro, muy pocos nacidos vivos han sido reportados con el uso de ovocitos criopreservados tras la maduración in vitro [19],[59],[60]. La maduración in vitro de ovocitos se encuentra en fase experimental y todavía necesita un mayor desarrollo antes de poder ofrecerse como una técnica convencional [22].
ii. Cultivo de folículos preantrales in vitro. Los folículos primordiales corresponden al reservorio de ovocitos en el ovario. Su desarrollo demora entre dos y tres ciclos menstruales [10],[61], por lo que su cultivo in vitro representa un desafío biotecnológico mayor [19],[62],[63]. A partir de folículos obtenidos de tejido ovárico humano y animal, se han desarrollado diversos métodos para el crecimiento in vitro de folículos. Su objetivo es reanudar la función ovárica reproductiva, junto con evitar el riesgo de reintroducir células malignas [62],[64]. Hasta la fecha, los avances en el cultivo y trasplante de folículos humanos han permitido el desarrollo de folículos pequeños y preantrales, sin embargo, no ha resultado en nacidos vivos [64]. Esta técnica se encuentra en fase experimental, aunque constituye una alternativa prometedora al reimplante de tejido ovárico, al evitar el riesgo de reintroducción de células malignas [60].
Los recientes avances en los tratamientos oncológicos permiten una alta sobrevida de las niñas y mujeres jóvenes afectadas por enfermedades malignas. Sin embargo, tales terapias deterioran la función gonadal y secundariamente la fertilidad futura de estas pacientes, constituyendo un problema emergente de salud.
Actualmente, existen tratamientos de preservación de fertilidad eficientes para los diferentes escenarios clínicos posibles, dando a las pacientes con cáncer la oportunidad de un embarazo exitoso cuando hayan superado su enfermedad. A pesar de tales avances, sólo una pequeña fracción de pacientes expuestos a tratamientos gonadotóxicos es referida a especialistas para recibir tratamientos oportunos y efectivos. La falta de conocimiento, la baja disponibilidad y cobertura por las aseguradoras son barreras importantes a superar antes de ver cambios significativos en la materia.
De igual forma, la conformación de equipos multidisciplinarios que incorporen la visión oncológica, reproductiva, apoyo psicosocial adecuado y las preferencias de los pacientes, son fundamentales para atender las necesidades de quienes se enfrentan a tratamientos gonadotóxicos.
El impulso y los recientes avances en la oncofertilidad presentan dificultades. No obstante, su progresiva implementación es una necesidad real, y una obligación moral y legal para los centros de derivación oncológicos. En el futuro próximo, los requerimientos de tratamientos de preservación de fertilidad por razones médicas y sociales serán crecientes. En este contexto, el trabajo colaborativo entre los profesionales de la salud, las pacientes y las autoridades será vital para poder dar respuesta a este desafío.
Declaración de conflictos de intereses
Los autores han completado el formulario de declaración de conflictos intereses del ICMJE traducido al castellano por Medwave, y declaran no haber recibido financiamiento para la realización del reporte; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado, en los últimos tres años; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. Los formularios pueden ser solicitados contactando al autor responsable o a la dirección editorial de la Revista.
Financiamiento
Los autores declaran que recibieron apoyo financiero del Programa de Mejoramiento Institucional PMI-UVA 1402.

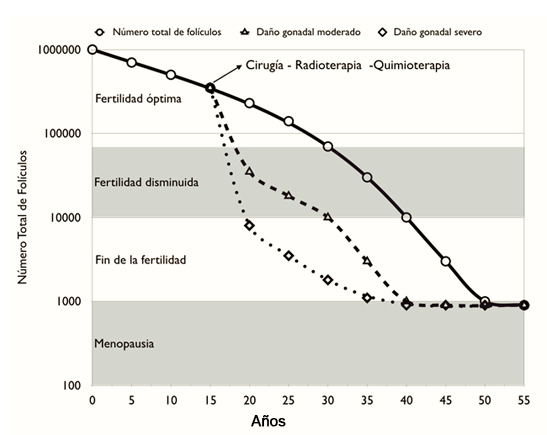 Figura 1. PÚrdida folicular normal y acelerada por la injuria gonadal.
Figura 1. PÚrdida folicular normal y acelerada por la injuria gonadal.

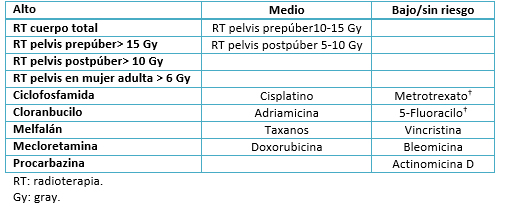 Tabla 1. Riesgo de falla ovßrica seg˙n tratamiento [23].
Tabla 1. Riesgo de falla ovßrica seg˙n tratamiento [23].

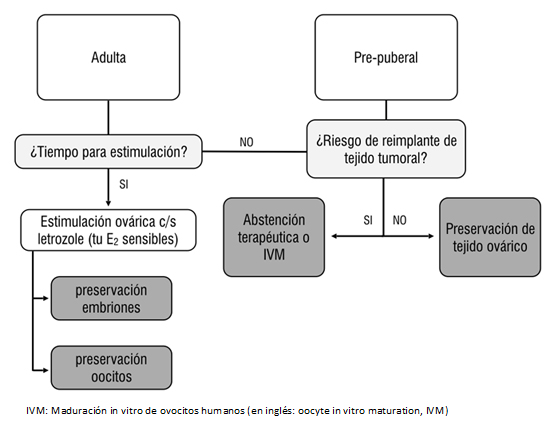 Figura 2. Opciones para preservaciˇn de la fertilidad en mujeres en riesgo de pÚrdida de funciˇn reproductiva.
Figura 2. Opciones para preservaciˇn de la fertilidad en mujeres en riesgo de pÚrdida de funciˇn reproductiva.

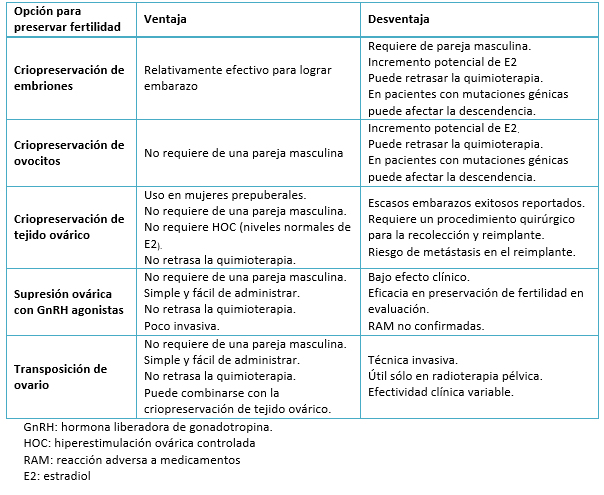 Tabla 2. Ventajas y desventajas de las estrategias de preservaciˇn de fertilidad.
Tabla 2. Ventajas y desventajas de las estrategias de preservaciˇn de fertilidad.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuciˇn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciˇn y reproducciˇn del artÝculo en cualquier medio, siempre y cuando se otorgue el crÚdito correspondiente al autor del artÝculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuciˇn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciˇn y reproducciˇn del artÝculo en cualquier medio, siempre y cuando se otorgue el crÚdito correspondiente al autor del artÝculo y al medio en que se publica, en este caso, Medwave.

In recent years, medical advances have substantially improved survival of cancer patients, generating growing concern about the quality of life of the survivors. Increased attention has been paid to reproductive problems after oncological treatments. International guidelines on fertility preservation in cancer patients require that healthcare teams discuss, as early as possible, the impact of cancer treatments on fertility and encourage access to fertility preservation techniques. The development of these techniques in women is a recent effort and many patients and health care providers are not familiar with their rapid expansion. This article discusses indications, results, and risks of the different options currently available.
 Autores:
Anibal Scarella Chamy[1,2], CÚsar DÝaz-GarcÝa[3,4,5], Sonia Herraiz [3,6], Jhenifer Kliemchen Rodrigues[7,8,9]
Autores:
Anibal Scarella Chamy[1,2], CÚsar DÝaz-GarcÝa[3,4,5], Sonia Herraiz [3,6], Jhenifer Kliemchen Rodrigues[7,8,9]

Citaciˇn: Scarella Chamy A, DÝaz-GarcÝa C, Herraiz S, Kliemchen Rodrigues J. Fertility preservation in the oncology patient. Medwave 2017 Nov-Dic;17(9):e7090 doi: 10.5867/medwave.2017.09.7090
Fecha de envÝo: 23/6/2017
Fecha de aceptaciˇn: 19/10/2017
Fecha de publicaciˇn: 16/11/2017
Origen: no solicitado
Tipo de revisiˇn: con revisiˇn por dos pares revisores externos, a doble ciego

Nos complace que usted tenga interÚs en comentar uno de nuestros artÝculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcciˇn editorial considera que su comentario es: ofensivo en alg˙n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polÝticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisiˇn por pares.
A˙n no hay comentarios en este artÝculo.
Para comentar debe iniciar sesiˇn
 Medwave publica las vistas HTML y descargas PDF por artÝculo, junto con otras mÚtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artÝculo, junto con otras mÚtricas de redes sociales.
 Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer J Clin. 2011 Mar-Apr;61(2):69-90. | CrossRef | PubMed |
Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer J Clin. 2011 Mar-Apr;61(2):69-90. | CrossRef | PubMed | DÝaz Sanzana N, JofrÚ Salazar AM, Moya CortÚs J, Uma˝a Cid ME, Vallebuona Stagno C, Vicu˝a Pruzzo P. Informe RPC Chile 2003-2007. Santiago, Chile: MINSAL; 2012.
DÝaz Sanzana N, JofrÚ Salazar AM, Moya CortÚs J, Uma˝a Cid ME, Vallebuona Stagno C, Vicu˝a Pruzzo P. Informe RPC Chile 2003-2007. Santiago, Chile: MINSAL; 2012.  Hayat MJ, Howlader N, Reichman ME, Edwards BK. Cancer statistics, trends, and multiple primary cancer analyses from the Surveillance, Epidemiology, and End Results (SEER) Program. Oncologist. 2007 Jan;12(1):20-37. | PubMed |
Hayat MJ, Howlader N, Reichman ME, Edwards BK. Cancer statistics, trends, and multiple primary cancer analyses from the Surveillance, Epidemiology, and End Results (SEER) Program. Oncologist. 2007 Jan;12(1):20-37. | PubMed | Siegel R, Naishadham D, Jemal A. Cancer statistics for Hispanics/Latinos, 2012. CA Cancer J Clin. 2012 Sep-Oct;62(5):283-98. | CrossRef | PubMed |
Siegel R, Naishadham D, Jemal A. Cancer statistics for Hispanics/Latinos, 2012. CA Cancer J Clin. 2012 Sep-Oct;62(5):283-98. | CrossRef | PubMed | Donnez J, Dolmans MM. Fertility preservation in women. Nat Rev Endocrinol. 2013 Dec;9(12):735-49. | CrossRef | PubMed |
Donnez J, Dolmans MM. Fertility preservation in women. Nat Rev Endocrinol. 2013 Dec;9(12):735-49. | CrossRef | PubMed | Hickey M, Peate M, Saunders CM, Friedlander M. Breast cancer in young women and its impact on reproductive function. Hum Reprod Update. 2009 May-Jun;15(3):323-39. | CrossRef | PubMed |
Hickey M, Peate M, Saunders CM, Friedlander M. Breast cancer in young women and its impact on reproductive function. Hum Reprod Update. 2009 May-Jun;15(3):323-39. | CrossRef | PubMed | Siegel RL, Miller KD, Jemal A. Cancer statistics, 2016. CA Cancer J Clin. 2016 Jan-Feb;66(1):7-30. | CrossRef | PubMed |
Siegel RL, Miller KD, Jemal A. Cancer statistics, 2016. CA Cancer J Clin. 2016 Jan-Feb;66(1):7-30. | CrossRef | PubMed | McLaren JF, Bates GW. Fertility preservation in women of reproductive age with cancer. Am J Obstet Gynecol. 2012 Dec;207(6):455-62. | CrossRef | PubMed |
McLaren JF, Bates GW. Fertility preservation in women of reproductive age with cancer. Am J Obstet Gynecol. 2012 Dec;207(6):455-62. | CrossRef | PubMed | Strauss J, Williams C. The ovarian life cycle. .en: Yen and Jaffeĺs reproductive endocrinology: physiology, pathophysiology, and clinical management. Philadelphia, PA: Elsevier; 2004.
Strauss J, Williams C. The ovarian life cycle. .en: Yen and Jaffeĺs reproductive endocrinology: physiology, pathophysiology, and clinical management. Philadelphia, PA: Elsevier; 2004.  Sonmezer M, Oktay K. Fertility preservation in female patients. Hum Reprod Update. 2004 May-Jun;10(3):251-66. | PubMed |
Sonmezer M, Oktay K. Fertility preservation in female patients. Hum Reprod Update. 2004 May-Jun;10(3):251-66. | PubMed | Morgan S, Anderson RA, Gourley C, Wallace WH, Spears N. How do chemotherapeutic agents damage the ovary? Hum Reprod Update. 2012 Sep-Oct;18(5):525-35. | CrossRef | PubMed |
Morgan S, Anderson RA, Gourley C, Wallace WH, Spears N. How do chemotherapeutic agents damage the ovary? Hum Reprod Update. 2012 Sep-Oct;18(5):525-35. | CrossRef | PubMed | Roness H, Gavish Z, Cohen Y, Meirow D. Ovarian follicle burnout: a universal phenomenon? Cell Cycle. 2013 Oct 15;12(20):3245-6. | CrossRef | PubMed |
Roness H, Gavish Z, Cohen Y, Meirow D. Ovarian follicle burnout: a universal phenomenon? Cell Cycle. 2013 Oct 15;12(20):3245-6. | CrossRef | PubMed | Morgan S, Lopes F, Gourley C, Anderson RA, Spears N. Cisplatin and doxorubicin induce distinct mechanisms of ovarian follicle loss; imatinib provides selective protection only against cisplatin. PLoS One. 2013 Jul 29;8(7):e70117. | CrossRef | PubMed |
Morgan S, Lopes F, Gourley C, Anderson RA, Spears N. Cisplatin and doxorubicin induce distinct mechanisms of ovarian follicle loss; imatinib provides selective protection only against cisplatin. PLoS One. 2013 Jul 29;8(7):e70117. | CrossRef | PubMed | Le Floch O, Donaldson SS, Kaplan HS. Pregnancy following oophoropexy and total nodal irradiation in women with Hodgkin's disease. Cancer. 1976 Dec;38(6):2263-8. | PubMed |
Le Floch O, Donaldson SS, Kaplan HS. Pregnancy following oophoropexy and total nodal irradiation in women with Hodgkin's disease. Cancer. 1976 Dec;38(6):2263-8. | PubMed | Bath LE, Critchley HO, Chambers SE, Anderson RA, Kelnar CJ, Wallace WH. Ovarian and uterine characteristics after total body irradiation in childhood and adolescence: response to sex steroid replacement. Br J Obstet Gynaecol. 1999 Dec;106(12):1265-72. | PubMed |
Bath LE, Critchley HO, Chambers SE, Anderson RA, Kelnar CJ, Wallace WH. Ovarian and uterine characteristics after total body irradiation in childhood and adolescence: response to sex steroid replacement. Br J Obstet Gynaecol. 1999 Dec;106(12):1265-72. | PubMed | Carter J, Rowland K, Chi D, Brown C, Abu-Rustum N, Castiel M, Barakat R. Gynecologic cancer treatment and the impact of cancer-related infertility. Gynecol Oncol. 2005 Apr;97(1):90-5. | PubMed |
Carter J, Rowland K, Chi D, Brown C, Abu-Rustum N, Castiel M, Barakat R. Gynecologic cancer treatment and the impact of cancer-related infertility. Gynecol Oncol. 2005 Apr;97(1):90-5. | PubMed | Loren AW, Mangu PB, Beck LN, Brennan L, Magdalinski AJ, Partridge AH, et al. Fertility preservation for patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol. 2013 Jul 1;31(19):2500-10. | CrossRef | PubMed |
Loren AW, Mangu PB, Beck LN, Brennan L, Magdalinski AJ, Partridge AH, et al. Fertility preservation for patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol. 2013 Jul 1;31(19):2500-10. | CrossRef | PubMed | De Vos M, Smitz J, Woodruff TK. Fertility preservation in women with cancer. Lancet. 2014 Oct 4;384(9950):1302-10. | CrossRef | PubMed |
De Vos M, Smitz J, Woodruff TK. Fertility preservation in women with cancer. Lancet. 2014 Oct 4;384(9950):1302-10. | CrossRef | PubMed | Lee SJ, Schover LR, Partridge AH, Patrizio P, Wallace WH, Hagerty K, et al. American Society of Clinical Oncology recommendations on fertility preservation in cancer patients. J Clin Oncol. 2006 Jun 20;24(18):2917-31. | PubMed |
Lee SJ, Schover LR, Partridge AH, Patrizio P, Wallace WH, Hagerty K, et al. American Society of Clinical Oncology recommendations on fertility preservation in cancer patients. J Clin Oncol. 2006 Jun 20;24(18):2917-31. | PubMed | Wallace WH, Kelsey TW. Human ovarian reserve from conception to the menopause. PLoS One. 2010 Jan 27;5(1):e8772. | CrossRef | PubMed |
Wallace WH, Kelsey TW. Human ovarian reserve from conception to the menopause. PLoS One. 2010 Jan 27;5(1):e8772. | CrossRef | PubMed | Rodriguez-Wallberg KA, Oktay K. Fertility preservation and pregnancy in women with and without BRCA mutation-positive breast cancer. Oncologist. 2012;17(11):1409-17. | CrossRef | PubMed |
Rodriguez-Wallberg KA, Oktay K. Fertility preservation and pregnancy in women with and without BRCA mutation-positive breast cancer. Oncologist. 2012;17(11):1409-17. | CrossRef | PubMed | Anderson RA, Weddell A, Spoudeas HA, Douglas C, Shalet SM, Levitt G, et al. Do doctors discuss fertility issues before they treat young patients with cancer Hum Reprod. 2008 Oct;23(10):2246-51. | CrossRef | PubMed |
Anderson RA, Weddell A, Spoudeas HA, Douglas C, Shalet SM, Levitt G, et al. Do doctors discuss fertility issues before they treat young patients with cancer Hum Reprod. 2008 Oct;23(10):2246-51. | CrossRef | PubMed | Peccatori FA, Azim HA Jr, Orecchia R, Hoekstra HJ, Pavlidis N, Kesic V, et al. Cancer, pregnancy and fertility: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2013 Oct;24 Suppl 6:vi160-70. | CrossRef | PubMed |
Peccatori FA, Azim HA Jr, Orecchia R, Hoekstra HJ, Pavlidis N, Kesic V, et al. Cancer, pregnancy and fertility: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2013 Oct;24 Suppl 6:vi160-70. | CrossRef | PubMed | Ataman LM, Rodrigues JK, Marinho RM, Caetano JP, Chehin MB, Alves da Motta EL, et al. Creating a Global Community of Practice for Oncofertility. J Glob Oncol. 2016 Apr;2(2):83-96. | PubMed |
Ataman LM, Rodrigues JK, Marinho RM, Caetano JP, Chehin MB, Alves da Motta EL, et al. Creating a Global Community of Practice for Oncofertility. J Glob Oncol. 2016 Apr;2(2):83-96. | PubMed | Knopman JM, Noyes N, Talebian S, Krey LC, Grifo JA, Licciardi F. Women with cancer undergoing ART for fertility preservation: a cohort study of their response to exogenous gonadotropins. Fertil Steril. 2009 Apr;91(4 Suppl):1476-8. | CrossRef | PubMed |
Knopman JM, Noyes N, Talebian S, Krey LC, Grifo JA, Licciardi F. Women with cancer undergoing ART for fertility preservation: a cohort study of their response to exogenous gonadotropins. Fertil Steril. 2009 Apr;91(4 Suppl):1476-8. | CrossRef | PubMed | Robertson AD, Missmer SA, Ginsburg ES. Embryo yield after in vitro fertilization in women undergoing embryo banking for fertility preservation before chemotherapy. Fertil Steril. 2011 Feb;95(2):588-91. | CrossRef | PubMed |
Robertson AD, Missmer SA, Ginsburg ES. Embryo yield after in vitro fertilization in women undergoing embryo banking for fertility preservation before chemotherapy. Fertil Steril. 2011 Feb;95(2):588-91. | CrossRef | PubMed | Wolff EF, Martel M, Gwin K, Lannin D. Synchronous primary breast and ovarian cancer with ovarian cancer metastases to a breast sentinel lymph node. Breast J. 2009 Mar-Apr;15(2):203-5. | CrossRef | PubMed |
Wolff EF, Martel M, Gwin K, Lannin D. Synchronous primary breast and ovarian cancer with ovarian cancer metastases to a breast sentinel lymph node. Breast J. 2009 Mar-Apr;15(2):203-5. | CrossRef | PubMed | Anderson RA, Kinniburgh D, Baird DT. Preliminary experience of the use of a gonadotrophin-releasing hormone antagonist in ovulation induction/in-vitro fertilization prior to cancer treatment. Hum Reprod. 1999 Oct;14(10):2665-8. | PubMed |
Anderson RA, Kinniburgh D, Baird DT. Preliminary experience of the use of a gonadotrophin-releasing hormone antagonist in ovulation induction/in-vitro fertilization prior to cancer treatment. Hum Reprod. 1999 Oct;14(10):2665-8. | PubMed | Turan V, Bedoschi G, Moy F, Oktay K. Safety and feasibility of performing two consecutive ovarian stimulation cycles with the use of letrozole-gonadotropin protocol for fertility preservation in breast cancer patients. Fertil Steril. 2013 Dec;100(6):1681-5.e1. | CrossRef | PubMed |
Turan V, Bedoschi G, Moy F, Oktay K. Safety and feasibility of performing two consecutive ovarian stimulation cycles with the use of letrozole-gonadotropin protocol for fertility preservation in breast cancer patients. Fertil Steril. 2013 Dec;100(6):1681-5.e1. | CrossRef | PubMed | Baynosa J, Westphal LM, Madrigrano A, Wapnir I. Timing of breast cancer treatments with oocyte retrieval and embryo cryopreservation. J Am Coll Surg. 2009 Nov;209(5):603-7. | CrossRef | PubMed |
Baynosa J, Westphal LM, Madrigrano A, Wapnir I. Timing of breast cancer treatments with oocyte retrieval and embryo cryopreservation. J Am Coll Surg. 2009 Nov;209(5):603-7. | CrossRef | PubMed | Lee S, Ozkavukcu S, Heytens E, Moy F, Oktay K. Value of early referral to fertility preservation in young women with breast cancer. J Clin Oncol. 2010 Nov 1;28(31):4683-6. | CrossRef | PubMed |
Lee S, Ozkavukcu S, Heytens E, Moy F, Oktay K. Value of early referral to fertility preservation in young women with breast cancer. J Clin Oncol. 2010 Nov 1;28(31):4683-6. | CrossRef | PubMed | Oktay K, Hourvitz A, Sahin G, Oktem O, Safro B, Cil A, Bang H. Letrozole reduces estrogen and gonadotropin exposure in women with breast cancer undergoing ovarian stimulation before chemotherapy. J Clin Endocrinol Metab. 2006 Oct;91(10):3885-90. | PubMed |
Oktay K, Hourvitz A, Sahin G, Oktem O, Safro B, Cil A, Bang H. Letrozole reduces estrogen and gonadotropin exposure in women with breast cancer undergoing ovarian stimulation before chemotherapy. J Clin Endocrinol Metab. 2006 Oct;91(10):3885-90. | PubMed | Azim AA, Costantini-Ferrando M, Oktay K. Safety of fertility preservation by ovarian stimulation with letrozole and gonadotropins in patients with breast cancer: a prospective controlled study. J Clin Oncol. 2008 Jun 1;26(16):2630-5. | CrossRef | PubMed |
Azim AA, Costantini-Ferrando M, Oktay K. Safety of fertility preservation by ovarian stimulation with letrozole and gonadotropins in patients with breast cancer: a prospective controlled study. J Clin Oncol. 2008 Jun 1;26(16):2630-5. | CrossRef | PubMed | Mandelbaum J, Bela´sch-Allart J, Junca AM, Antoine JM, Plachot M, Alvarez S, et al. Cryopreservation in human assisted reproduction is now routine for embryos but remains a research procedure for oocytes. Hum Reprod. 1998 Jun;13 Suppl 3:161-74;discussion175-7. | PubMed |
Mandelbaum J, Bela´sch-Allart J, Junca AM, Antoine JM, Plachot M, Alvarez S, et al. Cryopreservation in human assisted reproduction is now routine for embryos but remains a research procedure for oocytes. Hum Reprod. 1998 Jun;13 Suppl 3:161-74;discussion175-7. | PubMed | Rienzi L, Cobo A, Paffoni A, Scarduelli C, Capalbo A, Vajta G, et al. Consistent and predictable delivery rates after oocyte vitrification: an observational longitudinal cohort multicentric study. Hum Reprod. 2012 Jun;27(6):1606-12. | CrossRef | PubMed |
Rienzi L, Cobo A, Paffoni A, Scarduelli C, Capalbo A, Vajta G, et al. Consistent and predictable delivery rates after oocyte vitrification: an observational longitudinal cohort multicentric study. Hum Reprod. 2012 Jun;27(6):1606-12. | CrossRef | PubMed | Grifo JA, Noyes N. Delivery rate using cryopreserved oocytes is comparable to conventional in vitro fertilization using fresh oocytes: potential fertility preservation for female cancer patients. Fertil Steril. 2010 Feb;93(2):391-6. | CrossRef | PubMed |
Grifo JA, Noyes N. Delivery rate using cryopreserved oocytes is comparable to conventional in vitro fertilization using fresh oocytes: potential fertility preservation for female cancer patients. Fertil Steril. 2010 Feb;93(2):391-6. | CrossRef | PubMed | Practice Committee of Society for Assisted Reproductive Technology; Practice Committee of American Society for Reproductive Medicine. Preimplantation genetic testing: a Practice Committee opinion. Fertil Steril. 2008 Nov;90(5 Suppl):S136-43. | CrossRef | PubMed |
Practice Committee of Society for Assisted Reproductive Technology; Practice Committee of American Society for Reproductive Medicine. Preimplantation genetic testing: a Practice Committee opinion. Fertil Steril. 2008 Nov;90(5 Suppl):S136-43. | CrossRef | PubMed | Cobo A, GarcÝa-Velasco JA, Coello A, Domingo J, Pellicer A, RemohÝ J. Oocyte vitrification as an efficient option for elective fertility preservation. Fertil Steril. 2016 Mar;105(3):755-764.e8. | CrossRef | PubMed |
Cobo A, GarcÝa-Velasco JA, Coello A, Domingo J, Pellicer A, RemohÝ J. Oocyte vitrification as an efficient option for elective fertility preservation. Fertil Steril. 2016 Mar;105(3):755-764.e8. | CrossRef | PubMed | Goldman KN, Noyes NL, Knopman JM, McCaffrey C, Grifo JA. Oocyte efficiency: does live birth rate differ when analyzing cryopreserved and fresh oocytes on a per-oocyte basis? Fertil Steril. 2013 Sep;100(3):712-7. | CrossRef | PubMed |
Goldman KN, Noyes NL, Knopman JM, McCaffrey C, Grifo JA. Oocyte efficiency: does live birth rate differ when analyzing cryopreserved and fresh oocytes on a per-oocyte basis? Fertil Steril. 2013 Sep;100(3):712-7. | CrossRef | PubMed | Ginsburg ES, Yanushpolsky EH, Jackson KV. In vitro fertilization for cancer patients and survivors. Fertil Steril. 2001 Apr;75(4):705-10. | PubMed |
Ginsburg ES, Yanushpolsky EH, Jackson KV. In vitro fertilization for cancer patients and survivors. Fertil Steril. 2001 Apr;75(4):705-10. | PubMed | Donnez J, Dolmans MM, Demylle D, Jadoul P, Pirard C, Squifflet J, et al. Livebirth after orthotopic transplantation of cryopreserved ovarian tissue. Lancet. 2004 Oct 16-22;364(9443):1405-10. | PubMed |
Donnez J, Dolmans MM, Demylle D, Jadoul P, Pirard C, Squifflet J, et al. Livebirth after orthotopic transplantation of cryopreserved ovarian tissue. Lancet. 2004 Oct 16-22;364(9443):1405-10. | PubMed | Donnez J, Dolmans MM. Ovarian cortex transplantation: 60 reported live births brings the success and worldwide expansion of the technique towards routine clinical practice. J Assist Reprod Genet. 2015 Aug;32(8):1167-70. | CrossRef | PubMed |
Donnez J, Dolmans MM. Ovarian cortex transplantation: 60 reported live births brings the success and worldwide expansion of the technique towards routine clinical practice. J Assist Reprod Genet. 2015 Aug;32(8):1167-70. | CrossRef | PubMed | Van der Ven H, Liebenthron J, Beckmann M, Toth B, Korell M, KrŘssel J, et al. Ninety-five orthotopic transplantations in 74 women of ovarian tissue after cytotoxic treatment in a fertility preservation network: tissue activity, pregnancy and delivery rates. Hum Reprod. 2016 Sep;31(9):2031-41.
| CrossRef | PubMed |
Van der Ven H, Liebenthron J, Beckmann M, Toth B, Korell M, KrŘssel J, et al. Ninety-five orthotopic transplantations in 74 women of ovarian tissue after cytotoxic treatment in a fertility preservation network: tissue activity, pregnancy and delivery rates. Hum Reprod. 2016 Sep;31(9):2031-41.
| CrossRef | PubMed | Donnez J, Dolmans MM, Diaz C, Pellicer A. Ovarian cortex transplantation: time to move on from experimental studies to open clinical application. Fertil Steril. 2015 Nov;104(5):1097-8. | CrossRef | PubMed |
Donnez J, Dolmans MM, Diaz C, Pellicer A. Ovarian cortex transplantation: time to move on from experimental studies to open clinical application. Fertil Steril. 2015 Nov;104(5):1097-8. | CrossRef | PubMed | Donnez J, Silber S, Andersen CY, Demeestere I, Piver P, Meirow D, et al. Children born after autotransplantation of cryopreserved ovarian tissue. a review of 13 live births. Ann Med. 2011;43(6):437-50. | CrossRef | PubMed |
Donnez J, Silber S, Andersen CY, Demeestere I, Piver P, Meirow D, et al. Children born after autotransplantation of cryopreserved ovarian tissue. a review of 13 live births. Ann Med. 2011;43(6):437-50. | CrossRef | PubMed | Wallace WH, Smith AG, Kelsey TW, Edgar AE, Anderson RA. Fertility preservation for girls and young women with cancer: population-based validation of criteria for ovarian tissue cryopreservation. Lancet Oncol. 2014 Sep;15(10):1129-36. | CrossRef | PubMed |
Wallace WH, Smith AG, Kelsey TW, Edgar AE, Anderson RA. Fertility preservation for girls and young women with cancer: population-based validation of criteria for ovarian tissue cryopreservation. Lancet Oncol. 2014 Sep;15(10):1129-36. | CrossRef | PubMed | Waimey KE, Duncan FE, Su HI, Smith K, Wallach H, Jona K, et al. Future Directions in Oncofertility and Fertility Preservation: A Report from the 2011 Oncofertility Consortium Conference. J Adolesc Young Adult Oncol. 2013 Mar;2(1):25-30. | PubMed |
Waimey KE, Duncan FE, Su HI, Smith K, Wallach H, Jona K, et al. Future Directions in Oncofertility and Fertility Preservation: A Report from the 2011 Oncofertility Consortium Conference. J Adolesc Young Adult Oncol. 2013 Mar;2(1):25-30. | PubMed | Morris SN, Ryley D. Fertility preservation: nonsurgical and surgical options. Semin Reprod Med. 2011 Mar;29(2):147-54. | CrossRef | PubMed |
Morris SN, Ryley D. Fertility preservation: nonsurgical and surgical options. Semin Reprod Med. 2011 Mar;29(2):147-54. | CrossRef | PubMed | Martin JR, Kodaman P, Oktay K, Taylor HS. Ovarian cryopreservation with transposition of a contralateral ovary: a combined approach for fertility preservation in women receiving pelvic radiation. Fertil Steril. 2007 Jan;87(1):189.e5-7. | PubMed |
Martin JR, Kodaman P, Oktay K, Taylor HS. Ovarian cryopreservation with transposition of a contralateral ovary: a combined approach for fertility preservation in women receiving pelvic radiation. Fertil Steril. 2007 Jan;87(1):189.e5-7. | PubMed | Elgindy EA, El-Haieg DO, Khorshid OM, Ismail EI, Abdelgawad M, Sallam HN, et al Abou-Setta AM. Gonadatrophin suppression to prevent chemotherapy-induced ovarian damage: a randomized controlled trial. Obstet Gynecol. 2013 Jan;121(1):78-86. | CrossRef | PubMed |
Elgindy EA, El-Haieg DO, Khorshid OM, Ismail EI, Abdelgawad M, Sallam HN, et al Abou-Setta AM. Gonadatrophin suppression to prevent chemotherapy-induced ovarian damage: a randomized controlled trial. Obstet Gynecol. 2013 Jan;121(1):78-86. | CrossRef | PubMed | Gerber B, von Minckwitz G, Stehle H, Reimer T, Felberbaum R, Maass N, et al. Effect of luteinizing hormone-releasing hormone agonist on ovarian function after modern adjuvant breast cancer chemotherapy: the GBG 37 ZORO study. J Clin Oncol. 2011 Jun 10;29(17):2334-41. | CrossRef | PubMed |
Gerber B, von Minckwitz G, Stehle H, Reimer T, Felberbaum R, Maass N, et al. Effect of luteinizing hormone-releasing hormone agonist on ovarian function after modern adjuvant breast cancer chemotherapy: the GBG 37 ZORO study. J Clin Oncol. 2011 Jun 10;29(17):2334-41. | CrossRef | PubMed | Munster PN, Moore AP, Ismail-Khan R, Cox CE, Lacevic M, Gross-King M, et al. Randomized trial using gonadotropin-releasing hormone agonist triptorelin for the preservation of ovarian function during (neo)adjuvant chemotherapy for breast cancer. J Clin Oncol. 2012 Feb 10;30(5):533-8. | CrossRef | PubMed |
Munster PN, Moore AP, Ismail-Khan R, Cox CE, Lacevic M, Gross-King M, et al. Randomized trial using gonadotropin-releasing hormone agonist triptorelin for the preservation of ovarian function during (neo)adjuvant chemotherapy for breast cancer. J Clin Oncol. 2012 Feb 10;30(5):533-8. | CrossRef | PubMed | Elgindy E, Sibai H, Abdelghani A, Mostafa M. Protecting Ovaries During Chemotherapy Through Gonad Suppression: A Systematic Review and Meta-analysis. Obstet Gynecol. 2015 Jul;126(1):187-95. | CrossRef | PubMed |
Elgindy E, Sibai H, Abdelghani A, Mostafa M. Protecting Ovaries During Chemotherapy Through Gonad Suppression: A Systematic Review and Meta-analysis. Obstet Gynecol. 2015 Jul;126(1):187-95. | CrossRef | PubMed | Chen H, Lv JQ, Ge HS, Wu XM, Xi HT, Chi HH, et al. Live birth following vitrification of in vitro matured oocytes derived from sibling smaller follicles at follicle selection phase in the context of in vitro fertilization. Gynecol Endocrinol. 2014 Sep;30(9):624-6. | CrossRef | PubMed |
Chen H, Lv JQ, Ge HS, Wu XM, Xi HT, Chi HH, et al. Live birth following vitrification of in vitro matured oocytes derived from sibling smaller follicles at follicle selection phase in the context of in vitro fertilization. Gynecol Endocrinol. 2014 Sep;30(9):624-6. | CrossRef | PubMed | Kim SY, Kim SK, Lee JR, Woodruff TK. Toward precision medicine for preserving fertility in cancer patients: existing and emerging fertility preservation options for women. J Gynecol Oncol. 2016 Mar;27(2):e22.
| CrossRef | PubMed |
Kim SY, Kim SK, Lee JR, Woodruff TK. Toward precision medicine for preserving fertility in cancer patients: existing and emerging fertility preservation options for women. J Gynecol Oncol. 2016 Mar;27(2):e22.
| CrossRef | PubMed | Xu M, Barrett SL, West-Farrell E, Kondapalli LA, Kiesewetter SE, Shea LD, et al. In vitro grown human ovarian follicles from cancer patients support oocyte growth. Hum Reprod. 2009 Oct;24(10):2531-40. | CrossRef | PubMed |
Xu M, Barrett SL, West-Farrell E, Kondapalli LA, Kiesewetter SE, Shea LD, et al. In vitro grown human ovarian follicles from cancer patients support oocyte growth. Hum Reprod. 2009 Oct;24(10):2531-40. | CrossRef | PubMed | Rodrigues JK, Navarro PA, Zelinski MB, Stouffer RL, Xu J. Direct actions of androgens on the survival, growth and secretion of steroids and anti-MŘllerian hormone by individual macaque follicles during three-dimensional culture. Hum Reprod. 2015 Mar;30(3):664-74.
| CrossRef | PubMed |
Rodrigues JK, Navarro PA, Zelinski MB, Stouffer RL, Xu J. Direct actions of androgens on the survival, growth and secretion of steroids and anti-MŘllerian hormone by individual macaque follicles during three-dimensional culture. Hum Reprod. 2015 Mar;30(3):664-74.
| CrossRef | PubMed | Ting AY, Yeoman RR, Lawson MS, Zelinski MB. In vitro development of secondary follicles from cryopreserved rhesus macaque ovarian tissue after slow-rate freeze or vitrification. Hum Reprod. 2011 Sep;26(9):2461-72. | CrossRef | PubMed |
Ting AY, Yeoman RR, Lawson MS, Zelinski MB. In vitro development of secondary follicles from cryopreserved rhesus macaque ovarian tissue after slow-rate freeze or vitrification. Hum Reprod. 2011 Sep;26(9):2461-72. | CrossRef | PubMed | Salama M, Woodruff TK. New advances in ovarian autotransplantation to restore fertility in cancer patients. Cancer Metastasis Rev. 2015 Dec;34(4):807-822. | CrossRef | PubMed |
Salama M, Woodruff TK. New advances in ovarian autotransplantation to restore fertility in cancer patients. Cancer Metastasis Rev. 2015 Dec;34(4):807-822. | CrossRef | PubMed | Donnez J, Squifflet J, Jadoul P, Lousse JC, Dolmans MM, Donnez O. Fertility preservation in women with ovarian endometriosis. Front Biosci (Elite Ed). 2012 Jan 1;4:1654-62. | PubMed |
Donnez J, Squifflet J, Jadoul P, Lousse JC, Dolmans MM, Donnez O. Fertility preservation in women with ovarian endometriosis. Front Biosci (Elite Ed). 2012 Jan 1;4:1654-62. | PubMed | Ethics Committee of American Society for Reproductive Medicine. Fertility preservation and reproduction in patients facing gonadotoxic therapies: a committee opinion. Fertil Steril. 2013 Nov;100(5):1224-31. | CrossRef | PubMed |
Ethics Committee of American Society for Reproductive Medicine. Fertility preservation and reproduction in patients facing gonadotoxic therapies: a committee opinion. Fertil Steril. 2013 Nov;100(5):1224-31. | CrossRef | PubMed |