 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: Hantavirus, Epidemiology, Mathematics
Introducción
El síndrome cardiopulmonar por hantavirus es una enfermedad causada por un virus perteneciente al orden bunyanvirales, y transmitida hacia los humanos a través de roedores. Esta enfermedad en Chile es considerada endémica, la cual tiene una alta tasa de letalidad. En la actualidad existen estudios que evidencian el contagio entre personas del virus Andes, cuya localidad se concentra en los países de Argentina y Chile.
Objetivos
Analizar la posibilidad de transmisión de hantavirus entre humanos, mediante un modelo matemático tipo SEIR.
Métodos
Se plantea un modelo matemático tipo SEIR (susceptible, expuesto, infeccioso y recuperado) para expresar la dinámica de la enfermedad por hantavirus, incluyendo la posibilidad de transmisión entre humanos y la percepción del riesgo.
Resultados
El máximo de contagio entre humanos disminuye cerca de 25% tras aumentar la percepción de riesgo de las personas, mediante la reducción de la tasa de resistencia al cambio y aumento la velocidad de reaccionar de las personas.
Conclusiones
Es urgente revisar las estrategias de comunicación de riesgo y medidas de prevención ante esta posibilidad de contagios masivos entre humanos, además de fortalecer la investigación y proyectar el desarrollo de una vacuna para proteger las poblaciones expuestas a esta enfermedad con alta tasa de letalidad.
|
Ideas clave
|
El síndrome cardiopulmonar por hantavirus es una enfermedad causada por un virus perteneciente al orden bunyanvirales, y transmitida hacia los humanos a través de roedores [1]. Dentro de este orden, se encuentran el virus Sin Nombre y virus Andes, principales agentes que causan la enfermedad en humanos, cuyos roedores comúnmente transmisores son Peromyscus maniculatus (ratón ciervo) y Oligoryzomys (ratón de cola larga) [1],[2],[3]. La transmisión desde el roedor hacia el humano es a través de la inhalación de partículas virales por medio de orina, heces o saliva [4],[5]. También existen casos de transmisión vía mordeduras, pero estos son aislados.
El hantavirus es una enfermedad que es considerada endémica en Chile [4], que presentó 91, 33, 70 y 30 casos en los años 2017 a 2020 respectivamente [6]. Si bien anualmente no registra un alto número de casos positivos en relación a otras enfermedades, esta posee una alta tasa de letalidad que fluctúa entre el 30 y 60% [7].
Argentina y Chile son los países en donde se han encontrado casos de transmisión entre personas del virus Andes. El primer caso confirmado ocurrió en el año 1996 en Argentina, posteriormente el año 2014 en el mismo país, se confirmó la transmisión de tres casos [8]. En Chile el año 2019, se registró un posible caso de transmisión de una persona (caso índice) hacia su hija, al recién nacido de su hija y a la cuidadora de este [4]. Además, se detectó la presencia del virus en la leche materna, por lo que no se descarta una transmisión por esta vía. En Argentina, un estudio realizado entre noviembre de 2018 y febrero de 2019, registró 34 casos confirmados de contagio entre personas, ocurridos particularmente en la provincia de Chubut [9]. Según el mismo estudio [9], los pacientes con una carga viral alta y lesión hepática tenían más probabilidades que otros pacientes para propagar la infección.
Para entender la dinámica de la transmisión del hantavirus entre roedores, los modelos matemáticos han tenido un aporte significativo en la discusión [10],[11],[12],[13],[14],[15],[16]. Algunos estudios han modelado el efecto demográfico y variables ambientales asociadas [13],[14],[15],[16]. Otros analizaron la importancia del macho en la transmisión entre roedores [10],[11],[12]. Existen algunos que estudian la transmisión desde el roedor hacia el humano [17],[18]. Sin embargo, existe una escasez de modelos que incorporen la transmisión de hantavirus entre personas, novedad principal presentada en este trabajo. Para la dinámica de contagio entre roedores, los estudios mencionados se basan principalmente en que los roedores pueden estar en cuatro estados: susceptible (S), expuesto (E), infectado (I) y recuperado (R), comúnmente denotado por SEIR [19],[20],[21].
La infección en el humano presenta un periodo de incubación, cuya duración fluctúa entre una y seis semanas [6], luego se convierte en infeccioso, para posteriormente adquirir inmunidad o fallecer. Por lo tanto, también se puede asociar su evolución de la enfermedad mediante un modelo SEIR.
Un factor determinante en el control de enfermedades es la percepción del riesgo de los individuos [22],[23],[24],[25]. Particularmente la enfermedad por hantavirus tuvo una disminución de casos durante los años en que hubo una fuerte campaña publicitaria de prevención en Chile [4],[26],[27].
En este trabajo se presenta la dinámica de la enfermedad por hantavirus mediante un modelo matemático tipo SEIR [19],[20],[21] el cual incorpora la transmisión entre personas del virus Andes.
Modelo matemático
La dinámica de la enfermedad asociada al humano (h) es mediante un modelo SEIR: susceptible (S), expuesto (E), infectado (I) y recuperado (R), ya que el individuo al contraer la infección comienza con un periodo de incubación (E), cuya duración, como se mencionó anteriormente, fluctúa entre una y seis semanas. Posteriormente presenta síntomas (I), y posiblemente es capaz de transmitir la infección hacia otros humanos. Finalmente, el individuo adquiere inmunidad (R) o lamentablemente muere.
En lo que respecta a la transmisión entre roedores (m), se analiza a través del modelo SEIR. Es decir, al igual que en el humano, pero con tiempos de infección distintos. Así para distinguir los estados asociados a la enfermedad entre humanos y roedores, se utiliza el subíndice h para los humanos y m para los roedores (Tabla 1).
Tabla 1. Notación de los estados asociados con la enfermedad.
Un factor predeterminante en la transmisión desde el roedorhacia el humano del virus, es la percepción de riesgo (P) [28], que se refiere a los juicios subjetivos de las personas sobre laocurrencia de eventos negativos que podrían generar enfermedades,accidentes o muerte. Tiene un componente cognitivo (qué sabe sobre el hantavirus) y otro emocional (qué siente sobre el hantavirus) y es importante su estudio para generarpropuestas de intervención efectivas en temáticas de salud y comunicación de riesgo ya que informa sobre los peligros que perciben y las estrategias de afrontamiento. Al tomar las medidas pertinentes, y generar una campaña efectiva de comunicaciónde riesgo, la probabilidad de contagio puede llegar adisminuir significativamente. Esta variable (P) depende de una gran variedad de factores, de los cuales se expresará sobre la base de dos de ellos: resistencia al cambio (λ1 ) y velocidad dereaccionar ( λ2 ) ante el número de casos positivos.
El modelo que involucra la dinámica del hantavirus entre humanos y roedores está dado por el sistema de ecuaciones diferenciales en (1).
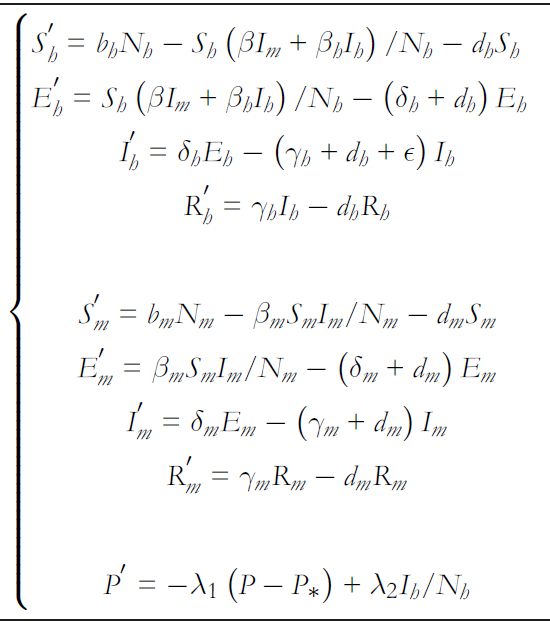
Desde el modelo βh, βm y β corresponden a las tasas de contagio entre humanos, entre roedores y desde el roedor hacia el humano respectivamente. En lo que respecta a las tasas de contagio hacia el humano ( βh y β ), estas son dependiente de la percepción del riesgo del humano, con βh = β*h (P*/P) y β = β* (P*/P) , donde β*h , β* y P* corresponden a la tasa de transmisión promedio entre humanos, desde el roedor hacia el humano, y la percepción del riesgo promedio cuantificada respectivamente. Luego, Nh y Nm denotan a la población de humanos y roedores, respectivamente. Es importante observar que la transmisión desde el roedor hacia el humano ( βShIm/Nm ) se ve afectada en el número de roedores por humano ( K = Nm/Nh ) [29],[30],[31]. Así, finalmente queda βSh ( Im/Nm) K = βShIm/Nh .
Las tasas de transición desde los estados exposición (E) a infeccioso (I), y de infeccioso a recuperado (R) están dadas por δ y γ respectivamente. Así δ−1 y γ−1 determinan el tiempo prome-dio en que permanecen en su condición de incubación e infec-cioso respectivamente. Los subíndices h y m diferencian las tasas asociadas a humanos y roedores respectivamente. Las tasas de natalidad y morta dad no por enfermedad) se expresan por bx y dx con x ∈ {h, m} espectivamente. Para la tasa asociada a la letalidad por enfermedad, está dada por ∈ .
En epidemiología matemática, un valor esencial para determi-nar condiciones de umbral, es el número reproductivo básico ( R0 ) [32],[33], que se define como “el número esperado de casos secundarios producidos por un primer infeccioso en una población completamente susceptible” [32], el cual establece que si R0>1 la enfermedad se propaga y si R0<1 no ocurre dicho fenómeno. Según el estudio realizado en Argentina [9], el número reproductivo básico de la transmisión de hantavirus entre humanos fue estimado en 2,12 antes de decretar medidas de aislamiento para los pacientes asintomáticos y auto cuarentena para pacientes de alto riesgo, tras el brote presentado en dicha localidad. Una vez aplicada las medidas de control, dicho valor disminuyó a 0,96 [9]. Desde el sistema (1), mediante el método de la siguiente generación, el número reproductivo básico en la transmisión entre personas está dado por
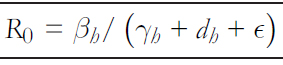
Antecedentes
Según el reporte entregado por el Ministerio de Salud de Chile [6], desde enero a marzo de 2021 ya se contabilizan 13 casos de hantavirus, en comparación a los 30 casos del año 2020 (Tabla 2). Se debe resaltar que en estos dos años, debido a la pandemia de COVID- 19, la movilidad de las personas ha sido reducida tras las medidas de mitigación propuesta por las autoridades de salud de dicho país. El año 2019 se registraron 70 casos, año que existía libre movimiento territorial.
Valores usados en las simulaciones numéricas
En la Tabla 3, se presenta los valores utilizados en las simulacio-nes numéricas. Estos valores son extraídos desde otras investi-gaciones y algunos de ellos han sido estimados desde los datos a disposición.
En lo que respecta a la población inicial, se considera Nh = 100 000 y toda la población humana sin enfermedad. Para la población de roedores se considera Nm = 100, con un solo roedor infectado.
Las simulaciones numéricas expresadas en las gráficas de los datos, fueron elaboradas vía software MATLAB.
Tabla 2. Número de casos por hantavirus en Chile.
Tabla 3. Resumen y valores de los parámetros para simulaciones numéricas.
Sin contagio entre humanos
Antes de observar el impacto de la transmisión entre humanos, es importante visualizar la cantidad de contagios que se produ- cen desde el roedor hacia el humano. Desde la Figura 1 se observa que, con los datos utilizados para simular en el modelo y anulando las tasas asociadas al contagio entre personas, la cifra
en un año asciende a 5,8 casos por cada 100 mil habitantes (Figura 1b), cuya variación durante ese periodo es de +0,06 (Figura 1(a)). Así, las simulaciones están acorde con la realidad de poblaciones en donde el trabajo de tipo agrícola y forestal es la principal fuente laboral.
El número de roedores infectados es muy difícil de estimar, ya que a la fecha no se cuenta con un registro sistematizado del roedor portador del virus Andes en el país. No obstante, desde la Figura 2 se visualiza la dinámica de roedores infectados que arroja el modelo planteado. La Figura 2a se observa una pequeña variación de +2 casos, y el total de casos acumulados durante un año, Figura 2b, asciende a 12.
Contagio entre humanos
En la Figura 3 se expresa la dinámica de la enfermedad en los humanos y su respectiva percepción del riesgo, cuyos valores numéricos se corresponden con los entregados en la Tabla 3. En la Figura 3a se observa la dinámica de la infección por hantavirus en los humanos durante un año, en el cual inicialmente no existen casos en este grupo. El máximo de contagios se produce casi al finalizar el año. Esto ocurre debido a los largos periodos de incubación que se pueden presentar. Se evidencia desde la Figura 3b que la percepción del riesgo tiene un comportamiento similar a la curva infecciosa, con variaciones diarias.
En la Figura 4, en comparación con la Figura 3, se aplica una disminución posicional decimal de la tasa de resistencia al cam- bio (λ1/10) y un aumento en misma magnitud a la velocidad de reacción (λ2 ∗ 10). Se observa desde la Figura 4a que el máximo de contagio disminuyó en casi un 25%, lo cual es altamente significativo tras aumentar la percepción del riesgo en los valo- res de λ1 y λ2 mencionados. Otro factor por observar es que en la Figura 4b a diferencia de la Figura 3b, no aparece la variabili- dad diaria en forma de “serrucho”. Además, se evidencia un aumento en la percepción del riesgo. Así, a mayor percepción del riesgo, disminuye la cantidad de contagiados humanos. Por lo que las campañas de prevención, juegan un rol fundamental ante la problemática planteada.
El diente de sierra que se presenta en la Figura 3b and a diferencia de la Figura 4b, ocurre debido a que la percepción del riesgo depende principalmente de dos factores en nuestro modelo: la tasa de resistencia al cambio y la velocidad de reacción de las personas. Esta última, además, depende de la cantidad de infectados humanos con hantavirus. Es por esto que, ante una mayor tasa de resistencia al cambio y menor velocidad de reacción, y tras un aumento de contagios humanos, existe una mayor variabilidad en la percepción del riesgo. Es decir, a mayor percepción del riesgo, más “suave” es la curva.
Tras disminuir y aumentar la tasa de resistencia al cambio y velocidad de reacción respectivamente, en comparación con la Figura 3, quedando λ1 = 0, 0065 y λ2 = 1, 5, se evidencia en la Figura 5 una disminución altamente significativa en el máximo de contagios (Figura 5a) tras el aumento de la percepción del riesgo (Figura 5b). A diferencia de las otras dos figuras asociadas con la percepción del riesgo (Figuras 3 y 4b), en esta (Figura 5b) el comportamiento de la curva no es acampanado durante el periodo graficado.
Figura 1. Personas con hantavirus sin considerar contagio entre humanos.
Figura 2. Dinámica del roedor.
Figura 3. Casos de hantavirus y percepción del riesgo, con λ
Figura 4. Casos de hantavirus y percepción del riesgo, con λ
Figura 5. Casos de hantavirus y percepción del riesgo, con λ
El modelo presentado que expresa la dinámica de la transmisión del hantavirus, incluyendo la posibilidad de contagio entre personas y la percepción del riesgo de la población general, muestra cómo esta última variable asociada al comportamiento de las personas es un factor determinante en la propagación de la enfermedad. La información que actualmente se encuentra disponible sobre el contagio entre personas es escasa y la generalidad del modelo, son las principales limitaciones del presente estudio. Sin embargo, desde el modelo planteado y sus respectivas gráficas asociadas a los casos de infección en humanos (Figuras 1, 3, 4 y 5), nos muestran que se deben aumentar las estrategias de vigilancia y prevención ante una posible mutación de virus hanta. Esto, debido a que de concretarse el contagio entre personas, las cifras de infectadas aumentan significativamente, sumando el posible riesgo de la intersección de rutas de enfermedades infecciosas como serían los casos reportados que han presentado COVID-19 y hantavirus [37]. Si a ello sumamos la alta tasa de letalidad del hantavirus, la población correría un grave peligro, en especial las zonas aledañas al hábitat del roedor hospedero [38].
Estudios previos han confirmado el contagio entre personas por hantavirus, particularmente del virus Andes [4],[8],[9]. Desde el estudio realizado en Argentina [9] se estimó que el número reproductivo básico es 2,12 antes de decretar cuarentena en la localidad en cuestión. Por lo que, ante una posible mutación del virus, se deben tomar medidas de prevención y monitoreo constante [39]. De lo contrario puede llegar a ocurrir una nueva pandemia, como las ya vivida por SARS-CoV-2 y H1N1, entre otras [38].
El cambio climático, la acelerada expansión de la agroindustria en las reservas naturales, el aumento de las temperaturas y los desastres antrópicos como los incendios forestales, producen la migración de roedores silvestres tras la escasez de alimento que se produce en su hábitat natural luego de estos siniestros [40],[41]. Por lo que, en su necesidad de búsqueda de alimento, es posible un mayor riesgo en el contacto entre humanos y roedores. Por lo tanto, ante el aumento de posibilidad de contacto, se incrementa la probabilidad de transmisión del virus desde el roedor hacia el humano [42].
Por otro lado, un estudio realizado con comunidades rurales chilenas [43], que evaluó la percepción de riesgo frente al hantavirus, demostró que un porcentaje significativo de los participantes tenían algún conocimiento sobre la enfermedad y habían oído hablar de su reservorio de roedores. Sin embargo, menos de 50% sabía que la enfermedad se transmite por los roedores y sus excrementos, y menos de la mitad de los participantes mencionaron la fiebre como síntoma principal. En este mismo estudio [43], se señaló que la televisión tuvo el mayor impacto comunicacional. Esto se debe a que la baja conectividad y acceso a internet en zonas rurales, los medios de comunicación masivos tradicionales como la televisión son los más efectivos. Los participantes sabían que la enfermedad por hantavirus puede ser muy grave y causar la muerte. Se percibieron a sí mismos, a sus familias y comunidades en riesgo de contraer esta enfermedad debido al lugar donde viven y sus ocupaciones. La mayoría teme a la enfermedad, probablemente como resultado de vivir en pequeñas comunidades donde se han producido casos y muertes. En síntesis, la percepción de riesgo hacia la enfermedad se debía principalmente al impacto que provocaron las muertes de personas afectadas con hantavirus, existiendo escaso conocimiento de la enfermedad por campañas de prevención y comunicación de riesgo.
A principios de marzo del año 2020 se produjo el primer caso de COVID-19 en Chile. Posterior a esto, dado el aumento significativo de casos, se tomaron medidas de control, principalmente reducción de la movilidad, uso de mascarilla obligatorio y distanciamiento físico. La reducción de la movilidad de las personas tuvo un impacto en el número de casos de hantavirus, ya que ese año se informaron 30 casos, menos de la mitad de casos que el año anterior. El presente año ha habido un desconfinamiento, el cual involucra dar mayor libertad en la movilidad de las personas, y durante los meses de enero y marzo 2021 ya se han registrado 13 casos [6].
Sin bien a nivel mundial se han desarrollado una serie de tratamientos con vacunas y antivirales probados tanto en modelos animales como en ensayos clínicos en humanos, no existen vacunas o tratamientos aprobados oficialmente por los organismos internacionales para las enfermedades por hantavirus [44]. Para el control o disminución de contagios de hantavirus en las personas es fundamental realizar campañas de prevención constantes y desarrollar estrategias de comunicación de riesgo efectivas. Estas deben involucrar la participación de la comunidad y ser atingentes a las realidades locales y culturales de las potenciales poblaciones afectadas [43],[45]. Además, se debe fortalecer la investigación básica desde las universidades y centros de investigación de enfermedades infecciosas; que se concentren en implementar nuevas estrategias de vigilancia epidemiológica genómica virales de los reservorios naturales. A todo ello se debe sumar el trabajo multidisciplinario con epidemiólogos, ecólogos, médicos, inmunólogos, investigadores de las ciencias del comportamiento, entre otros, para ayudar a identificar la fuente infecciosa y el lugar de las enfermedades provocadas por hantavirus [39]. Esto se evidencia en la disminución de casos tras aumentar la percepción del riesgo desde el modelo matemático planteado. Además, se verifica que en Chile en los periodos de mayor aplicación de campañas de prevención a través de diversos medios de comunicación, afiches en consultorios y establecimientos educacionales, entre otros, se produjo una disminución significativa de casos [4],[26],[27].
En este trabajo hemos presentado un modelo matemático tipo SEIR para expresar la dinámica de la infección por hantavirus, donde hemos incluido la posibilidad de contagio entre personas y la percepción del riesgo de la población hacia la enfermedad.
Los resultados del modelo, vía simulaciones numéricas, se elaboraron desde los escasos datos sobre el contagio entre humanos y, principalmente, desde la información entregada por el Ministerio de Salud de Chile y otros estudios.
Tras las simulaciones generadas por el modelo, se observa que la percepción del riesgo determina una sensibilidad en el máximo de la curva infecciosa tras la variación de esta, por lo que juega un rol fundamental en la propagación de la enfermedad.
Por lo tanto, aumentar la percepción del riesgo en la población general, mediante medidas de mitigación por parte de las autoridades sanitarias, es relevante para disminuir los casos de hantavirus y estar alerta ante un posible nuevo brote epidémico mediante vía de transmisión entre personas.
Autoría
JPGJ: conceptualización, metodología, análisis formal, investigación, redacción (revisiones y ediciones), gestión de datos, presentación de datos, administración del proyecto. MTMQ: conceptualización, metodología, análisis formal, investigación, redacción (revisiones y ediciones), supervisión.
Agradecimientos
Agradecemos a la Vicerrectoría de Investigación y Postgrado (VRIP) y al Centro de Investigación de Estudios Avanzados del Maule (CIEAM), ambos pertenecientes a la Universidad Católica del Maule.
Conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este trabajo.
Financiamiento
Los autores declaran que no hubo fuentes de financiación externas.
Origen y arbitraje
No solicitado. Con revisión por pares externa, por tres árbitros a doble ciego.
Idioma del envío
Español.

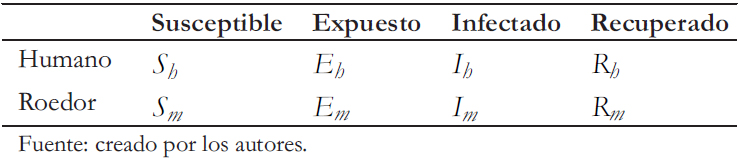 Tabla 1. Notación de los estados asociados con la enfermedad.
Tabla 1. Notación de los estados asociados con la enfermedad.

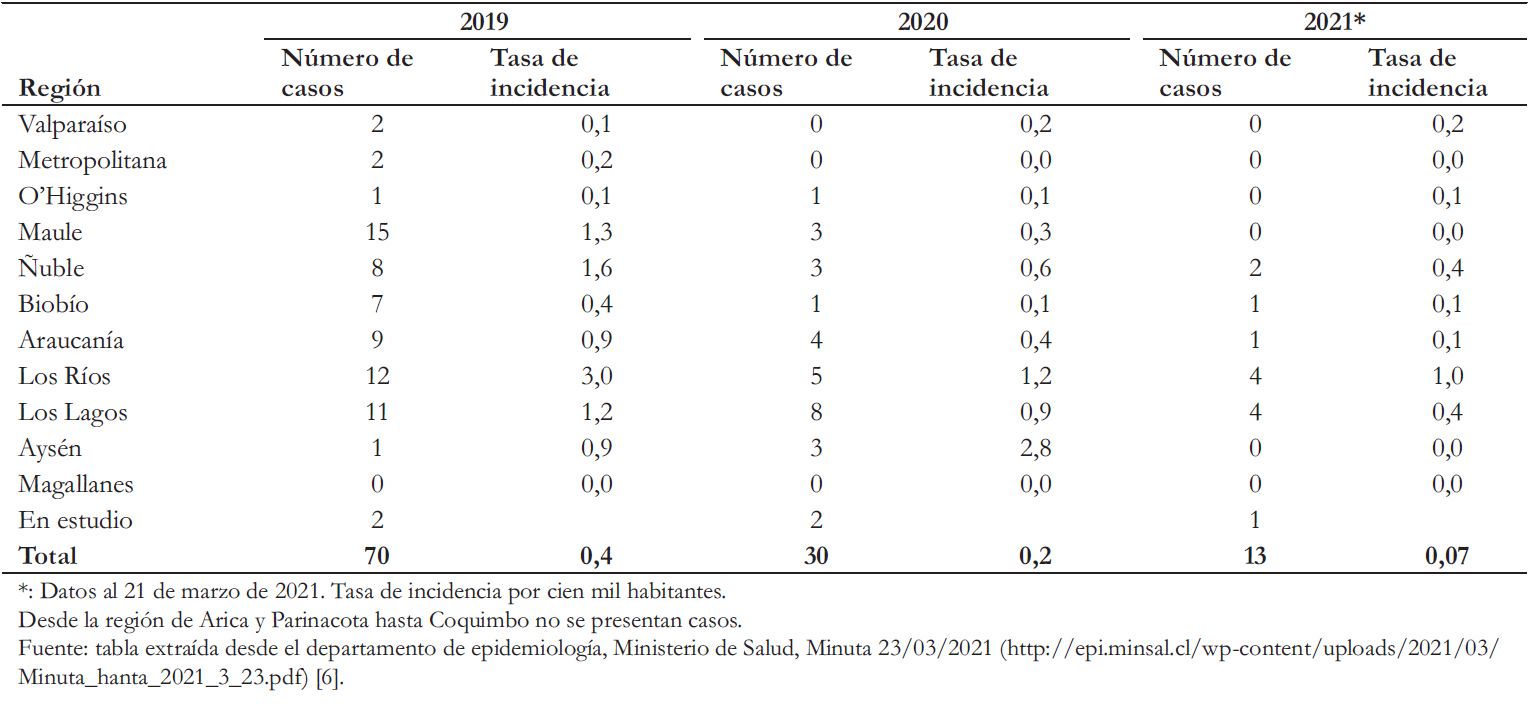 Tabla 2. Número de casos por hantavirus en Chile.
Tabla 2. Número de casos por hantavirus en Chile.

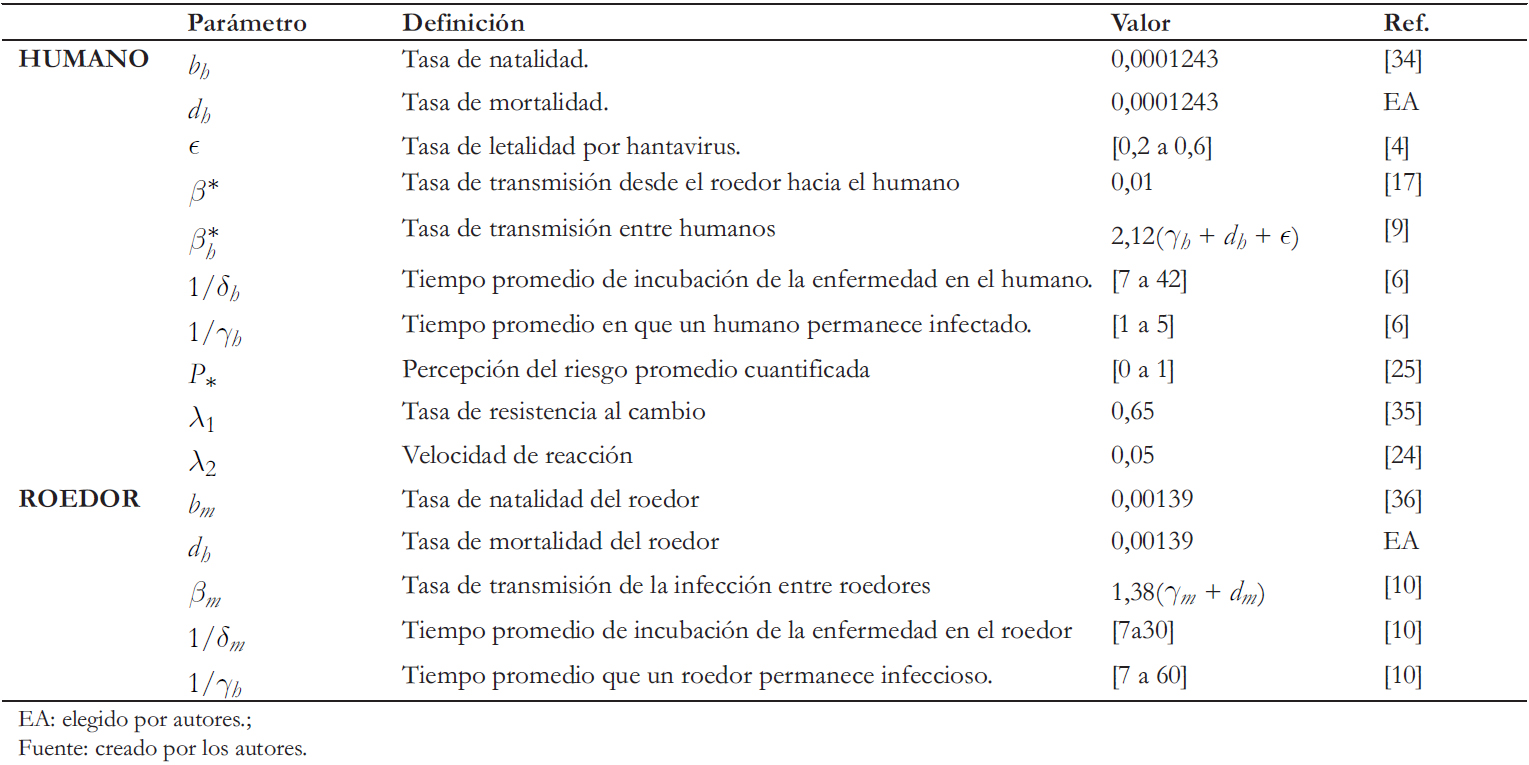 Tabla 3. Resumen y valores de los parámetros para simulaciones numéricas.
Tabla 3. Resumen y valores de los parámetros para simulaciones numéricas.

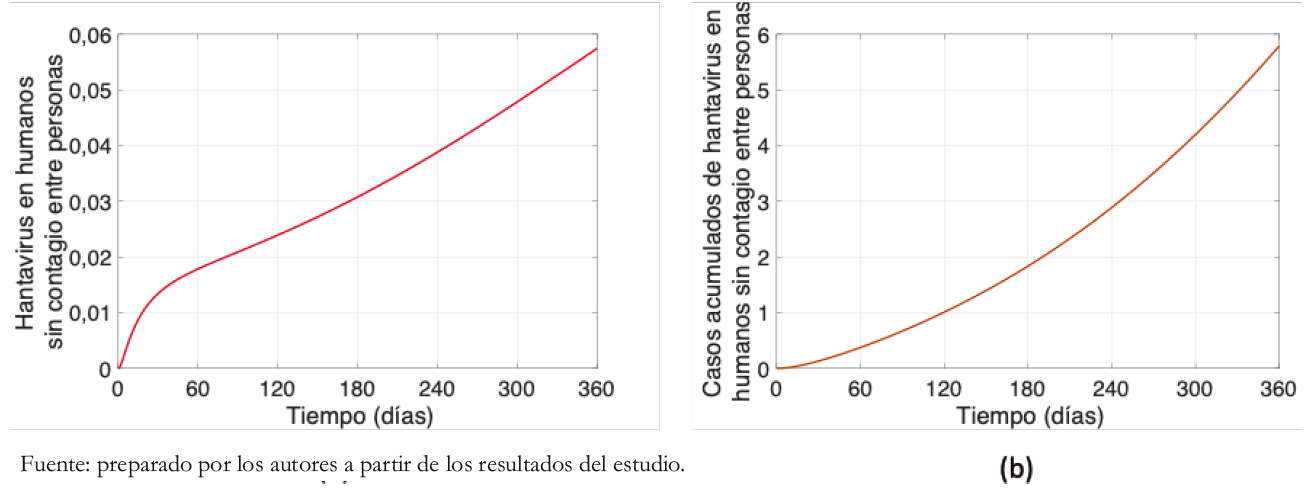 Figura 1. Personas con hantavirus sin considerar contagio entre humanos.
Figura 1. Personas con hantavirus sin considerar contagio entre humanos.

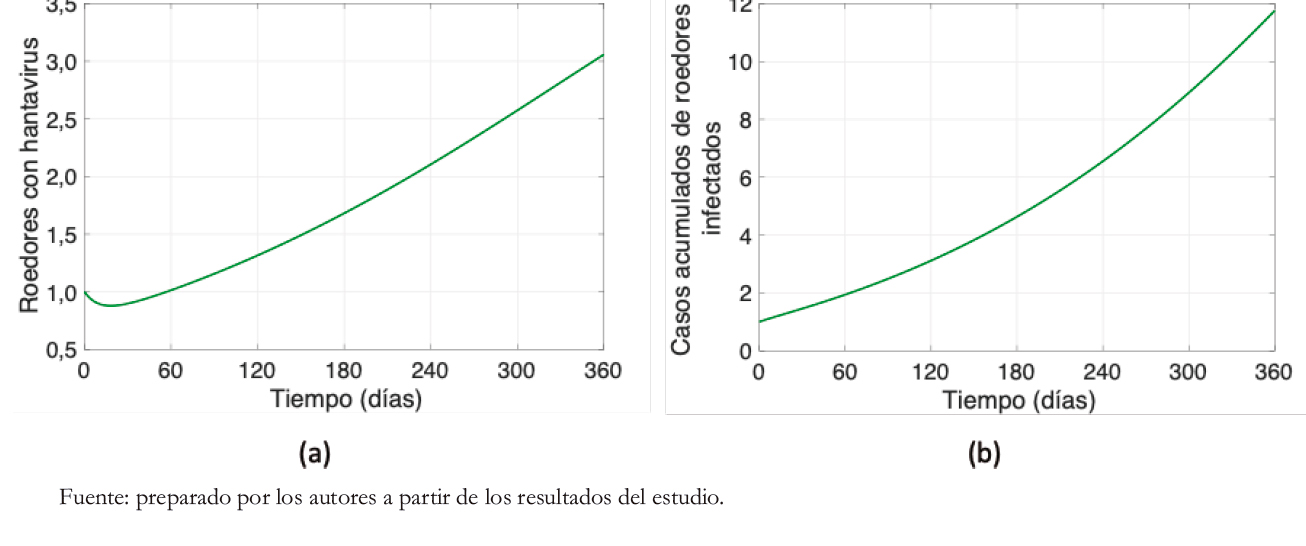 Figura 2. Dinámica del roedor.
Figura 2. Dinámica del roedor.

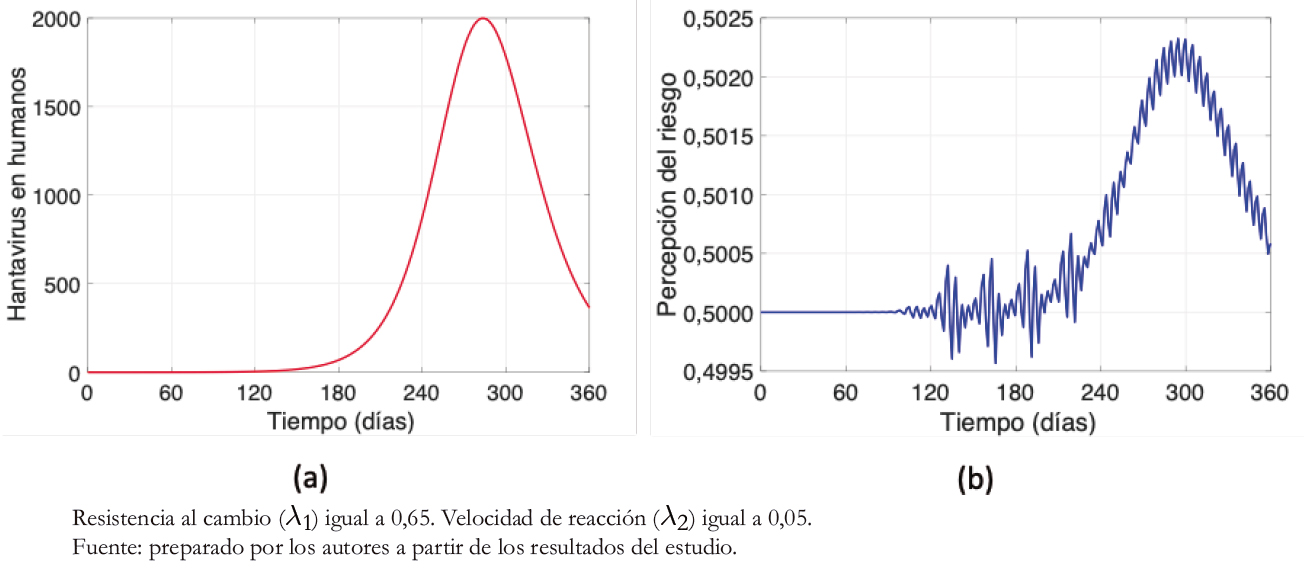 Figura 3. Casos de hantavirus y percepción del riesgo, con λ
Figura 3. Casos de hantavirus y percepción del riesgo, con λ

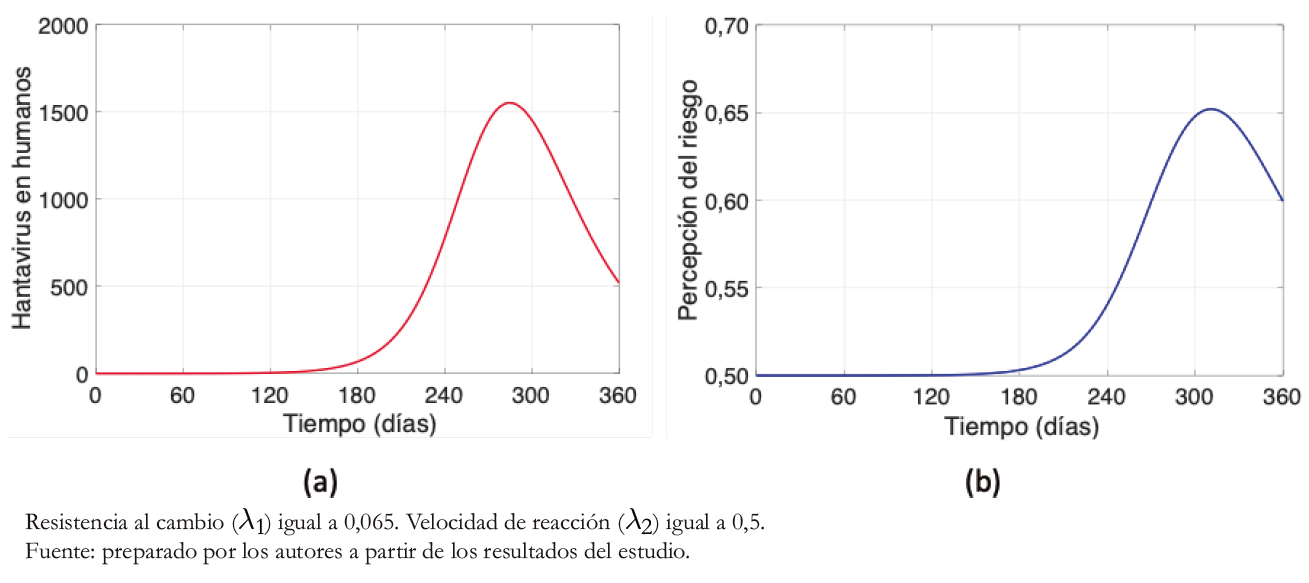 Figura 4. Casos de hantavirus y percepción del riesgo, con λ
Figura 4. Casos de hantavirus y percepción del riesgo, con λ

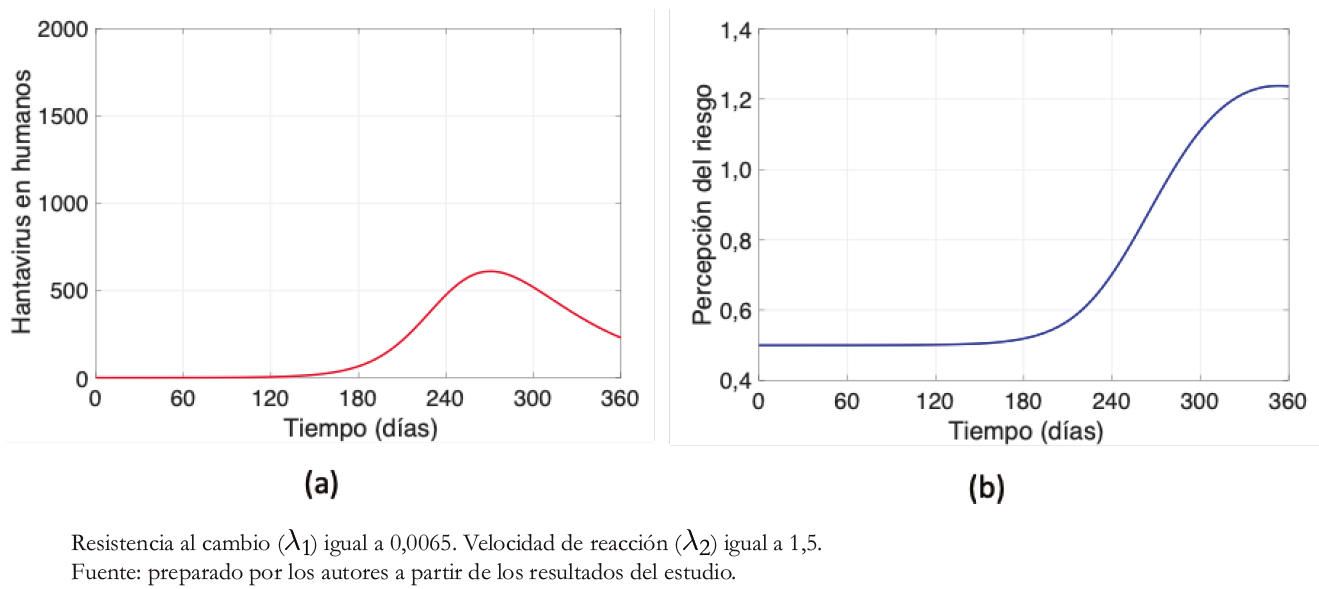 Figura 5. Casos de hantavirus y percepción del riesgo, con λ
Figura 5. Casos de hantavirus y percepción del riesgo, con λ

Introduction
Hantavirus cardiopulmonary syndrome is an infection caused by rodents of the Bunyanvirales family towards humans. This disease in Chile is considered endemic, which has a high fatality rate. At present, some studies show the contagion between people of the Andes virus, whose locality is concentrated in Argentina and Chile.
Objectives
Analyze the possibility of hantavirus transmission between humans using an SEIR-type mathematical model.
Methods
An SEIR (Susceptible, Exposed, Infectious and Recovered) mathematical model to express the dynamics of hantavirus disease is proposed, including the possibility of human-to-human transmission and the perception of risk.
Results
The peak of human-to-human contagion decreases by about 25% after increasing people’s perception of risk by reducing the rate of resistance to changeand increasing the speed of people’s reaction.
Conclusions
It is urgent to review risk communication strategies and prevention measures in the face of this possibility of massive human-tohuman infections, in addition to strengthening research and planning the development of a vaccine to protect populations exposed to this disease with a high fatality rate.
 Autores:
Juan Pablo Gutiérrez Jara[1], María Teresa Muńoz Quezada[2]
Autores:
Juan Pablo Gutiérrez Jara[1], María Teresa Muńoz Quezada[2]

Citación: Gutiérrez Jara JP, Muńoz Quezada MT. Modeling of hantavirus cardiopulmonary syndrome. Medwave 2022;22(3):e002526 doi: 10.5867/medwave.2022.03.002526
Fecha de envío: 7/9/2021
Fecha de aceptación: 1/3/2022
Fecha de publicación: 26/4/2022
Origen: No solicitado
Tipo de revisión: Con revisión por pares externa, por tres árbitros a doble ciego

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Kuhn JH, Adkins S, Alioto D, Alkhovsky SV, Amarasinghe GK, Anthony SJ, et al. 2020 taxonomic update for phylum Negarnaviricota (Riboviria: Orthornavirae), including the large orders Bunyavirales and Mononegavirales. Arch Virol. 2020;165: 3023–3072. | CrossRef | Link |
Kuhn JH, Adkins S, Alioto D, Alkhovsky SV, Amarasinghe GK, Anthony SJ, et al. 2020 taxonomic update for phylum Negarnaviricota (Riboviria: Orthornavirae), including the large orders Bunyavirales and Mononegavirales. Arch Virol. 2020;165: 3023–3072. | CrossRef | Link | Filippone C, Castel G, Murri S, Ermonval M, Korva M, Avšič-Županc T, et al. Revisiting the genetic diversity of emerging hantaviruses circulating in Europe using a pan-viral resequencing microarray. Sci Rep. 2019;9. | CrossRef | Link |
Filippone C, Castel G, Murri S, Ermonval M, Korva M, Avšič-Županc T, et al. Revisiting the genetic diversity of emerging hantaviruses circulating in Europe using a pan-viral resequencing microarray. Sci Rep. 2019;9. | CrossRef | Link | Ministerio de Salud, Gobierno de Chile. Boletín Epidemiológico Trimestral, Hantavirus. 2020. | CrossRef | Link |
Ministerio de Salud, Gobierno de Chile. Boletín Epidemiológico Trimestral, Hantavirus. 2020. | CrossRef | Link | Sabino-Santos G Jr, Maia FGM, Martins RB, Gagliardi TB, Souza WM de, Muylaert RL, et al. Natural infection of Neotropical bats with hantavirus in Brazil. Sci Rep. 2018;8.
| CrossRef | Link |
Sabino-Santos G Jr, Maia FGM, Martins RB, Gagliardi TB, Souza WM de, Muylaert RL, et al. Natural infection of Neotropical bats with hantavirus in Brazil. Sci Rep. 2018;8.
| CrossRef | Link | Departamento de Epidemiología, Ministerio de Salud de Chile. Síndrome Cardiopulmonar por Hantavirus. 2021. | Link |
Departamento de Epidemiología, Ministerio de Salud de Chile. Síndrome Cardiopulmonar por Hantavirus. 2021. | Link | Reyes Zaldívar FT, Ferrés M. Hantavirus: Descripción de dos décadas de endemia y su letalidad. ARS med. 2019;44: 30–39. | CrossRef | Link |
Reyes Zaldívar FT, Ferrés M. Hantavirus: Descripción de dos décadas de endemia y su letalidad. ARS med. 2019;44: 30–39. | CrossRef | Link | Alonso DO, Pérez-Sautu U, Bellomo CM, Prieto K, Iglesias A, Coelho R, et al. Person-to-Person Transmission of Andes Virus in Hantavirus Pulmonary Syndrome, Argentina, 2014. Emerg Infect Dis. 2020;26: 756–759.
| CrossRef | Link |
Alonso DO, Pérez-Sautu U, Bellomo CM, Prieto K, Iglesias A, Coelho R, et al. Person-to-Person Transmission of Andes Virus in Hantavirus Pulmonary Syndrome, Argentina, 2014. Emerg Infect Dis. 2020;26: 756–759.
| CrossRef | Link | Martínez VP, Di Paola N, Alonso DO, Pérez-Sautu U, Bellomo CM, Iglesias AA, et al. “Super-Spreaders” and Person-to-Person Transmission of Andes Virus in Argentina. N Engl J Med. 2020;383: 2230–2241.
| CrossRef | Link |
Martínez VP, Di Paola N, Alonso DO, Pérez-Sautu U, Bellomo CM, Iglesias AA, et al. “Super-Spreaders” and Person-to-Person Transmission of Andes Virus in Argentina. N Engl J Med. 2020;383: 2230–2241.
| CrossRef | Link | Allen LJS, McCormack RK, Jonsson CB. Mathematical models for hantavirus infection in rodents. Bull Math Biol. 2006;68: 511–24.
| CrossRef | Link |
Allen LJS, McCormack RK, Jonsson CB. Mathematical models for hantavirus infection in rodents. Bull Math Biol. 2006;68: 511–24.
| CrossRef | Link | Abramson G. Mathematical modelling of hantavirus: From the mean field to the individual level. Progress in Mathematical Biology Research; 2008.
| Link |
Abramson G. Mathematical modelling of hantavirus: From the mean field to the individual level. Progress in Mathematical Biology Research; 2008.
| Link | Bürger R, Chowell G, Gavilán E, Mulet P, Villada LM. Numerical solution of a spatio-temporal gender-structured model for hantavirus infection in rodents. Math Biosci Eng. 2018;15: 95–123.
| CrossRef | Link |
Bürger R, Chowell G, Gavilán E, Mulet P, Villada LM. Numerical solution of a spatio-temporal gender-structured model for hantavirus infection in rodents. Math Biosci Eng. 2018;15: 95–123.
| CrossRef | Link | Gedeon T, Bodelón C, Kuenzi A. Hantavirus transmission in sylvan and peridomestic environments. Bull Math Biol. 2010;72: 541–64.
| Link |
Gedeon T, Bodelón C, Kuenzi A. Hantavirus transmission in sylvan and peridomestic environments. Bull Math Biol. 2010;72: 541–64.
| Link | Liu JL. Threshold dynamics of a time-delayed hantavirus infection model in periodic environments. Math Biosci Eng. 2019;16: 4758–4776.
| CrossRef | Link |
Liu JL. Threshold dynamics of a time-delayed hantavirus infection model in periodic environments. Math Biosci Eng. 2019;16: 4758–4776.
| CrossRef | Link | Xiao Y, Zhang Y, Gao M. Modeling hantavirus infections in mainland China. Applied Mathematics and Computation. 2019;360: 28–41.
| CrossRef | Link |
Xiao Y, Zhang Y, Gao M. Modeling hantavirus infections in mainland China. Applied Mathematics and Computation. 2019;360: 28–41.
| CrossRef | Link | Wesley CL, Allen LJS, Langlais M. Models for the spread and persistence of hantavirus infection in rodents with direct and indirect transmission. Math Biosci Eng. 2010;7: 195–211.
| CrossRef | Link |
Wesley CL, Allen LJS, Langlais M. Models for the spread and persistence of hantavirus infection in rodents with direct and indirect transmission. Math Biosci Eng. 2010;7: 195–211.
| CrossRef | Link | Sauvage F, Langlais M, Pontier D. Predicting the emergence of human hantavirus disease using a combination of viral dynamics and rodent demographic patterns. Epidemiol Infect. 2007;135: 46–56.
| CrossRef | Link |
Sauvage F, Langlais M, Pontier D. Predicting the emergence of human hantavirus disease using a combination of viral dynamics and rodent demographic patterns. Epidemiol Infect. 2007;135: 46–56.
| CrossRef | Link | Nsoesie EO, Mekaru SR, Ramakrishnan N, Marathe MV, Brownstein JS. Modeling to predict cases of hantavirus pulmonary syndrome in Chile. Bausch DG, editor. PLoS Negl Trop Dis. 2014;8.
| CrossRef | Link |
Nsoesie EO, Mekaru SR, Ramakrishnan N, Marathe MV, Brownstein JS. Modeling to predict cases of hantavirus pulmonary syndrome in Chile. Bausch DG, editor. PLoS Negl Trop Dis. 2014;8.
| CrossRef | Link | Kermack WO, McKendrick AG. A Contribution to the Mathematical Theory of Epidemics. Proc R Soc A Math Phys Eng Sci. 1927;1: 700–21. | Link |
Kermack WO, McKendrick AG. A Contribution to the Mathematical Theory of Epidemics. Proc R Soc A Math Phys Eng Sci. 1927;1: 700–21. | Link | Kermack WO, McKendrick AG. Contributions to the mathematical theory of epidemics. II. —The problem of endemicity. Proc R Soc Lond A. 1997;138: 55–83.
| CrossRef | Link |
Kermack WO, McKendrick AG. Contributions to the mathematical theory of epidemics. II. —The problem of endemicity. Proc R Soc Lond A. 1997;138: 55–83.
| CrossRef | Link | Kermack WO, McKendrick AG. III. Further Studies of the Problem of Endemicity. Proc R Soc A Math Phys Eng Sci. 1933;3: 94–122. | CrossRef | Link |
Kermack WO, McKendrick AG. III. Further Studies of the Problem of Endemicity. Proc R Soc A Math Phys Eng Sci. 1933;3: 94–122. | CrossRef | Link | Córdova-Lepe FD, Gutiérrez Jara JP, Muńoz Quezada MT. An index to quantify individual social responsibility in the decision to be vaccinated. Medwave. 2018;18: e7237. | CrossRef |
Córdova-Lepe FD, Gutiérrez Jara JP, Muńoz Quezada MT. An index to quantify individual social responsibility in the decision to be vaccinated. Medwave. 2018;18: e7237. | CrossRef | Córdova-Lepe F, Cabrera Hernández M, Gutiérrez-Jara JP. Modeling the epidemiological impact of a preventive behavioral group. Medwave. 2018;18: e7396–e7396.
| CrossRef | Link |
Córdova-Lepe F, Cabrera Hernández M, Gutiérrez-Jara JP. Modeling the epidemiological impact of a preventive behavioral group. Medwave. 2018;18: e7396–e7396.
| CrossRef | Link | Cabrera M, Córdova-Lepe F, Gutiérrez-Jara JP, Vogt-Geisse K. An SIR-type epidemiological model that integrates social distancing as a dynamic law based on point prevalence and socio-behavioral factors. Sci Rep. 2021;11. | CrossRef | Link |
Cabrera M, Córdova-Lepe F, Gutiérrez-Jara JP, Vogt-Geisse K. An SIR-type epidemiological model that integrates social distancing as a dynamic law based on point prevalence and socio-behavioral factors. Sci Rep. 2021;11. | CrossRef | Link | Muńoz-Quezada MT, Lucero BA, Gutiérrez-Jara JP, Buralli RJ, Zúńiga-Venegas L, Muńoz MP, et al. Longitudinal exposure to pyrethroids (3-PBA and trans-DCCA) and 2,4-D herbicide in rural schoolchildren of Maule region, Chile. Sci Total Environ. 2020;749: 141512.
| CrossRef | Link |
Muńoz-Quezada MT, Lucero BA, Gutiérrez-Jara JP, Buralli RJ, Zúńiga-Venegas L, Muńoz MP, et al. Longitudinal exposure to pyrethroids (3-PBA and trans-DCCA) and 2,4-D herbicide in rural schoolchildren of Maule region, Chile. Sci Total Environ. 2020;749: 141512.
| CrossRef | Link | Ministerio de Salud del Gobierno de Chile. Guía clínica de prevención, diagnóstico y tratamiento del Síndrome Cardiopilmonar por Hantavirus. 2013.
| Link |
Ministerio de Salud del Gobierno de Chile. Guía clínica de prevención, diagnóstico y tratamiento del Síndrome Cardiopilmonar por Hantavirus. 2013.
| Link | Paek H-J, Hove T. Risk Perceptions and Risk Characteristics. Oxford University Press; 2017.
| CrossRef | Link |
Paek H-J, Hove T. Risk Perceptions and Risk Characteristics. Oxford University Press; 2017.
| CrossRef | Link | MacDonald G. The Measurement of Malaria Transmission. Proceedings of the Royal Society of Medicine. 2016;48: 295–302.
| CrossRef | Link |
MacDonald G. The Measurement of Malaria Transmission. Proceedings of the Royal Society of Medicine. 2016;48: 295–302.
| CrossRef | Link | Simoy MI, Aparicio JP. Ross-Macdonald models: Which one should we use? Acta Trop. 2020;207: 105452.
| CrossRef | Link |
Simoy MI, Aparicio JP. Ross-Macdonald models: Which one should we use? Acta Trop. 2020;207: 105452.
| CrossRef | Link | van den Driessche P, Watmough J. Reproduction numbers and sub-threshold endemic equilibria for compartmental models of disease transmission. Math Biosci. 2002;180: 29–48.
| CrossRef | Link |
van den Driessche P, Watmough J. Reproduction numbers and sub-threshold endemic equilibria for compartmental models of disease transmission. Math Biosci. 2002;180: 29–48.
| CrossRef | Link | Gutiérrez-Jara JP, Córdova-Lepe FD, Muńoz-Quezada MT. Dynamics between infectious diseases with two susceptibility conditions: A mathematical model. Math Biosci. 2019;309: 66–77. | CrossRef | Link |
Gutiérrez-Jara JP, Córdova-Lepe FD, Muńoz-Quezada MT. Dynamics between infectious diseases with two susceptibility conditions: A mathematical model. Math Biosci. 2019;309: 66–77. | CrossRef | Link | MINSAL, Gobierno de Chile. Instituto Nacional de Estadísticas - Estadísticas vitales. 2018.
| Link |
MINSAL, Gobierno de Chile. Instituto Nacional de Estadísticas - Estadísticas vitales. 2018.
| Link | Boada-Cuerva M, Boada-Grau J, Prizmic-Kuzmica AJ, De Diego NG, Vigil-Colet A. RTC-11: Adaptación de la escala de resistencia al cambio en dos países (Espańa y Argentina). AN PSICOL-SPAIN. 2018;34: 360.
| CrossRef | Link |
Boada-Cuerva M, Boada-Grau J, Prizmic-Kuzmica AJ, De Diego NG, Vigil-Colet A. RTC-11: Adaptación de la escala de resistencia al cambio en dos países (Espańa y Argentina). AN PSICOL-SPAIN. 2018;34: 360.
| CrossRef | Link | Organización de las Naciones Unidas para la Alimentación y la Agricultura. Biología general de los roedores. FAO;
| Link |
Organización de las Naciones Unidas para la Alimentación y la Agricultura. Biología general de los roedores. FAO;
| Link | Wilson TM, Paddock CD, Reagan-Steiner S, Bhatnagar J, Martines RB, Wiens AL, et al. Intersecting Paths of Emerging and Reemerging Infectious Diseases. Emerg Infect Dis. 2021;27: 1517–1519. | CrossRef | Link |
Wilson TM, Paddock CD, Reagan-Steiner S, Bhatnagar J, Martines RB, Wiens AL, et al. Intersecting Paths of Emerging and Reemerging Infectious Diseases. Emerg Infect Dis. 2021;27: 1517–1519. | CrossRef | Link | Khan A, Khan M, Ullah S, Wei D-Q. Hantavirus: The Next Pandemic We Are Waiting For? Interdiscip Sci. 2021;13: 147–152. | CrossRef | Link |
Khan A, Khan M, Ullah S, Wei D-Q. Hantavirus: The Next Pandemic We Are Waiting For? Interdiscip Sci. 2021;13: 147–152. | CrossRef | Link | Kim W-K, Cho S, Lee S-H, No JS, Lee G-Y, Park K, et al. Genomic Epidemiology and Active Surveillance to Investigate Outbreaks of Hantaviruses. Front Cell Infect Microbiol. 2020;10.
| CrossRef | Link |
Kim W-K, Cho S, Lee S-H, No JS, Lee G-Y, Park K, et al. Genomic Epidemiology and Active Surveillance to Investigate Outbreaks of Hantaviruses. Front Cell Infect Microbiol. 2020;10.
| CrossRef | Link | Prist PR, Uriarte M, Fernandes K, Metzger JP. Climate change and sugarcane expansion increase Hantavirus infection risk. Munoz-Zanzi C, editor. PLoS Negl Trop Dis. 2017;11.
| CrossRef | Link |
Prist PR, Uriarte M, Fernandes K, Metzger JP. Climate change and sugarcane expansion increase Hantavirus infection risk. Munoz-Zanzi C, editor. PLoS Negl Trop Dis. 2017;11.
| CrossRef | Link | Carbajo AE, Vera C, González PL. Hantavirus reservoir Oligoryzomys longicaudatus spatial distribution sensitivity to climate change scenarios in Argentine Patagonia. Int J Health Geogr. 2009;8.
| CrossRef | Link |
Carbajo AE, Vera C, González PL. Hantavirus reservoir Oligoryzomys longicaudatus spatial distribution sensitivity to climate change scenarios in Argentine Patagonia. Int J Health Geogr. 2009;8.
| CrossRef | Link | Watson DC, Sargianou M, Papa A, Chra P, Starakis I, Panos G. Epidemiology of Hantavirus infections in humans: A comprehensive, global overview. Crit Rev Microbiol. 2014;40: 261–72. | CrossRef | Link |
Watson DC, Sargianou M, Papa A, Chra P, Starakis I, Panos G. Epidemiology of Hantavirus infections in humans: A comprehensive, global overview. Crit Rev Microbiol. 2014;40: 261–72. | CrossRef | Link | Valdivieso F, Gonzalez C, Najera M, Olea A, Cuiza A, Aguilera X, et al. Knowledge, attitudes, and practices regarding hantavirus disease and acceptance of a vaccine trial in rural communities of southern Chile. Hum Vaccin Immunother. 2017;13: 808–815.
| CrossRef | Link |
Valdivieso F, Gonzalez C, Najera M, Olea A, Cuiza A, Aguilera X, et al. Knowledge, attitudes, and practices regarding hantavirus disease and acceptance of a vaccine trial in rural communities of southern Chile. Hum Vaccin Immunother. 2017;13: 808–815.
| CrossRef | Link |