Este texto completo es la transcripción editada y revisada de la conferencia dictada en Simposio organizado por Laboratorios Wyeth.
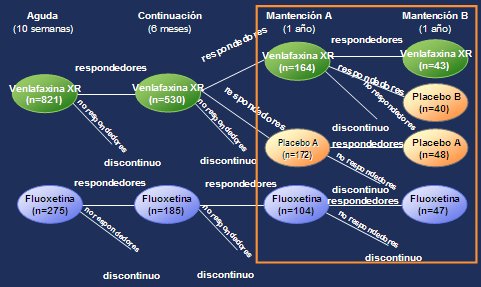
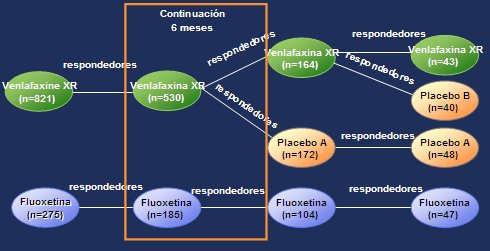
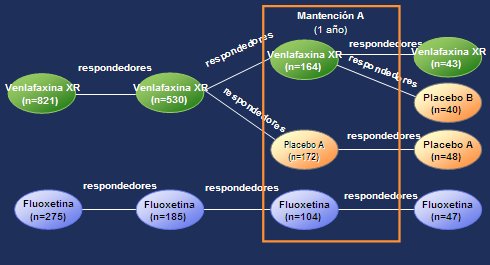
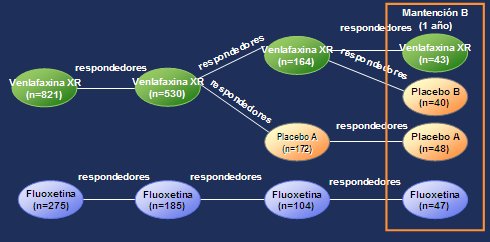
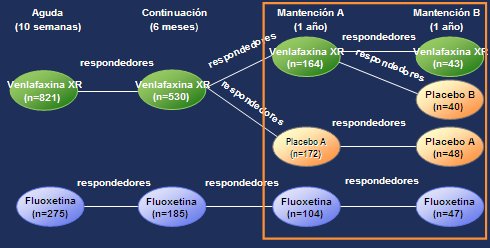
Figura 1. Diseńo del estudio PREVENT
Los pacientes que tuvieron respuesta terapéutica satisfactoria o remisión luego de 36 semanas de tratamiento, fuera con venlafaxina XR o con fluoxetina, durante las fases aguda y de continuación, ingresaron a la fase de mantención A, en cuyo inicio, aquellos pacientes que habían respondido a venlafaxina XR al final de la fase de continuación se asignaron, mediante sistema doble ciego, para recibir venlafaxina XR o placebo.
Los pacientes que continuaron respondiendo a fluoxetina al final de la fase de continuación permanecieron en tratamiento doble ciego con fluoxetina durante la fase de mantención A; debido a que este grupo no fue reasignado durante las fases de mantención, sólo se puede hacer la comparación entre venlafaxina XR y placebo y no se puede hacer comparación alguna entre venlafaxina XR y fluoxetina. El grupo con fluoxetina siguió como un grupo de referencia durante las fases de mantención. Tanto los pacientes como los investigadores permanecieron “ciegos” a la asignación del tratamiento.
Los pacientes que progresaron a la fase de mantención B habían demostrado una respuesta terapéutica satisfactoria o remisión al terminar la fase de mantención A, ya sea usando tratamiento con venlafaxina XR, placebo o fluoxetina. Al inicio de la fase de mantención B, los pacientes que estaban recibiendo venlafaxina XR y habían continuado con respuesta terapéutica satisfactoria o con remisión al terminar la fase de mantención A, fueron asignados en forma aleatoria para recibir venlafaxina XR o placebo (en adelante, grupo placebo B) durante 12 meses adicionales, en la fase de mantención B. Los pacientes que siguieron respondiendo al placebo (en adelante, grupo placebo A) al terminar la fase de mantención A, continuaron con placebo por 12 meses más en la fase de mantención B.
Los pacientes que continuaron respondiendo a fluoxetina al final de la fase de mantención A continuaron con un tratamiento doble ciego con fluoxetina por 12 meses adicionales en la fase de mantención B, como grupo de referencia.
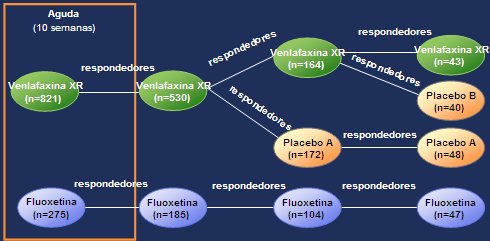
Figura 2. Fase aguda
La fase de continuación de seis meses, en la que participaron los pacientes que alcanzaron los criterios de respuesta terapéutica satisfactoria o remisión en la fase aguda, tuvo como objetivo principal comparar la eficacia de venlafaxina XR y fluoxetina para mantener la respuesta terapéutica satisfactoria o la remisión que se lograron en la etapa anterior.
Las fases de mantención A y B, conformadas por pacientes que respondieron o remitieron durante la fase de continuación y que fueron reasignados aleatoriamente para recibir placebo o venlafaxina XR, tuvieron como objetivo principal comparar la eficacia de venlafaxina XR y placebo para prevenir recurrencias de depresión mayor, en pacientes con trastorno depresivo recurrente que fueron respondedores al inicio de cada fase de mantención.
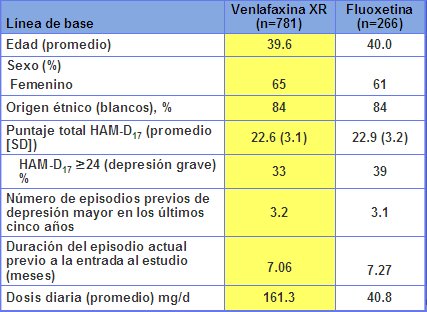
Tabla I. Línea de base. Características de la fase aguda
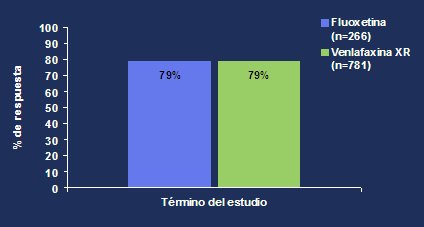
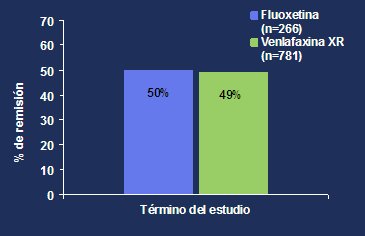
La tasa de respuesta terapéutica satisfactoria en la fase aguda, tanto para fluoxetina como para venlafaxina XR, fue de 79%, con p=0,841 (Fig. 7). Al término de esta fase, 50% de los pacientes que recibió fluoxetina logró la remisión versus 49% en el grupo que recibió venlafaxina XR. No hubo diferencias significativas entre los dos grupos, con p=0,719 (Fig. 8).
Figura 3. Porcentaje de respuesta en la fase aguda al término del estudio
Figura 4. Porcentaje de remisión en la fase aguda al término del estudio
Figura 5. Fase de continuación
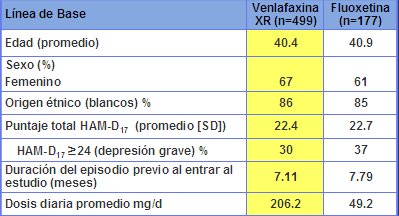
Tabla II. Línea de base. Características de la fase de continuación
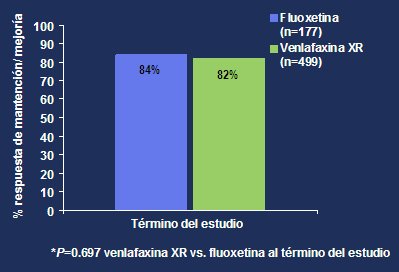
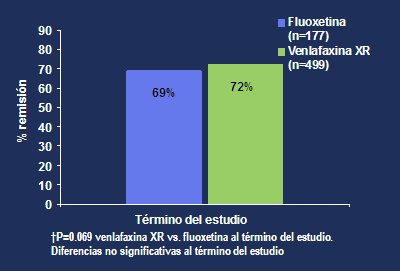
La tasa de respuesta fue 82% en el grupo de venlafaxina XR y 84% en el grupo de fluoxetina. No hubo diferencias significativas al comparar los dos grupos (p=0,697) (Fig. 10). Al final de esta fase del estudio, 72% de los pacientes que recibieron venlafaxina lograron la remisión, versus 69% de los pacientes del grupo que recibió fluoxetina; tampoco hubo diferencias significativas al comparar los dos grupos (p=0,069).
Figura 6. Porcentaje de respuesta mantención/mejoría en la fase de continuación, al término del estudio
Figura 7. Porcentaje de remisión de la fase de continuación al término del estudio
Figura 8. Fase de mantención A
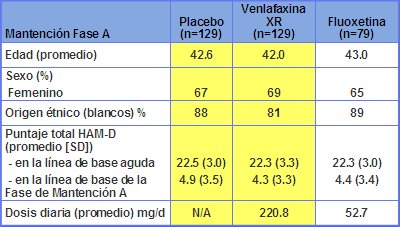
Los tres grupos de pacientes de la fase de mantención A tenían características demográficas comparables: se trató principalmente de mujeres de raza blanca, de 40 ańos de edad promedio; las dosis diarias promedio fueron 221 mg de venlafaxina XR y 53 mg de fluoxetina (Tabla IV).
Tabla III. Línea de base. Características de la fase de mantención A
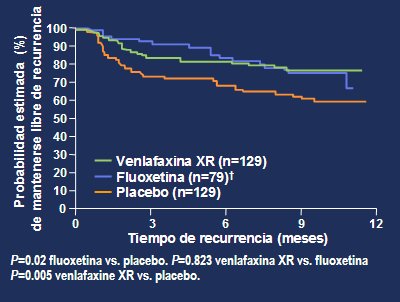
Con base en la definición primaria de recurrencia, hubo significativamente menor probabilidad de sufrir una recurrencia a los 12 meses con venlafaxina XR que con placebo: la probabilidad de prevenir un nuevo episodio de depresión al ańo de tratamiento fue de 77% con venlafaxina XR versus 58% usando placebo (Fig. 13). Como se ha mencionado, debido al diseńo del estudio el grupo de fluoxetina se incluyó en esta fase sólo como un grupo de referencia.
Figura 9. Probabilidad estimada de mantenerse libre de recurrencias. Fase de mantención A
Figura 10. Fase de mantención B
Los pacientes que continuaron respondiendo a fluoxetina (n=47) continuaron en tratamiento con fluoxetina durante los 12 meses que duró la fase de mantención B. En esta oportunidad tampoco se reasignó al grupo tratado con fluoxetina, por lo que no se pueden hacer comparaciones entre venlafaxina XR y fluoxetina. Los pacientes de esta fase se seleccionaron por su respuesta continua usando venlafaxina XR, placebo o fluoxetina y estos tres grupos fueron similares en aspectos demográficos y otras características de base.
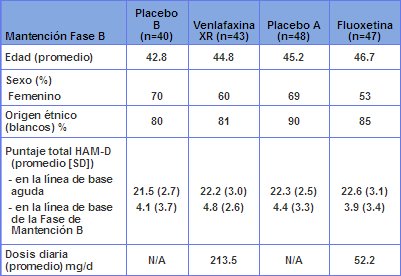
La Tabla V muestra la edad promedio y la predominancia de población femenina de raza blanca. Además se muestran los puntajes basales HAM-D17, tanto de la fase aguda como en la fase de mantención y la dosis promedio que se utilizó en cada uno de los grupos.
Tabla IV. Línea de base. Fase de mantención B
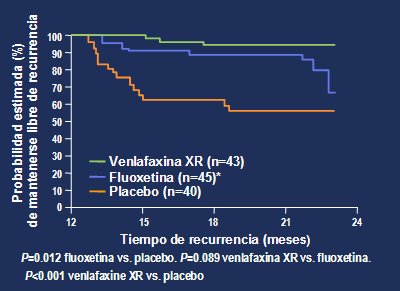
De acuerdo con la definición primaria de recurrencia, hubo menor probabilidad de recurrencia a los seis meses y mayor tiempo libre de recurrencia al mes 12 con venlafaxina XR que con placebo: la probabilidad de prevenir un nuevo episodio fue de 92% usando venlafaxina XR durante el ańo 2 de mantención, versus 55% usando placebo (Fig. 15). Por las razones mencionadas, no se pueden hacer comparaciones entre venlafaxina XR y fluoxetina.
Figura 11. Probabilidad estimada de mantenerse libre de recurrencias. Fase de mantención B
Figura 12. Fase de mantención A y B combinadas
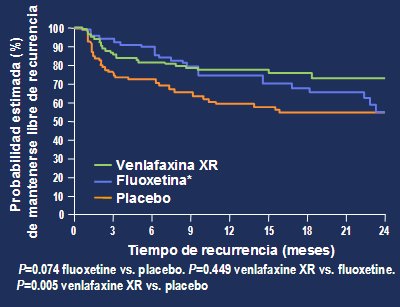
La probabilidad acumulada de prevenir un nuevo episodio de depresión fue de 72% usando venlafaxina XR y de 53% usando placebo (Fig. 17).
Figura 13. Probabilidad estimada de mantenerse libre de recurrencias. Fase de mantención A y B combinadas.
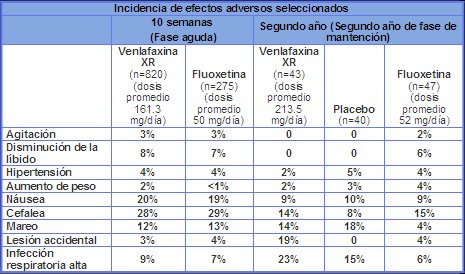
Tabla V. Incidencia de efectos adversos seleccionados
Se desconoce si la dosis de venlafaxina/venlafaxina XR que se necesita para el tratamiento de mantención es idéntica a la necesaria para lograr una respuesta inicial.
Tabla VI. PREVENT. Resumen de resultados
La edición y publicación de esta conferencia han sido posibles gracias al auspicio de Laboratorio Wyeth.
Medwave Ańo VII, No. 8, Septiembre 2007. Derechos Reservados.




















 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de la conferencia dictada en Simposio organizado por Laboratorios Wyeth.
 Expositor:
Philip Ninan[1]
Expositor:
Philip Ninan[1]

Citación: Ninan P. Long-term management of major depressive illness (II) - PREVENT Study. Medwave 2007 Sep;7(8):e2457 doi: 10.5867/medwave.2007.08.2457
Fecha de publicación: 1/7/2009

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión