La publicaci¾n de estas Actas CientĒficas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y la Sociedad Chilena de NefrologĒa.
Esta presentaci¾n consiste en una revisi¾n de los conceptos mßs relevantes de la insuficiencia renal como problema de salud, en relaci¾n a los siguientes aspectos: enfermedad renal cr¾nica como problema de salud; situaci¾n de la VII regi¾n; herramientas para el manejo del problema y estrategia de manejo.
La prevalencia y la incidencia de la insuficiencia renal cr¾nica (IRC) estßn aumentando en todo el mundo en forma cada vez mßs acelerada, fen¾meno que tambiķn ocurre en Chile.
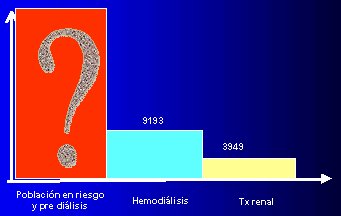
Seg·n datos de la Sociedad Chilena de NefrologĒa, en nuestro paĒs existen 3.949 pacientes transplantados renales, de los cuales se conoce su evoluci¾n, cußndo se complican, cußndo se infectan y su domicilio. Ademßs, en Agosto de 2003 existĒan 9.193 pacientes en hemodißlisis, de quienes tambiķn se conoce la mortalidad, los tratamientos que reciben, los que estßn con eritropoyetina, etc.
Estos datos se ilustran en la figura 1, en la que se puede ver que existe una gran poblaci¾n en riesgo, predißlisis, que ya ha iniciado una enfermedad renal cr¾nica, y que representa el problema futuro del paĒs.
Los mķdicos suelen poner poca atenci¾n a esta poblaci¾n de pacientes que ya tiene enfermedad renal cr¾nica, es decir, una creatininemia de 1,5 mg/dl y mßs, cuya verdadera magnitud es prßcticamente desconocida. En la figura 2 se muestra una estimaci¾n del n·mero de personas que existen en Chile con IRC en sus distintas etapas.
Figura 1. Poblaci¾n en hemodißlisis y transplante renal y estimaci¾n de poblaci¾n en riesgo. Datos del Registro de Dißlisis de la Sociedad Chilena de NefrologĒa, 2003.
Figura 2. Prevalencia de IRC, por etapas, en Chile. Estimaci¾n seg·n Censo de 2002.
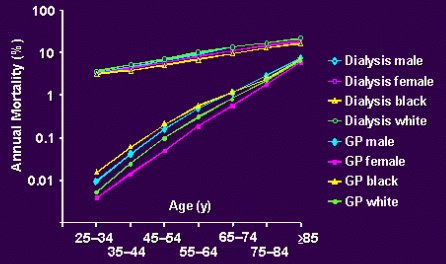
Los mķdicos se preocupan de los pacientes con enfermedad renal cr¾nica por varios factores. Primero, porque produce gran mortalidad a cualquier edad, siendo 20 veces mayor en pacientes j¾venes, pero a cualquier edad, sexo y raza, el hecho de tener insuficiencia renal aumenta el riesgo de morir de un infarto, como se muestra claramente en el grßfico de la figura 3.
Figura 3. Mortalidad cardiovascular en la poblaci¾n general (National Center for Health Statistics) y en pacientes con IRC terminal en dißlisis (Renal Data System de los Estados Unidos).
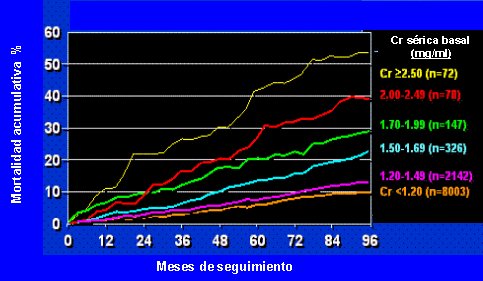
Se sabe desde hace a±os que el hecho de tener una creatininemia mßs alta aumenta la tasa de mortalidad acumulativa por infarto, y que el corte, a nivel poblacional, estß en los niveles mayores de 1,5 mg/dl (vķase figura 4).
Figura 4. Nivel de creatinina como predictor de mortalidad (adaptado de Shulman NB, Hypertension 1989).
Si se analiza desde el punto de vista de la salud p·blica, se sabe que el hßbito de fumar, la hipertensi¾n arterial y la diabetes mellitus son factores de riesgo cardiovascular, pero la creatininemia alta es un factor de riesgo cardiovascular que tiene tanta importancia como la diabetes.
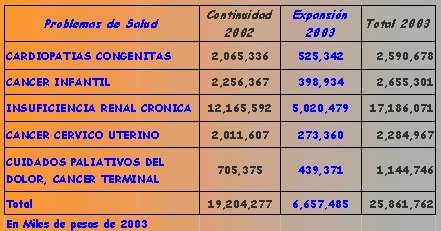
Ademßs, la insuficiencia renal en su fase terminal produce un aumento de los costos. Del dinero destinado al AUGE en el a±o 2003, 25 millones se fueron al servicio de salud, y de ese monto la IRC ocup¾ 17 millones, cifra que va en aumento. Los datos se pueden ver en detalles en la tabla I.
Tabla I. Recursos financieros piloto AUGE. Estimado a±o 2003.
El mayor nivel de creatinina plasmßtica tambiķn se correlaciona con un aumento del riesgo de utilizar camas hospitalarias. Por otra parte, en un trabajo espa±ol, que incluy¾ pocos casos, se observ¾ una diferencia significativa en la sobrevida a 48 meses entre el grupo de pacientes con ingreso programado a dißlisis y el grupo de ingreso no programado (NefrologĒa 2002; 22:49-59).
En suma, la IRC produce una gran mortalidad, por un lado, y por otro, si los pacientes llegan de manera tardĒa a la dißlisis, disminuye su sobrevida.
Ademßs de los problemas epidemiol¾gicos, existe una dificultad importante para establecer quķ significa la insuficiencia renal, existiendo distintas denominaciones en la literaura de habla inglesa para referirse a ella, lo que dificulta los intentos de realizar estudios comparativos. Igualmente, a la hora de establecer cortes para catalogar a un paciente como insuficiente renal, existen varias definiciones, basadas en la creatinina sķrica, el clearance de creatinina, el nitr¾geno ureico y la hemodißlisis, factor que tambiķn dificulta la comparaci¾n.
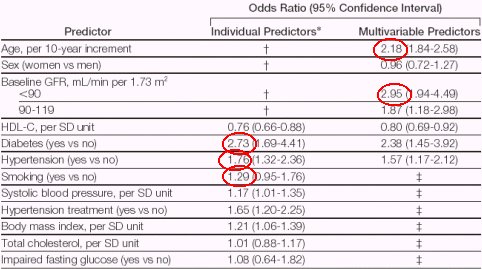
En un estudio publicado en la revista JAMA en 2004, en el que se incluyeron casi 3.000 pacientes catalogados como poblaci¾n sana, que fueron seguidos durante 18 a±os, se describen los hallazgos en el primer corte, que se hizo a los 41 a±os en promedio, y el segundo corte del seguimiento, que se efectu¾ a los 65 a±os (Figura 5).
Se encontr¾ que el riesgo de desarrollar insuficiencia renal en 18 a±os se doblaba con cada 10 a±os de incremento en la edad, se triplicaba si el sujeto partĒa con una funci¾n renal menor de 90 ml/min por 1,73 m2 y casi se triplicaba si era diabķtico. La hipertensi¾n aportaba un riesgo de 1,76 y otro factor de riesgo importante era el hßbito de fumar (1,29).
Lo interesante de este trabajo es que se hizo en una poblaci¾n sin da±o renal que fue seguida durante 18 a±os, en la que se pudo medir el valor predictivo de cada una de las variables, destacando la edad, el clearance inicial, la diabetes, la hipertensi¾n arterial y el hßbito de fumar, llamando la atenci¾n el hecho de que el tratamiento de la hipertensi¾n no alteraba el pron¾stico de desarrollar da±o renal, en comparaci¾n con no realizar tratamiento.
Figura 5. Anßlisis de predictores de desarrollo de enfermedad renal individual y multivariable; 18 a±os de seguimiento.
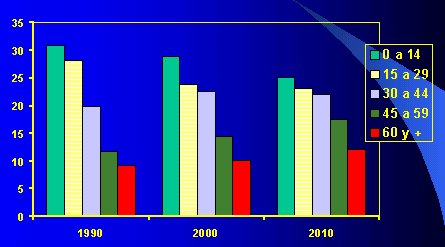
En cuanto a la edad, en la figura 6 se observa que un alto porcentaje de la poblaci¾n estimada para el 2010 serß mayor de 45 a±os y que mßs del 12% tendrß 60 a±os y mßs, es decir, va a aumentar la poblaci¾n de alto riesgo de da±o renal cr¾nico, mientras que los pacientes pedißtricos tenderßn a desaparecer, lo que se correlaciona con el hecho de que las camas pedißtricas han disminuido en todo Chile, por su bajo uso.
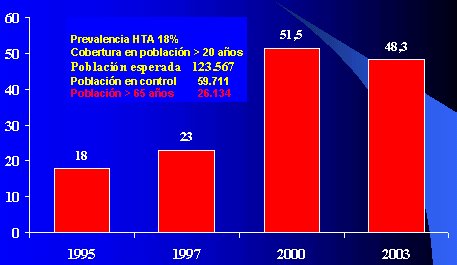
En lo que se refiere a la hipertensi¾n arterial, la prevalencia oscila en torno al 18%, incluyendo a los mayores de 20 a±os del sector p·blico y privado, lo que corresponderĒa a 123.567 pacientes; sin embargo, s¾lo 59.711 estßn bajo control. Existen 26.134 mayores de 65 a±os, siendo importante recordar que la edad y la hipertensi¾n son factores de riesgo importantes (vķase figura 7).
Figura 6. Evoluci¾n de la estructura de edad de la poblaci¾n. Chile, VII Regi¾n.
En lo que se refiere a la hipertensi¾n arterial, la prevalencia oscila en torno al 18%, incluyendo a los mayores de 20 a±os del sector p·blico y privado, lo que corresponderĒa a 123.567 pacientes; sin embargo, s¾lo 59.711 estßn bajo control. Existen 26.134 mayores de 65 a±os, siendo importante recordar que la edad y la hipertensi¾n son factores de riesgo importantes (vķase figura 7).
Figura 7. Cobertura de la hipertensi¾n arterial. Servicio de Salud del Maule, Chile, VII Regi¾n.
En ese mismo trabajo se estudiaron los factores acumulativos, aumentando el riesgo de desarrollar insuficiencia renal en presencia de dos factores, de manera tal que, en una de las poblaciones de la VII regi¾n, se puede esperar un crecimiento importante de los pacientes que van a requerir dißlisis dentro de los pr¾ximos seis a±os.
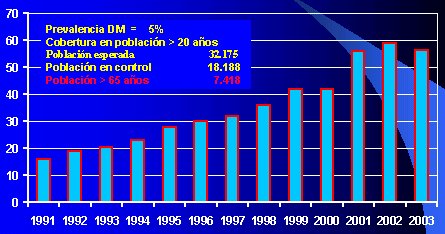
Sobre la Diabetes Mellitus, el estudio del Ministerio de Salud informa que los diabķticos chilenos corresponden a 2,5 a 3% de la poblaci¾n. En la sķptima regi¾n se realiz¾ un estudio de prevalencia de diabetes, que arroj¾ una prevalencia de 5%, es decir, el doble de lo estimado por el ministerio, por lo que se espera una poblaci¾n de 32.000, estando en control 18.188 pacientes y una poblaci¾n mayor de 65 a±os de 7.418 (vķase figura 8). Por lo tanto, en seis a±os mßs va a existir una cantidad importante de pacientes a±osos que requerirßn dißlisis, a un costo elevado.
Figura 8. Cobertura de la Diabetes Mellitus. Servicio Salud del Maule, Chile, VII Regi¾n.1991-2003.
En cuanto a costos, en la medida en que la expectativa de vida aumenta, aumenta el gasto en salud, y aunque despuķs de los 65 a±os la expectativa de vida no aumenta mayormente, este gasto sigue incrementßndose en forma permanente. La VII regi¾n y el paĒs estßn entrando en esta etapa, por lo tanto, aunque el Ministerio indique que se debe mejorar la eficacia, no existe la posibilidad de que los gastos disminuyan.
A nivel nacional, se gastan 55 mil millones de pesos en 9.113 pacientes. En la VII regi¾n hay 420 pacientes, 60 de ellos hospitalizados, y 75% del dinero destinado al AUGE se gasta en ellos.
Desde el punto de vista de camas, es la tercera causa de hospitalizaci¾n en el Servicio de Medicina, estando en primer lugar los accidentes vasculares y luego los linfomas, (que ingresan muchas veces para recibir los ciclos), aunque los insuficientes renales, con el AUGE, estßn comenzando a desplazarse hacia el segundo lugar.
Por lo tanto, el paĒs tiene un problema importante, y si bien es cierto que se han dado pasos para resolverlo, se parti¾ asegurando la dißlisis y no cuidando a los que estßn en riesgo de desarrollar la enfermedad a futuro, lo que es comparable a que, en el manejo de la cardiopatĒa coronaria, se hubiesen construido muchas unidades coronarias y no se hubieran manejado primero los factores de riesgo, como la hipertensi¾n y la diabetes.
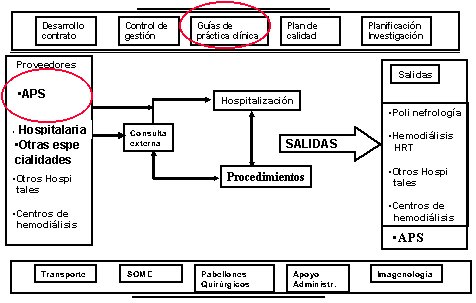
Para enfrentar este problema, lo primero es conocer el mapa de procesos de NefrologĒa, que se resume en la figura 9, donde se ve que el anßlisis desde el punto de vista clĒnico, la mayorĒa de la veces se centra en la consulta externa, en la que se deciden la hospitalizaci¾n y los procedimientos, con una salida, que en el caso de la nefrologĒa hospitalaria y de especialidad, va hacia el policlĒnico de nefrologĒa, la hemodißlisis, el Hospital Regional de Talca (VII regi¾n) u otros hospitales seg·n corresponda, hacia otros centros de dißlisis y hacia la atenci¾n primaria de salud, porque al igual que en el caso de los diabķticos o hipertensos, no todos los enfermos pueden ser atendidos por el especialista.
Figura 9. Mapa de procesos en NefrologĒa.
Este proceso debe ser dise±ado, guiado y controlado por varios elementos:
Cuando los mķdicos planifican, no siempre desarrollan una metodologĒa de investigaci¾n correcta; los centros pueden asesorarla y revisarla. Los pacientes provienen de la atenci¾n primaria de salud, de otras unidades de los hospitales, de otras especialidades y centros de dißlisis.
Tambiķn se necesita el apoyo logĒstico: transporte, SOME, pabellones quir·rgicos, apoyo administrativo y de imßgenes. Si no estßn presentes todos estos factores, los resultados son pobres, invirtiķndose muchos recursos en tratar de solucionar el problema de imßgenes, c¾mo tratar a los enfermos, c¾mo conseguirse pabellones para realizar fĒstulas, etc. Para solucionar el problema se±alado, son ·tiles las guĒas de prßctica clĒnica, destinadas fundamentalmente a la atenci¾n primaria de salud.
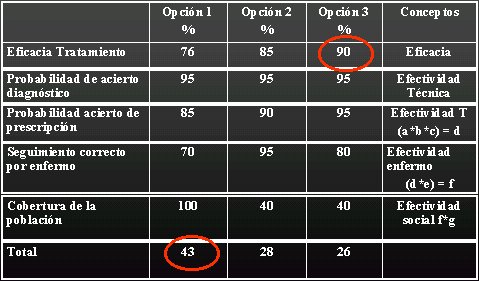
Ademßs, habrĒa que buscar un instrumento para determinar la eficacia del tratamiento, existiendo distintas opciones, con distintas eficacias. La tabla II es un ejemplo de los parßmetros que se utilizan para evaluar las terapias en los centros importantes, existiendo siempre un nivel de incertidumbre con respecto a lo que ocurrirß en la aplicaci¾n prßctica final.
En estas evaluaciones se determina la ōeficacia clĒnicaö, que estß dada por las probabilidades de acierto diagn¾stico que se tienen al usar una opci¾n determinada y por la probabilidad de acierto en la prescripci¾n, que da la ōefectividad tķcnicaö y por el seguimiento correcto del enfermo (┐se toma los fßrmacos?), que es de 70, 95 y 80% en las opciones 1, 2 y 3, respectivamente, y que da lugar a la llamada ōefectividad del enfermoö. A esto se agrega la cobertura de la poblaci¾n, que alcanza al 100% en la opci¾n 1 y s¾lo a 40% en las opciones restantes, obteniķndose totales distintos en las diferentes opciones.
En este caso, se parti¾ con la opci¾n 3 como elecci¾n primaria, por su alta efectividad clĒnica (90%), pero al aplicar el resto de los criterios se determin¾ que la mejor opci¾n desde el punto de vista del impacto era la opci¾n 1, por lo tanto, esta ·ltima constituye una opci¾n de primera lĒnea, porque cumple con todos los requisitos: fßcil, simple y se aplica a una gran poblaci¾n.
Tabla II. Complejidad sanitaria creciente; nivel de incertidumbre.
La Kidney Disease Outcomes Quality Initiative (K/DOQI) ha establecido guĒas acerca de cuatro objetivos importantes a conseguir en la enfermedad renal, y al menos en tres revistas destacadas han aparecido editoriales reafirmando la importancia que tienen estas guĒas (Nephrol Dial Transplant 18;2003:1466; NEJM 347;2002:1505; BMJ 325;2002:85). Los cuatro objetivos son:
Con respecto a las etapas de la enfermedad renal cr¾nica (ERC), en primer lugar, la presencia de ķsta debe ser establecida sobre la base de la presencia de da±o renal y/o nivel de funci¾n renal (velocidad de filtraci¾n glomerular), independientemente del diagn¾stico. Es una definici¾n operacional, que permite clasificar a la poblaci¾n y establecer criterios de manejo. Luego, en pacientes con enfermedad renal cr¾nica, la etapa de la enfermedad debe ser asignada de acuerdo al nivel de funci¾n renal, independientemente del diagn¾stico, de acuerdo a la clasificaci¾n K/DOQI.
Se define la ERC como:
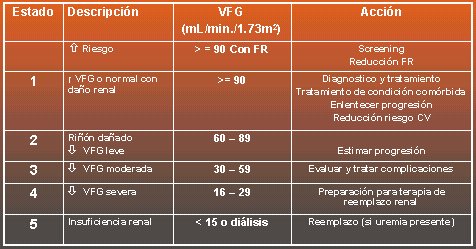
Para la clasificaci¾n de los estados se establece una herramienta intelectual muy ·til, porque asigna un n·mero a las distintas categorĒas, que podrß tener detractores en cuanto a la capacidad de definir con claridad el estado de la funci¾n renal, pero frente a cada n·mero indica una conducta clĒnica determinada. Ademßs, establece la idea de una enfermedad como proceso, dentro del cual se encuentra poblaci¾n normal, a la que puede realizarse un tamizaje para evaluar los factores de riesgo; poblaci¾n con riesgo aumentado; poblaci¾n con da±o; poblaci¾n con da±o mßs disminuci¾n de la velocidad de filtraci¾n glomerular (VFG), y poblaci¾n que cae en la categorĒa de ERC (Tabla III).
Tabla III. Clasificaci¾n de estados en la ERC.
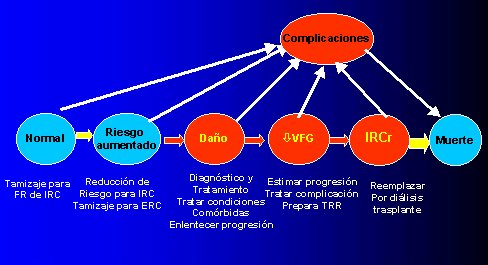
Se establece el concepto de la enfermedad renal como proceso, tal como se ilustra en la figura 10. El paciente que ingresa va a estar siempre junto al equipo mķdico, pudiendo presentar en alg·n momento complicaciones y abandona el sistema s¾lo con la muerte. Frente a cada una de las categorĒas mencionadas, se realiza una actividad determinada, por ejemplo: en el riesgo aumentado, reducci¾n de riesgo y tamizaje para enfermedad renal cr¾nica. En el caso de da±o, diagn¾stico de base y tratamiento, tratar comorbilidades y enlentecer la progresi¾n. Si estß disminuida la VFG, se debe estimar la velocidad de da±o renal, tratar las complicaciones y preparar para terapia de reemplazo, que puede centrarse en la clĒnica o en la atenci¾n primaria.
Este esquema establece acciones que deben realizarse normalmente y no son de alto costo, ademßs de determinar criterios para pedir exßmenes de un costo mßs elevado o mßs difĒciles de conseguir.
Figura 10. Enfermedad renal como proceso.
Con respecto a los exßmenes de laboratorio, calcular el clearance de creatinina por la f¾rmula es mejor que realizar el clearance de creatinina, desde el punto de vista del riesgo. Establece que existen diferencias en las f¾rmulas, sobreestimßndose en algunos casos la VFG.
McClellan, en un AJKD de 1997, recopil¾ todos estos antecedentes en 587 pacientes de alto riesgo que ingresaron a un Hospital Universitario y encontr¾ que el examen de orina se realiz¾ s¾lo en 68% de los diabķticos y en no mßs que 59% de los hipertensos, tomßndose muestra para creatininemia en 97% de los pacientes diabķticos y no mßs de 91% de los hipertensos.
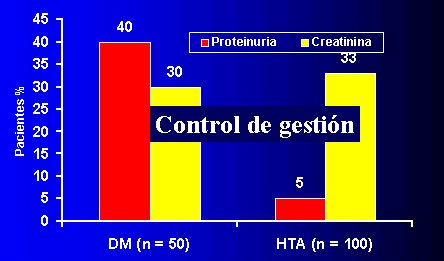
En la figura 11 el Servicio de Salud del Maule (SSM), se evaluaron 100 pacientes hipertensos y 50 diabķticos, atendidos en un consultorio durante todo el a±o 2003; en Enero de 2004, s¾lo 40% de los diabķticos tenĒan examen de orina y 30% creatinina plasmßtica, mientras que en el grupo de los hipertensos, se habĒan realizado en el 5 y 33% respectivamente. Es importante destacar que ķste es un consultorio de atenci¾n primaria, mientras que los datos de McClellan se obtuvieron en un hospital Universitario.
Figura 11. Tamizaje de ERC en Pacientes de Alto Riesgo (Diabetes, HTA). APS SSM 2003.
Existen m·ltiples factores de riesgo potenciales para susceptibilidad y/o inicio de enfermedad renal cr¾nica, los que se subdividen en factores clĒnicos (diabetes, hipertensi¾n, enfermedades autoinmunes, infecci¾n del tracto urinario, urolitiasis, obstrucci¾n del tracto urinario, neoplasias, historia familiar de insuficiencia renal cr¾nica, recuperaci¾n de insuficiencia renal aguda, reducci¾n de masa renal, exposici¾n a drogas y bajo peso al nacer) y factores sociodemogrßficos (envejecimiento; minorĒas ķtnicas como afroamericanos, hispßnicos, asißticos o isle±os del pacĒfico; exposici¾n a poluci¾n ambiental o productos quĒmicos; ingresos bajos y baja educaci¾n).
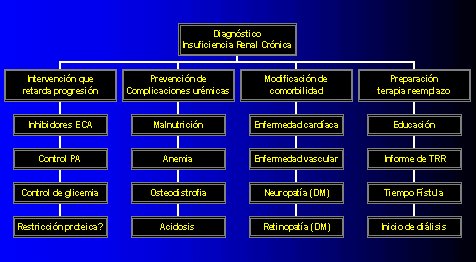
Una vez realizado el diagn¾stico de insuficiencia renal cr¾nica, se pueden efectuar intervenciones para retardar la progresi¾n, prevenir las complicaciones urķmicas, modificar las comorbilidades y preparar al paciente para terapia de reemplazo, todas las cuales se resumen en la figura 12.
Figura 12. Cuidado predißlisis ¾ptimo.
Las intervenciones que apuntan a retardar la progresi¾n son el uso de inhibidores de la enzima convertidora, el control de la presi¾n de arterial y de la glicemia y, en interrogativo, la restricci¾n proteica.
Con respecto a quiķn la realiza, y a quiķn, los espa±oles dan la respuesta. En varios artĒculos de una revista espa±ola llamada NefrologĒa Extrahospitalaria, afirman estar convencidos de que en la medida en que el manejo de la atenci¾n primaria mejore, los resultados van a ser mejores, y para eso dise±aron esta revista, como una herramienta de capacitaci¾n para los mķdicos de atenci¾n primaria en el ßmbito de la nefrologĒa.
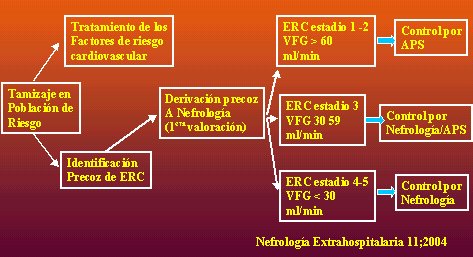
Aunque existen distintos esquemas, todos llegan a la misma conclusi¾n, como se muestra en la figura 13: tamizaje de la poblaci¾n en riesgo, tratamiento de factores de riesgo cardiovascular, identificaci¾n precoz de la insuficiencia renal cr¾nica y derivaci¾n precoz a nefrologĒa (en la primera evaluaci¾n). Luego existen varios caminos posibles. Con VFG mayor a 60 ml/min/1,73m2 (estadios 1 y 2), control en la atenci¾n primaria; con VFG de 30 a 59 (estadio 3), control mixto, y en estadios 4 y 5, control por nefrologĒa.
Figura 13. Evaluaci¾n y manejo de pacientes con ERC.
Los estudios demuestran que si los pacientes son derivados de manera precoz a nefrologĒa, la sobrevida mejora en todo evento, sobre todo en hemodißlisis. Existe una diferencia de un 30% entre la primera consulta comparada con 5 consultas, y hay diferencias si entre la primera consulta al nefr¾logo y la dißlisis transcurren 1, 2, 3 ¾ 4 meses, siendo lo mßs razonable hacer el corte a los 4 meses, aunque existe un trabajo espa±ol que concluye que incluso con tres a±os, cambia la sobrevida de los pacientes derivados de manera precoz, porque el consenso de los 4 meses aparentemente no es posible de lograr.
Alrededor de 10% de la poblaci¾n tiene enfermedad renal cr¾nica en algunas de sus etapas, controlßndose en hospitales docentes con nefr¾logos. La atenci¾n primaria necesariamente tendrĒa que hacerse cargo de la poblaci¾n que ya tiene da±o renal y de la que estß en riesgo, lo que ya estß haciendo. Nosotros controlamos alrededor de 60% de los hipertensos y la mitad de los diabķticos.
Flores dise±¾ un protocolo para determinar quķ pacientes pueden ser atendidos en la atenci¾n primaria (AP) y cußles deben ser derivados; en ķl se establece que deben permanecer en la AP los diabķticos con/sin microalbuminuria y los pacientes con hipertensi¾n que responde a terapia IRC etapas 1-2-3 (Cl creat>30 ml/min), mientras que deben ser derivados aquellos con nefropatĒa con macroproteinuria, con sospecha de nefropatĒa glomerular, los con hipertensi¾n refractaria o sospecha de HA secundaria y los pacientes con IRC en etapas 4 y 5 (Cl creat<30 ml/min).
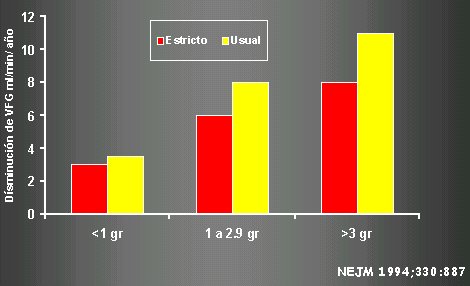
Sobre c¾mo retardar la progresi¾n, lo primero es hacer un control agresivo de la presi¾n arterial. En pacientes con proteinuria > 3g, esto es mucho mejor que tratamientos mßs laxos en relaci¾n a la velocidad de progresi¾n de da±o renal, por lo que no hay desacuerdo en cuanto a este punto (vķase figura 14).
Figura 14. El control agresivo de la PA preserva funci¾n en pacientes protein·ricos.
Las intervenciones recomendadas para enlentecer el deterioro de la funci¾n renal en pacientes con Diabetes Mellitus tipo 2, y sus objetivos, son las siguientes (NEJM 2002;346:1145):
En algunas nefropatĒas es posible utilizar una combinaci¾n de fßrmacos, pareciendo ser mejor que usar cada uno por separado. Pese a esto, en 1997 s¾lo 33% de los diabķticos y el 13% de los hipertensos con proteinuria mayor de 1g, utilizaban inhibidores de la enzima convertidora al alta de un hospital universitario. Cuando la creatininemia era mayor de 1,5 mg/dl, s¾lo 32% de los diabķticos y 26% de los hipertensos tenĒa indicado el uso de estos fßrmacos al alta. Los resultados serĒan menores de un 50%, y en nuestros 100 pacientes hipertensos y 50 diabķticos, las cifras son similares.
A pesar de que es un tema conocido y publicado, siguen llegando pacientes ancianos, diabķticos e hipertensos que utilizaron durante mucho tiempo nefrot¾xicos, especialmente antiinflamatorios. En un estudio publicado en 1997, el 6% de los diabķticos y 8,8% de los hipertensos fueron dados de alta con nefrot¾xicos.
La glicemia es una forma excelente de controlar la progresi¾n de la nefropatĒa diabķtica. En la literatura existen series con pocos casos, entre 20 y 94, pero todas coinciden en que un manejo estricto de la glicemia enlentece la progresi¾n del da±o renal. Sin embargo, la mayorĒa de los trabajos tienen un tama±o muestral muy escaso, por lo tanto, no son significativos desde el punto de vista estadĒstico, excepto el SDI y el agrupamiento del total.
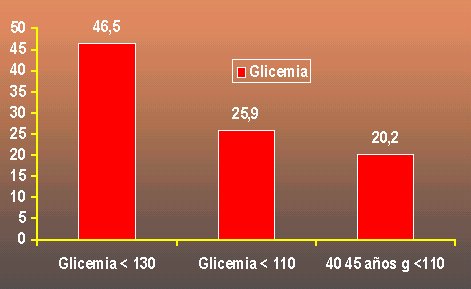
En el Servicio de Salud del Maule, de los 20.000 pacientes diabķticos en control, 46,5% tiene glicemias menores de 130 mg/dl; 25,9% tiene glicemias menores de 110 y s¾lo 20,2% tiene glicemias menores de 110, en el grupo etario comprendido entre los 40 y 45 a±os, el que podrĒa ser muy productivo. Estos datos se ilustran en la figura 15.
Figura 15. Porcentaje de pacientes que logra eficacia en el tratamiento. Servicio de Salud del Maule, 2003.
Como consecuencia del estudio CARMEN, se realiz¾ la hemoglobina glicosilada en 220 pacientes, encontrßndose que s¾lo el 15% tenĒa valores menores de 7%, de manera que de nuevo, un factor de riesgo muy importante en pacientes bajo control, no tiene resultados satisfactorios, no s¾lo a nivel chileno, sino que en todas las series hay cifras similares.
La prevenci¾n de las complicaciones urķmicas comprende prevenir malnutrici¾n, anemia, acidosis y osteodistrofia.
Los estudios demuestran que, a medida que el clearance de creatinina disminuye, la ingesta de proteĒnas disminuye, pudiendo llegar a ser tan baja como 0,5 g/kg/dĒa cuando el clearance es menor de 10 ml/min. Al disminuir el clearance de creatinina tambiķn disminuye la alb·mina sķrica, con lo que el riesgo de mortalidad aumenta al doble con respecto a niveles plasmßticos de 3,5 a 4, independiente de la hemodißlisis o de la peritoneodißlisis. A pesar de esto, un bajo porcentaje de la poblaci¾n en hemo o peritoneodißlisis ha consultado a nutricionista; de hecho, la mitad nunca consult¾.
Las estrategias para optimizar la nutrici¾n predißlisis son:
El uso juicioso de las dietas hipoproteicas se refiere a que los pacientes con clearance menores de 30 ml/min dejan de comer proteĒnas, corriendo un riesgo mayor de morir por desnutrici¾n, en comparaci¾n con el impacto que tiene la dieta hipoproteica en la disminuci¾n de la velocidad de progresi¾n del da±o renal.
Tambiķn se sabe que los pacientes ingresan anķmicos. En un anßlisis de 51 pacientes que ingresaron entre Enero y Julio de 2002 a nuestros centros de dißlisis, el hematocrito promedio era de 28,4% y la hemoglobina promedio, de 8,2. S¾lo 8 pacientes tenĒan un hematocrito mayor de 30%. Las consecuencias de la anemia no serßn analizadas.
Las estrategias para optimizar el manejo predißlisis en pacientes con anemia son:
En lo que se refiere a la modificaci¾n de comorbilidades, lo mßs importante es modificar la enfermedad cardiovascular y la neuropatĒa y retinopatĒa diabķticas.
Frente a cualquier evento cardiovascular, existe un riesgo de mortalidad mayor, y son muchos los factores que influyen. En 1999 se public¾ un estudio en el que 147 pacientes fueron seguidos durante 10 a±os (1985 a 1994). En el 42% de los casos, el primer evento cardiovascular se produjo antes de iniciar la dißlisis, y los eventos cardiovasculares fueron 3 veces mßs frecuentes que en la poblaci¾n general (Jungers, Nephro Dial Transplant, 1999; French cohort, n =147).
La prevalencia de eventos cardiovasculares en insuficientes renales cr¾nicos, antes de la dißlisis, se distribuy¾ de la siguiente manera, seg·n grupo etario: Entre 45 y 54,9 a±os, 7,6 en insuficientes renales y 3,4 en la poblaci¾n general; entre 55 y 64,9 a±os, 18,2 en insuficientes renales y 8,9 en la poblaci¾n general, y en mayores de 65 a±os, correspondi¾ a 27,8 y 10,4 respectivamente. Por lo tanto, estß claro que los pacientes en dißlisis tienen un riesgo mayor de morir por infarto, pero el pacientes predißlisis dobla, a cualquier edad, el riesgo de tener un infarto, y lo triplica en la poblaci¾n mayor de 65 a±os.
En cuanto a la probabilidad de morir despuķs de un infarto, en 563 pacientes seguidos durante un a±o, el riesgo aument¾ en 53% si la creatinina era mayor de 1,5 mg/dl, es decir, un nivel de creatinina elevado, independientemente de si se dializa, se asocia a un riesgo mayor de presentar eventos cardiovasculares y de morir al presentar este evento (Chertown, Am J Kidney Dis 2000).
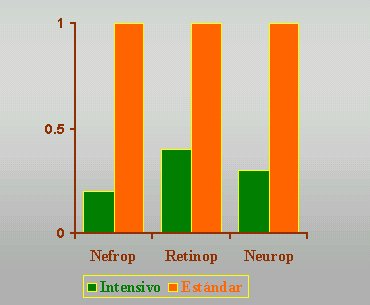
En el caso de los diabķticos, se sabe que si existe una intervenci¾n multifactorial, que incluya el manejo de la hipertensi¾n arterial de manera muy estricta, la adquisici¾n de hßbitos de vida saludables, el manejo del nivel de lĒpidos, ejercicio, dieta y uso de inhibidores de la enzima convertidora, el riesgo de da±o renal disminuye en un 65%, el de retinopatĒa casi en 60% y el de neuropatĒa, alrededor de un 65%, comparando una poblaci¾n con cuidados estßndar con una poblaci¾n con manejo intensivo (vķase figura 16).
Figura 16. Intervenci¾n multifactorial en DM tipo 2. Gaede P, et al. Lancet 353:617, 1999. Estudio aleatorio abierto: Manejo intensivo de factores de riesgo vs cuidado estßndar;160 pacientes, 4 a±os. Rx: hßbitos, CG, PB, lĒpidos, ejercicio, dieta IECA. Endpoint primario: nefropatĒa; secundario: retinopatĒa y neuropatĒa.
Un estudio realizado en Canadß demuestra que este problema no afecta solamente a la VII regi¾n, ya que de 304 pacientes referidos a nefr¾logo, con un clearance de creatinina promedio de 31 ml/minuto, el 39% habĒa tenido un evento cardiovascular previo; el 80% tenĒa hipertensi¾n; 43%, dislipidemia; 38%, diabetes mellitus, y el 27% fumaba (AJKD 2001;37:484-9). De esta poblaci¾n, s¾lo el 35% tenĒa presiones menores de 140/90 mm Hg; el 65% usaba inhibidores de la enzima convertidora, el 27% usaba Aspirina y el 18%, estatinas, cifras que son similares a las de la VII regi¾n.
En lo que se refiere a la preparaci¾n para terapia de reemplazo, ķsta incluye educaci¾n, informe acerca de la terapia de reemplazo, tiempo de fĒstula e inicio de dißlisis.
La indicaci¾n precoz de acceso vascular permanente es crĒtica, debido a que s¾lo tiene efectos positivos para el paciente: aumenta la maduraci¾n de fĒstula, mejora la cicatrizaci¾n del injerto y evita el acceso vascular temporal, lo que influye de manera beneficiosa en el costo, estenosis venosa, infecci¾n e incomodidad.
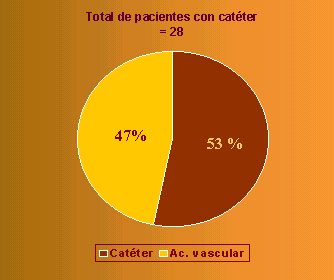
Seg·n datos obtenidos del American Journal Kidney Disease, en un estudio que incluy¾ a 1.997 pacientes, 48% de ellos no tenĒan fĒstula al momento del ingreso, 43,9% la tenĒan y en 7,9% el dato se desconocĒa. En nuestra experiencia, que se grafica en la figura 17, de 51 pacientes, 28 ingresaron con catķteres endovenosos, 47% con catķter y 53% con acceso vascular, siendo las causas edema pulmonar, en un caso, hiperkalemia en dos y sĒndrome urķmico en tres. De los 51 pacientes, el 10% consult¾ por primera vez en el servicio de urgencia por v¾mitos, es decir, por un sĒndrome urķmico, sin haber tenido con anterioridad contacto alguno con el sistema p·blico de salud.
Figura 17. Presencia de acceso vascular permanente al inicio de la Hemodißlisis.
El costo de una fĒstula electiva es de 2.992 d¾lares y el de una fĒstula hospitalizada, con catķter, alcanza a 10.000 d¾lares. De los pacientes que tienen manifestaciones urķmicas antes de un mes, el 30% lleg¾ a la dißlisis; el 20% lleg¾ con un clearance entre 15 y 29; el 20% tenĒa un clearance entre 30 y 59, y el resto un clearance menor. Pero la principal poblaci¾n, que corresponde a 30%, ya llega con indicaci¾n de dißlisis en cualquier parte del mundo.
En resumen, parece ser que la epidemiologĒa chilena se estß acercando a la de los paĒses desarrollados, cuyos problemas pueden estar mejor tabulados, pero son igualmente graves a los que se viven en nuestro paĒs, de modo que surge la pregunta de si se puede hacer mßs gastando menos, o quķ ocurrirß con este problema en el futuro. Existen varios datos alentadores al respecto.
Pregunta: Las cosas se miden por el impacto numķrico. Siempre me ha preocupado el hablar de prevenci¾n de insuficiencia renal cr¾nica. ┐Cußles son las medidas a adoptar? Seg·n el impacto numķrico, son pocas: manejar bien a los diabķticos y a los hipertensos, sin duda alguna.
Respuesta: El antecedente de desnutrici¾n pesa. En cuanto al n·mero de pacientes a salvar, es fundamental evitar los nefrot¾xicos. Otro punto que es muy importante, del cual no se habla, porque es poco frecuente, son las vasculitis autoinmunes. El diagn¾stico precoz de estas glomerulopatĒas permite salvar glomķrulos, antes de que se produzca la fibrosis. Desgraciadamente, los pacientes llegan a la urgencia con edema agudo de pulm¾n, y la derivaci¾n precoz de los pacientes es poco frecuente. El gran problema es el costo originado por las complicaciones de la fĒstula y el catķter, el reemplazo de vßlvulas, los ķmbolos sķpticos cerebrales, las sepsis, etc. Es importante la derivaci¾n precoz al nefr¾logo, ya que los pacientes llegan con creatinina promedio de 3,25, habiendo muy poco que hacer a este nivel, en cuanto a prevenci¾n. El cambio se va a lograr con la educaci¾n, recalcando la derivaci¾n precoz en la atenci¾n primaria.
Comentario: ╔ste es un problema en ascenso en todo el mundo occidental, habiendo cada vez mßs casos. Pienso que los nefr¾logos nos incorporamos muy tarde a la atenci¾n del paciente, porque ┐quķ podemos hacer? En el paciente que estß en la primera etapa de la enfermedad renal, es importante tratar de aminorar su velocidad de progresi¾n hacia la falla renal terminal y disminuir la aparici¾n de enfermedades cardiovasculares, que son muy frecuentes. Lo segundo, en un paciente con una enfermedad renal muy avanzada, que ya no se puede detener, es realizar las acciones necesarias en forma oportuna para que el paciente puede entrar a dißlisis de manera electiva y no de urgencia, evitando todas las complicaciones y costos que ello implica.
Creo que los nefr¾logos entramos tarde en ambas cosas: la posibilidad de realizar algo para enlentecer la progresi¾n de la enfermedad renal, lo que es muy relevante, porque si alguien inicia su enfermedad renal a los 60 a±os, y el nefr¾logo interviene de manera precoz, es posible que nunca desarrolle una enfermedad renal terminal, porque se puede postergar la aparici¾n hasta nueve a±os, por lo tanto, desde el punto de vista de poblaci¾n es mucho lo que se puede realizar; sin embargo, es frecuente que en el policlĒnico de nefrologĒa se reciban pacientes diabķticos que han sido controlados por a±os en policlĒnicos de atenci¾n perifķrica y que son enviados en etapa terminal, quedando como ·nica opci¾n hospitalizar al paciente para que se haga una fĒstula y entre a dißlisis.
Medwave. A±o 4, No. 9, Edici¾n Octubre 2004. Derechos Reservados.





















 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

La publicaci¾n de estas Actas CientĒficas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y la Sociedad Chilena de NefrologĒa.
 Expositor:
Gonzalo DĒaz[1]
Expositor:
Gonzalo DĒaz[1]

Citaci¾n: DĒaz G. Predialysis management of chronic renal failure. Medwave 2004 Dic;4(9):e2314 doi: 10.5867/medwave.2004.09.2314
Fecha de publicaci¾n: 1/10/2004

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n