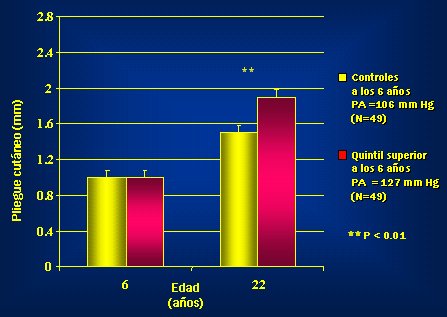
Desde hace muchos ańos se sabe que el riesgo de desarrollar obesidad en 10 ańos aumenta a mayor nivel de presión arterial actual (Kannel WB et al. Ann Intern Med. 67;48-59,1967). En un estudio realizado en nińos por Julius et al (Fig. 1) se comparó la ganancia de peso entre los 6 y los 22 ańos de edad en un grupo de nińos que tenían presiones normales a los 6 ańos (106 mmHg), grupo control, y un grupo que estaba en el quintil superior de presión arterial a esa edad, grupo hipertenso (127 mmHg). Demostraron que este último grupo ganó, en forma estadísticamente significativa más peso que el grupo control. Esto, claramente, sugirió una relación entre obesidad e hipertensión.
Figura 1. Nińos con mayor nivel de presión arterial a los 6 ańos ganan más peso a la edad de 22 ańos (The Tecumseh Blood Pressure Study; Julius S, Valentini M, Palatini P. Hypertension 2000; 35 807-813)
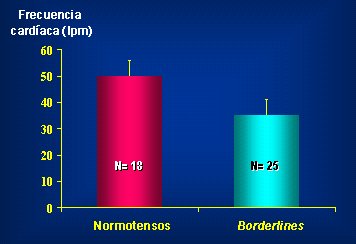
Cuando se habla de obesidad, es importante conocer la relación entre el gasto energético basal de estos individuos, el desarrollo de hipertensión y la perpetuación de la insulinorresistencia. En los individuos insulinorresistentes (Fig. 2) hay una alteración de la respuesta de los receptores betaadrenérgicos a isoproterenol, que es un agonista beta. En los sujetos normotensos, la frecuencia cardíaca aumenta en forma importante en respuesta al isoproterenol; en los sujetos hipertensos límite (borderline) se ha visto que esta respuesta es menor. Este hecho es de importancia, ya que en los sujetos obesos insulinorresistentes, como son la mayoría de ellos, se puede presentar una respuesta metabólica que determine una disminución del gasto energético a la estimulación adrenérgica. Esto se traduce en que estos sujetos podrían requerir una gran restricción calórica para bajar de peso, ya que su gasto de energía por otras vías, como la de estimulación adrenérgica sería menor (ejemplo, menos gasto calórico en ejercicio). Como se ve en la figura 2, la respuesta de la frecuencia cardíaca en los sujetos hipertensos es menor que en los sujetos controles y el gasto energético también, de manera que es importante tener presente este dato cuando se trata a estos pacientes y se les pide que bajen de peso.
Figura 2. Cambio en la frecuencia cardíaca en respuesta a isoproterenol (3 ug/min ev), desde medición de reposo, en sujetos normotensos e hipertensos límite (Julius et al, Cir Research 1975; 36-37 (suppl): 199)
El concepto de obesidad que se relaciona con hipertensión es el de obesidad intraabdominal, que se refiere a la adiposidad o grasa visceral, la que está en los órganos o entre ellos, para diferenciarla de la grasa subcutánea. La grasa visceral se puede medir por escáner. La adiposidad intraabdominal está muy relacionada con los factores que causan el síndrome metabólico o también ahora llamado cardiometabólico, compuesto por dislipidemia, hipertensión, resistencia a la insulina, diabetes mellitus 2, inflamación y trombosis. En la grasa visceral existe un aumento en la producción de angiotensinógeno, comparada con la grasa subcutánea; esto es muy importante, ya que como se dijo, el angiotensinógeno es un sustrato para producir más hipertensión en los pacientes obesos. Por otra parte, la grasa visceral cumple un papel preponderante en la aparición de diabetes e hipertensión, al generarse en ella mayor cantidad de ácidos grasos libres. Además, como también antes se dijo, se asocia a una respuesta aumentada a catecolaminas, lo que en algunos pacientes se ha relacionado a mayor ocurrencia de eventos cardiovasculares. La grasa visceral también es más resistente a la acción de la insulina y, por último, esta grasa es muy activa endocrinológicamente hablando y secreta más adipoquinas (IL-6 y PAI 1) y menos adiponectina.
En un estudio en el ańo 2005 se analizó la asociación entre los niveles de presión arterial y la circunferencia abdominal en una población general en Canadá. La medición de la cintura se relacionó en forma estrecha con la grasa abdominal (r = 0,9) y fue un mejor marcador de variabilidad interindividual de la hipertensión arterial que el HOMA (Homeostatic Model Assessment), que mide el grado de resistencia a la insulina, y que el índice de masa corporal (IMC) e incluso la insulinemia de ayuno (Poirier et al, Hypertension 2005). En consecuencia, hoy se piensa que la grasa visceral podría ser el mediador común de todos los efectos metabólicos de la resistencia insulínica y el síndrome que se desencadena.
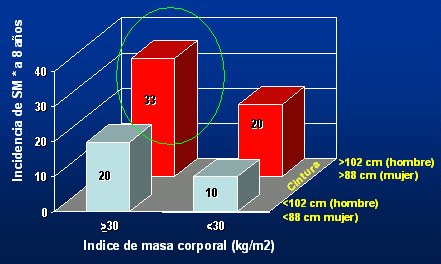
Se ha visto en algunos estudios, que la obesidad intraabdominal predice mejor el desarrollo del síndrome metabólico que el IMC, como lo demuestra el estudio de Han et al (Fig. 3). En los sujetos que no tienen mayor cantidad de grasa abdominal, pero que sí son obesos, la prevalencia de síndrome metabólico es de 20%; en cambio, en los sujetos obesos abdominales la cifra sube a 33%. Esto, en parte explica el porqué la medición de la cintura se esté exigiendo a quienes se dedican a prevención cardiovascular. Otro resultado que apoya el que la obesidad intraabdominal podría ser “el mediador” en la relación resistencia insulínica/hipertensión, es el hecho de que los sujetos hipertensos tienen 60% más de grasa visceral, independiente del IMC.
Figura 3. La obesidad abdominal predice el síndrome metabólico (Han et al, 2002)
Fisiopatológicamente, este efecto ocurre porque los adipocitos son células endocrinas muy activas. Como ya se dijo, la obesidad abdominal causa dislipidemia aterogénica, hipertensión, intolerancia a la glucosa, insulinorresistencia y aumento significativo del riesgo cardiometabólico. Los adipocitos aumentan la producción de ácidos grasos libres y de glucosa, causan hiperglicemia y aumentan la resistencia a la insulina y la producción de triglicéridos, lo que favorece la dislipidemia aterogénica, y, por otro lado, disminuyen la producción de adiponectina y aumentan la producción de IL-6 y factor de necrosis tumoral. Estos últimos causan más resistencia a la insulina y un estado inflamatorio crónico que es el factor común en el síndrome metabólico. La grasa visceral se relaciona con la insulinorresistencia y a medida que aumenta el volumen de grasa visceral, disminuye la captación de la glucosa a nivel del músculo esquelético.
Uno de los últimos fenómenos que se han descrito en relación con este síndrome de resistencia a la insulina es la relación con algunas adipoquinas, que son proteínas que se producen en la grasa. Una de las más importante es la adiponectina, hormona insulinosensibilizadora. Los niveles de adiponectina van en relación inversa con el aumento en la resistencia a la insulina, es decir, a menor nivel de adiponectina, mayor resistencia a la insulina, mayor hipertensión y mayor probabilidad de llegar a diabetes. Se ha visto que esta adipoquina es una hormona que causa un efecto antiaterogénico a nivel de la pared vascular, incluso de las arterias coronarias. Esta proteína fue identificada por primera vez en 1990 y se ha demostrado que sus niveles están disminuidos en pacientes obesos con diabetes mellitus 2 y con enfermedad cardiovascular. En estudios en ratones knock out para adiponectina se ha demostrado que es fundamental para evitar el desarrollo de resistencia insulínica, con todas las consecuencias ya descritas. En pacientes portadores de una mutación del gen de adiponectina, por otro lado, se ha visto que estos presentan glicemias de ayuno alteradas y que casi 90% de ellos presentan hipertensión arterial y una dislipidemia aterogénica, propia del síndrome metabólico (Matzuzawa et al, ATVB 2004;24:29).
La proteína C reactiva (PCR) es también un mediador importante en la resistencia insulínica y la hipertensión arterial; sin embargo, no es un factor causal. Se ha demostrado que es un potente predictor de resistencia insulínica y diabetes mellitus 2 y se ha asociado con riesgo de hipertensión, lo que plantea que habría una relación entre ésta y la resistencia a la insulina, pero sólo en el contexto del estado proinflamatorio que se presenta. Es importante saber que la PCR puede predecir la aparición de diabetes y síndrome metabólico, como lo ha demostrado Haffner et al, quien en un estudio midió resistencia a la insulina y comprobó que la PCR tenía la misma capacidad de predicción del síndrome metabólico y la diabetes que el HOMA combinado con IMC (Diabetes Care; 25(11) Nov 2002; 2016-2021).
El síndrome metabólico constituye una nueva forma de hablar de resistencia a la insulina y, a la vez, es un objetivo de tratamiento dirigido a disminuir la morbimortalidad cardiovascular. En este síndrome participan todos los actores que se han mencionado, los que están determinados por la resistencia insulínica, pero lo más importante en este momento es la relación de este síndrome con el mayor desarrollo de ateroesclerosis. żPorqué tanta importancia? Hoy se estima que el 25% de la población “mundial” tiene síndrome metabólico, es decir, el 25% de la población en el mundo tiene algún grado de resistencia a la insulina, con todo lo que ello implica: dislipidemia, hipertensión, etc. (Cameron, End Met Clin NA, 2004;33:351).
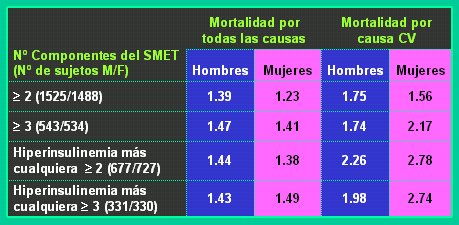
Nuestro país no se salva. En la Encuesta Nacional de Salud 2003 se encontraron las mismas cifras que en el resto del mundo (22,6% en la población general), y lo peor es que el problema ha aumentado en la juventud. Hoy se sabe que el síndrome metabólico otorga un mayor riesgo de eventos cardiovasculares y que la sobrevida de las personas con síndrome metabólico es menor que la de quienes no tienen este síndrome. Los datos del estudio DECODE (Diabetes Epidemiology: Collaborative Analysis of Diagnostic Criteria in Europe) (Tabla I) muestran claramente cómo el síndrome metabólico aumenta la morbilidad y mortalidad cardiovascular.
Tabla I. Metaanálisis de la asociación del síndrome metabólico con el riesgo de mortalidad cardiovascular y por todas las causas en 7 cohortes del estudio DECODE, por sexo (Adaptado de Hu G. et al. Arch Intern Med 2004;164:1066-1076).
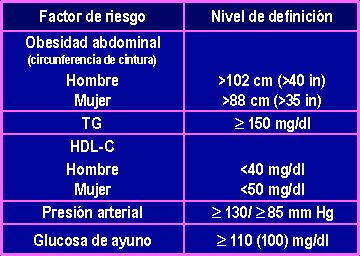
La Organización Mundial de la Salud (OMS) definió, hace ya varios ańos, el síndrome como un síndrome de resistencia a la insulina. Hoy día, el concepto se ha simplificado, y no se exige un test de resistencia a la insulina para decir que existe. Esta es la definición que hoy se utiliza y es la del ATP III. Esta definición se dio a conocer en el ańo 2001 y establece que si una persona presenta más de tres de los siguientes factores: cintura aumentada, triglicéridos altos, HDL bajo, presión arterial aumentada o glicemia de ayuno aumentada (más de 100), la persona tiene síndrome metabólico. Con esta definición se evita hacer el HOMA u otros estudios de resistencia y se facilita la detección de una persona en riesgo. Obviamente, que como siempre en medicina, han aparecido nuevos intentos de simplificar su detección; la última propuesta es la de la Federación Internacional de Diabetes, que exige la obesidad intraabdominal (cintura aumentada), aparte de los otros factores. Esta última clasificación ha aumentado en 15% la prevalencia de síndrome metabólico, pero, para efectos prácticos y aplicación clínica, aún es más usada la ATP III (Tabla II).
Tabla II. El diagnóstico de síndrome metabólico se establece cuando se presentan tres de estos factores de riesgo (ATP III. JAMA 2001;285:2486-2497)
La prevalencia de hipertensión en personas con síndrome el síndrome metabólico, como se ha definido, es de 80%. Por lo tanto, aunque no se haya comprobado una relación causal, se podría decir que “casi” todos los hipertensos tienen algún grado de resistencia a la insulina.
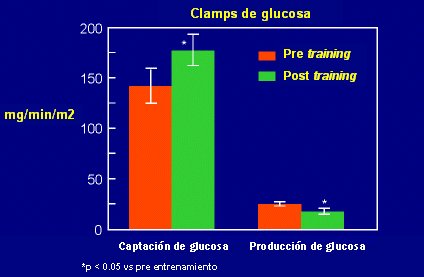
En cuanto a tratamiento de estos pacientes, en general se debe recomendar medidas no farmacológicas. Una de ellas, y que ha sido exitosa, es la dieta mediterránea, que puede revertir el síndrome metabólico. Por otro lado, el ejercicio aeróbico es fundamental, porque (Fig. 4) mejora la captación de glucosa, disminuye la resistencia a la insulina y mejora el control de la hipertensión. Se ha demostrado que si las personas cambian su estilo de vida, reducen su peso en 7% y hacen dos horas de ejercicio aeróbico a la semana, la tasa de progresión a la diabetes disminuye casi en 60%. Un fármaco, la metformina, en el mismo grupo de sujetos, disminuyó la progresión en alrededor de 40%.
Figura 4. El ejercicio aeróbico mejora la sensibilidad a la insulina (DeFronzo R et al. Diabetes 1987 (36):1379-1385)
En cuanto a fármacos y síndrome metabólico, la estrategia más novedosa es la modulación de los receptores nucleares PPAR (Peroxisome Proliferator Activated Receptor) mediante la administración de agonistas de estos receptores, como las glitazonas, que mejoran el patrón hipertensivo y la dislipidemia, disminuyen la hiperglicemia, mejoran la sensibilidad a la insulina, disminuyen la PCR y disminuyen la trombosis. Estudios realizados con rosiglitazona demuestran que este fármaco mejora la presión arterial, tanto diastólica como sistólica, y mejora la resistencia a la insulina. Como ya se dijo, en hipertensión se ha demostrado que los IECA y los ARA II mejoran no sólo la hipertensión, sino que disminuyen la resistencia a la insulina y retrasan la aparición de diabetes, entre otros efectos.
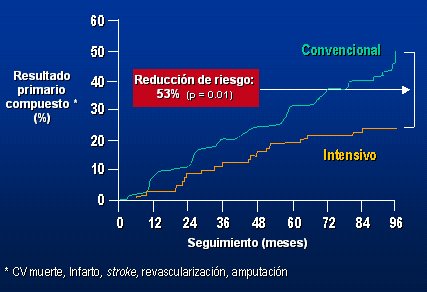
Un ejemplo exitoso de una intervención agresiva de todos los factores de riesgo en pacientes diabéticos, se hizo en el estudio STENO-2 (Multifactorial Intervention and Cardiovascular Disease in Patients with Type 2 Diabetes), en el cual se trató la hipertensión en forma agresiva, hubo un control metabólico muy agresivo con hemoglobina glicosilada menor de 6,5 y se trató la dislipidemia, en forma también agresiva, con LDL menor de 100. Este tratamiento intensivo dio mucho mejor resultado que el tratamiento convencional, logrando una disminución del 50% de eventos cardiovasculares (Fig. 5).
Figura 5. STENO-2: Efecto de la intervención multifactorial sobre el riesgo cardiovascular: n = 160 pacientes con diabetes tipo 2 y microalbuminuria (Gćde P et al. N Engl J Med. 2003;348:383-93)
Una nueva droga llamada rimonabant, que es un bloqueador del receptor CB1 del sistema endocanabinoide, será motivo de análisis en el futuro mediato. Esta droga actúa principalmente en el sistema nervioso central disminuyendo el apetito, de modo que favorece la baja de peso. Sin embargo, se ha probado que esta droga también actúa bloqueando los receptores CB1 en otras locaciones, como por ejemplo en el tejido adiposo, aumentando la producción de adiponectina con mejoría de la resistencia a la insulina. En el músculo mejora la captación de la glucosa. Ya van más de 15.000 pacientes tratados y se cree que podría ser una gran ayuda para el manejo multifactorial del síndrome metabólico.
Es difícil evaluar causas y consecuencias entre variables biológicas tan estrechamente relacionadas, aún usando análisis estadísticos cuidadosos. Es posible que nunca se resuelva completamente la pregunta si hay o no una relación causal entre resistencia a la insulina e hipertensión. Sin embargo, en clínica lo más importante es detectar a las personas que están en mayor riesgo y actuar antes de que se presente la cadena de eventos que se ha descrito.







 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Expositora:
Mónica Acevedo[1]
Expositora:
Mónica Acevedo[1]

Citación: Acevedo M. Insulin resistance and hypertension II: obesity and hypertension. Medwave 2006 Jul;6(6):e2306 doi: 10.5867/medwave.2006.06.2306
Fecha de publicación: 1/7/2006

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión