La publicaci¾n de estas Actas CientĒficas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y la Sociedad Chilena de NefrologĒa.
El i¾n potasio (K) se distribuye tanto en el lĒquido intracelular (LIC) como en el extracelular (LEC), pero la cantidad absoluta es muy distinta en cada uno, siendo mucho mayor dentro de la cķlula que fuera de ella. La concentraci¾n de K en el LIC, cuyo volumen aproximado es de 27 litros, es de 140 mEq/l, lo que da un total de 3.780 mEq; en cambio, en el LEC, cuyo volumen es de 14 litros, la concentraci¾n de K es de 4,5 mEq/l, de modo que su cantidad absoluta alcanza a s¾lo 63 mEq. Lo dicho tiene una serie de connotaciones, sobre todo con respecto al potencial de membrana.
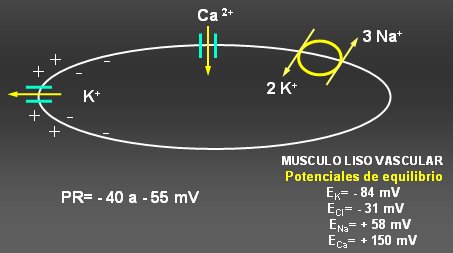
El potencial de membrana es generado por la bomba sodio potasio ATPasa (Na/K ATPasa), que bombea K hacia el interior de la cķlula y saca Na hacia el exterior de ella, lo que aumenta la cantidad de K y disminuye la cantidad de Na a nivel intracelular. Esto ocurre con gasto de energĒa. Si la membrana fuese permeable a todos los iones por igual, el gradiente generado se perderĒa rßpidamente; pero, como la permeabilidad es mayor para el K que para el Na, lo mßs importante en la gķnesis de este potencial de membrana, a nivel del m·sculo liso y de otras cķlulas, es la salida de potasio, que tanto por su concentraci¾n como por el gradiente elķctrico, tiende a salir de la cķlula. El potencial de membrana del m·sculo liso vascular fluct·a entre ¢40 a ¢55 (vķase Figura 1).
Figura 1. Regulaci¾n del potencial de membrana y tono vascular por canales de potasio.
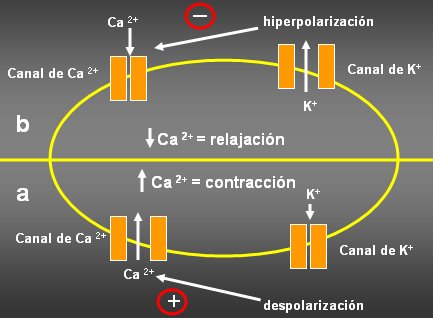
En la Figura 2 se explica c¾mo se acopla esta funci¾n con la contracci¾n del m·sculo liso y quķ relaci¾n tiene con el tono vascular y la hipertensi¾n. En estas cķlulas hay canales de calcio regulados por voltaje, entre ellos los clßsicos canales tipo L, que se pueden bloquear con los bloqueantes de cßlcicos que se utilizan en la clĒnica. Cuando la membrana se despolariza, los canales de calcio se abren, permiten mayor entrada de calcio al interior de la cķlula, y esto conduce a una mayor contracci¾n de la cķlula. Al contrario, cuando la membrana se hiperpolariza, los canales se cierran, hay menos calcio disponible para al aparato miocontrßctil y la cķlula se relaja.
Figura 2. Interacci¾n entre canales de K y Ca.
Mientras mßs tiempo estķn abiertos los canales de potasio o mayor cantidad de ellos estķn abiertos, la salida de potasio serß mayor; en consecuencia, la membrana se hiperpolariza, los canales de calcio se cierran, el calcio intracelular disminuye y hay relajaci¾n. A la inversa, cuando se cierran los canales de K, hay despolarizaci¾n, activaci¾n de canales de calcio, mayor entrada de calcio y contracci¾n del m·sculo liso. Hay un excelente review de Davis y Smith (Physiol Rev 79: 387-423, 1999), sobre este tema.
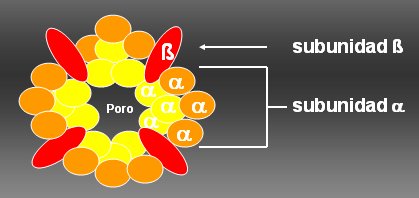
La Figura 3 ilustra la estructura hipotķtica de un canal de K regulado por voltaje, que se compone de subunidades alfa y beta. Las subunidades alfa estßn formadas por una proteĒna con seis segmentos transmembrana, con el extremo amino y carboxi terminal hacia la cķlula, y un sensor de voltaje. Una subunidad alfa tiene seis segmentos que atraviesan la membrana y una subunidad beta, que habitualmente es intracelular. Con la uni¾n de cuatro subunidades beta y cuatro subunidades alfa se forma el poro del canal funcional. La subunidad beta se une a sustancias intracelulares y regula (favorece o disminuye) el pasaje de K por el canal. Diversos investigadores estßn abocados a estudiar las alteraciones en la subunidad alfa o en la subunidad beta que modifican la conductancia de K.
Figura 3. Modelo hipotķtico de un canal de potasio regulado por voltaje tipo Shaker.
Existen distintos tipos de canales de potasio en el m·sculo liso vascular: regulados por voltaje; regulados por calcio; y rectificadores internos.
Los canales regulados por voltaje se llaman Kv y tienen muchos miembros en esta clase; especĒficamente los que estßn presentes en el m·sculo liso son el Kv 1.5 y quizßs el Kv 1.1. Hay inhibidores especĒficos de estos canales (4-Aminopiridina, quinina e hipoxia).
Los canales regulados por calcio intracelular tienen la misma disposici¾n, pero en el segmento carboxi terminal pueden unir calcio. Hay canales de conductancia mayor, llamados hslo (tambiķn Maxi K o BK), que son los mßs abundantes de todos los canales de potasio en los vasos sanguĒneos; los activan el calcio intracelular y las proteĒn kinasas A y G; tienen inhibidores especĒficos (iberiotoxina, charibdotoxina y TEA). Hay ademßs canales regulados por calcio que permiten menor conductancia de K, llamados de ōconductancia menorö.
Los canales rectificadores internos, en lugar de tener seis segmentos transmembrana, tienen solamente dos; tambiķn deben unirse cuatro subunidades alfa con cuatro subunidades beta para formar el canal funcional. Una subclase estß constituida por el canal Kir (inward rectifier), sus componentes principales son Kv 2.0 y quizßs Kv 1.0, son activados por hiperpolarizaci¾n e inhibidos por bario y 4-Aminopiridina y se postula que participan en la vasodilataci¾n por hiperkalemia.
Otra subclase es el K-ATP, habitualmente estßn inhibidos por el ATP intracelular; pero cuando sobreviene hipoxia y disminuyen los niveles de ATP, estos canales se abren, la membrana se hiperpolariza, entra calcio y el vaso arterial se dilata. Esto ocurre, por ejemplo, en el shock sķptico, en que la hipoxia causa la apertura de los canales de potasio, lo que se suma a los mecanismos clßsicos de vasodilataci¾n en el shock sķptico. Los canales K-ATP tienen una subunidad llamada SUR (unidad receptora unida a sulfonilureas) a nivel del pßncreas, las sulfonilureas se unen a este canal, se activa el canal de potasio y se inicia la liberaci¾n de insulina.
Otra clase de canal de potasio es el canal de dos poros, que tiene cuatro segmentos transmembrana. En los nemßtodos se han descrito mßs de 80 canales distintos, muchos de ellos ya tienen un hom¾logo humano y algunos estßn presentes a nivel de la vasculatura. A estos canales no me voy a referir en esta charla.
Por lo tanto, hay distintos canales de potasio en distintos tejidos y, dependiendo de la subunidad beta, habrß distintos reguladores.
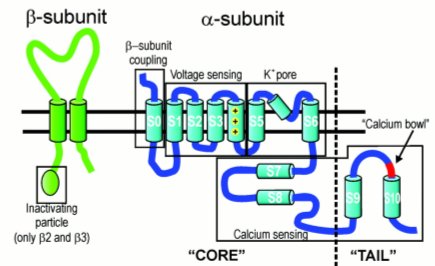
En la Figura 4 se muestra la estructura del canal Maxi K, que tiene una subunidad alfa con seis segmentos transmembrana y un segmento extra; a·n se discute si es intracelular o estß en la membrana, pero tiene en el extremo carboxi terminal un lugar al que se puede unir el calcio. Ademßs, tiene una subunidad beta, de las cuales hay cuatro descritas en distintos tejidos; el tipo 1 es el que se encuentra en m·sculo liso vascular.
Figura 4. Estructura del canal Maxi K.
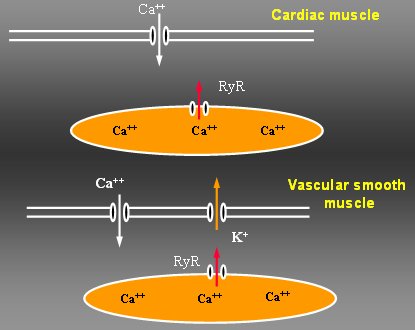
Explicar el hecho de como la entrada de calcio produce la contracci¾n del m·sculo liso vascular es un poco mßs complejo. Si bien el calcio sirve para que se una la actina con la miosina y se active la contracci¾n, el aumento del calcio intracelular determina que este i¾n se una al receptor de rionidina que se encuentra en el retĒculo sarcoplßsmico e induzca la liberaci¾n de calcio; con ella se activan los canales Maxi K, cuya apertura permite la salida de potasio (vķase Figura 5).
Figura 5. Papel del receptor rionidina.
La importancia de este fen¾meno radica en que la contracci¾n causa, por un mecanismo de retroalimentaci¾n positiva, tambiķn la relajaci¾n, ya que la salida de potasio hiperpolariza la membrana, cierra el canal y relaja el m·sculo liso. Los receptores rionidina estßn en Ēntimo contacto con los canales Maxi K y por lo tanto permiten esta retroalimentaci¾n negativa. En cambio, en el m·sculo cardĒaco no hay Maxi K, de modo que, cuando entra calcio en la cķlula y se libera calcio del receptor rionidina, el calcio participa solamente en la contracci¾n de la cķlula cardĒaca.
En el m·sculo liso vascular, la liberaci¾n de calcio de dep¾sito sirve para relajar el vaso sanguĒneo previamente contraĒdo; por lo tanto, el tono vascular estß regulado por este mecanismo, que es totalmente aut¾nomo y ocurre in vitro, sin regulaci¾n hormonal ni del sistema nervioso. Si se saca un vaso sanguĒneo del cuerpo, ese vaso estß totalmente flßcido, pero, a medida que se presuriza al mismo, la membrana plasmßtica comienza a despolarizarse, se abren los canales de calcio tipo L, entra calcio a la cķlula y se incrementa el tono arterial; pero, como ya se ha dicho, esto produce apertura de los canales maxi K, la membrana se hiperpolariza y el vaso se relaja. Por medio de este mecanismo de feedback negativo, las arterias se encuentran en estado de semi contracci¾n, denominado tono vascular.
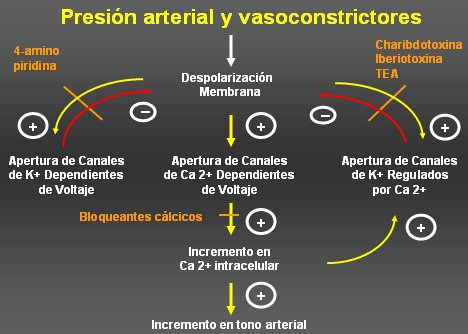
En la Figura 6 se muestra el mecanismo por el cual la presurizaci¾n de una arteria aumenta la presi¾n arterial. ExistirĒan canales sensibles al estiramiento; son canales cati¾nicos inespecĒficos y censan el estiramiento de la cķlula; un mayor estiramiento produce una despolarizaci¾n inicial por cierre de canales de potasio que desencadena la apertura de los canales de calcio dependientes de voltaje, con incremento en el calcio intracelular y luego incremento en el tono arterial.
Por otra parte, existen los canales de K dependientes de voltaje, que se activan con la despolarizaci¾n y al abrirse se repolarizan o hiperpolarizan. Este mecanismo es muy importante en la mantenci¾n del tono vascular y es muy conocido clĒnicamente, porque cuando se administran bloqueadores del calcio se produce vasodilataci¾n y cuando se administra inhibidores de canales de potasio regulados por calcio, como la iberiotoxina, la arteria no puede relajarse.
Figura 6. Presi¾n arterial y vasoconstrictores.
Las alteraciones de los canales de K podrĒan hipotķticamente producir hipotensi¾n o hipertensi¾n. Una de las primeras evidencias concretas surgi¾ en 2000, cuando el grupo de Brenner y Nelson estudi¾ la importancia de la subunidad beta uno, que tiene cuatro exones, en un rat¾n knock out carente del segundo ex¾n.
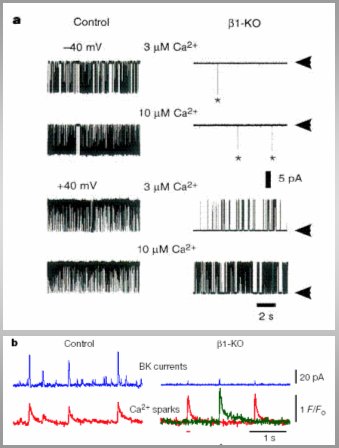
Al estudiar los canales de K con mķtodos electrofisiol¾gicos, se comprob¾ que en el grupo control la actividad del canal era normal permitiendo la entrada de K; en cambio, en el rat¾n knock out el canal no permitĒa prßcticamente pasaje de este i¾n. Al incrementar la cantidad de calcio, con lo que el canal deberĒa abrirse mucho mßs, tampoco hubo salida de K (Figura 7 panel a).
En ratones control, al activarse el canal de rionidina se producĒa una ōchispaö (spark), salida de calcio que induce un aumento concomitante de corriente del canal Maxi K. Pero en el rat¾n knock out, la presencia de chispas no se correspondĒan con corriente en los canales de K debido a la insuficiente valoraci¾n de niveles intracelulares de calcio por la subunidad beta mutada (Figura 7 panel b).
Figura 7. Regulaci¾n del tono vascular por la subunidad beta del canal de K activado por calcio (Brenner et al. Nature 2000; 407:870-76).
Cuando se midi¾ la presi¾n arterial de estos animales, se encontr¾ que el promedio fue de 114 ▒ 6,0 mm Hg en el grupo control (n = 6) y de 134 ▒ 5 mmHg en el grupo de ratones knock out (n = 6), diferencia estadĒsticamente significativa (p < 0,029).
En 2004, el Dr. Ram¾n Latorre, junto con un grupo espa±ol, estudi¾ la correlaci¾n, en seres humanos, entre las alteraciones de los canales de potasio y la presi¾n arterial, y observ¾ que una mutaci¾n que hace aumentar la funci¾n de la subunidad beta se asociaba con baja presi¾n arterial. En ese estudio, un trabajo epidemiol¾gico muy interesante, se utiliz¾ una base de datos espa±ola de 3.000 individuos en quienes se determin¾ el genotipo de la subunidad beta; se encontr¾ una mutaci¾n a nivel del aminoßcido 65, con reemplazo del ßcido glutßmico por glicina. Del total de 3.000 casos, 80% tenĒan el gen EE, o sea, tenĒan ßcido glutßmico en sus dos cromosomas; 20% tenĒan una forma heterocigota u homocigota, pero los ·ltimos eran muy pocos, menos de 1%. Luego se midi¾ la presi¾n arterial en funci¾n del genotipo y se comprob¾ que, cuanto menor era la presi¾n arterial, mayor era la prevalencia de la mutaci¾n; cuanto mßs alta era la presi¾n, mßs frecuente era la condici¾n de homocigoto de los dos ßcidos glutßmicos (Clin Invest 113:1032¢1039 (2004).
A continuaci¾n se hicieron mutantes de los canales de potasio con esa alteraci¾n del ADN, se fabric¾ ARN mensajeros que fueron inyectados en ovocitos para luego determinar la corriente que se producĒa a travķs de esa membrana plasmßtica; es un experimento simple de electrofisiologĒa. Cuando s¾lo se inyectaba la unidad alfa, a medida que aumentaba el calcio habĒa mßs corriente y mßs K pasando a travķs del canal; cuando se ponĒa la subunidad alfa y beta normales (wild type) aumentaba la corriente y la subunidad alfa se hacĒa mucho mßs sensible al calcio, y pasaba mßs K. Cuando se introducĒa una subunidad alfa y una beta con la misma mutaci¾n que se encontr¾ en esa poblaci¾n, pasaba a·n mßs potasio, ya que esta subunidad beta mutada es mßs sensible al calcio.
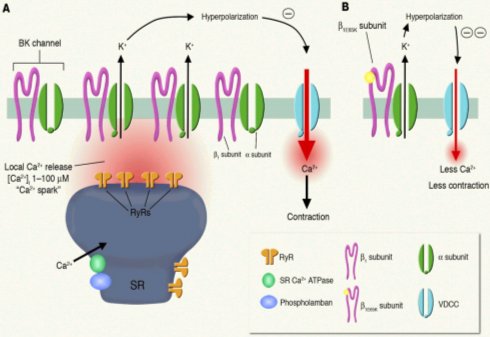
En la Figura 8 se observa el receptor de rionidina y, arriba, la zona donde se libera el calcio y el canal de K, con las subunidades beta y alfa por donde pasa el i¾n. En un individuo normal esta liberaci¾n causa hiperpolarizaci¾n que cierra el canal de calcio y origina contracci¾n; cuando la subunidad beta estß mutada, se censa mßs el calcio que se libera de los receptores de rionidina, lo que causa mayor salida de K, con hiperpolarizaci¾n, menor calcio intracelular y menor contracci¾n (arriba a la derecha). Los autores concluyeron que, debido a esta mutaci¾n, el canal era hipersensible y que con valores normales de calcio intracelular habĒa mayor hiperpolarizaci¾n.
Figura 8. Mutaci¾n de la subunidad beta del canal de K, asociada con menor presi¾n arterial.
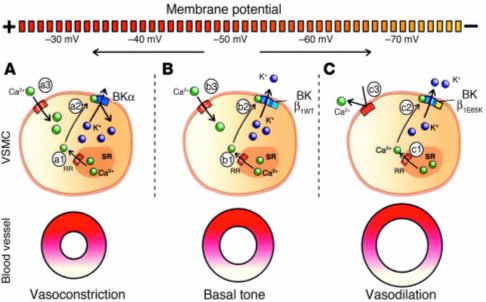
En la Figura 9 se ve una representaci¾n de un individuo normal, en el cual, cuando entra calcio, se libera calcio del receptor de rionidina, se permite la salida de potasio y con ello, se mantiene un tono arterial basal. En cambio, en el knock out de beta1, la entrada de calcio produce la salida normal de chispas de calcio, pero sale menos K a travķs del canal por sensado inadecuado del nivel de calcio intracelular, la membrana estß mßs despolarizada y el vaso estß mßs contraĒdo. Al contrario, en presencia de la mutaci¾n descrita por Latorre, sale mßs potasio que en controles normales, la membrana se hiperpolariza y causa vasodilataci¾n.
Figura 9. Efecto de la entrada de calcio en situaci¾n normal y en knock out de beta1.
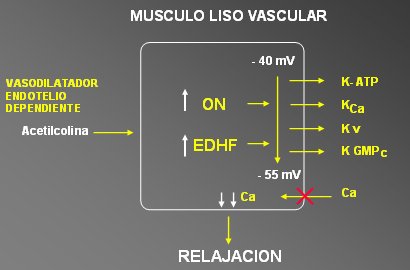
Actualmente se sabe que la L-arginina se convierte en citrulina en el endotelio, donde se une al ¾xido nĒtrico (ON), el que, a nivel del m·sculo liso vascular, llega a GMP cĒclico (GMPc) a travķs de la guanilatociclasa (GCS); el GMPc causa vasodilataci¾n mediante hiperpolarizaci¾n, al cerrar los canales de calcio, pero este mecanismo estß todavĒa en discusi¾n. Con esta pensamiento en mente, nuestro grupo comenz¾ a buscar canales de K que tuvieran alg·n elemento regulado por GMPc, a travķs del cual el ON y el factor hiperpolarizante derivado del endotelio (EDHF) pudiesen producir hiperpolarizaci¾n, con la consiguiente reducci¾n de la entrada de calcio y relajaci¾n del m·sculo liso vascular (vķase Figura 10).
Figura 10. Canales de potasio y regulaci¾n del tono vascular.
AsĒ se encontr¾ el canal denominado hKCNA10, cuyo gen tiene aproximadamente 1500 pares de bases en un solo ex¾n y estß ubicado en el brazo corto del cromosoma 1, a la altura del 13,1. En los estudios electrofisiol¾gicos se demostraron las siguientes propiedades:
En estudios realizados en ratas para demostrar que el anticuerpo es sensible, ya que ķste no funcionaba tan bien en tejido humano, se realiz¾ hibridizaci¾n in situ y se encontr¾ a nivel renal, en el endotelio de los vasos sanguĒneos, en el m·sculo liso vascular y en distintos sitios del glomķrulo, asĒ como en el endotelio de grandes vasos y en el m·sculo liso vascular (J Am Soc Nephrol 13: 2831¢2839, 2002).
Como la subunidad alfa no deja pasar tanta corriente de K en condiciones fisiol¾gicas, se utiliz¾ el sistema de doble hĒbrido para identificar una subunidad beta reguladora de KCNA10 (Tian et al Am J Physiol Renal Physiol, 2002). AsĒ se encontr¾ la denominada KCNA4B, que estß localizada en el cromosoma 13 y tiene 16kb, 5 exones y 141 aminoßcidos. Tiene similitud estructural con la superfamilia de oxidorreductasas NAD(P)H dependientes y se expresa principalmente en el coraz¾n, m·sculo esquelķtico, ri±¾n, intestino delgado y placenta.
Cuando se inyectaba agua o KCNA4B no pasaba casi nada de corriente, pero cuando se inyectaba junto con KCNA4B se producĒa una gran activaci¾n y salida de K. Como este canal de K es regulado por GMPc y ķste es uno de los intermediarios por los cuales act·a el ¾xido nĒtrico en estos sitios, se plante¾ la hip¾tesis de que las alteraciones en este canal producirĒan alteraciones en el tono vascular.
En el lado apical del ri±¾n hay una serie de canales, como el KCNA10 y otros, el que causa el sĒndrome del QT prolongado y canales de calcio que participan en la hiperpolarizaci¾n de la membrana, sobre todo cuando en el lado basolateral se produce salida de K y activaci¾n de la bomba. Creemos que este canal, a nivel renal, no tiene relaci¾n con la presi¾n arterial; se estß tratando de determinar c¾mo influye en el metabolismo del az·car y en el funcionamiento de la bomba de co-transporte de Na/glucosa y Na/aminoßcidos.
Es probable que este canal tenga influencia en los vasos sanguĒneos, arterias y venas. Por este motivo estamos buscando mutaciones en el canal que puedan estar asociadas con alg·n cuadro hipertensivo.
Entre los pacientes hipertensos se destacan dos grupos, por su presi¾n de pulso: los que presentan hipertensi¾n sist¾lica aislada, cuya presi¾n de pulso es amplia, por ejemplo, 160/88; y los que tienen hipertensi¾n diast¾lica aislada, cuya presi¾n de pulso estß disminuĒda, por ejemplo, 130/94. Los sisto-diast¾licos son habitualmente una mezcla de hipertensos con presi¾n de pulso amplia, normal y disminuĒda, y constituyen un grupo muy heterogķneo: hay pacientes con 164/92 (predominantemente sist¾licos), 140/90 (proporcionados, pulso normal), etc.
Estas categorĒas son artificiales y responden a nuestra clasificaci¾n actual de estadios de hipertensi¾n. Para intentar obtener subgrupos mßs homogķneos en cuanto a fisiopatologĒa, estudiamos pacientes con presi¾n de pulso disminuida y los denominamos hipertensos esenciales con predominio diast¾lico (HTA PD), tķrmino que abarca a pacientes con hipertensi¾n diast¾lica aislada y sisto-diast¾licos con presi¾n de pulso disminuida, por ejemplo, 130/94 y 140/100.
Analizando los factores que regulan la presi¾n arterial, que es el resultado del gasto cardĒaco por la resistencia vascular perifķrica, era l¾gico no buscar receptores de vasodilatadores, sino factores que afectaran la vasodilataci¾n y el tono miogķnico, entre los cuales los canales de K pueden ser importantes. La hipertensi¾n diast¾lica siempre ha sido muy discutida y hay muchos trabajos al respecto, pues en un principio se pensaba que no existĒa verdaderamente, que podĒa ser s¾lo un fen¾meno auscultatorio, y habĒa mucho escepticismo.
Estudiamos este punto midiendo la presi¾n con otro mķtodo distinto del auscultatorio, el MAPA (Monitoreo Ambulatorio de la Presi¾n Arterial), y observamos que, entre los pacientes que por mķtodo auscultatorio eran diast¾licos aislados o sisto-diast¾licos predominantemente diast¾licos, s¾lo cuatro no encajaban en alguna de estas dos categorĒas; por lo tanto, la mayorĒa de los pacientes que son hipertensos diast¾licos predominantes por mķtodo auscultatorio tambiķn lo son por MAPA.
Por lo tanto, estamos trabajando con los hipertensos diast¾licos predominantes, este grupo incluye pacientes diast¾licos aislados, y sisto-diast¾licos con presi¾n de pulso disminuida.
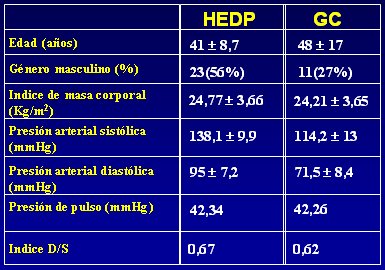
Fue difĒcil fomar el grupo control, porque el hecho de que una persona de cuarenta a±os sea normotensa no asegura que en dos a±os mßs no desarrolle hipertensi¾n, de modo que este grupo qued¾ conformado por personas normotensas mayores de 65 a±os y personas mßs j¾venes, cercanas a los 40 a±os, que no tuvieran familiares hipertensos (ni padres ni ninguno de los cuatro abuelos). Los parßmetros clĒnicos de ambos grupos se muestran en la Tabla I.
Tabla I. Parßmetros clĒnicos de hipertensos esenciales predominantemente diast¾licos (HEDP) y grupo control (GC).
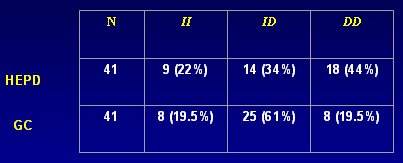
Tambiķn se determin¾ la relaci¾n con el genotipo ID de la enzima convertidora de angiotensina (ACE), la que tiene dos tipos, con inserci¾n o deleci¾n; muchos estudios han demostrado que los pacientes portadores de II tienen menos ACE en plasma que los individuos DD. Los resultados se muestran en la Tabla II. Si se observa las presiones del grupo control, 114/71, que son bastante mßs bajas que los grupos control del resto de la literatura, se puede ver que en los pacientes hipertensos predominantemente diast¾licos la proporci¾n de DD es mucho mayor que en el grupo control, aunque esto no es significativo, probablemente por el peque±o n·mero de pacientes, pero podrĒa estar ocurriendo un mecanismo distinto y quizßs no todos los diast¾licos tienen su problema en los canales de K; podrĒan existir fenotipos que produzcan mayor vasoconstricci¾n y por lo tanto, desarrollen mßs hipertensi¾n.
Tabla II. Determinaci¾n de genotipo I/D ACE. Test Chi cuadrado: DD vs. ID vs. II (p <0,0301).
Por ·ltimo, en lo que se refiere a ciencias bßsicas, estamos estudiando la uni¾n entre KCNA 10 y KCNA4B. Se sabe que ambos se unen por un segmento de 50 aminoßcidos en KCNA10. Estamos haciendo constructos con deleciones sucesivas del gen para identificar exactamente el sitio de uni¾n entre ambas subunidades.
Tambiķn estamos tratando de hacer la co-localizaci¾n de KCNA10 y KCNA4B en tejidos humanos y en ri±¾n. Queremos demostrar que ademßs de estar estas subunidades en el ri±¾n, estßn tambiķn en la misma cķlula e incluso, en el mismo lado de la membrana, ya sea apical o basolateral.












 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

La publicaci¾n de estas Actas CientĒficas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y la Sociedad Chilena de NefrologĒa.
 Expositor:
Marcelo OrĒas[1]
Expositor:
Marcelo OrĒas[1]

Citaci¾n: OrĒas M. The role of potassium channels in regulating blood pressure. Medwave 2005 Ago;5(7):e2312 doi: 10.5867/medwave.2005.07.2312
Fecha de publicaci¾n: 1/8/2005

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n