Resumen
Este texto completo es la transcripción editada y revisada de la conferencia dictada en reunión clínica del Departamento de Medicina, Hospital Clínico Universidad de Chile. La publicación de estas actas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
Epidemiología de VIH y SIDA
El Síndrome de Inmunodeficiencia Adquirida (SIDA) se describió en 1981, en un grupo de hombres jóvenes, de tendencia homosexual, que presentaron sarcoma de Kaposi, tumor poco frecuente en la población humana, incluso entre inmunodeprimidos, y neumonía por
Pneumocystis carinii, hoy
Pneumocystis jiroveci.
En el último informe de personas infectadas con el Virus de Inmunodeficiencia Humana (VIH) y portadoras de SIDA, se estimó que en diciembre de 2006, alrededor de 39,5 millones de personas en el mundo vivían con el virus; de ellas, 37 millones eran adultos, de los cuales 17 millones eran mujeres y 2,3 millones eran menores de 15 ańos. Durante 2006 hubo 4,3 millones de nuevos infectados, de los cuales 3,8 millones de casos se produjeron en adultos y el resto, en menores de 15 ańos y durante ese ańo hubo 2,9 millones de defunciones por SIDA (2,6 de éstas, en adultos).
De los 40 millones de personas que vivían con el VIH en el mundo en el ańo 2006, más de la mitad, es decir, casi 25 millones de personas, vivían en África subsahariana, hecho muy preocupante, porque en esta zona, al igual que en Europa Oriental y Asia, no hay acceso adecuado al tratamiento con triterapia. De los 4,3 millones de casos nuevos que hubo en 2006, casi 3 millones ocurrieron en África subsahariana, mientras que en América Latina hubo 140.000 nuevas infecciones durante ese ańo. En cuanto a los fallecimientos, de los 3 millones ocurridos en 2006, más de 2 millones ocurrieron en África subsahariana. En algunas zonas de África, más de 30% de la población está infectada con el virus.
Se estima que cada día aparecen alrededor de 11.000 a 14.000 nuevos casos de infección por VIH, de los cuales: más de 95% se producen en países de bajos y medianos ingresos; cerca de 1500 corresponden a nińos menores de 15 ańos y cerca de 10.000, a adultos (15 ańos o más); de éstos, 50% son mujeres y 40% tienen entre 15 y 24 ańos de edad.
América Latina y el Caribe se caracterizan por la diversidad de patrones de transmisión del VIH. En el Caribe la transmisión es, en general, heterosexual, constituye la segunda región del mundo en cuanto a magnitud de la epidemia y la prevalencia en embarazadas alcanza a 13%; en Uruguay y Argentina, más de 20% de la transmisión de la infección tiene lugar por vía endovenosa, principalmente por uso de drogas inyectables; en cambio, en Chile predomina la transmisión por vía sexual, sea homo o bisexual, al igual que en Brasil, que tiene un patrón de transmisión similar al de Chile.
La realidad chilena se encuentra cuantificada hasta noviembre de 2005; los datos son los siguientes:
- El primer caso de SIDA en Chile data de 1984, y a noviembre de 2005 hay 15.853 personas infectadas, incluyendo portadores de infección asintomática por VIH y casos de SIDA, de las cuales, 85% son hombres y 15%, mujeres.
- La tasa de incidencia acumulada promedio del país es de 58 por 100.000 habitantes; en cuanto a la distribución de los casos, tanto de SIDA como de infección asintomática por VIH, en las distintas regiones del país, la casuística se concentra principalmente en la Región Metropolitana, seguida de las regiones I, II y V.
- La relación hombre/mujer, en los casos tanto de SIDA como de VIH, se ha ido estrechando y hoy se acerca a 4 ó 5 hombres por 1 mujer.
- En relación con la edad, 90% de los casos de SIDA se concentran entre los 20 y 49 ańos, mientras que en los de infección asintomática por VIH, la mayor parte de la población se concentra en el grupo etario entre los 20 y 39 ańos.
- Con respecto a las vías de transmisión, en 94% de los casos SIDA acumulados en Chile la infección se adquiere por transmisión sexual.
- En la mayoría de los casos la transmisión ocurre por contacto homo-bi sexual, pero también ocurre por contacto heterosexual, lo que hace que en Chile haya ocurrido una feminización de los casos.
- En 4% de los casos la vía de transmisión es sanguínea, debido casi exclusivamente al uso de drogas endovenosas.
- La transmisión vertical se ha logrado reducir a menos de 2% en Chile, gracias al programa de control y tratamiento de embarazadas durante el embarazo, parto y posparto.
Virus y patogenia
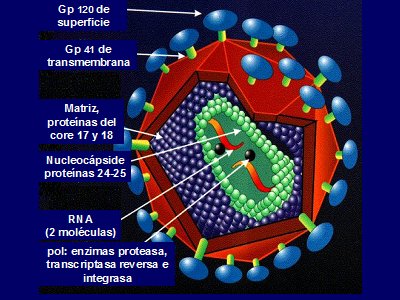
El VIH es un retrovirus, cuya estructura presenta una envoltura en la que se encuentran insertas la glicoproteína (gp) 41 de transmembrana y gp 120 de superficie; ésta se ubica hacia el exterior y constituye un elemento muy importante para el ingreso del virus a la célula. Hacia el interior se ubican la matriz, las proteínas 17 y 18, que forman parte del núcleo y las proteínas 24 y 25, que forman parte de la nucleocápside. Más al interior se encuentran las dos hebras de RNA que codifican los tres genes estructurales del virus. También en la núcleocápside se encuentran enzimas muy importantes para la replicación del virus, como la proteasa, la transcriptasa reversa y la integrasa (Fig. 1).
Figura 1. Estructura del VIH
El genoma es relativamente pequeńo: contiene poco menos de 10.000 pares de bases y posee tres genes estructurales, que son los genes gag, pol y env. El gen gag codifica para proteínas de la nucleocápside y la matriz, el pol codifica para las enzimas del virus y el gen env codifica para el precursor gp160, que da origen a las dos glicoproteínas de envoltura, la gp120 y la gp41. Hay por lo menos seis otros genes importantes en la regulación de la expresión y de la replicación del virus. En ambos extremos del genoma se ubican las LTR (regiones laterales del genoma), que corresponden a secuencias nucleotídicas repetidas que permiten que el virus se inserte al azar en el genoma humano. La gp120 tiene seis dominios constantes y cinco dominios variables.
El estudio genético de las secuencias del gen de la envoltura ha permitido identificar tres grupos de VIH-1: M (principal), O (outliyer) y N (new); dentro del grupo M se han identificado varios subtipos, que se denominan con letras de la A a la K. Esto ha permitido establecer la epidemiología molecular del VIH en todo el mundo. Según un estudio conjunto, que realizó nuestra sección en colaboración con Francia y se publicó en la revista AIDS, 75 a 80% de las cepas chilenas pertenecen al subtipo B, al igual que en América del Norte y Europa. El grupo O se encuentra en Camerún, Gabón y Francia y el grupo N, descrito recientemente, está principalmente en Camerún. También han aparecido subtipos recombinantes circulantes, como BF, AC, BC, entre otros, y en Chile, igual que en Argentina y Brasil, se ha logrado identificar el subtipo BF. La importancia clínica de hacer la genotipificación está dada porque existen diferencias entre los distintos subtipos en cuanto a tropismo, virulencia y susceptibilidad del virus frente a las drogas anti-retrovirales; por ejemplo, hoy se sabe que el subtipo C es resistente en forma natural a Efavirenz, fármaco que se usa en primera línea en el mundo occidental y también en Chile.
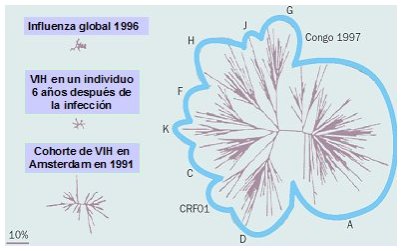
En la Fig. 2 se observa la diferencia de la variabilidad genética entre el VIH y el virus de la Influenza. Es evidente la distancia genética entre un subtipo y otro, si se hace una comparación entre lo que se encuentra en la epidemia global de influenza de 1996 y lo que se ve seis ańos después de la infección en un solo individuo; esto se debe a la alta tasa de replicación del virus y a la alta tasa de error de la transcriptasa reversa, que va incorporando mutaciones muy frecuentemente. En una cohorte de 18 pacientes en Amsterdam, en 1991, las distancias son aun mayores y en una cohorte del Congo, en 1997, ya hay entre 20% y 30% de diferencia genética.
Figura 2. Diferencias en el árbol filogenético del HIV con el paso del tiempo
Tropismo del VIH
Se denomina tropismo a tendencia del virus a infectar un tipo celular en forma preferencial. En el caso del VIH, su principal receptor en la célula es la molécula CD4, que se encuentra principalmente en los linfocitos T CD4 y también en la línea de monocitos y macrófagos; pero hoy se sabe que la molécula CD4 por sí sola no basta para permitir el ingreso del virus a la célula, sino que requiere de otras estructuras, que son los co-receptores de quemoquinas. El VIH puede utilizar 2 co-receptores: CCR5 (R5), o CXCR4 (X4), o tener tropismo dual; las cepas que utilizan las líneas de monocitos y macrófagos, que son las primeras seleccionadas para ingresar, se denominan R5 o monocitotropas; después el virus va evolucionando y cambia su tropismo a cepas X4, que son las que utilizan la línea de linfocitos.
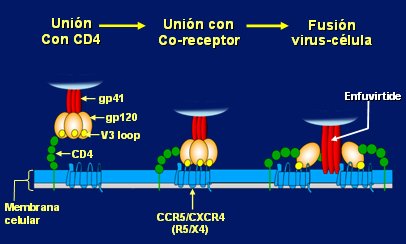
Cuando el VIH tiene tropismo CCR5, inicialmente infecta a monocitos y macrófagos, pero no los destruye, de modo que éstos constituyen una especie de reservorio celular. En cambio, las cepas que ingresan a la línea de linfocitos T utilizando el co-receptor CXCR4, son mucho más agresivas y destruyen a los linfocitos. El virus, por intermedio de la gp120, se une a la molécula CD4 e interacciona con uno u otro co-receptor, dependiendo del tropismo, produciendo un cambio estructural en la molécula; como consecuencia, la gp 41, que está unida a la gp120, se inserta en la membrana de la célula huésped y permite el proceso de fusión entre el virus y la célula. El enfuvirtide (nombre comercial T-20, Fuzeon) bloquea el proceso mencionado; es un medicamento de uso limitado en la actualidad y se utiliza en pacientes en falla virológica y que han recibido varios tratamientos (Fig. 3).
Figura 3. Tropismo VIH (Moore JP, Doms RW. PNAS 2003; 100:10598-10602)
Una vez que se cumple el proceso de fusión y el virus ingresa como pro-virus a la célula, en la nucleocápside quedan libres las dos hebras de RNA y, por acción de la transcriptasa reversa, que es una DNA polimerasa, se forma el DNA y adquiere una forma circular. Después, por acción de la integrasa, el DNA ingresa al núcleo, se inserta al azar en él y se establece una infección crónica, latente; por distintos estímulos se puede reactivar la replicación y formación de RNA mensajero de las proteínas que codificaba este material, dando inicio al proceso de ensamblaje y maduración de nuevas partículas virales. Cada uno de estos puntos o etapas es un potencial blanco de acción de medicamentos, de los cuales los que más se utilizan en la actualidad son los inhibidores de la transcriptasa reversa, los análogos y no análogos de nucleósidos y los inhibidores de la proteasa viral, aunque también existen inhibidores de fusión y nuevos medicamentos que están apareciendo, como los inhibidores de CCR5, y los inhibidores de integrasa.
Es importante recordar que el virus no sólo afecta a los linfocitos T, monocitos y macrófagos, sino también a muchas otras células; por ejemplo, a nivel hematopoyético compromete a células precursoras, como promielocitos, células dendríticas y células madre (stem cells); en el sistema nervioso central, puede atravesar precozmente la barrera hematoencefálica e infectar a células epiteliales, oligodendrocitos, astrocitos y microglía; en el tubo digestivo hoy se sabe que hay distintos receptores a través de los cuales el virus se puede fijar directamente a la mucosa e ingresar, afectando a células enterocromafines, células de epitelio columnar, macrófagos y linfocitos estromales.
El tropismo es importante en la evolución de la infección por VIH, que en su etapa inicial se caracateriza por una selección natural de las cepas monocitotropas o R5, que ingresan a los monocitos y macrófagos, por tanto, tienen escaso efecto citopático y de destrucción del sistema inmune; pero, a medida que va transcurriendo el tiempo, el tropismo va adoptando una forma dual, de tal modo que el virus ingresa a la línea de monocitos y macrófagos, pero también a la línea de los linfocitos. En una etapa más tardía las células son más bien linfocitotropas, con efecto citopático importante y formación de sincicios, lo que se asocia a una destrucción acelerada del sistema inmune.
Múltiples mecanismos de transmisión sexual del VIH
El virus puede ingresar al epitelio columnar del tubo digestivo de tres maneras: por medio de un receptor que se sitúa en el epitelio columnar y que es un glicolípido, denominado galactosilceramida, al cual el virus se puede unir y así infectar directamente esa célula, empezando a producir virus a partir de ella; o bien, por transcitosis, uniéndose a haspartán sulfato; o por transmigración. Desde allí el virus atraviesa la lámina propia e infecta en especial a las células dendríticas, encargadas de transportar el virus, vía aferente hacia los ganglios linfáticos regionales. En cambio, en la piel debe haber una lesión para que el virus pueda ingresar a las células; no hay infección con piel indemne.
A nivel de mucosas, el proceso de infección ocurre cuando se produce una exposición a cepas R5, que ingresan a las células dendríticas, las que se fusionan con los linfocitos CD4 y permiten, de este modo, que el virus llegue a los ganglios linfáticos regionales, por vía aferente. Alrededor de dos días después de la exposición de riesgo el virus ya se encuentra a nivel ganglionar, donde queda secuestrado y comienza a formar centros germinales; luego se infectan otros linfocitos, se activa la respuesta inmune contra el virus y éste comienza a migrar hacia territorios ganglionares a distancia. Tres a cinco días después de ocurrido el contagio, el virus puede estar circulando en el torrente sanguíneo.
Es muy importante conocer la dinámica de la infección por VIH. Las partículas virales libres circulantes, o viriones, provienen en 90% a 99% de linfocitos CD4 activados que se infectan con el virus, los cuales comienzan a formar nuevos virus a razón de 2,6 días por generación, produciendo de 10^9 a 10^10 partículas virales. La vida media de los viriones circulantes es de seis horas y la vida media de una célula infectada es de 1,6 días. Entre 1% y 7% de los viriones provienen de otras líneas celulares, entre ellas células de larga sobrevida, como los monocitos y macrófagos, y linfocitos CD4 infectados en forma latente, en reposo. Lo importante es que el tratamiento que hoy se utiliza puede bloquear en forma efectiva la replicación del virus desde células T activadas, y reducir la carga viral en 90% a 99%, pero si se suspende, hay otras poblaciones celulares capaces de regenerar la carga viral, a pesar de ser minoritarias.
En el sistema nervioso central, el virus puede infectar y atravesar la barrera hematoencefálica, infectar astrocitos, oligodendrocitos y producir un microambiente de citoquinas y partículas virales en el líquido cefalorraquídeo. Además, el sistema nervioso central constituye un reservorio anatómico importante. La acción de las citoquinas y las partículas virales produce neurotoxicidad directa y además bloquea la conducción neurosináptica, lo que ocasiona diversos síntomas neurológicos como cuadros de encefalopatía subaguda, que se manifiesta como un complejo de demencia asociada a VIH, mielopatía vacuolar y neuropatía periférica, que se presenta como síndrome de Guillain-Barré.
Historia natural de la infección
Durante la infección primaria, el virus ingresa al organismo y se replica rápidamente, de modo que en las primeras semanas se produce la mayor carga viral, en forma concomitante a una caída transitoria de los linfocitos CD4 que por lo general no es muy marcada, aunque nunca se recuperan los valores normales; a veces esta baja es marcada y puede llevar a confusión; por ejemplo, hay casos de pacientes que se presentan con candidiasis esofágica o neumonía por
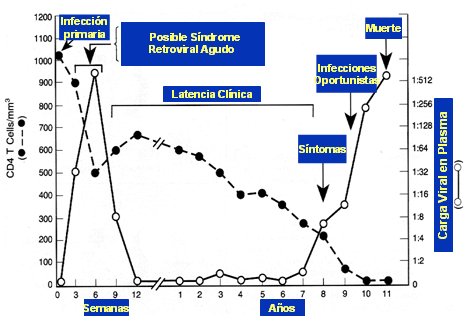
Pneumocystis jiroveci, por lo que se piensa que se encuentran en un estado avanzado de la enfermedad, pero, en realidad, las infecciones se deben a la baja de linfocitos CD4 propia de la infección primaria; si bien esta situación es excepcional, no hay que descartarla. Después de esta fase puede aparecer un síndrome retroviral agudo y después de seis semanas de ocurrida la infección primaria comienza un largo período de latencia clínica, que dura entre 7 y 10 ańos, en que el paciente se encuentra asintomático, a pesar de tener algunas alteraciones de laboratorio. Después aparece el cuadro clínico florido, con síntomas constitucionales y luego, infecciones oportunistas y muerte. Estas son las fases de la historia natural de la infección viral sin tratamiento (Fig. 4).
Figura 4. Historia natural de la infección VIH
Con la introducción de la terapia antirretroviral la situación de la infección por VIH ha cambiado notablemente, a tal punto que ya no se considera una enfermedad mortal, sino una enfermedad crónica y controlable, que no debiera avanzar hacia su estado final, a menos que el diagnóstico se haga en forma muy tardía en presencia de estas patologías indicadoras, y con importante destrucción del sistema inmune.
Los compartimentos tisulares de distribución del VIH explican su patogenia. En general, el virus se encuentra en el plasma, en las células mononucleadas circulantes y en los ganglios y órganos linfáticos, los que constituyen un importante sitio de replicación viral. También se ubica en las gónadas, que son otro reservorio, en el sistema nervioso central y en otros tejidos, como el timo y la médula ósea.
En las etapas iniciales los niveles de viremia disminuyen, a medida que el virus va siendo secuestrado a nivel ganglionar, donde forma centros germinales; a medida que avanza la enfermedad, los ganglios comienzan a presentar infiltración grasa, pérdida de la arquitectura, fibrosis y aumento de la carga viral en plasma; en etapas tardías, sin tratamiento, casi la totalidad del virus se encuentra circulando y se observa pérdida de la arquitectura ganglionar, con infiltración grasa e intensa fibrosis.
En suma, el tejido linfoide cumple un rol clave en la patogenia de la infección por VIH, ya que es reservorio del virus, sitio de replicación viral en todas las etapas de la enfermedad, sitio de secuestro de viriones libres por las células dendrítico foliculares y sitio de exposición de células susceptibles a numerosos virus; así, las células sanas tienen grandes probabilidades de infectarse al pasar por los ganglios linfáticos.





Esta
obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.








 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Expositor:
Alejandro Afani[1]
Expositor:
Alejandro Afani[1]

