Este texto completo es la transcripci¾n editada de una conferencia dictada en reuni¾n clĒnica del Departamento de Medicina, Hospital ClĒnico Universidad de Chile. La publicaci¾n de estas actas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y el Departamento de Medicina del Hospital ClĒnico Universidad de Chile. El director del Departamento de Medicina es el Dr. Alejandro Cotera.
El cßncer es la segunda causa de muerte en Chile; la morbilidad y letalidad son importantes en la mayorĒa de las etapas y en casi todos los tumores. Frente a esto, la terapia oncol¾gica ha mostrado grandes avances y en la actualidad consiste en un tratamiento multidisciplinario, que se basa en dos pilares: las terapias locales, representadas por dos alternativas terapķuticas: la cirugĒa y la radioterapia; y las terapias sistķmicas: quimioterapia, terapias target, inmunoterapia y hormonoterapia. Todas ellas tienen su indicaci¾n precisa en determinadas situaciones oncol¾gicas.
En Chile s¾lo hay estudios de mortalidad, no de morbilidad, por lo que las causas de muerte por cßncer se conocen por los certificados de defunci¾n (Figs. 1 y 2). En mujeres, la primera causa de mortalidad es el cßncer de vesĒcula y vĒa biliar, seguido por el cßncer de mama, est¾mago, cervicouterino, pulm¾n, que ha aumentado en relaci¾n con el hßbito tabßquico, y otros. En el hombre, la primera causa de muerte por cßncer a·n es el cßncer gßstrico, aunque ha disminuido un poco en los ·ltimos a±os, seguido por el cßncer de pulm¾n y pr¾stata; en cambio, la incidencia de cßncer de vĒa biliar en varones es mucho menor en Chile, de modo que su importancia como causa de muerte es muy inferior; despuķs vienen es¾fago, linfomas, colon y otros.
Figura 1. Principales causas de muerte por cßncer en la mujer, Chile 2001 (Fuente: MINSAL).
Figura 2. Principales causas de muerte por cßncer en el hombre, Chile 2001 (Fuente: MINSAL).
En la Tabla I aparece un resumen de las principales causas de muerte. En el caso de pr¾stata y mama, la tasa es especĒfica por sexo, pero el cßncer de est¾mago es la principal causa de muerte por cßncer, seguido por el de pr¾stata en varones y el de mama en mujeres. Despuķs viene el cßncer de pulm¾n y vĒa biliar y mßs abajo quedan el cßncer cervicouterino, linfoma y otros.
El diagn¾stico precoz permite realizar un tratamiento con mßs impacto y eficacia, lo que cambiarĒa la evoluci¾n natural de la enfermedad, pero tambiķn influyen otros aspectos, como el tipo de tumor, su origen y la histologĒa. Por ejemplo, en ciertos tumores avanzados el tratamiento altera muy poco la evoluci¾n, con algunas excepciones, como el cßncer testicular, en el cual es posible lograr curaciones incluso en etapas muy avanzadas.
Para tener una idea de la importancia que se le asigna en la actualidad a todo lo que se relaciona con el cßncer, se hizo una revisi¾n en Pubmed con el objetivo de determinar cußntos artĒculos se habĒan publicado en Medline sobre diferentes temas en los ·ltimos 5 y 10 a±os; y se encontraron mßs de 100.000 artĒculos sobre diabetes; alrededor de 150.000 artĒculos sobre enfermedades renales, mßs de 200.000 sobre coraz¾n y 650.000 sobre cßncer (Fig. 3).
Figura 3. Investigaci¾n publicada en los 5 y 10 ·ltimos a±os.
Al analizar el ·ltimo a±o, la tendencia es similar: hay alrededor de 70.000 publicaciones sobre cßncer y las cifras son mucho menores en las otras ßreas. El cßncer de mama representa una cantidad muy importante de estas publicaciones. Por otra parte, no todas las publicaciones tienen la misma importancia; al buscar por estudios clĒnicos aleatorios en el ·ltimo a±o, se encontraron 100 publicaciones sobre insuficiencia renal y casi 200 sobre cßncer de mama, que s¾lo fue sobrepasado por la cardiopatĒa coronaria, con 300 publicaciones.
A continuaci¾n se revisarßn algunos ejemplos emblemßticos, por los avances que ha habido en su tratamiento.
El cßncer gßstrico tiene alta prevalencia en Chile y alta letalidad, incluso en etapas precoces; en algunas series se describe que cuando el paciente tiene cuatro o mßs ganglios comprometidos, la probabilidad de sobrevida libre de enfermedad al a±o es prßcticamente cero. El mejor tratamiento siempre ha sido la cirugĒa; hubo m·ltiples intentos de tratamientos adyuvantes, pero ninguno de ellos logr¾ buenos resultados, hasta que en New England Journal of Medicine, en 2001, se public¾ el estudio Macdonald, llamado asĒ por el primer autor del artĒculo (1), en el que se compar¾ el resultado de la quimio-radioterapia despuķs de la cirugĒa versus la cirugĒa sola, para determinar si los pacientes operados con intenci¾n curativa podrĒan mejorar su sobrevida, con tratamiento adicional. Macdonald incluy¾ casi todos los estadios TNM en que la cirugĒa es curativa y excluy¾ s¾lo las etapas metastßsicas. En la figura 4, la curva de Kaplan-Meier muestra la diferencia entre las curvas de sobrevida de los pacientes que recibieron quimio-radioterapia adicional, y los que se trataron solamente con cirugĒa (Fig. 4).
En cßncer de colon tambiķn ha habido avances notables, dentro del ambiente de la oncologĒa. Respecto a la sobrevida, hace varios a±os se demostr¾ que el tratamiento adyuvante con quimioterapia, con base en 5-fluoracilo, despuķs de una cirugĒa con intenci¾n curativa, mejora la sobrevida global de los pacientes; tambiķn mejora la sobrevida global en pacientes con enfermedad metastßsica que reciben tratamiento con quimioterapia, con intenci¾n paliativa. Aunque a·n se utiliza la clasificaci¾n de Dukes, seg·n la clasificaci¾n TNM la sobrevida a cinco a±os de los pacientes en etapa IV es 5% a 7%. En un metaanßlisis de ocho artĒculos sobre el efecto de la quimioterapia basada en 5-fluoracilo, se evalu¾ si la adyuvancia con quimioterapia mejoraba la sobrevida libre de enfermedad y la global, y se vio que casi todos los subgrupos se beneficiaban, siendo la excepci¾n el caso de los pacientes que no tienen ganglios comprometidos. De hecho, a·n hay controversia acerca de si hacer o no hacer quimioterapia en este grupo de pacientes.
Otro avance es la aparici¾n de nuevas drogas, entre las cuales se cuentan tres citot¾xicos: irinotecan, oxaliplatino y capecitabina, siendo esta ·ltima una forma de fluoracilo de administraci¾n oral; y dos anticuerpos monoclonales: bevacizumab y cetuximab. En 2004 se public¾ en N Engl J Med un estudio sobre el uso de oxaliplatino, realizado por investigadores del grupo MOSAIC (Multicenter International Study of Oxaliplatin/5-Fluorouracil/Leucovorin in the Adjuvant Treatment of Colon Cancer) con el objetivo de determinar si la administraci¾n de oxaliplatino, cuyo costo es elevado, sumada al fluoracilo, mejoraba la sobrevida de los pacientes (2). Se comprob¾ que en la etapa III hay un beneficio evidente en cuanto a sobrevida libre de enfermedad, pero en etapa II el beneficio no es tan claro. Se supone que a largo plazo, la mejorĒa en la sobrevida libre de enfermedad se traduce en mejorĒa de la sobrevida global, que es lo que interesa a los pacientes.
La vasculatura cambia en los procesos tumorales, en los cuales existe mayor cantidad de vasos sanguĒneos, pero ademßs aparecen vasos tortuosos, lo cual conlleva un mecanismo importante de resistencia a los medicamentos citot¾xicos. El bevacizumab (Avastin) es un anticuerpo monoclonal, cuyo blanco es el factor de crecimiento vascular endotelial; su uso hace que la vasculatura tumoral disminuya y las tortuosidades anormales desaparezcan, lo que mejora la llegada de la quimioterapia. En un estudio de laboratorio se encontr¾ que los cambios en la vasculatura aparecĒan a los tres dĒas de la administraci¾n de este medicamento (Fig. 5).
Figura 5. MicrofotografĒa. Cambios en la vasculatura tras la administraci¾n de bevacizumab.
Estos datos se llevaron a la prßctica en 2004 en otro estudio, publicado en N Engl J Med (3), en el que se adicion¾ esta molķcula a irinotecan, fluoracilo y leucovorina en pacientes con cßncer de colon metastßsico. Como se sabe, las terapias nuevas se prueban primero en pacientes con cßncer metastßsico, porque tienen menos que perder, y despuķs se trata de extrapolar esa experiencia a la adyuvancia. La adici¾n de bevacizumab gener¾ un impacto significativo en la sobrevida global.
El EGFR (Epidermal Growth Factor Receptor) es un receptor de membrana con dominio extracelular, transmembrana e intracelular. Mediante la fosforilaci¾n y una serie de otros mecanismos, este receptor se sobreexpresa en las cķlulas tumorales, lo que hace que se activen genes de progresi¾n del ciclo celular, aumentando la proliferaci¾n, la sobrevida, la angiogķnesis y la capacidad de generar metßstasis. Un anticuerpo monoclonal podrĒa limitar todo este proceso, al igual que molķculas peque±as que a nivel intracelular inhiban una etapa especĒfica. El estudio de este receptor permiti¾ dise±ar un anticuerpo monoclonal dirigido contra ķl, el cetuximab, que se prob¾ inicialmente en pacientes refractarios a la quimioterapia con irinotecan, que es el tratamiento de primera lĒnea en cßncer de colon metastßsico. Si bien se evidenci¾ un peque±o beneficio con la adici¾n de cetuximab en pacientes no respondedores a irinotecan, se presume que hay un mecanismo adicional, que estß en estudio, mediante el cual esta molķcula harĒa que las cķlulas tumorales que habĒan dejado de responder, recuperen la sensiblilidad a este fßrmaco.
En resumen, cuando s¾lo existĒa tratamiento quir·rgico, la sobrevida media en cßncer de colon metastßsico era de seis meses; despuķs de la aparici¾n de quimioterapia con fluoracilo, la sobrevida lleg¾ a 10 ¾ 12 meses. Al agregar alg·n fßrmaco citot¾xico nuevo, como irinotecan u oxaliplatino, la sobrevida media aument¾ a entre 14 y 16 meses. En la actualidad, con la combinaci¾n secuencial de fßrmacos citot¾xicos mßs terapias target, la sobrevida es superior a 20 meses.
Es un tumor maligno, mßs frecuente en adultos, que tiene una sobrevida media de un a±o desde el momento del diagn¾stico y una mortalidad cercana a 100% antes de dos a±os. El tratamiento estßndar es la cirugĒa y la radioterapia, a lo que se ha agregado la adyuvancia con nitrosureas desde hace varios a±os, tanto en los Estados Unidos como en Chile, aunque ning·n trabajo de fase 3 aleatorio ha demostrado que esta quimioterapia adyuvante mejore la sobrevida. En 2005 se public¾ en N Engl J Med un artĒculo sobre radioterapia y terapia adyuvante con temozolomide en glioblastoma multiforme (4), en el que se encontr¾ una diferencia importante en la sobrevida total de los pacientes sometidos a tratamiento asociado, en comparaci¾n con el grupo que recibi¾ tratamiento estßndar, que es s¾lo radioterapia (Fig. 6).
Una de las crĒticas frecuentes que se hace a la oncologĒa es que obliga a los pacientes a gastar grandes sumas de dinero para lograr discretas mejorĒas en la sobrevida; por ejemplo, en el estudio anterior la sobrevida media con la terapia estßndar fue de doce meses, mientras que con la radioterapia mßs temozolomide fue de catorce meses, diferencia que muchos pueden estimar de poca cuantĒa. Sin embargo, si se analiza desde otra perspectiva, s¾lo 20% de los pacientes tratados con radioterapia estßn vivos, cifra que alcanza a casi 40% entre los pacientes que recibieron tratamiento asociado. Por eso, en la FDA de los Estados Unidos aprob¾ este tratamiento y nadie lo cuestiona mayormente, salvo en el aspecto econ¾mico, porque ademßs la toxicidad de la terapia es bastante baja en el tratamiento oral.
Antes, el tratamiento estßndar de este tipo de cßncer era la cirugĒa radical, porque se decĒa que este tumor era quimiorrefractario. Los pacientes con esta patologĒa tienen una sobrevida relativamente larga, porque no es un cßncer tan agresivo como otros; sin embargo, es una sobrevida de mala calidad, por la patologĒa ¾sea que se genera en forma secundaria. Hoy se sabe que la radioterapia es una alternativa terapķutica como tratamiento primario; es decir, la radioterapia es un excelente tratamiento en algunos pacientes como alternativa a la cirugĒa, dado que las tasas de sobrevida son bastante parecidas. Lo anterior es vßlido, sobre todo, en pacientes a±osos en quienes la cirugĒa puede ser bastante complicada. En pacientes que se han sometido a cirugĒa curativa radical, pero persisten con mßrgenes positivos o tienen otros factores de riesgo, la radioterapia coadyuvante postoperatoria cumple un papel fundamental. Por otro lado, en algunos estudios se describe que el uso de bifosfonatos reduce el dolor y el riesgo de episodios ¾seos en pacientes con enfermedad basal. La hormonoterapia tambiķn es un tratamiento potente y eficaz en el manejo de los tumores hormonosensibles.
Hay interacciones entre las cķlulas metastßsicas prostßticas, los osteoclastos y los osteoblastos: las cķlulas tumorales estimulan, a travķs de citoquinas, el crecimiento osteoblßstico y osteoclßstico, con lo que se altera el equilibrio, aumenta la actividad osteoblßstica y, a su vez, las mismas citoquinas que liberan los osteoblastos estimula el crecimiento de las cķlulas tumorales. Al principio se usaron bifosfonatos de primera generaci¾n en pacientes con metßstasis, pero no se consigui¾ un alivio significativo con ninguna de estas sustancias. El ßcido zoledr¾nico tiene mßs ventajas que el pamidronato, pero ķste es el que mßs se utiliza, por razones de costo. El zolendronato reduce el riesgo de fracturas y de dolor ¾seo.
Antes se consideraba al cßncer de pr¾stata como un tumor quimiorresistente y su tratamiento estßndar era mitoxantrona con prednisona, porque esta combinaci¾n mejoraba la calidad de vida de los pacientes, aunque no la sobrevida, hasta fines de 2004, en que se public¾ un estudio en el que se describi¾ una diferencia significativa en la sobrevida global al asociar docetaxel, cada tres semanas, a la combinaci¾n mitoxantrona mßs prednisona (5). Entonces, en la era actual el cßncer de pr¾stata se considera quimiosensible y se han desarrollado quimioterapias capaces de mejorar la sobrevida global. Una crĒtica frecuente a los tratamientos oncol¾gicos se refiere a la calidad de vida; en este caso, como el tratamiento quimioterßpico estßndar era mitoxantrona-prednisona, se evalu¾ la calidad de vida mediante un cuestionario y se encontr¾ que la asociaci¾n con docetaxel mejoraba la calidad de vida en forma significativa, en comparaci¾n con el tratamiento estßndar.
El tratamiento clßsico del cßncer de mama ha sido la cirugĒa. En 1976 apareci¾ el primer trabajo que mostraba que la sobrevida era superior cuando la paciente ingresaba a una poliquimioterapia despuķs de la cirugĒa (6). En la era moderna, ciertos metaanßlisis demuestran la superioridad del uso de antraciclinas respecto a las quimioterapias antiguas, como CMF (ciclofosfamida, metotrexato y fluorouracilo). En la actualidad han aparecido los taxanos, una nueva familia de fßrmacos que ha demostrado una mejorĒa peque±a, pero significativa, frente a la quimioterapia con antraciclinas. En el mayor estudio aleatorio sobre adyuvancia en cßncer de mama, se encontr¾ que la adici¾n de taxanos, en este caso paclitaxel y docetaxel, mejora en forma sigificativa la sobrevida global, en comparaci¾n con las terapias estßndar basadas en antraciclinas. Tambiķn se han estudiado tratamientos neoadyuvantes, es decir, tratamientos preoperatorios; si bien no se ha demostrado una sobrevida global mayor como en la adici¾n de taxanos, sĒ mejora la tasa de respuesta local, lo que permite realizar cirugĒas mßs completas o menos radicales.
Para estimar los beneficios de las quimioterapias en pacientes con cßncer, existen bases de datos lo bastante grandes para saber lo que pasa cuando se usa uno u otro tratamiento, o cuando no se indica tratamiento, en tres tipos de cßncer. Para cßncer de mama se puede consultar el sitio www.adyuvantonline.com, cuya base de datos es de los Estados Unidos. La quimioterapia adyuvante depende de la decisi¾n del paciente y de su percepci¾n del beneficio y la toxicidad de la quimioterapia. En los Estados Unidos se entrevist¾ a un grupo de pacientes con cßncer antes de empezar tratamiento, para saber con quķ porcentaje de vida libre de enfermedad a 10 a±os ellos se someterĒan a un tratamiento cuya toxicidad no era despreciable. Se encontr¾ que cuando se ofrecĒa un beneficio de mßs de 10% todos los pacientes decidĒan tratarse, a pesar de la toxicidad; con cifras menores de 5% ¾ 3% los pacientes rechazaban el tratamiento y con valores intermedios la respuesta era variable. Esto confirma nuestra postura, en el sentido de que la decisi¾n de efectuar un tratamiento adyuvante o paliativo debe ser tomada por el paciente; el mķdico siempre va a querer hacer el tratamiento, pero tanto los beneficios como la toxicidad de ķste recaerßn sobre el paciente, de modo que el deber del mķdico es entregarle en la mejor forma posible la informaci¾n disponible, con cifras y datos objetivos, para que pueda tomar su decisi¾n.
En la Figura 7 se muestra un ejemplo de c¾mo cualquier persona puede estimar los beneficios de una quimioterapia adyuvante, por ejemplo, en cßncer de mama. Se muestra el caso de una mujer de 60 a±os, sin comorbilidad significativa, con receptores de estr¾geno positivos y grado tumoral 3, en un tumor de 2,5 cm, es decir, peque±o, T2, con seis ganglios positivos. El riesgo de recaĒda de esta paciente a 10 a±os es de 84%; el riesgo de muerte por cßncer a 10 a±os es de 63%. En verde se muestran las pacientes que van a estar vivas a diez a±os; en rojo, los que van a haber muerto de cßncer en ese lapso; y en azul, las muertes por otras causas. La hormonoterapia entrega un beneficio de 12,7%; la quimioterapia, de 10% y el tratamiento combinado, de 21,4%. Ademßs del cßncer de mama, esta base de datos tambiķn existe para cßncer de colon y para melanoma; asĒ se puede ofrecer al paciente un dato objetivo y preguntarle si por ese beneficio estß dispuesto a tratarse, en este caso, con la quimioterapia citot¾xica. La decisi¾n y la recomendaci¾n de hacer quimioterapia es mßs objetiva de lo que algunas personas creen.
Trastuzumab (Herceptin) es un anticuerpo monoclonal que ha revolucionado la adyuvancia y el cßncer de mama metastßsico. Esta molķcula bloquea el receptor HER2 (Human Epidermal Growth Factor Receptor-2), cuyo oncogen estß amplificado en 40% de los casos de cßncer de mama. Es probable que el factor de crecimiento epidķrmico, ligando de este receptor, genere multiplicaci¾n celular, metßstasis, supervivencia de la cķlula y bloquee la vĒa de la apoptosis. En 2001 se vio que la adici¾n de trastuzumab en pacientes con cßncer de mama metastßsico que recibĒan quimioterapia mejoraba significativamente la sobrevida, en comparaci¾n con la quimioterapia sola (7). En 2005 apareci¾ un estudio (8) en el que se evaluaron pacientes con cßncer de mama con HER2 positivo, con cirugĒas curativas, es decir, pacientes no metastßsicas, para ver si este anticuerpo mejoraba la sobreviva. El informe inicial, que fue publicado en tiempo rķcord, demostr¾ que la sobrevida libre de enfermedad era significativamente mayor despuķs de un a±o de uso de trastazumab, en comparaci¾n con las pacientes que usaron s¾lo la terapia estßndar con quimioterapia.
En el cßncer de mama se ha comenzado a explorar una serie de alternativas terapķuticas; cada una de estas molķculas no es la soluci¾n del cßncer, pero aporta un porcentaje de beneficio que se suma al de los tratamientos existentes.
El tratamiento estßndar del cßncer de pulm¾n de cķlulas no peque±as fue, hasta hace poco tiempo, la cirugĒa. En m·ltiples trabajos se ha tratado de demostrar el beneficio de hacer quimioterapia adyuvante a estos pacientes; un metaanßlisis de 1995 demostr¾ que habĒa un peque±o beneficio, pero no era significativo; los italianos, en un estudio mundial que incluy¾ a muchos pacientes tratados con cisplatino, publicaron que podĒa haber un beneficio de 4% a 5%, muy discreto, pero estadĒsticamente significativo. En un estudio publicado en New England Journal of Medicine se encontr¾ un aumento en la sobrevida global en los pacientes operados con cßncer pulmonar en etapa II, de cķlulas no peque±as, si recibĒan cisplatino y vinorelbine, con un beneficio de 15% (9). La sobrevida global siempre depende de cisplatino, que sigue siendo la piedra angular en la terapia del cßncer de pulm¾n de cķlulas no peque±as. El estudio CALGB 9633, que abarc¾ un n·mero importante de casos, demostr¾ que la combinaci¾n carboplatino y paclitaxel genera un 12% de beneficio; y el estudio ANITA (Adjuvant Navelbine International Trialist Association), que utiliz¾ nabelvine-cisplatino, demostr¾ un 8,6% de beneficio.
La guĒa oncol¾gica actual es obra de la NCCN (National Comprehensive Cancer Network), de los Estados Unidos y exige un nivel de evidencia importante para modificar un estßndar de tratamiento. En 2006, en cßncer de pulm¾n, la NCCN consider¾ que la quimioterapia adyuvante en etapa II y III estß en categorĒa uno, es decir, una recomendaci¾n de primera lĒnea. En Chile todavĒa estamos lejos de esa realidad.
Los avances en oncologĒa ocurren a una velocidad vertiginosa, lo que exige una actualizaci¾n constante. La cantidad de informaci¾n se ha potenciado con la respuesta de las industrias farmacķuticas, que han producido nuevos fßrmacos y han generado una gran cantidad de informaci¾n, aunque lamentablemente, muchas veces los adelantos no se pueden financiar en paĒses como Chile. Existen importantes avances en el manejo del cßncer en todas las ßreas; en esta conferencia se mostraron algunos ejemplos, pero tambiķn se podrĒa hablar de cßncer de ovario, cabeza y cuello, testĒculo, cevicouterino, renal, tiroides, pßncreas, etc.
La cirugĒa todavĒa es el pilar fundamental en el tratamiento, pero es posible que pronto ceda su lugar a la oncologĒa mķdica. Por ejemplo, antes, el estßndar de tratamiento del cßncer de ano era la cirugĒa de Miles, que dejaba al paciente colostomizado de por vida, pero ahora se hace tratamiento con quimiorradioterapia, la cual permite mantener el esfĒnter, con tasas de respuesta equivalentes. En la medida en que la oncologĒa siga avanzando, es probable que esta situaci¾n se extrapole a otros tumores.
El tratamiento integral sigue siendo fundamental. Muchas veces se ven pacientes que han sido evaluados por un mķdico que no se dedica a cßncer y que realiza indicaciones inadecuadas, con lo que marcan el pron¾stico del paciente; tambiķn hay mķdicos que s¾lo hacen el diagn¾stico de cßncer, pero no se dedican a hacer el seguimiento ni a conocer la respuesta. El primer tratamiento del cßncer es fundamental para definir el pron¾stico del paciente; por eso, siempre se debe presentar el caso a los onc¾logos mķdicos y a un comitķ multidisciplinario que se haya constituido especialmente para diagnosticar y tratar el cßncer, para asĒ recomendarle al paciente la mejor alternativa terapķutica.

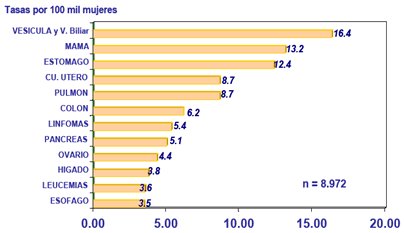 Figura 1. Principales causas de muerte por cßncer en la mujer, Chile 2001 (Fuente: MINSAL).
Figura 1. Principales causas de muerte por cßncer en la mujer, Chile 2001 (Fuente: MINSAL).

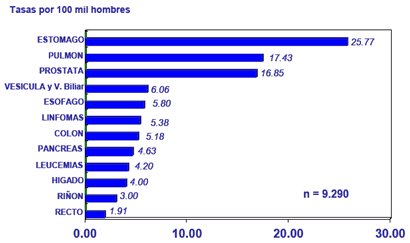 Figura 2. Principales causas de muerte por cßncer en el hombre, Chile 2001 (Fuente: MINSAL).
Figura 2. Principales causas de muerte por cßncer en el hombre, Chile 2001 (Fuente: MINSAL).

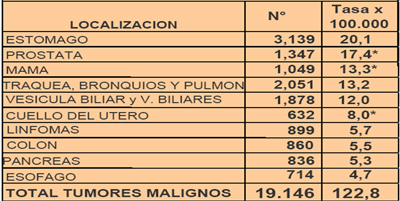 Tabla I. N·mero y tasa de mortalidad por cßncer: 10 principales localizaciones, Chile 2002 (Fuente: INE DEIS MINSAL Unidad de Cßncer).
Tabla I. N·mero y tasa de mortalidad por cßncer: 10 principales localizaciones, Chile 2002 (Fuente: INE DEIS MINSAL Unidad de Cßncer).

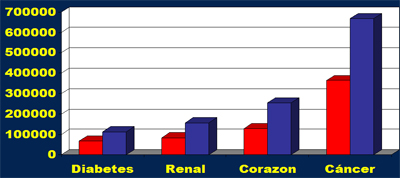 Figura 3. Investigaci¾n publicada en los 5 y 10 ·ltimos a±os.
Figura 3. Investigaci¾n publicada en los 5 y 10 ·ltimos a±os.

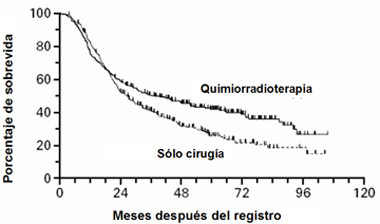 Figura 4. Sobrevida global entre todos los pacientes elegidos, seg·n el grupo de tratamiento asignado (Macdonald JS. N Engl J Med 2001).
Figura 4. Sobrevida global entre todos los pacientes elegidos, seg·n el grupo de tratamiento asignado (Macdonald JS. N Engl J Med 2001).

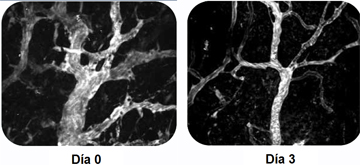 Figura 5. MicrofotografĒa. Cambios en la vasculatura tras la administraci¾n de bevacizumab.
Figura 5. MicrofotografĒa. Cambios en la vasculatura tras la administraci¾n de bevacizumab.

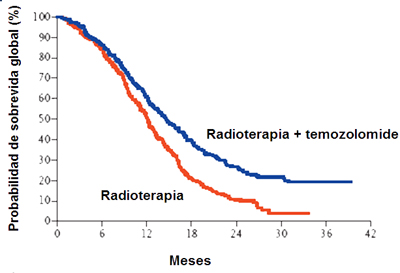 Figura 6. Estimaci¾n de sobrevida global de pacientes con glioblastoma multiforme, seg·n tipo de tratamiento (Stupp R. N Engl J Med 2005).
Figura 6. Estimaci¾n de sobrevida global de pacientes con glioblastoma multiforme, seg·n tipo de tratamiento (Stupp R. N Engl J Med 2005).

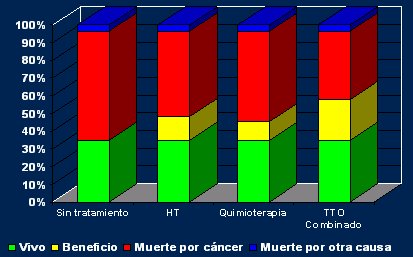 Figura 7. Estimaci¾n de riesgo de muerte y beneficio de tratamiento a 10 a±os (Fuente: www.adyuvantonline.com).
Figura 7. Estimaci¾n de riesgo de muerte y beneficio de tratamiento a 10 a±os (Fuente: www.adyuvantonline.com).
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada de una conferencia dictada en reuni¾n clĒnica del Departamento de Medicina, Hospital ClĒnico Universidad de Chile. La publicaci¾n de estas actas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y el Departamento de Medicina del Hospital ClĒnico Universidad de Chile. El director del Departamento de Medicina es el Dr. Alejandro Cotera.
 Expositor:
Claudio Painemal[1]
Expositor:
Claudio Painemal[1]

Citaci¾n: Painemal C. Advances in cancer treatments. Medwave 2007 Ene;7(1):e2541 doi: 10.5867/medwave.2007.01.2541
Fecha de publicaci¾n: 1/1/2007

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n