 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
La radiografía de tórax es un método diagnóstico fundamental y se deben solicitar de rutina las proyecciones posteroanterior y lateral. Tiene 50% de rendimiento diagnóstico, es decir, permite definir con bastante precisión el origen del sangrado en 50% de los casos. En pacientes menores de 40 ańos, sin lesiones en la radiografía de tórax, no fumadores y con un cuadro de evolución aguda se puede hacer un tratamiento conservador, porque lo más probable es que se trate de una bronquitis que está cursando con desgarro hemoptoico. Los pacientes mayores de 40 ańos y fumadores tienen mayor riesgo, por lo tanto, se debe investigar en forma más acuciosa la etiología de la hemoptisis. Si ésta es masiva, la radiografía facilita la decisión sobre lateralizar, el tipo de intubación, etc.
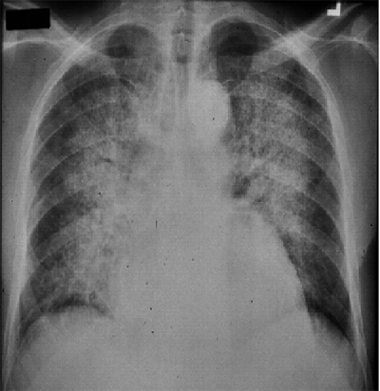
En la Fig. 1 se muestra una radiografía con signos de edema pulmonar agudo y cardiomegalia, frente a lo cual, lo más probable es que el origen de la hemoptisis sea cardiogénico.
Figura 1. Radiografía de tórax posteroanterior en paciente con hemoptisis. Se observa edema pulmonar agudo y cardiomegalia.
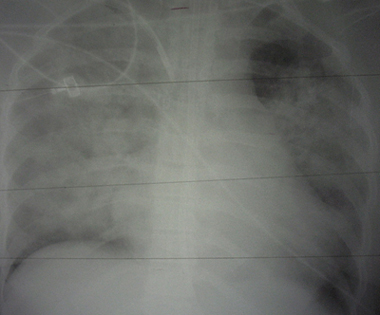
En la Fig. 2 se observa un infiltrado difuso con compromiso periférico; la silueta cardiovascular está dentro de rangos normales y el paciente está intubado. Probablemente se trata de una hemorragia alveolar, una enfermedad pulmonar difusa o una neumonía viral.
Figura 2. Radiografía de tórax posteroanterior con infiltrado difuso y compromiso periférico
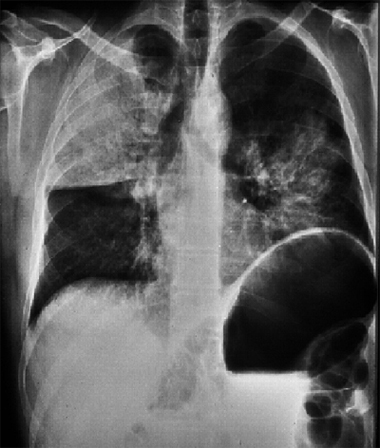
En una neumonía con hemoptisis secundaria a destrucción del parénquima pulmonar, la radiografía permite hacer el diagnóstico (Fig. 3).
Figura 3. Radiografía de tórax posteroanterior en paciente con neumonía y necrosis del parénquima pulmonar.
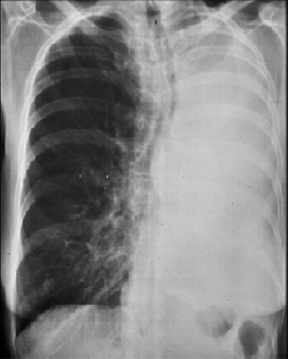
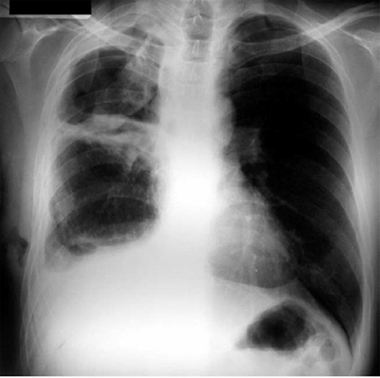
En la imagen de la Fig. 4 se observa opacidad total del pulmón, con retracción de los elementos mediastínicos hacia la zona opaca, lo que sugiere la presencia de un tumor endoluminal que está colapsando el pulmón comprometido.
Figura 4. Radiografía de tórax posteroanterior: opacidad total del pulmón izquierdo
La presencia de lesiones tuberculosas cavitadas, como las que se observan en la Fig. 5, permite sospechar fuertemente que éste es el origen del sangrado. Esto permite, en caso de hemoptisis masiva, lateralizar en decúbito lateral derecho para evitar que el sangrado inunde el campo pulmonar izquierdo.
Figura 5. Radiografía de tórax posteroanterior: lesiones tuberculosas cavitadas en campo pulmonar derecho
El siguiente método diagnóstico es la broncoscopía, que permite visualizar la mayoría de los sitios de sangrado, considerando que 80% son de origen bronquial. Se debe realizar en todos los casos de hemoptisis masiva, idealmente con broncoscopio rígido, porque éste tiene una visión y un canal de aspiración más amplio, que permite limpiar rápidamente la hemorragia, al mismo tiempo que se mantiene la vía aérea protegida. El mayor rendimiento se logra durante las primeras 24 horas, durante las cuales se puede identificar el sitio de sangrado en 90% de los casos, aunque no se conozca la etiología; este porcentaje baja a 50% cuando pasan más de 48 horas.
La broncoscopía precoz es motivo de controvesia, porque, aunque puede identificar rápidamente el sitio de sangrado, el rendimiento no varía en términos del diagnóstico, ya que con la broncoscopía tardía se va a hacer el diagnóstico de todas maneras. Siempre se discute sobre el momento correcto de realizar la broncoscopía; en el Hospital Clínico de la Universidad de Chile se suele hacer en forma precoz.
La broncoscopía puede ser diagnóstica y terapéutica. Por ejemplo, la aplicación de cianoacrilato, un pegamento biológico, permite taponar el bronquio en el que se originó el sangrado; también se pueden introducir balones que permiten taponar la zona afectada, facilitar la coagulación y evitar el sangrado; y es posible hacer un control hemostático mecánico en el bronquio, con un broncoscopio o con un balón e incluso, con un catéter de Swan-Ganz o un Fogarty, que permiten bloquear el bronquio. Con esta técnica es difícil acceder a algunos lugares, como los lóbulos superiores, porque el ángulo que se debe usar para taponar hace que el broncoscopio y los catéteres se salgan. El lavado con suero fisiológico frío tiene una tasa de respuesta de 20% en hemoptisis masiva. Otras técnicas hemostáticas broncoscópicas son: instilación de adrenalina diluida; taponamiento con material hemostático derivado de celulosa o cianoacrilato; fotocoagulación con láser; electrocoagulación; crioterapia y radioterapia.
El broncoscopio permite, además, guiar la intubación monobronquial, sobre todo cuando se desea intubar en forma selectiva el bronquio principal izquierdo, que es más difícil de intubar a ciegas; el catéter de Fogarty se impacta en el bronquio tributario de la hemoptisis y se puede dejar por varios días, para taponar la zona afectada.
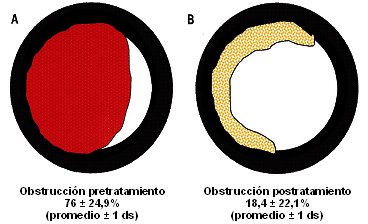
El láser con argón quema con una profundidad máxima de medio centímetro en la lesión. En un estudio realizado en 70 pacientes que tenían bloqueado el lumen bronquial en 76%, en promedio, el láser con argón logró reducir la estenosis a 18% (Fig. 6) (3). Para aplicar esta técnica es necesario tener experiencia, no está disponible en el Hospital Clínico de la Universidad de Chile y es difícil hacerla, sobre todo con broncoscopio flexible, porque con la sangre no se ve nada. Es más fácil hacerla con broncoscopio rígido.
Figura 6. Grado de obstrucción endoluminal antes (A) y después del tratamiento (B) con láser argón. (Adaptado de Morice RC et al. Chest 2001; 119(3): 781-787)
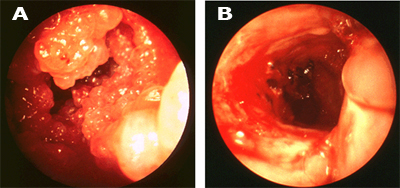
En la Fig. 7 se observa un tumor endobronquial que ocluye el lumen del bronquio. El láser, aplicado a través del broncoscopio rígido, que tiene un bisel, permite disecar el tumor.
Figura 7. Tumor endobronquial antes (A) y después (B) de aplicación de láser (B) a través de broncoscopio rígido
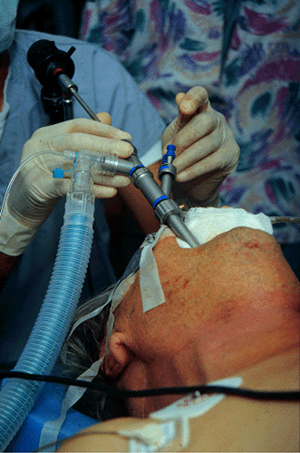
La introducción del broncoscopio rígido es traumática, especialmente en pacientes con cifosis acentuada, porque es difícil intubarlos, pero tiene la gran ventaja de que asegura la vía aérea. El broncoscopio rígido permite ventilar con un sistema de jet y cuenta con un canal de aspiración y un canal para visualizar y realizar procedimientos, como la extracción de un tumor (Fig. 8). También es posible hacer braquiterapia, para lo cual se instala una sonda con indio que cauteriza la zona; se indica en hemoptisis leve a moderada, que no requiere una intervención inmediata.
Figura 8. Resección de un tumor mediante broncoscopía
Cuando la radiografía de tórax es normal, hay que decidir si se va a realizar una broncoscopía u otra técnica. Todo paciente de sexo masculino, mayor de 40 ańos, con tabaquismo superior a 40 paquetes/ańo o hemoptisis de evolución subaguda, es decir, más de t días, se debe estudiar con broncoscopía con o sin escáner previo, ya que el riesgo de un tumor endobronquial es de alrededor de 10%. Si estos factores de riesgo no están presentes bastaría con la radiografía de tórax normal, porque en el seguimiento de grandes series de pacientes se ha descrito que menos de 3% de estos enfermos desarrollan una causa grave de hemoptisis.
El escáner de tórax también es motivo de controversia. Siempre se pregunta qué se hace primero, la broncoscopía o el escáner; en la práctica, son complementarios y el momento de indicar uno u otro dependerá del cuadro clínico y de la información que se desea obtener con el examen. Por ejemplo, si en la radiografía se observan infiltrados parenquimatosos pulmonares y en el hemograma hay anemia, lo más probable es que se trate de una hemorragia alveolar y lo más lógico, en ese caso, es solicitar un escáner y luego decidir si se realiza o no la broncoscopía; por lo tanto, el orden de la broncoscopía y el escáner depende mucho del contexto clínico. También se debe considerar que por una parte, no se ha comprobado la utilidad del escáner en términos de costo/beneficio y no hay estudios en que se demuestre que este examen mejore el resultado y pronóstico de estos enfermos; sin embargo, cuando la radiografía de tórax es normal, en 30% de los casos se encuentra alguna anormalidad, por lo que se podría concluir que en un paciente con radiografía de tórax normal es aconsejable realizar un escáner.
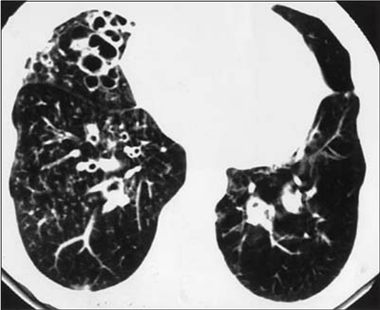
El escáner se indica especialmente ante la sospecha de bronquiectasias (Fig. 9) e infiltrados pulmonares difusos. El diagnóstico radiológico de bronquiectasias es equívoco, a veces no aparecen elementos en la radiografía que permitan concluir que el paciente tiene estas lesiones; estaría dentro del 30% de los hallazgos detectados por escáner. En las bronquiectasias se genera un círculo vicioso de inflamación que, a su vez, libera factores de crecimiento que producen vasos de neoformación, los que tienen paredes de mala calidad y son irrigados por regímenes de circulación sistémica de origen bronquial. Es frecuente que durante los procesos inflamatorios, que se conocen como exacerbaciones de las bronquiectasias, se presente hemoptisis. Cuando las bronquiectasias están en los lóbulos superiores suelen ser secas, es decir, no dan sintomatología de tos ni expectoración purulenta de predominio matinal, ya que por su posición superior drenan en forma espontánea; por lo tanto, puede haber bronquiectasias asintomáticas de los lóbulos superiores, salvo por la presencia de hemoptisis.
Figura 9. Bronquiectasias en escáner de tórax
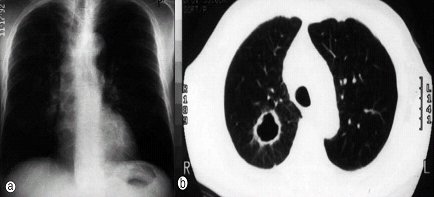
El paciente que se muestra en la Fig. 10 tenía una radiografía de tórax normal, pero el escáner reveló la presencia de un carcinoma escamoso totalmente cavitado; por lo tanto, en caso de radiografía de tórax normal conviene contar con un escáner.
Figura 10. Radiografía de tórax normal (a) y escáner de tórax que muestra la presencia de un carcinoma (b)
Con el desarrollo de los escáneres multicorte es posible inyectar medio de contraste y realizar angioescáner; por ejemplo, en un paciente que tenía infiltrados en el lóbulo superior en la radiografía de tórax, el angioescáner permitió determinar que se trataba de una caverna con un aneurisma de Rasmussen, que es secundario a la inflamación granulomatosa de las paredes de los vasos pulmonares, la que genera dilataciones que sangran. El diagnóstico se confirmó con angiografía y se embolizó el aneurisma.
Una serie demostró en forma retrospectiva que todos los sangrados provenientes de arterias bronquiales se pudieron identificar antes de la angiografía por angioescáner, no así cuando los sangrados provenían de la circulación pulmonar o de la circulación sistémica no bronquial, es decir, de arteria axilar, ramas intercostales o mamarias.
Cuando hay riesgo vital y el paciente está con una hemoptisis masiva, el manejo de la vía aérea es difícil. Las técnicas endoscópicas cohíben el sangrado en 20 a 40% de las hemoptisis masivas, en las mejores series; si no es posible frenar el sangrado, el siguiente paso lógico sería realizar una angiografía, pero esto exige experiencia y disponibilidad. En la mayoría de las grandes series retrospectivas, particularmente la de la Clínica Mayo, se destaca la importancia de la experiencia del operador, ya que el rendimiento de esta técnica mejora en forma significativa cuando la realiza un operador hábil y experimentado. Un problema frecuente de la mayoría de los trabajos es que no incluyen en sus series los intentos, es decir, en cuántos enfermos se intentó hacer la técnica y se fracasó; todos descartan estos enfermos y publican sólo los casos logrados. En 18% de los pacientes que van a angiografía el angiografista es incapaz de acceder a la femoral o de estabilizar al enfermo como para realizar la técnica o canular la arteria bronquial.
Cuando se revisan las series en que se logró canular, el éxito inicial es de 85 a 95%, pero los resultados son bastante malos cuando se desea embolizar arterias que irrigan un aspergiloma o un tumor necrosado, en los que esta técnica no es de elección. Hay 10% de recidiva, pero es posible repetir la embolización, con 50% de respuesta. La recidiva típica es bimodal, se concentra en la primera semana y luego aparece a largo plazo. Si hay recurrencia se debe considerar un origen múltiple del sangrado o un compromiso vascular pulmonar; por ejemplo, en pacientes con antecedentes de lesiones pulmonares antiguas, secundarias a tuberculosis en la juventud, es probable que existan vasos colaterales que se desarrollaron en relación a ese proceso inflamatorio y, por lo tanto, habría que sospechar que aparte del compromiso bronquial hay compromiso de arteria mamaria, intercostales, frénicas, etc.
Las complicaciones más importantes de la angiografía son la necrosis pulmonar, la disección arterial y el infarto medular, que se debe a que en 4% de los pacientes la arteria espinal anterior se origina en los vasos bronquiales, de modo que si se emboliza esa arteria, se puede originar una paraplejia. En la actualidad hay técnicas de canulación supraselectiva, mediante catéteres que pueden pasar a través de la primera colateral, o arteria espinal anterior, lo que permite realizar embolizaciones con mayor seguridad. En series que utilizaron esta técnica se informó de sólo 4% de parestesias transitorias en las extremidades inferiores.
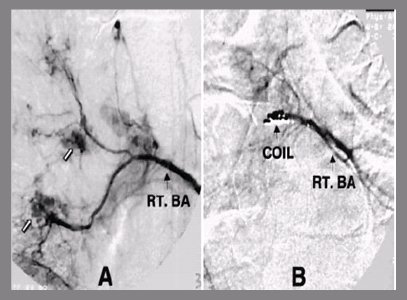
En la Fig. 11 se observa una arteria bronquial con extravasación de medio de contraste, en la que se introduce un material embolígeno, que suele ser alcohol vinílico o coils; en general se utilizan sustancias esclerosantes, porque de lo contrario se generan colaterales y nuevos episodios de hemoptisis.
Figura 11. Angiografía de arteria bronquial con extravasación de medio de contraste (a) y post instalación de coil (b)
El último recurso para manejar a un paciente con hemoptisis con riesgo vital es la cirugía, que tiene una altísima mortalidad (20%), pero es menor en comparación con la que presentan los pacientes que no se intervienen después de que la broncoscopía y la angiografía han logrado cohibir la hemorragia, en los cuales la mortalidad oscila entre 60% y 80%; por lo tanto, aunque la mortalidad es alta y también la morbilidad, que consiste en el desarrollo de fístulas broncopleurales, empiemas e infecciones, la cirugía se justifica.
Para que la cirugía tenga éxito, es crucial conocer el origen del sangrado y por ello es fundamental realizar en forma escalonada los métodos diagnósticos, porque llegar de inmediato a la cirugía significa, probablemente, un pésimo resultado final. El resultado también depende de la resecabilidad de la causa y de la reserva funcional del paciente; si un paciente tiene extensas lesiones tuberculosas, está sangrando de un micetoma y su VEF1 está muy diminuido, su riesgo es altísimo y se debe evitar la operación. Se han utilizado varios tratamientos de salvación en estos enfermos, como la instilación de anfotericina dentro de la cavidad, la introducción de instrumental para aspirar el micetoma, la administración de itraconazol, etc.
De regla, el aspergiloma es de resolución quirúrgica, ya que una vez que sangra un aspergiloma, los resultados del tratamiento médico son malos. Lo único que se ha logrado con el tratamiento antifúngico es reducir el compromiso del estado general, la astenia y la adinamia que generan estos cuadros, pero no cohibir la hemorragia ni menos, el desarrollo y crecimiento del aspergiloma.
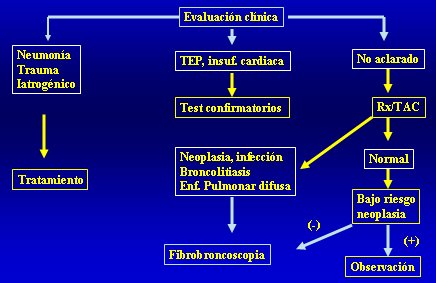
Sobre la base de todo lo expuesto hemos desarrollado un algoritmo para el manejo de la hemoptisis leve a moderada (Fig. 12), que parte por la evaluación clínica para determinar el diagnóstico; si éste está claro, por ejemplo, si el paciente tuvo una neumonía, un trauma por una herida penetrante o contusión pulmonar o se trata de una iatrogenia por una broncoscopía con biopsia transbronquial, simplemente se hace el tratamiento, sin necesidad de mayor esfuerzo diagnóstico. Si la evaluación clínica plantea fuertemente un diagnóstico no tiene sentido plantear una broncoscopía, sino que se indica directamente un test confirmatorio; por ejemplo, si el enfermo tuvo un infarto pulmonar como consecuencia de un tromboembolismo pulmonar. Si la hemoptisis no está aclarada se debe realizar de regla una radiografía y un escáner, que tiene un rendimiento diagnóstico adicional, especialmente cuando las radiografías son normales, para hacer el diagnóstico de neoplasia, infecciones, broncolitiasis, enfermedad pulmonar difusa, etc.; además, permite precisar mejor el lugar donde se va realizar la broncoscopía, en caso necesario. Si este estudio es normal y el paciente tiene bajo riesgo de neoplasia, es decir, es menor de 40 ańos, sin hábito tabáquico y la hemoptisis es de evolución aguda, basta con la observación; no es necesario hacer mayor esfuerzo diagnóstico; en cambio, si tiene alto riesgo se debe hacer una broncoscopía, que va a servir para el manejo de varios cuadros.
Figura 12. Algoritmo diagnóstico y de manejo de hemoptisis leve a moderada
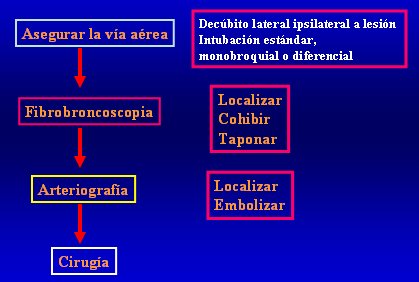
En el caso de la hemoptisis masiva (Fig. 13) la prioridad es asegurar la vía aérea, colocando al paciente en decúbito lateral, ipsilateral a la lesión sospechosa, o mediante la intubación estándar, monobronquial o diferencial, es decir, tubos con doble lumen, uno más largo que otro, para asegurar y separar ambos pulmones y evitar la inundación del pulmón sano. La intubación diferencial la debe realizar personal con experiencia, porque tiene muchas complicaciones: desplazamiento del tubo, necesidad de sondas específicas para aspirar, que no están disponibles en todos los centros, etc. Si el paciente requiere ventilación mecánica, ésta debe ser diferencial y lo más apropiado es sincronizar los dos ventiladores para evitar el bamboleo mediastínico, que tiene graves repercusiones hemodinámicas.
Una vez que se asegura la vía aérea se debe hacer de inmediato una broncoscopía, con el fin de localizar el sitio de sangrado: cuanto más precoz, mayor probabilidad de localizarlo. Luego se debe cohibir la hemorragia y taponar como sea posible en forma mecánica, con lavados de suero, adrenalina, láser o cianoacrilato. Si no se logra esto, se debe realizar una angiografía, cuyo primer objetivo es ubicar las arterias bronquiales, salvo en casos de enfermedad pulmonar difusa; o antecedente claro de uso de catéter de Swan-Ganz en un paciente con hipertensión pulmonar, porque en ese caso el origen más probable es pulmonar; o en caso de sospecha de lesiones tuberculosas o de un aneurisma de Rasmussen. Una vez localizado el sitio de sangrado, se debe tratar de embolizar. Si no se logra cohibir la hemorragia, la lesión que provoca la hemorragia debe ser sometida a cirugía (aspergiloma o cáncer resecable) y el tratamiento definitivo será la cirugía, que tiene altísima mortalidad en el período agudo, pero si se logra estabilizar y operar en forma electiva al paciente para resecar el aspergiloma o un tumor endobronquial, la cirugía mejorará su rendimiento en forma significativa.
Figura 13. Algoritmo diagnóstico y de manejo de hemoptisis masiva













 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
 Expositor:
Mauricio Ruiz[1]
Expositor:
Mauricio Ruiz[1]

Citación: Ruiz M. Hemoptysis II: study and management. Medwave 2006 Sep;6(9):e2543 doi: 10.5867/medwave.2006.09.2543
Fecha de publicación: 1/10/2006

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Herth F, Ernst A, Becker HD. Long-term outcome and lung cancer incidence in patients with hemoptysis of unknown origin. Chest. 2001 Nov;120(5):1592-4. | CrossRef | PubMed |
Herth F, Ernst A, Becker HD. Long-term outcome and lung cancer incidence in patients with hemoptysis of unknown origin. Chest. 2001 Nov;120(5):1592-4. | CrossRef | PubMed |