La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
Uno de errores en el manejo de los pacientes con EII es subvalorar el diagnóstico de Síndrome Intestino Irritable (SII), cuya prevalencia alcanza hasta un 15% en la población general. En este grupo de pacientes, las crisis de SII pueden ocurrir de manera independiente de la gravedad de la inflamación de la mucosa. La presencia de síntomas como diarrea o dolor abdominal, por sí solos, no indican que se deba modificar el tratamiento de la EII, aumentando la dosis de 5-ASA o agregando tratamiento esteroidal, o inmunosupresores. Es necesario evaluar la situación clínica, incluso con estudio colonoscópico, antes de tomar estas medidas, las cuales pueden ser innecesarias, con un costo económico importante y el riesgo de aumentar la probabilidad de eventos adversos a los diferentes fármacos. Es indudable que si el paciente tiene diarrea, dolor abdominal o diarrea con sangre, está cursando una crisis, pero si la diarrea es sin sangre y predomina el meteorismo, hay que descartar una patología asociada, evaluar el costo-beneficio, en términos de episodios adversos de estas drogas y, ante la duda, solicitar colonoscopía o rectoscopía.
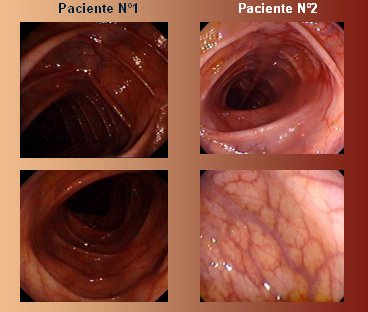
Dos de los pacientes controlados en el HCUCH habían sido tratados anteriormente por médicos del extrasistema, quienes les indicaron cirugía para resecar el colon. La colonoscopía (Figura 1) mostró que uno de ellos tenía el colon totalmente normal, por lo que, probablemente, el paciente tenía un Síndrome de Intestino Irritable o la presencia de Sobrecrecimiento Bacteriano Intestinal asociado con su EII. El otro paciente sólo tenía en la colonoscopía un aumento de la vasculatura de la submucosa, lo que fue confirmado con la biopsias escalonadas, sin duda estas alteraciones no explicaban los cambios en la sintomatología de estos pacientes.
Figura 1. Casos clínicos.
Los principales objetivos en el tratamiento de las EII son lograr la remisión de la enfermedad y mantenerla inactiva en el tiempo, y así mejorar la calidad de vida de los pacientes. La elección del mejor tratamiento es difícil, porque no hay una definición clara del control de la actividad de la enfermedad, debido a la pobre correlación que existen entre los síntomas y los hallazgos endoscópicos e histológicos, además del costo económico elevado. La terapia dependerá del diagnóstico (CU o EC), gravedad, localización etapa de la enfermedad (inducción de remisión o mantención de la remisión).
En cuanto a los aminosalicilatos, se debe elegir dosis y vías de administración adecuadas, teniendo en cuenta el área comprometida.
En cuanto a la elección entre sulfasalazina y 5-ASA derivados, no hay estudios que hayan demostrado que los 5-ASA derivados sean mejores que la sulfasalazina. De hecho, no son ni más baratos ni más efectivos; su única ventaja es que permiten aumentar las dosis sin aumentar el riesgo de efectos adversos asociados a la sulfapiridina. En caso de usar sulfasalazina, no se debe olvidar el suplemento de ácido fólico, por el riesgo de anemia megaloblástica y porque se ha demostrado que el ácido fólico podría tener un efecto protector en el riesgo de desarrollar cáncer colorrectal asociado con EII.
El costo del tratamiento local es muy alto, lo que explica por qué muchos pacientes con proctitis o rectosigmoiditis se mantengan por largo tiempo con tratamiento oral, incluso con dosis subóptimas; en el caso de los enemas, el costo es mayor. El costo del tratamiento por vía oral con 2 g/día, que es la dosis mínima para mantener la remisión, es tan alto que se hace insostenible para los pacientes que se atienden en el HCUCH, lo que podría explicar la mayor prevalencia de EII más extensa, severa y mayor necesidad de cirugía comparado con los pacientes atendidos en la CLC. A continuación se detalla el costo actual de estos tratamientos.
Costo del tratamiento local:
Costo del tratamiento por vía oral:
Los corticoides no son ni eficaces ni seguros en las siguientes situaciones:
La budesonida ha demostrado beneficio sólo cuando hay compromiso de íleon o colon ascendente, ya que es la zona en que se absorbe, pero no tiene utilidad para mantener la remisión por un período prolongado. Además, no se debe utilizar en pacientes que no responden al tratamiento habitual (Greenberg GR. Gastroenterology 2000; 119: 895-902).
Cuando se usa esteroides, no hay que olvidar aportar calcio, vitamina D y bifosfonato, por el riesgo de osteoporosis. También se debe recordar que el tratamiento esteroidal se inicia con una dosis de 40 - 60 mg/día y que, cuando la evolución es favorable, la dosis se disminuye de manera progresiva según esquema, requiriendo un período de a lo menos 12 semanas.
En relación con la etapa de remisión, el objetivo es prolongarla tanto como sea posible, para lo cual se debe usar dosis mayor o igual a 2 gr/día de sulfasalazina o 5-ASA derivados. Si el paciente no evoluciona bien y recae, se pueden utilizar antimetabolitos (azatioprina o 6-mercaptopurina); antibióticos (metronidazol o ciprofloxacino) por un tiempo corto, especialmente el metronidazol, porque causa compromiso neurológico; anticuerpos monoclonales (anti-TNF, de los cuales el único aprobado es infliximab, pues los demás se encuentran en fase dos o fase tres); y cirugía, que es el tratamiento final.
Respecto a los antimetabolitos, el riesgo de efectos adversos no significa prescindir de ellos ni esperar mucho tiempo para indicarlos; con frecuencia se administran sólo después de varias crisis.
En el caso de azatioprina y 6-mercaptopurina, son errores frecuentes:
El metotrexato tendría beneficios para inducir y mantener la remisión en pacientes con EC (Feagan BG. N Engl J Med 2000; 342: 1627-32). Sin embargo, en nuestro estudio no hay pacientes con metrotexato.
Es importante no olvidar el control regular del hemograma, cada 2-3 meses, y recordar que los antimetabolitos potencian el efecto de infliximab (Sandborn WJ. Am J Gastroenterol 2002; 97: 2962-72). En cuanto a infliximab, se está estudiando si se requiere una monodosis o un tratamiento de mantención cada seis o doce semanas. En Chile, los anticuerpos monoclonales cuestan sobre $500.000 y en su utilización suelen cometerse errores, como los siguientes:
La ciclosporina es subutilizada, a pesar de que sus indicaciones son claras:
En casos de CU severa refractaria a tratamiento esteroidal o CU fulminante la ciclosporina puede tener un rol, sin embargo siempre su uso debe ser evaluado por un equipo multidisciplinario integrado por gastroenterólogo, cirujano y radiólogo, ya que siempre existe la posibilidad de una cirugía. Otras complicaciones como hemorragia grave, perforación, absceso, megacolon tóxico, tienen indicación quirúrgica y contraindican el uso de ciclosporina. Es necesario evaluar las posibilidades de cada paciente a futuro, por lo que la ciclosporina se debe tomar como un puente al tratamiento definitivo y no como un tratamiento a largo plazo.
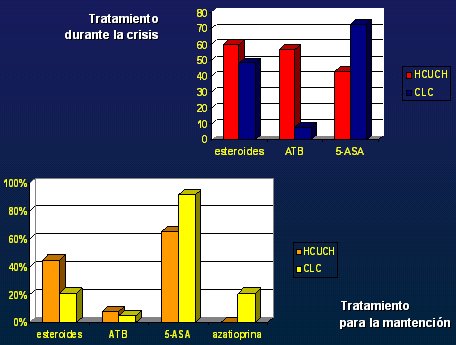
En el estudio descrito, el uso de terapia esteroidal fue más frecuente en el HCUCH que en la CLC, probablemente porque los pacientes eran más graves y tenían mayor extensión de sus lesiones. En el tratamiento de mantención, llama la atención el número de pacientes con este esquema, que no tiene ningún papel, y, por otra parte, el escaso número de pacientes que usa sulfasalazina o 5-ASA (Figura 2).
Figura 2. Tratamiento de la colitis ulcerosa (experiencia nacional).
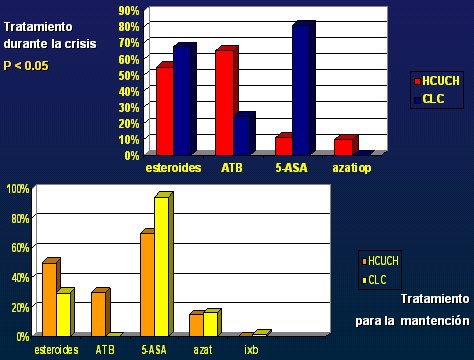
En relación con EC, ocurre lo mismo durante la crisis: el número de pacientes que necesita corticoides en el Hospital es mucho menor y llama la atención que en la CLC se traten con 5-ASA, cuando se sabe que los pacientes con EC responden menos que los pacientes con CU. Una posible explicación para esto es que los pacientes con EC atendidos en la CLC tengan una enfermedad más leve. A la inversa, en el Hospital Clínico, el tratamiento con esteroides de mantención es alto, a pesar de que no cumplen ningún papel (Figura 3).
Figura 3. Tratamiento de la enfermedad de Crohn (experiencia nacional).
Del estudio se puede concluir lo siguiente:
Las terapias biológicas con anticuerpos monoclonales han sido motivo de intensa investigación en los últimos ańos y se ha logrado desarrollar en está área. Sin embargo, hasta ahora el infliximab es el único fármaco que ha sido aprobado por la FDA, estudios recientes han demostrado incluso su uso en pacientes con CU. El infliximab se caracteriza por poseer un 75% de estructura humana.
Otros fármacos de este tipo son el CDP571, que tiene 95% de características humanas. Pese a ser más humanizado, estudios han demostrado resultados inferiores que con infliximab. El adalimumab, anticuerpo monoclonal 100% humano se ha probado en estudios fase dos y tres, con buenos resultados, especialmente en pacientes con resistencia a infliximab, siendo posible que en el futuro pueda ser agregado dentro de las estrategias terapéuticas de las EII.
El infliximab (nombre comercial Remicade) ofrece las siguientes características:
Los anticuerpos anti IL-12, de desarrollo reciente, actúan contra esta interleuquina, la que cumple un papel en la cascada inmunológica de la EC. En un estudio doble ciego, aleatorio, publicado en New Eng J Med, se demostró que el uso de estos anticuerpos era mejor que el placebo para inducir remisión, pero son estudios experimentales en fase dos que requieren de estudios que confirmen los resultados.
El trasplante de células troncales en pacientes refractarios, incluso a los anticuerpos monoclonales, podría ser eficaz. Un estudio reciente demostró que pacientes con EII podrían responder de manera favorable a esta estrategia, sin embargo sólo 12 pacientes fueron incluidos por lo que se requieren nuevos estudios para confirmar sus resultados (Gastroenterology 2005, 128:552-563).
Los probióticos, dado su mecanismo de acción sobre la flora bacteriana, podrían desempeńar algún papel en el tratamiento de las EII. Ellos actúan en la cascada inmunológica a partir de la competencia con las bacterias a nivel entérico y estimulación del epitelio intestinal y su actividad antimicrobiana. Algunos estudios han evaluado la respuesta en distintos fenotipos con resultados variables según la población incluida o el probiótico utilizado. En una revisión realizada por nuestro servicio se concluyó que no existe una cepa ideal, ya que pueden tener diferentes mecanismos de acción; que al asociar cepas se produce antagonismo y que los resultados no son claros en la selección de la cepa, dosis, vía de administración y monitorización (Probióticos en Gastroenterología. Rev Gastroenterología Latinoam 2005). Si bien estos compuestos son una potencial estrategia terapéutica, todavía no se dan las condiciones para validar su uso de manera generalizada.
Sobre el uso de ciertos parásitos, existen varios artículos recientes en los cuales se han utilizado helmintos (Trichuris) para producir un estímulo de tipo TH2 que es capaz de frenar la respuesta TH1, generadora de enfermedades autoinmunes como la EC y CU (Gut 2005; 54: 87-90 y Gastroenterology 2005; 128:85-832). Faltan estudios en distintas poblaciones de pacientes con EII para poder confirmar y validar el uso de parásitos en el tratamiento de las EII.



 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Departamento de Medicina del Hospital Clínico Universidad de Chile.
 Expositor:
Rodrigo Quera[1]
Expositor:
Rodrigo Quera[1]

Citación: Quera R. Inflammatory bowel disease: treatment. Medwave 2005 Oct;5(9):e2528 doi: 10.5867/medwave.2005.09.2528
Fecha de publicación: 1/10/2005

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Nombre/name: Carolina Vargas
Fecha/date: 2019-11-28 05:10:23
Comentario/comment:
Los tratamientos para esta enfermedad son muy caros. Hay algún contacto para adquirir en Chile salofalk más barato?
Para comentar debe iniciar sesión