En esta conferencia se intentará determinar si el síndrome metabólico es una entidad con existencia real, o si sólo es un conjunto de piezas diversas adosadas entre sí, aparentando una unidad. Para esto, lo primero es revisar el concepto de resistencia a la insulina, que ha fascinado durante los últimos tres cuartos de siglo a los endocrinólogos, acostumbrados a comprender las enfermedades endocrinas como un exceso de una hormona, en cuyo caso bastaba remover el tumor o controlar la función autónoma de la glándula para mejorar la enfermedad, o como una deficiencia hormonal, caso en que bastaba con sustituir la hormona para restablecer la fisiología normal. En cambio, la enfermedad metabólica más común en el mundo es la diabetes tipo 2, que se asocia, no a una deficiencia completa de la hormona, sino a una resistencia a su acción y el reconocimiento de este hecho continúa confundiendo y fascinando a los especialistas. Hoy se sabe que la resistencia a la insulina no sólo tiene que ver con la captación de glucosa por el músculo o la regulación de la producción de glucosa en el hígado, sino que es parte de un fenómeno que se ilustra en la Fig.1 como un rompecabezas en el que participan la hipertensión, las alteraciones de los lípidos y la inflamación, entre otros factores, en conjunto con la glucosa elevada.
En muchos de los pacientes que se ven en la clínica se pueden encontrar uno o más de estos trozos del rompecabezas. El reconocimiento de que factores como tabaquismo, aumento de la adiposidad abdominal, LDL y triglicéridos elevados, HDL disminuido, aumento de la presión arterial, aumento de la glicemia y resistencia a la insulina, se tienden a agrupar, fue un gran aporte de investigadores como Gerald Reaven.
Los criterios diagnósticos de síndrome metabólico han evolucionado y personas como el Profesor Scott Grundy, de la Universidad de Texas, en Dallas, ayudaron a impulsar y defender esta categorización que en gran parte no es mecanicista, en el sentido de mecanicismo científico, sino pragmática, ya que se basa en mediciones que la mayoría de los clínicos, no sólo endocrinólogos, sino internistas y médicos generales, podrían efectuar con facilidad y bajo costo (Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. JAMA. 2001;285:2486-2497). Estos criterios son:
En los estudios NHANES, en que se aplicaron estos criterios diagnósticos en estudios de población, en los Estados Unidos, se encontró que una gran cantidad de individuos cumplen con los requisitos para síndrome metabólico y que su prevalencia se incrementa con la edad, ya que se ve en uno de cada 10 hombres menores de 40 ańos, en uno de cada cinco hombres de edad intermedia (entre 40 y 60 ańos), aunque recientemente se dice que es uno de cada tres, y en 40% de los hombres mayores de 60 ańos. En las mujeres se observa la misma dependencia de edad, pero con una tendencia temporal más fuerte: una de cada cinco mujeres jóvenes cumple con los criterios diagnósticos, una de cada tres mujeres de edad mediana y casi una de cada dos mujeres mayores (Ford ES, et al. Diabetes Care. 2004;27:2444-2449). Esto no significa que la mitad de las personas de una población tengan una enfermedad, pero demuestra que los elementos relacionados con la resistencia a la insulina son altamente prevalentes, lo que prepara el terreno para el desarrollo de enfermedades metabólicas.
Se ha tratado de establecer la capacidad predictiva del síndrome metabólico y se ha encontrado que sí la tiene para la diabetes, la que se encuentra aumentada tres a cuatro veces, según estudios de grandes poblaciones, en presencia del síndrome. De tal modo, es importante buscar y reconocer esta enfermedad en la práctica clínica, para iniciar en forma precoz la intervención dirigida a prevenir el desarrollo de la diabetes (Fig. 2).
En el caso de la enfermedad cardiovascular el riesgo no es tan marcado como para la diabetes, tal vez aumenta en 60 a 65% (Fig. 3). Esto se debe a que todos los componentes del síndrome metabólico son factores de riesgo y la agrupación de todos ellos constituye riesgo cardiovascular. Lo expuesto se utiliza como argumento para promover el reconocimiento del síndrome metabólico, ya que éste ayuda a identificar clínicamente a individuos que están en riesgo de enfermedad metabólica.
Para entender cómo se mantienen juntos estos factores se hizo un análisis matemático de los componentes del síndrome metabólico en el estudio poblacional de Framingham, un estudio epidemiológico de cohorte realizado en la comunidad de Framingham, que se ubica en las afueras de Boston. Esta población ha sido seguida por largo tiempo por investigadores, en gran parte de la Universidad de Harvard, para determinar los factores de riesgo de enfermedad cardiaca, cáncer y otras enfermedades. En esta oportunidad, Jane Meigs, de Harvard, analizó los componentes del síndrome de resistencia a la insulina o síndrome metabólico en forma matemática, mediante análisis de grupos; así, identificó tres factores alrededor de los cuales giran todos los demás. Uno de ellos es la agrupación de dislipidemia, triglicéridos y HDL, junto a la obesidad, reflejada en el índice de masa corporal (IMC) y la proporción cintura/cadera, además de algunas mediciones de resistencia a la insulina per se: insulina en ayuno elevada, insulina a las dos horas elevada. La hipertensión no encaja en este conjunto per se, sino que se superpone con la obesidad, en el sentido de que sí se asocia con la obesidad, que es un factor de riesgo conocido para hipertensión, pero no se agrupa bien con los triglicéridos y el HDL. Esto se ve en algunas etnias, por ejemplo, en los Estados Unidos se ha visto que las personas con ancestro africano tienen mucha tendencia a la hipertensión, pero no a la dislipidemia o a la acumulación de grasa visceral, a pesar de que son muy susceptibles a la obesidad, de modo que existe un grado de segregación de estos factores. La diabetes tampoco se asocia directamente con la hipertensión, sino más bien ocupa su propio círculo y se sobrepone a los marcadores de resistencia a la insulina y mediciones de insulinemia, lo que no es sorprendente.
Siglas de la Figura 4: PAS=presión arterial sistólica; PAD=presión arterial diastólica
Todo esto lleva a preguntarse si existe una raíz común o si existen varias vías coexistentes que se entrecruzan para conducir al síndrome metabólico. En el último ańo aparecieron varias publicaciones co-patrocinadas por la Asociación Americana de Diabetes y la Asociación Europea para el Estudio de la Diabetes, en las que se cuestionó la noción de síndrome metabólico o, más bien, del valor que tienen los criterios actuales. Ellos no cuestionan que el síndrome metabólico sea un predictor de diabetes, pero plantean que con este objetivo, “probablemente no es mejor que la glicemia de ayunas elevada y, sin duda, no es mejor que el aumento de la glicemia frente a una sobrecarga de glucosa, que son mucho mejores como marcadores de diabetes. Utilizar el síndrome metabólico para predecir personas con diabetes no ayuda más que la medición de la glicemia, que es sólo un componente del síndrome metabólico, de modo que éste tiene un valor limitado”.
Con el mismo argumento seńalan que “el síndrome metabólico no es un predictor sólido de enfermedad cardiaca”, y que “si se analiza solamente la hipertensión, el colesterol LDL por sí solo, aunque éste ni siquiera es un componente del síndrome metabólico, o el HDL por sí solo, cada uno de estos parámetros por sí mismo tiene un gran valor predictivo para patología cardiovascular, que es igual al valor del síndrome metabólico”. Y argumentan que el síndrome metabólico es un artefacto, una agrupación conveniente de factores de riesgo, pero no una entidad en sí misma, ya que “se desconoce el hilo común para el síndrome metabólico y no se ha demostrado que exista un factor único que lo dirija”.
Frente a esto, es importante recordar que existen muchos diagnósticos a los cuales se ha llegado después de largos períodos de tiempo, en los que no se comprendían los mecanismos o bien se había llegado a cumbres falsas, como ocurrió con la úlcera péptica, cuya patogenia parecía estar totalmente aclarada hasta que se descubrió que tenía una causa infecciosa, cosa que habría sido motivo de risa si se hubiera planteado diez ańos antes. Por lo tanto, no porque no comprendamos los mecanismos celulares de una enfermedad no podremos ver la enfermedad. La primera es una tarea para los científicos, pero no es indispensable para los médicos. Por otra parte, el reconocimiento del síndrome metabólico tiene varios méritos, uno de los cuales es hacer que el médico que ejerce la medicina general o familiar se acostumbre a ver al paciente de manera más completa. Es fácil para los médicos generales ver a un paciente que tiene hipertensión, dislipidemia y diabetes y, aunque no vea todas las raíces, sí puede ver que se agrupan en conjunto, como lo demuestra el hecho de que el concepto de síndrome de resistencia a la insulina y las piezas que lo conforman ha sido bien recibido por médicos generales, estudiantes y becados, porque les resulta lógico y les ayuda a tener una visión más amplia de las enfermedades metabólicas comunes. Por lo tanto, este concepto no se debe desechar, porque está claro que existe una agrupación de diversos elementos alrededor de la resistencia a la insulina; nuestra tarea es continuar investigando acerca de esta definición, en vez de desecharla por completo, ya que tiene implicancias clínicas importantes.
Las curvas de mortalidad de la Fig. 5 muestran un hecho que debe causar inquietud entre los endocrinólogos, y es que la mortalidad por algunas enfermedades ha disminuido claramente en las últimas dos décadas, en especial la mortalidad por enfermedad cardiovascular y accidente vascular, que se han reducido en forma impresionante gracias a los esfuerzos realizados para controlar la hipertensión y al reconocimiento del peligro del tabaquismo, con el consiguiente éxito en la suspensión del hábito tabáquico. A esto se agrega el reconocimiento de objetivos de tratamiento para el colesterol LDL y la aceptación de la terapia con estatinas; en el caso del cáncer también ha habido cierta mejoría. En cambio, la diabetes va en el sentido equivocado, ya que está aumentando rápidamente.
En la época actual existe una epidemia de diabetes tipo 2 entre adolescentes, nińos y adultos jóvenes, a tal punto que ya se está descartando el término de “diabetes de inicio en el adulto”. A pesar de los avances en el tratamiento farmacológico y al desarrollo de numerosas preparaciones de insulinas de acción rápida y lenta, además de múltiples fármacos que permiten controlar la hiperglicemia mucho mejor de lo que se podía hacer diez o quince ańos atrás, no se ha observado el impacto que se esperaba sobre la mortalidad. Por eso es importante que los médicos comiencen a pensar en la diabetes, no como una enfermedad del azúcar, sino como una enfermedad más amplia; en este contexto, nociones como el síndrome metabólico tienen el valor de haber cambiado la forma de abordar a los pacientes.
Es interesante comentar el estudio Steno-2, que no estaba enfocado en el síndrome metabólico, pero es un ejemplo de la forma en que se debe abordar a la diabetes tipo 2, con una intervención multifacética. Este fue un estudio relativamente pequeńo que incluyó a 160 pacientes de 55 ańos de edad promedio, obesos y con mal control de su glicemia, los que se asignaron en forma aleatoria a tratamiento convencional o tratamiento intensivo y fueron seguidos durante ocho ańos. Al final del estudio, los pacientes de la rama de manejo intensivo tenían una HbA1c de aproximadamente 8%, que era algo mejor que el resultado del grupo convencional (9%); la presión arterial sistólica fue de 148 en el grupo convencional, versus 132 en el intensivo, o sea, 16 puntos menos; el colesterol LDL también se controló sustancialmente mejor (130 versus 75), al igual que los triglicéridos (260 versus 150). Esto demuestra que el enfoque del problema como síndrome metabólico mejora todos los parámetros, porque se interviene sobre la dislipidemia, el colesterol LDL y la hipertensión. El riesgo compuesto de muerte por causa cardiovascular, infarto no fatal, amputación y cirugía post enfermedad aterosclerótica arterial, entre otros eventos, fue sustancialmente menor con este enfoque (Gaede P, et al. N Engl J Med. 2003;348:383-393). En el UKPDS no se obtuvo el mismo resultado, porque el manejo se enfocó en los niveles de glucosa.
Con respecto a lo que mantiene unidos a los componentes del síndrome metabólico, se debe analizar muy cuidadosamente la obesidad y el balance energético. Los mapas de prevalencia de obesidad y diabetes en los Estados Unidos muestran una tendencia alarmante a un acelerado incremento de estas condiciones; por eso es importante enfocar el rol de la adiposidad visceral como un tema y la formación de grasa ectópica, como otro tema. Dentro de la obesidad, es importante conocer el concepto de adiposidad visceral, que se ha ligado a muchos de los componentes del síndrome metabólico, principalmente diabetes, mediciones fisiológicas de resistencia a insulina, dislipidemia, hipertensión y otros elementos descritos en forma reciente y que probablemente se encuentran en la raíz, que son la disfunción cardiovascular y la inflamación.
El interés en la adiposidad visceral radica en que es un fuerte marcador de riesgo. El porcentaje de adiposidad abdominal que se atribuye a la grasa visceral es bastante bajo, entre 10 y 15, hasta 20% y es levemente más bajo en mujeres que en hombres. En la Fig. 6 se muestra el escáner de dos individuos que tienen exactamente la misma medida de circunferencia de cintura; se ve la columna lumbar, los músculos lumbares, la pared abdominal y el tejido adiposo, de color gris. Por fuera de la pared abdominal, el individuo A tiene muy poca grasa subcutánea y la mayor parte de la adiposidad abdominal es grasa visceral (75%), en inglés VAT (visceral adipose tissue): es un individuo delgado, pero el problema de esta persona no es la cantidad de grasa visceral, sino su proporción en relación a su escasa grasa subcutánea. En comparación, el individuo B tiene la misma circunferencia de cintura, pero con gran cantidad de grasa subcutánea. Lo interesante es que el individuo A, el delgado, tiene diabetes mellitus tipo 2, dislipidemia, hipertensión e hígado graso, mientras que el individuo B, a pesar de tener un índice de masa corporal equivalente, no tiene dislipidemia, su tolerancia a la glucosa es normal y no tiene hígado graso.
Figura 6. Importancia de la adiposidad visceral dentro de la grasa abdominal total.
En un estudio horizontal efectuado en una población de gran tamańo con diabetes tipo 2, se analizó la capacidad de la insulina para estimular el metabolismo de la glucosa; se observó que aquellos individuos muy sensibles a la insulina tenían menor cantidad de tejido adiposo visceral, de modo que había una fuerte correlación entre la cantidad de grasa visceral y la resistencia insilínica (Fig. 7). De la misma forma, se ha demostrado que la adiposidad abdominal y por ende la circunferencia de cintura, es un predictor poderoso de diabetes tipo 2, más aún que la obesidad per se (Fig. 8).
Siglas de la Figura 8: WHR = relación cintura-cadera; WC = circunferencia de cintura; BMI = IMC = índice de masa corporal
Está claro que la adiposidad visceral favorece el desarrollo del síndrome metabólico, lo que se podría explicar por varios mecanismos patogénicos. Uno de ellos es la producción de moléculas inflamatorias y de proteína C reactiva (PCR) como marcador, que se sintetiza en el hígado por influencia de las citoquinas que provienen del tejido adiposo. En los últimos dos ańos han aparecido estudios muy interesantes que demuestran que algunas de las citoquinas que parecían provenir del tejido adiposo, en realidad provienen de macrófagos que están infiltrados en este tejido y no de los adipocitos per se; habría, entonces, una comunicación entre las células inflamatorias y el tejido adiposo, de modo que las primeras son reclutadas por éste. Es fácil ver que existe cierta analogía entre la inflamación de la pared vascular que se produce en la ateroesclerosis y la inflamación del tejido adiposo, que constituye un factor de riesgo para la aterosclerosis. Otro mecanismo se relaciona con la producción hormonal en el tejido adiposo, de la cual se ha hablado mucho últimamente. Finalmente, se describe cada vez más la importancia de la producción de ácidos grasos libres en el tejido adiposo y su des-regulación, como elemento patogénico de la resistencia a la insulina en el síndrome metabólico, que además se relaciona con la homeostasis de la glucosa y la dislipidemia.
Es importante recordar que una de las acciones principales de la insulina es controlar los niveles plasmáticos de los ácidos grasos y permitir que ocurra el metabolismo de la glucosa. En el diagrama de la Fig.9, en el que se resume la fisiopatología de la diabetes mellitus tipo 2, se puede ver que las principales causas de hiperglicemia son: reducción de la producción de insulina, aumento de la salida de glucosa desde el hígado y disminución del ingreso de glucosa hacia el músculo esquelético. Sin embargo, detrás de cada uno de estos elementos se encuentra la influencia del aumento de los ácidos grasos plasmáticos, que impulsan la gluconeogénesis y si no se controlan en forma adecuada tienden a elevar la producción de glucosa hepática; además compiten con la captación de glucosa hacia el músculo, de modo que disminuyen la captación de glucosa en presencia de insulina. En el corto plazo, los ácidos grasos plasmáticos estimulan la secreción de insulina, pero la exposición crónica de la célula beta a ácidos grasos elevados induce un estado de lipotoxicidad que puede contribuir en forma fundamental a la disfunción de las células beta. Detrás de estos tres mecanismos de des-regulación del metabolismo de la glucosa se encuentra el tejido adiposo, impidiendo regular la lipólisis y controlar los niveles de ácidos grasos (Fig 9.).
Figura 9. Resistencia a insulina y disfunción de células beta en la diabetes tipo 2.
Existe una conexión entre la adiposidad visceral y el hígado graso y entre éste y los componentes del síndrome metabólico, como la dislipidemia. El hígado graso se puede evaluar en forma no invasiva, mediante imágenes de escáner (TAC) o espectroscopía de resonancia magnética, que no son métodos de diagnóstico clínico, pero son muy útiles en el campo de la investigación para determinar la composición corporal. Las imágenes de la TAC se describen mediante los coeficientes de atenuación, que se han codificado en la escala de unidades Hounsfield, donde las imágenes menos brillantes (hipodensas) tienen los valores más bajos y las más brillantes (hiperdensas), los valores más altos, siendo el valor del agua igual a 0 UH. Existe un histograma normal para cada tejido y, a través de los ańos, se ha observado que el músculo esquelético, el hígado e incluso el tejido adiposo, tienen un patrón característico de atenuación de los valores del TAC, los que se pueden medir fácilmente. El hígado graso es bastante homogéneo; se puede usar el bazo como órgano de referencia y los valores menores de 1 indican hígado graso, que se correlaciona fuertemente con la grasa visceral.
En la Fig. 10 se muestra la técnica de TAC que se utiliza para medir los factores de atenuación para el hígado; nuevamente, valores menores de uno indican hígado graso, lo que ocurre en forma extremadamente frecuente en la diabetes tipo 2. Utilizando sólo este criterio, es probable que tres cuartos de los pacientes con sobrepeso y diabetes tipo 2 tengan esteatosis hepática, lo que no significa que tengan el estado inflamatorio propio del NASH (steatohepatitis sin alcohol), pero tienen más esteatosis hepática que individuos obesos sin diabetes, a pesar de que algunos de ellos también presentan hígado graso.
Figura 10. Estudio no invasivo del hígado graso.
El hígado graso es un fuerte determinante de la sensibilidad a la insulina. Los individuos que tienen alto contenido graso en el hígado tienden a tener mayor resistencia a la insulina que aquellos que tienen un contenido graso hepático relativamente bajo; pero probablemente lo más importante es la relación entre grasa visceral, niveles de ácidos grasos, grasa hepática y dislipidemia, que son parte de los criterios del síndrome metabólico y que se conectarían de la siguiente manera. Normalmente, la insulina controlaría la liberación de ácidos grasos, en parte, a través de sus efectos sobre el control de la lipasa sensible a hormonas y otras lipasas que han sido identificadas; en el marco de resistencia a la insulina, la lipasa sensible a hormonas es más activa de lo que debería ser, originando mayor producción de ácidos grasos, particularmente dentro de los lechos troncales, los que son entregados al hígado, donde inducen la formación de triglicéridos, a través de la formación de partículas de VLDL. La entrada de partículas VLDL de mayor tamańo, que intercambian triglicéridos con partículas de HDL, lleva a cambios en la conformación y cantidad de HDL, lo que se asocia a un rápido clearance de HDL. Esta es la razón por la cual los triglicéridos elevados se asocian a reducción de HDL. Pero además, el intercambio de triglicéridos con los LDL los hace más vulnerables a la interacción con la lipasa hepática, aumentando la formación de LDL de baja densidad, que son aterogénicas y constituyen otro componente de la dislipidemia.
En un estudio publicado recientemente por Toledo se analizó una gran cohorte de individuos con diabetes tipo 2, en los que se determinó la presencia de hígado graso y su composición de lipoproteínas mediante imágenes de resonancia. En este grupo de individuos, aquellos que presentaban esteatosis hepática moderada a grave tenían mayor dislipidemia que aquellos que no tenían esteatosis, los que representaban alrededor de un tercio de los individuos diabéticos; de hecho, los individuos diabéticos sin hígado graso no presentaban ningún tipo de dislipidemia. Primero se planteó que esta dislipidemia se debía a una sobreproducción de ApoB, cuyos niveles están elevados en la diabetes tipo 2, pero estos niveles no se elevan más por la presencia de hígado graso; luego se comprobó que la estatosis hepática estaba asociada a la producción de partículas VLDL, extremadamente grandes.
Una forma de comenzar a conceptuar el síndrome metabólico es pensar que la acumulación de grasa corporal produce una des-regulación de los niveles de ácidos grasos libres, los que ingresan al músculo, donde disminuyen la utilización de la glucosa y aumentan la neoglucogénesis, lo que lleva a hiperglicemia, y al hígado, donde disminuyen el colesterol HDL y aumentan el LDL y las partículas LDL pequeńas y densas, lo que configura un perfil lipídico aterogénico y aumenta el riesgo cardiovascular (Fig. 12).
En el músculo, los ácidos grasos libres tienen un fuerte efecto inductor de resistencia a la insulina. En un estudio experimental, se infundieron lípidos para elevar los niveles de ácidos grasos en el plasma en presencia de una infusión de insulina, con el objetivo de determinar en qué medida el elevar los niveles de ácidos grasos interfiere con la acción de la insulina. Los resultados fueron sorprendentes, porque dentro de un lapso de tres a cuatro horas se pudo inducir un perfil metabólico de resistencia a insulina muy similar al de la diabetes tipo 2, en individuos delgados y sanos, tal como se muestra en la Fig. 13, en la que se observan reducciones importantes de la acción de la insulina en respuesta al aumento de los ácidos grasos libres producido por la infusión lipídica. De hecho, la mayor parte de esta inhibición ocurre frente a los ácidos grasos que se encuentran en la diabetes tipo 2 y la obesidad.
En la Fig. 14 se resumen datos de nuestro laboratorio, donde se analizó la sensibilidad del músculo a la insulina con tomografía de emisión de positrones y se midió simultáneamente los niveles de ácidos grasos en individuos que eran portadores de diabetes tipo 2 y, por lo tanto, de elementos de resistencia a la insulina, en los que el nivel de ácidos grasos puede ser un elemento pronóstico muy importante.
Figura 14. Diabetes tipo 2: resistencia insulínica muscular y niveles plasmáticos de ácidos grasos (Kelley et al., JCEM, 2001)
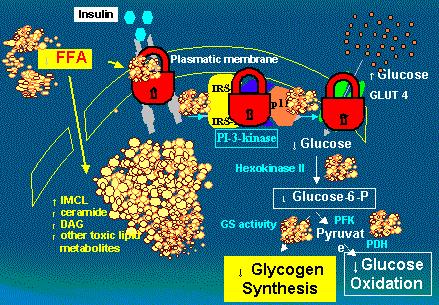
En la Fig. 15 se resumen los mecanismos a través de los cuales actúa esta acumulación de grasa a nivel muscular: se induce la producción de mediadores como diacilglicerol, que influencia la actividad de la P-1-3 kinasa, o ceramidas, que interfieren con la fosforilación de tirosina y favorecen, en cambio, la fosforilación de la serina en el receptor de la insulina, lo que, finalmente, bloquea la acción de la insulina para el metabolismo de la glucosa.
Figura 15. Efecto de los ácidos grasos plasmáticos elevados sobre la seńal de insulina en humanos (Belfort, Cusi et al, Diabetes 54: 1640-48, 2005)
En el estudio de Belfort, que ya se mencionó, la infusión de ácidos grasos en individuos sanos redujo la fosforilación del receptor de insulina, la fosforilación de IRS-1 (insulin receptor substrate 1) y la fosforilación de Akt y por estos mecanismos indujo rápidamente resistencia a la insulina en el músculo esquelético.
La visión tradicional del tejido adiposo como productor de ácidos grasos está quedando atrás, ya que cada día hay más evidencia de la importancia de este tejido en la inducción de la resistencia a la insulina y como concepto unificador del síndrome metabólico. Esto se confirma al analizar el rol endocrino del tejido adiposo, que es una gran fuente de sustancias como la adiponectina, que es un sensibilizador de la insulina, además de leptina, ácidos grasos, TNF alfa, PAI-1 (plasminógeno tipo 1) y citoquinas, que se ubican en el centro del síndrome metabólico; por lo tanto, es muy difícil conceptualizar el síndrome metabólico sin entender el rol central del tejido adiposo.
Unger planteó la hipótesis de que el síndrome metabólico es impulsado por la formación de grasa ectópica en el hígado y músculo, que es realmente el proceso clave. En un individuo delgado hay un buen equilibrio entre la ingestión y la utilización de triglicéridos, de modo que se acumula muy poca grasa en el hígado o músculo y el metabolismo es normal, mientras que, en un individuo con sobrepeso, se produce acumulación de grasa como triglicéridos dentro del tejido adiposo, lo que aumenta la leptina, que regula la oxidación grasa en los tejidos magros, de modo que se almacena muy poca grasa dentro de estos tejidos. La mayoría de estos individuos presentará una resistencia leve a la insulina.
En el último ańo, nuestro grupo, en conjunto con algunos investigadores de la Universidad de Columbia, en Pennington, estudió los patrones de distribución grasa en pacientes con diabetes tipo 2 y resistencia a la insulina y encontró que en estos pacientes existe disminución de la cantidad de tejido adiposo abdominal, aumento de la adiposidad visceral y disminución de la adiposidad gluteofemoral, que por largo tiempo se ha reconocido que no se asocia a síndrome metabólico ni a riesgo cardiovascular. En condiciones como la lipodistrofia, la ausencia de grasa glúteofemoral constituye un riesgo metabólico grave. En la diabetes tipo 2 este fenómeno no es de magnitud tan pronunciada, pero en el individuo promedio con diabetes tipo 2, que es obeso, existe menor proporción de masa grasa dentro del tejido subcutáneo (grasa subcutánea) y más grasa en y alrededor del músculo, por debajo de la fascia, lo que también se relaciona con resistencia a la insulina.
Finalmente, se sabe que los adipocitos de gran tamańo son mucho más resistentes a la supresión de la lipólisis y que la disminución del tono parasimpático y el aumento del tono simpático aumentan la lipólisis y disminuyen el almacenamiento, lo que se relaciona con algunas de las complicaciones de la obesidad, tales como la hipertensión, menor eficiencia en el depósito de triglicéridos y mayor producción de moléculas inflamatorias. Los individuos propensos a desarrollar síndrome metabólico probablemente llegan a una situación o momento en sus vidas en que, ya sea debido a origen étnico, envejecimiento o género, desarrollan este síndrome. Las personas con ancestros asiáticos tienen un índice de masa corporal relativamente bajo, tienden a tener un nivel muy elevado de adiposidad visceral y son propensos a hígado graso.
Nuestro grupo, junto a un grupo japonés, analizó una gran cantidad de escáneres de abdomen de hombres japoneses de edad media y encontró que, a pesar de que el IMC promedio de esta población es menor de 20, es decir, no son obesos, muchos de ellos tenían una cantidad considerable de adiposidad visceral, hígado graso, dislipidemia y resistencia a la insulina, lo que se asocia a cantidades relativamente pequeńas de grasa subcutánea. Lo mismo se puede encontrar en zonas del sudeste asiático en general. Las mujeres, en general, tienden a tener una gran capacidad de proliferación de la grasa subcutánea, en especial a nivel gluteofemoral, lo que, desde la perspectiva metabólica, les protege contra la resistencia a la insulina; pero después de la menopausia, esa capacidad protectora se pierde y la ganancia de peso tiende a acentuar la adiposidad visceral, ya que el envejecimiento, en general, se asocia a un aumento de este tipo de adiposidad. Esta acumulación de grasa subcutánea, compuesta por adipocitos de mayor tamańo, predispone a la infiltración de grasa en músculo, hígado y páncreas y favorece el desarrollo del síndrome metabólico.
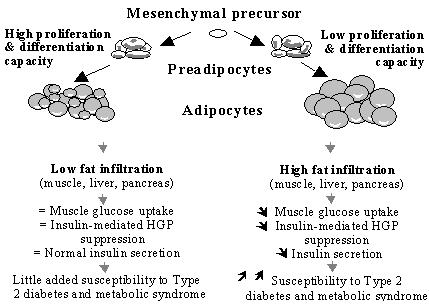
En el diagrama conceptual de Unger, que se muestra en la Fig.16, se propone que, una vez que un individuo obeso desarrolla una población de adipocitos de gran tamańo, comienza a acumular grasa dentro de los tejidos magros y esto lleva al desarrollo del síndrome metabólico; mientras que un individuo que tenga incluso mayor cantidad de adiposidad, pero cuya distribución grasa sea de predominio gluteofemoral y generalizado, más que exclusivamente visceral, protegerá a los tejidos delgados contra la acumulación de grasa y por lo tanto, aunque pueden manifestar algún grado de resistencia a la insulina, no serían tan vulnerables a las otras manifestaciones del síndrome metabólico.
Figura 16. Modelo secuencial de desarrollo de la ganancia de peso y la resistencia a la insulina
En resumen, para encontrar las causas del síndrome metabólico, no sólo es necesario pensar en diferentes sistemas y órganos, sino en la interacción entre los adipocitos, en términos de su rol fundamental como almacenadores y liberadores de energía y como productores de adipoquinas y otros marcadores inflamatorios, y órganos como el hígado y el músculo, que participan en el desarrollo de dislipidemia y resistencia a la insulina.
La edición y publicación de esta conferencia han sido posibles gracias a un auspicio sin restricciones de Roche.
Medwave. Ańo VII No. 2 Marzo 2007. Derechos Reservados.

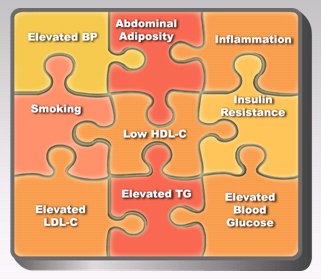 Figura 1. Los factores de riesgo cardiometabólicos tienden a agruparse como “el síndrome metabólico”.
Figura 1. Los factores de riesgo cardiometabólicos tienden a agruparse como “el síndrome metabólico”.

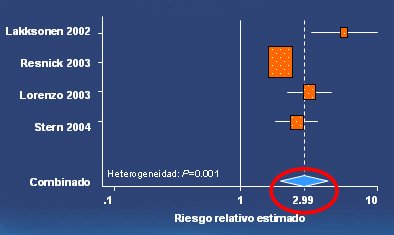 Figura 2. El síndrome metabólico aumenta el riesgo relativo de diabetes (Ford ES. Diabetes Care 2005).
Figura 2. El síndrome metabólico aumenta el riesgo relativo de diabetes (Ford ES. Diabetes Care 2005).

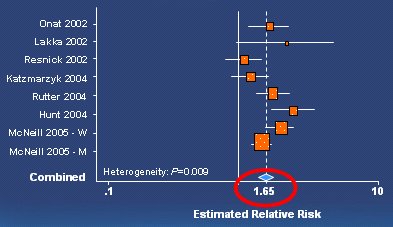 Figura 3. El síndrome metabólico aumenta el riesgo relativo de enfermedad cardiovascular (Ford ES. Diabetes Care. 2005).
Figura 3. El síndrome metabólico aumenta el riesgo relativo de enfermedad cardiovascular (Ford ES. Diabetes Care. 2005).

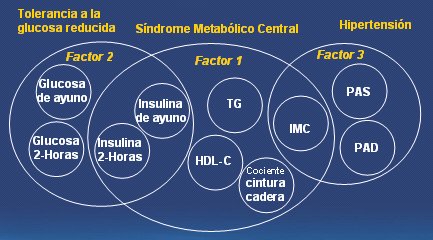 Figura 4. Agrupación del riesgo cardiometabólico. Análisis de las variables del estudio de Framingham. (Meigs J, et al. Diabetes 1997).
Figura 4. Agrupación del riesgo cardiometabólico. Análisis de las variables del estudio de Framingham. (Meigs J, et al. Diabetes 1997).

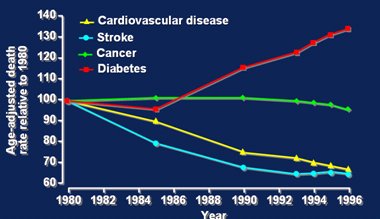 Figura 5. Tasa de mortalidad por enfermedades crónicas. La mortalidad por diabetes ha aumentado entre 1980 y 1996.
Figura 5. Tasa de mortalidad por enfermedades crónicas. La mortalidad por diabetes ha aumentado entre 1980 y 1996.

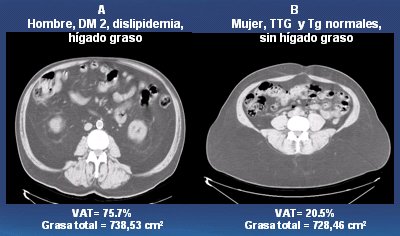 Figura 6. Importancia de la adiposidad visceral dentro de la grasa abdominal total.
Figura 6. Importancia de la adiposidad visceral dentro de la grasa abdominal total.

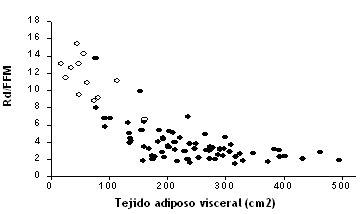 Figura 7. Relación entre VAT (cantidad de grasa visceral) y resistencia a la insulina. Rd/FFM=Relationship between muscle attenuation and insulin sensitivity (Kelley 2003).
Figura 7. Relación entre VAT (cantidad de grasa visceral) y resistencia a la insulina. Rd/FFM=Relationship between muscle attenuation and insulin sensitivity (Kelley 2003).

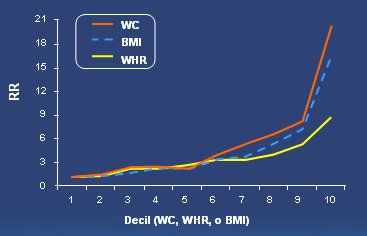 Figura 8. La adiposidad abdominal es mayor predictor de diabetes tipo 2 que la obesidad total. (Wang Y, et al. Am J Clin Nutr 2005).
Figura 8. La adiposidad abdominal es mayor predictor de diabetes tipo 2 que la obesidad total. (Wang Y, et al. Am J Clin Nutr 2005).

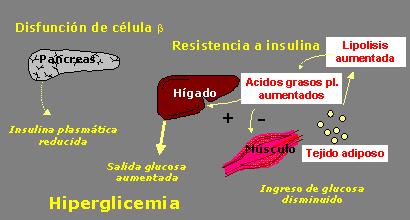 Figura 9. Resistencia a insulina y disfunción de células beta en la diabetes tipo 2.
Figura 9. Resistencia a insulina y disfunción de células beta en la diabetes tipo 2.

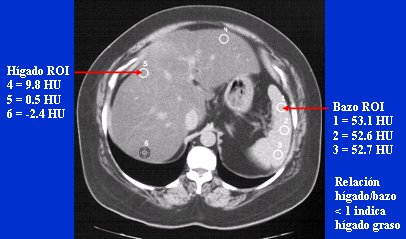 Figura 10. Estudio no invasivo del hígado graso.
Figura 10. Estudio no invasivo del hígado graso.

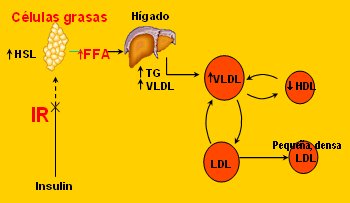 Figura 11. Mecanismos que relacionan la resistencia insulínica, la grasa tisular y hepática y la dislipidemia.
Figura 11. Mecanismos que relacionan la resistencia insulínica, la grasa tisular y hepática y la dislipidemia.

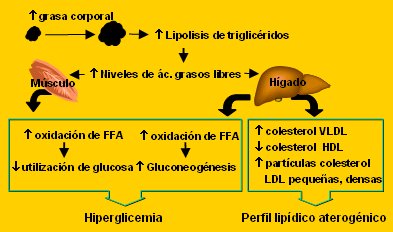 Figura 12. Consecuencias metabólicas del aumento de la grasa corporal (Adaptado de Pi-Sunyer. Obes Res. 2002).
Figura 12. Consecuencias metabólicas del aumento de la grasa corporal (Adaptado de Pi-Sunyer. Obes Res. 2002).

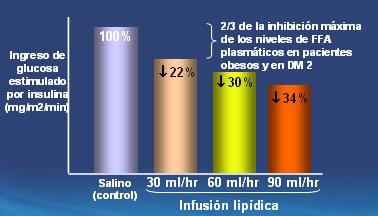 Figura 13. Efecto dosis-respuesta de los ácidos grasos libres (FFA) plasmáticos elevados sobre la seńal de insulina en individuos sanos, delgados (Belfort, Cusi et al. Diabetes 2005).
Figura 13. Efecto dosis-respuesta de los ácidos grasos libres (FFA) plasmáticos elevados sobre la seńal de insulina en individuos sanos, delgados (Belfort, Cusi et al. Diabetes 2005).

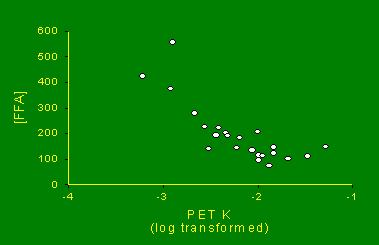 Figura 14. Diabetes tipo 2: resistencia insulínica muscular y niveles plasmáticos de ácidos grasos (Kelley et al., JCEM, 2001).
Figura 14. Diabetes tipo 2: resistencia insulínica muscular y niveles plasmáticos de ácidos grasos (Kelley et al., JCEM, 2001).


 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Expositor:
David Kelley[1]
Expositor:
David Kelley[1]

Citación: Kelley D. Does the metabolic syndrome exist?. Medwave 2007 Mar;7(2):e2371 doi: 10.5867/medwave.2007.02.2371
Fecha de publicación: 1/3/2007

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión