La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Servicio de Pediatría del Hospital Clínico San Borja Arriarán.
Edición científica: Dr. Luis Delpiano.
Frente a la sospecha clínica de hipercortisolismo, se debe evaluar la función suprarrenal mediante las siguientes pruebas:
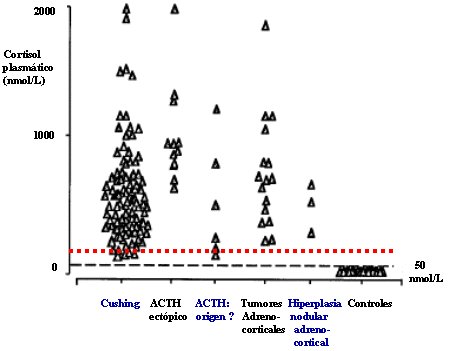
A) La producción de cortisol se puede evaluar mediante la determinación de cortisol libre urinario. Normalmente se excreta una mínima parte de la producción diaria de cortisol, por lo que, frente a un exceso de cortisol urinario, se debe sospechar un estado de hipercortisolismo. Se necesita una recolección de orina de 24 horas, que no es fácil de conseguir, en la que se mide la secreción integrada de cortisol. Esto permite plantear el diagnóstico, pero no tener certeza de hipercortisolismo, pues hay otros cuadros clínicos en los que puede aumentar la secreción integrada de cortisol, como la depresión, el ayuno en pacientes obesos, el embarazo y el tratamiento con estrógenos. Otra forma de evaluar la producción diaria de cortisol es mediante la evaluación del ritmo circadiano del cortisol, cuya máxima producción ocurre entre las 6 y las 9 de la mańana, y la mínima, a las 23 horas. Todos los estados de hipercortisolismo presentan niveles de cortisol elevados en la medición nocturna, niveles que son bajos en todos los pacientes controles, por lo que es un muy buen parámetro. En lo posible, el paciente debe estar hospitalizado, durmiendo y con una vía instalada previamente para tomar la muestra con la mayor tranquilidad posible a la medianoche. Los niveles de cortisol a medianoche (Fig. 1) son bajos en los controles y se mantienen elevados, tanto en los pacientes con síndrome de Cushing como en los que presentan secreción ectópica de ACTH.
Figura 1. Cortisol plasmático de medianoche (J Newell-Price et al. Clin Endocrinol 1995;43:545-550)
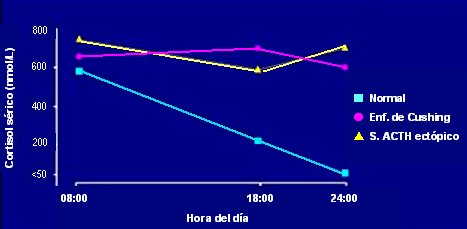
B) Otra forma es frenar el eje con dexametasona, la que se puede utilizar en dosis bajas o altas. Se aporta dexametasona en la noche y se evalúa la producción de cortisol en la mańana. Lo habitual es que la dexametasona, que es un corticoide, actúe como freno hipotálamo-hipofisiario, por lo que los niveles de cortisol de la mańana deberían disminuir. Si hay un tumor hipofisiario, este tumor actuará en forma independiente y, en consecuencia, las dosis bajas no frenarán el eje; pero si se aportan dosis más altas de lo necesario, se frenará la producción de ACTH a nivel hipofisiario. En el caso del tumor suprarrenal, a pesar de que se actúe sobre el eje, éste se encuentra frenado en forma autónoma por el tumor y habrá niveles aumentados de cortisol, lo mismo que ocurrirá cuando haya secreción ectópica. Por lo tanto, la administración de dexametasona en dosis bajas permitirá realizar el diagnóstico de hipercortisolismo y el aporte de dexametasona en dosis altas, al actuar sobre el eje, permitirá determinar si este hipercortisolismo tiene un origen ACTH dependiente o independiente. En la actualidad se cuenta, además, con la medición de ACTH, lo que, sumado al test de dexametasona, permite determinar si el hipercortisolismo es dependiente de ACTH; en cuyo caso este hecho significa que el origen es hipofisiario o ectópico; o bien si es independiente de ACTH, situación que corresponde a un tumor suprarrenal (Fig. 2).
Figura 2. Ritmo circadiano de los niveles de cortisol
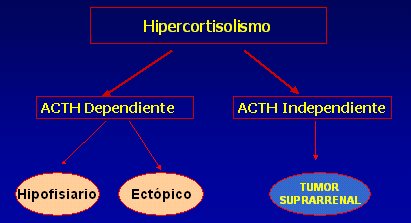
C) Para localizar el origen del hipercortisolismo, lo primero es saber que puede ser hipofisiario, ectópico o suprarrenal (Fig. 3). En la edad pediátrica, cuando es ACTH dependiente, lo más frecuente es que sea de origen hipofisiario; en este caso la resonancia nuclear magnética es de gran utilidad y, en cambio, el escáner cerebral no ayuda mucho, porque no permite visualizar bien la hipófisis. Si hay una fuerte sospecha de que el hipercortisolismo es ACTH dependiente y la imagen hipofisiaria no es concluyente, se deberá realizar un rastreo sistémico.
Figura 3. Diagnóstico diferencial de hipercortisolismo
En la actualidad hay otro método para localizar el tumor cuando se sospecha una causa hipofisiaria: la cateterización de los senos petrosos mediante una técnica invasiva, que debe efectuar una persona con mucha experiencia. Este examen permite determinar si el tumor es hipofisiario, mediante la comparación del nivel plasmático de ACTH, central y periférico, en respuesta a la administración de hCRH endovenosa. Antes se pensaba que este examen era el gold standard para definir la localización y orientar la cirugía, pero hace poco apareció un artículo en Journal of Clinical Endocrinology and Metabolism en el que se seńala que en los nińos no es tan certero, ya que orienta si el tumor es hipofisiario, pero no localiza claramente el tumor.
Frente a la sospecha clínica de hipercortisolismo, la conducta que se ha de seguir se resume como sigue (Fig.4). En primer lugar, se deben evaluar los niveles de cortisol libre urinario, lo que permitirá confirmar que existe un hipercortisolismo; lo anterior, sumado a la evaluación del ritmo circadiano que se puede realizar con la medición matinal y nocturna, y a la pérdida de supresión con dosis bajas de dexametasona, confirmará el diagnóstico. Después se deberá ubicar la causa: si los niveles de ACTH son bajos, no hay supresión con dexametasona en dosis altas y hay una imagen sugerente a nivel suprarrenal, con una hipófisis normal, el origen del hipercortisolismo será suprarrenal y el tumor podrá ser benigno o maligno. Si los niveles de ACTH están normales o elevados, hay supresión con dosis altas, la imagen suprarrenal es normal y la imagen hipofisiaria plantea un tumor, es sumamente probable que la lesión sea de origen hipofisiario. Por último, la presencia de niveles altos o normales de ACTH, sin supresión y con imágenes normales, orienta a que la causa es ectópica.
Figura 4. Diagnóstico diferencial de hipercortisolismo





 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Servicio de Pediatría del Hospital Clínico San Borja Arriarán.
Edición científica: Dr. Luis Delpiano.
 Expositora:
María Isabel Hernández C.[1]
Expositora:
María Isabel Hernández C.[1]

Citación: Hernández MI. Assessment of adrenal function in Cushing's syndrome II: clinical case discussion. Medwave 2006 Ago;6(7):e2420 doi: 10.5867/medwave.2006.07.2420
Fecha de publicación: 1/8/2006

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión