La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Servicio de Pediatría del Hospital Clínico San Borja Arriarán.
Edición científica: Dr. Luis Delpiano.
La influenza marca hitos históricos con una gran letalidad a causa de epidemias y pandemias:
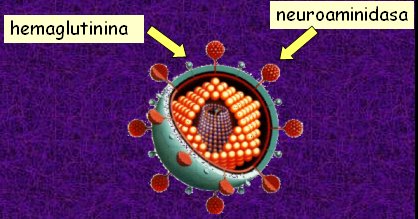
El virus influenza se subdivide en tres subtipos: A, B y C, de los cuales, el C no tiene implicancias patogénicas en el ser humano. Es un virus ARN con forma circular y su poder patogénico está dado principalmente por la neuraminidasa y la hemaglutinina, según cuyas características el virus, sobre todo el virus A, se subdivide en tipos, denominados H1, H2, etc., hasta el 15, según el tipo de hemaglutinina; y N1 hasta N9, según la neuraminidasa. En la Figura 1 se ilustra la estructura del virus Influenza A.
Figura 1. Influenza A según hemaglutinina y neuroaminidasa. Subtipos H (1-15) N (1-9).
En los últimos ańos han predominado 3 ó 4 subtipos o cepas, de las cuales, las de importancia para la especie humana son la H1N1, (hemaglutinina 1, neuraminidasa 1), y la H3N2.
El virus influenza A es el más temido, porque es el único que puede experimentar cambios antigénicos, que pueden ser puntuales o menores (llamados drift), que corresponden a acumulación de pequeńas mutaciones en la neuraminidasa o en la hemaglutinina, o pueden ser cambios completos o mayores (denominados shift), que implican la captación de una hemaglutinina o neuraminidasa diferente, desde otros subtipos, por ejemplo, de H1N1 a H5N1. Este cambio completo es el responsable de la generación de epidemias, porque no existen anticuerpos que reconozcan a este nuevo subtipo (Lancet 1999;354:1277-82).
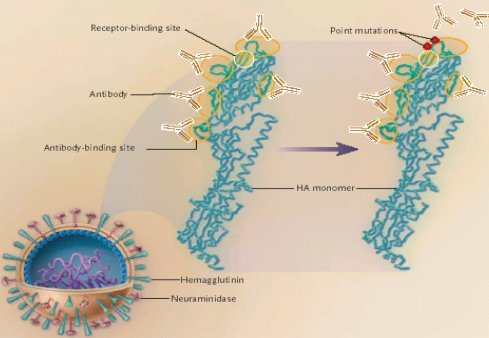
En la Figura 2 se observa un diagrama del virus influenza, con la neuraminidasa y la hemaglutinina en su superficie; hacia la derecha se ve una hemaglutinina normal, amplificada, a la cual que se están uniendo los anticuerpos, en sitios reconocidos desde el punto de vista proteico. Cuando se producen los drift o cambios menores, los anticuerpos no llegan a estas zonas, pero quedan otros sectores en los cuales podrían actuar; en el caso del cambio shift ocurre un cambio estructural de los aminoácidos de esta proteína, por lo que no hay anticuerpos históricos que la puedan reconocer y actuar como defensa.
Figura 2. Diagrama del virus influenza. Unión de anticuerpos a la hemaglutinina.
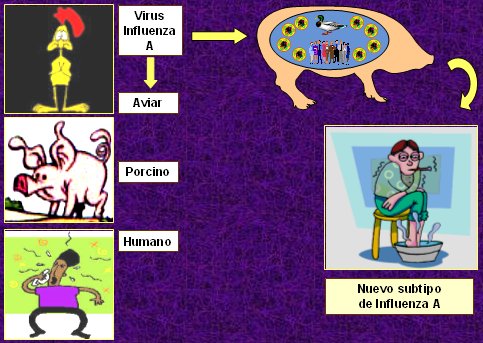
En la Figura 3 se ilustra el mecanismo de generación de un nuevo subtipo viral. En países como China y en general, en el continente asiático, existe una convivencia con virus influenza de tipo animal, que pueden ser traspasados al ser humano; éste es el caso del virus influenza aviar, que afecta y mata a los pollos, pero puede tener como intermediario al cerdo, al igual que el virus influenza humano; este animal es criado en las habitaciones, en la población china, dándose una situación propicia para que se produzca una mezcla de antígenos virales y eventualmente se origine un nuevo subtipo de influenza A y, por lo tanto, una pandemia.
Figura 3. Generación de un nuevo subtipo de virus influenza A.
La influenza tiene una elevada morbimortalidad. En los Estados Unidos ha llegado a causar 51.000 muertes al ańo, pero últimamente la cifra bordea las 5.000 defunciones. Como morbilidad, afecta a 20 a 30% de la población general y a 30 a 40% de los nińos. Los nińos sanos, sin comorbilidades, que se enferman, transmiten el virus a la comunidad y menos de 10% de ellos desarrollan complicaciones de la influenza, por lo tanto, es una población de riesgo menor (NEJM 1998 (338); 20: 1459-1461).
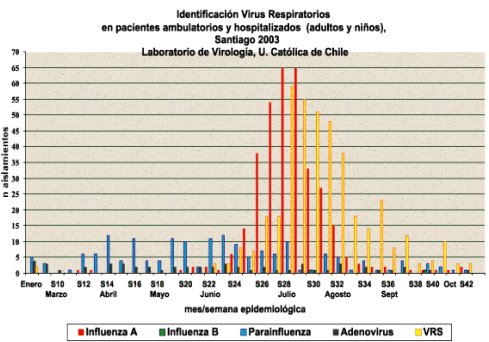
En la Figura 4 se observa el patrón chileno de los virus respiratorios de Santiago el ańo 2003. En rojo aparece la influenza A, que corresponde a alrededor de 95% de las infecciones por influenza, predominando desde julio a agosto, con niveles un poco superiores a la detección de VRS, que aparece en amarillo. Hacia la izquierda se observa que el número de aislamientos nunca sobrepasó los 70 por semana, o sea, 2003 fue un ańo tranquilo en cuanto a influenza. La cepa de ese ańo fue H3N2, igual que en 2001, mientras que en 2002 fue H1N1.
Figura 4. Virus respiratorios en Chile ańo 2003.
En 2004, el número de aislamientos de virus influenza llegó a 300 por semana; por eso, las consultas por infección respiratoria aguda (IRA) fueron de mucho mayor volumen en todos los hospitales de Chile, en comparación con los ańos anteriores. Los aislamientos por VRS llegaron a más de 500 por semana, es decir, fue un gran brote epidémico. La influenza precedió al gran brote de VRS, que es el gran causante de los ingresos por IRA que nosotros hospitalizamos.
En nuestro estudio prospectivo realizado durante 1999 en el hospital, publicado en el ańo 2003 en la Revista Chilena de Infectología, se analizó el comportamiento clínico y epidemiológico de la infección por virus influenza en nińos hospitalizados. El diagnóstico fue realizado por inmunofluorescencia directa, que es un método diagnóstico muy bueno, y se determinó las características clínicas, epidemiológicas y evolutivas de 175 nińos con influenza, que fueron divididos en dos grupos. El grupo 1 constituido por 46 nińos con influenza confirmada y que tenían condiciones de base como prematurez o dańo pulmonar, neurológico o cardíaco, mientras que el grupo 2 estaba formado por 129 pacientes sin comorbilidades.
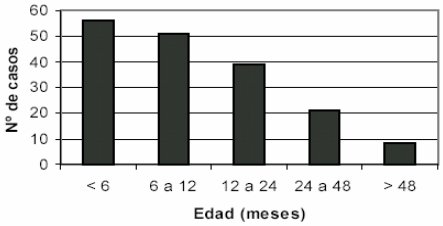
En cuanto a la distribución etaria de los pacientes con influenza, que se encuentra graficada en la Figura 5, alrededor de un tercio de los afectados eran menores de 6 meses, que no tuvieron acceso a vacuna, por lo tanto, siempre va a existir una población preponderante que no va a estar protegida por la vacuna y que tiene mayor riesgo de contagiarse. La mayoría de los pacientes afectados eran menores de 24 meses y muy pocos tenían más de 48 meses.
Figura 5. Distribución por edad de pacientes con Influenza. Mayo – Agosto 1999. Pediatría HCSBA (n = 175).
Respecto a las complicaciones observadas:
En cuanto al requerimiento de oxígeno, el grupo 1 de nińos con coexistencias, recibió oxígeno por 9,3 días en promedio, en comparación con 4,1 días del grupo 2; la diferencia también fue significativa.
La duración de la estadía hospitalaria del grupo 2 fue similar al promedio pediátrico del hospital San Borja Arriarán, alrededor de 5,9 días, en comparación con los 13,6 días, en promedio, que tardó en egresar un nińo con comorbilidades.





 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

La publicación de estas Actas Científicas ha sido posible gracias a una colaboración editorial entre Medwave y el Servicio de Pediatría del Hospital Clínico San Borja Arriarán.
Edición científica: Dr. Luis Delpiano.
 Expositor:
Luis Delpiano Méndez[1]
Expositor:
Luis Delpiano Méndez[1]

Citación: Delpiano L. Influenza vaccine: overview. Medwave 2005 Jun;5(5):e2392 doi: 10.5867/medwave.2005.05.2392
Fecha de publicación: 1/6/2005

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión