 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en reuni¾n clĒnica del Departamento de Medicina, Hospital ClĒnico Universidad de Chile. La publicaci¾n de estas actas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y el Departamento de Medicina del Hospital ClĒnico Universidad de Chile. El director del Departamento de Medicina es el Dr. Alejandro Cotera.
El diagn¾stico de n¾dulo pulmonar ha aumentado notablemente en los ·ltimos a±os debido a los avances en los mķtodos diagn¾sticos, sobre todo en el campo de las imßgenes. Se entiende como n¾dulo pulmonar a una imagen que re·ne las siguientes caracterĒsticas:
Todas estas caracterĒsticas se deben analizar en conjunto para catalogar al n¾dulo como maligno o benigno.
El escßner de t¾rax permite identificar n¾dulos menores de 1 mm de dißmetro. En una cohorte de 1.500 pacientes fumadores, en 74% se detect¾ un n¾dulo pulmonar solitario (NPS) en cinco a±os de seguimiento; por esa raz¾n el n·mero de consultas por derivaci¾n de pacientes portadores de n¾dulos pulmonares ha aumentando mucho en los ·ltimos a±os; no obstante, la mayorĒa de ellos son benignos (1). La radiografĒa de t¾rax es capaz de discriminar n¾dulos de mßs de 5 mm; cuando se usa como screening el porcentaje de pesquisa disminuye a 20% (2).
En un estudio efectuado en paĒses asißticos, 31.567 pacientes fumadores se estudiaron con escßner de t¾rax y en 4.186 casos se encontr¾ un n¾dulo pulmonar; de ellos 405 resultaron malignos. En una segunda evaluaci¾n de los pacientes que no tuvieron n¾dulos en el estudio inicial, se encontr¾ otros cinco casos de cßncer; en el resto de los pacientes se hizo un tamizaje con escßner, con el que se pesquis¾ 74 casos mßs. En resumen, en alrededor de 31.000 pacientes de alto riesgo se encontraron 484 casos de cßncer. Con estos resultados se demuestra que con la TAC de t¾rax aumenta la posibilidad de pesquisa precoz de cßncer pulmonar, no obstante lo que no queda claro es si esta polĒtica serĒa costo efectiva (3).
En la evaluaci¾n clĒnica de un n¾dulo pulmonar, lo primero es descartar lesiones extrapulmonares. Por ejemplo en la Fig. 1 se observa una peque±a imagen nodular que corresponde a una calcificaci¾n pleural secundaria a la exposici¾n a asbesto (4).
Figura 1. N¾dulo pulmonar: descartar lesi¾n extrapulmonar sobreproyectada en el campo pulmonar.
Tambiķn es importante que el n¾dulo tenga aspecto de tal en todas las proyecciones: cuando la relaci¾n entre el ancho y el alto es de un 1,8:1 existe 100% de probabilidades de que el n¾dulo sea benigno En el escßner de la Fig. 2 se observa un n¾dulo adosado a la pared torßcica, que en el corte sagital toma una forma ovalada y aplanada; se trata de una adenopatĒa calcificada, es decir, una lesi¾n benigna. Por tal raz¾n es necesario confirmar la naturaleza esfķrica del n¾dulo en todas sus dimensiones (5).
Figura 2. Relaci¾n ancho/alto >1,8:1 tiene 100% de sensibilidad para n¾dulo benigno.
En la siguiente imagen se observa un n¾dulo en un paciente que consulta por un cuadro pulmonar agudo, con tos, fiebre y desgarro purulento. En este caso se administr¾ antibi¾tico y se repiti¾ el escßner a las seis semanas. Se puede observar una regresi¾n parcial, aunque esto no asegura que el n¾dulo sea benigno (Fig. 3).
Una vez que se confirma el hallazgo de un n¾dulo, porque se ha descartado que sea artefacto, pez¾n o lesi¾n extrapulmonar, se debe determinar las siguientes caracterĒsticas (2).
En estudios de pacientes con n¾dulos pulmonares, el anßlisis multivariado ha demostrado que el riesgo de cßncer es muy alto en los fumadores, en pacientes de mayor edad y en los que tienen n¾dulos de mayor tama±o, mientras que los a±os que el paciente ha dejado de fumar constituyen un factor protector. Por lo tanto, estos elementos son los pilares de la evaluaci¾n clĒnica del paciente (6).
En la morfologĒa del NPS interesa el tama±o, la forma, los mßrgenes y la composici¾n del n¾dulo: si tiene calcificaci¾n, grasa, cavitaci¾n, broncograma o aspecto de vidrio esmerilado. Ademßs interesa la tasa de crecimiento y la respuesta al medio de contraste. Estos cinco elementos permiten establecer el riesgo de cßncer.
Tama±o: En un estudio de la clĒnica Mayo efectuado en 1.500 enfermos se encontr¾ que los n¾dulos de 3 cm o mßs tienen 90% de probabilidades de cßncer, mientras que los de menos de 4 mm tienen 1% de malignidad, por lo tanto si un paciente no es fumador y tiene un n¾dulo de 4 mm o menos se podrĒa asegurar que no requiere mayor estudio (4). La primera recomendaci¾n que desarroll¾ la Sociedad de Radi¾logos de los Estados Unidos se bas¾ en el tama±o del n¾dulo y la presencia de factores de riesgo: los pacientes sin riesgo y con un n¾dulo menor de 4 mm no necesitan ning·n tipo de estudio, no obstante la mayorĒa de los n¾dulos menores de 1 cm requieren seguimiento, cuya periodicidad depende de los factores de riesgo y se debe prolongar al menos por dos a±os (7). En n¾dulos de mßs de 1 cm se debe hacer estudio y seguimiento mßs activos (Tabla I).
Tabla I. GuĒa para el manejo del n¾dulo pulmonar solitario peque±o pesquisado en el escßner.
Forma y mßrgenes: Cuando un n¾dulo tiene contorno liso en la mayor parte de su superficie es muy probable que sea benigno, aunque hay excepciones, especialmente en las metßstasis de mamas, colon, carcinoide y tumores del sistema urogenital. En la Fig. 4 se muestra un n¾dulo benigno en la parte superior y un n¾dulo metastßtico en la parte inferior: en el recuadro C aparece como un n¾dulo de contorno liso, pero posteriormente adopt¾ una forma lobulada (Fig. 4).
Figura 4. A, B: N¾dulo pulmonar benigno. C, D: n¾dulo maligno, de origen metastßtico.
El borde espiculado de un NPS es muy sugerente de malignidad, mßs a·n si es mayor de de 1 cm; el borde lobulado tiene riesgo intermedio y se dice que la lobulaci¾n de mßrgenes c¾ncavos se asocia a carßcter benigno, mientras que la lobulaci¾n convexa se asocia a lesiones malignas. La presencia de cola es de riesgo intermedio para malignidad. En la siguiente imagen se muestran ejemplos n¾dulos especulado, lobulado y con cola; este ·ltimo ademßs estß cavitado (Fig. 5).
Figura 5. A: n¾dulo pulmonar espiculado. B: lobulado. C: n¾dulo pulmonar con ōcolaö.
Cuando un n¾dulo posee lesiones satķlites es altamente probable que se trate de una lesi¾n granulomatosa, que en Chile lleva a pensar en tuberculosis y en otros paĒses, en lesiones f·ngicas (Fig. 6).
Figura 6. N¾dulo con lesiones satķlites: imagen muy sugerente de granulomas.
La siguiente imagen corresponde a un estudio con contraste en el que se observa un n¾dulo alimentado por un vaso arterial y drenado por un vaso venoso. Esto corresponde a una malformaci¾n arteriovenosa y no requiere mßs estudio (Fig.7).
Figura 7. La identificaci¾n de vasos que alimentan al n¾dulo sugiere MAV.
Patr¾n de calcificaci¾n: La calcificaci¾n total o central es muy sugerente de lesi¾n benigna. En caso de que los n¾dulos sean demasiado peque±os para determinar si estßn o no calcificados se puede medir su densidad en unidades Hounsfield (UH) mediante el procesador del escßner; si la densidad de igual o mayor de 200 UH significa que el n¾dulo estß calcificado y por lo tanto, es benigno (Fig. 8).
Las calcificaciones granulares con forma de pop corn son prßcticamente patognom¾nicas de hamartoma, que es una lesi¾n benigna. En cambio, la presencia de calcificaciones principales excķntricas o distr¾ficas es propia de las lesiones malignas, como la que aparece en la parte inferior de la siguiente imagen, que ademßs tiene bordes especulados y mide mßs de 2 cm: en este caso la biopsia revel¾ un adenocarcinoma (Fig. 9).
En la Fig. 10 se observa una imagen oscura de densidad similar a la de la grasa. La presencia de grasa en el interior de un n¾dulo tambiķn es patognom¾nico de un hamartoma, salvo que se trate de un liposarcoma, que rara vez se presenta en los pulmones.
Figura 10. N¾dulo con densidades compatibles con grasa son muy sugerentes de hamartoma.
Cavitaci¾n: La cavitaci¾n suele estar presente en lesiones benignas, como granuloma o vasculitis, no obstante un grosor de pared de 15 mm o mayor sugiere malignidad: generalmente se trata de tumores espinocelulares que se necrosan en el centro, lo que dificulta el diagn¾stico ya que los estudios de actividad metab¾lica no tienen buen rendimiento debido a esta necrosis (Fig. 11).
Vidrio esmerilado: Los n¾dulos con aspecto de vidrio esmerilado, que se caracterizan porque el observador puede ver a travķs de la lesi¾n, son malignos hasta en 60% de los casos; corresponden a carcinoide o carcinomas bronquioloalveolares que son muy difĒciles de diagnosticar mediante imßgenes, tanto con el PET scan como con la adquisici¾n de contraste. La figura 12 muestra una lesi¾n con broncograma aķreo que sugiere fuertemente un carcinoma bronquioloalveolar (Fig. 12). Las hiperplasias adenomatosas tambiķn pueden dar una imagen en vidrio esmerilado.
La tasa de crecimiento de un n¾dulo pulmonar no es fßcil de determinar debido a que son estructuras tridimensionales que tienen volumen, motivo por el cual basta que el contorno aumente en 30% para que la masa doble su tama±o; por ejemplo, si un n¾dulo de 4 mm crece a 5 mm su tama±o aumentarß al doble, pero radiol¾gicamente esto es muy difĒcil de apreciar, lo que determina una gran variabilidad entre los distintos observadores.
Se ha usado como criterio de malignidad el hecho de que el n¾dulo doble su masa en un periodo mayor de 30 dĒas y menor de dos a±os; las lesiones que doblan su tama±o en menos de un mes suelen ser de origen infeccioso y las que tardan mßs de dos a±os tambiķn suelen ser benignas. Los cßnceres bronquioloalveolares y el carcinoide tĒpico son excepciones a esta regla, ya que son de crecimiento lento y pueden tener tasas de doblaje mayores de dos a±os.
Para evitar el problema de la variabilidad interobservador se utilizan programas computacionales, como el que estß disponible en el Hospital ClĒnico de la Universidad de Chile. Este programa establece que una tasa de doblaje menor de 500 dĒas tiene: sensibilidad de 91%; especificidad de 90%; valor predictivo positivo de 67% y valor predictivo negativo de 98%, es decir, si la tasa de doblaje no es menor de 500 dĒas casi se puede asegurar que el paciente no tiene cßncer (8). En la siguiente imagen se observa a simple vista que el n¾dulo no cambio de tama±o; la medici¾n de masa a travķs del ßrea de interķs entrega un valor de doblaje de 290 dĒas, lo que sugiere que es maligno.
Figura 13. Determinaci¾n del tiempo de doblaje de un n¾dulo pulmonar.
Se ha demostrado que 5 a 10% de los n¾dulos malignos se reducen de tama±o en intervalos cortos de seguimiento; por lo tanto si una lesi¾n de mal aspecto se reduce, pero no desaparece no significa que no sea cßncer y se debe continuar el seguimiento durante el plazo indicado de dos a±os (9).
El uso de medio de contraste se basa en el principio de que las lesiones neoplßsicas, que poseen mayor cantidad vasos de neoformaci¾n, captan mßs medio de contraste. Esto es cierto siempre y cuando el n¾dulo benigno no corresponda a una lesi¾n inflamatoria en fase aguda, que tambiķn tiene aumento de la vascularizaci¾n, por lo que existe un traslape. Los tumores benignos inflamatorios ganan contraste, pero los malignos ya tienen ganancia; por lo tanto si un n¾dulo no aumenta en al menos 15 UH su intensidad en la captaci¾n de contraste, lo mßs probable es que no sea cßncer. Esto tiene elevada sensibilidad (98%), pero baja especificidad (58%). Si el examen sale negativo se puede afirmar que el n¾dulo es benigno, pues el valor predictivo negativo es 98% (Fig. 14).
Figura 14. Estudios complementarios: evaluaci¾n del n¾dulo con contraste.
La ganancia de medio de contraste se determina mediante observaci¾n, seg·n protocolo, al minuto y a los dos, tres y cuatro minutos. Esto es importante, pues existen lesiones que no aparecen en la tomografĒa de emisi¾n de positrones, pero sĒ tienen ganancia de contraste, como el tumor carcinoide, que es vascularizado (10).
En la tķcnica de medicina nuclear PET (TomografĒa de Emisi¾n de Positrones) se administra glucosa marcada con fl·or, la cual es captada ßvidamente por las cķlulas que poseen un metabolismo activo; como las cķlulas neoplßsicas tienen mayor recambio celular y elevada tasa metab¾lica, en presencia de cßncer la se±al se intensifica. Gould hizo un metaanßlisis en el que demostr¾ que este examen es ·til para evaluar n¾dulos de 1 cm o mayores, con sensibilidad 97% y especificidad 78%, por lo que recomienda su uso en n¾dulos indeterminados en pacientes de alto riesgo. Como es un anßlisis de cuerpo entero permite encontrar tumores en otros lugares y cambiar la etapificaci¾n, de modo que es un gran aporte al manejo del paciente; esto sin olvidar que la tķcnica que no ha sido validada para tumores menores de 1 cm (11). Pueden dar falsos negativos los tumores carcinoide, bronquioloalveolar y adenocarcinoma de bajo grado, y falsos positivos todos los tumores con alta tasa metab¾lica, como los secundarios a enfermedades infecciosas o inflamatorias, la sarcoidosis y la enfermedad de Wegener. Tiene bajo rendimiento en n¾dulos menores de 1 cm y en n¾dulos con aspecto de vidrio esmerilado. En la siguiente figura se observa, en la parte superior, una imagen de PET negativo en un paciente con un adenocarcinoma que no gan¾ mßs contraste que el resto de las estructuras. Abajo se observa un PET positivo con intensa captaci¾n, que corresponde a un granuloma por tuberculosis (Fig. 15).
Figura 15. A: PET negativo, adenocarcinoma. B: PET falso positivo, granuloma tuberculoso.
Punci¾n transtorßcica del n¾dulo. Mientras mßs cerca estķ el n¾dulo de la pared torßcica y mientras mßs grande sea, mßs fßcil serß efectuar este procedimiento; asimismo, a mayor cercanĒa de la pared menor serß la probabilidad de provocar un neumot¾rax, complicaci¾n que ocurre en 30% de los enfermos aunque en la mayorĒa de los casos no tiene importancia clĒnica, pues mejora espontßneamente. La sensibilidad de de la punci¾n transtorßcica para cßncer es 80 a 95% y la especificidad, entre 50 y 88%. Cuando se sospecha que la lesi¾n es benigna es mejor utilizar una aguja que permita extraer un trozo de tejido, como la aguja core (Fig. 16).
Figura 16. Punci¾n percutßnea guiada por TAC.
BroncoscopĒa: Esta tķcnica es poco ·til para el estudio de los n¾dulos perifķricos, ya que tiene bajo rendimiento y sensibilidad, alrededor de 20 a 40%, porque es muy difĒcil llegar a una lesi¾n de este tipo por vĒa bronquial, si bien el rendimiento puede llegar a 70% en lesiones con broncograma aķreo. Actualmente se estß aplicando esta tķcnica combinada con ultrasonografĒa, que identifica la posici¾n del n¾dulo y dirige la introducci¾n del instrumento a travķs de los bronquios, lo que incrementa el rendimiento a 88%. En el futuro la broncoscopĒa podrĒa llegar a ser una buena herramienta para obtener muestras histol¾gicas de los n¾dulos (12).

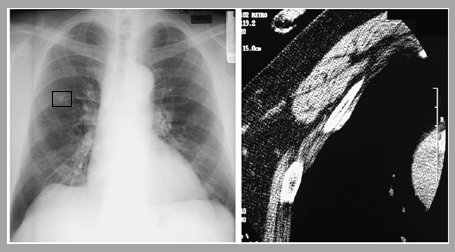 Figura 1. N¾dulo pulmonar: descartar lesi¾n extrapulmonar sobreproyectada en el campo pulmonar.
Figura 1. N¾dulo pulmonar: descartar lesi¾n extrapulmonar sobreproyectada en el campo pulmonar.

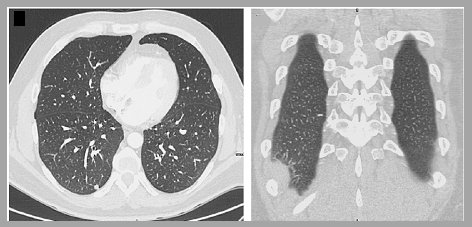 Figura 2. Relaci¾n ancho/alto >1,8:1 tiene 100% de sensibilidad para n¾dulo benigno.
Figura 2. Relaci¾n ancho/alto >1,8:1 tiene 100% de sensibilidad para n¾dulo benigno.

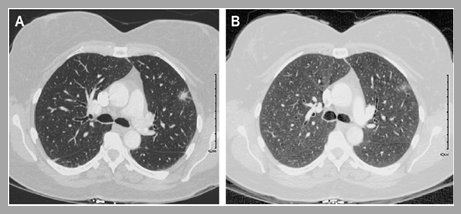 Figura 3. Cuando el hallazgo del n¾dulo estß en el contexto de un cuadro pulmonar agudo se debe considerar tratamiento antibi¾tico empĒrico y evaluaci¾n posterior.
Figura 3. Cuando el hallazgo del n¾dulo estß en el contexto de un cuadro pulmonar agudo se debe considerar tratamiento antibi¾tico empĒrico y evaluaci¾n posterior.

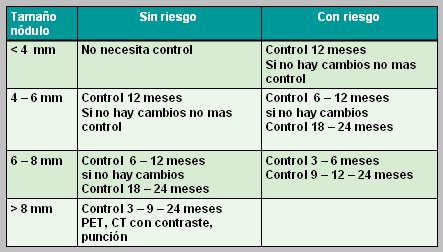 Tabla I. GuĒa para el manejo del n¾dulo pulmonar solitario peque±o pesquisado en el escßner.
Tabla I. GuĒa para el manejo del n¾dulo pulmonar solitario peque±o pesquisado en el escßner.

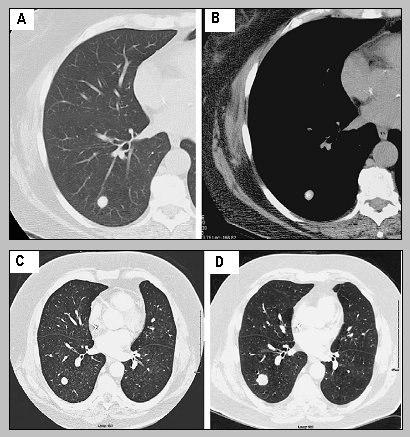 Figura 4. A, B: N¾dulo pulmonar benigno. C, D: n¾dulo maligno, de origen metastßtico.
Figura 4. A, B: N¾dulo pulmonar benigno. C, D: n¾dulo maligno, de origen metastßtico.

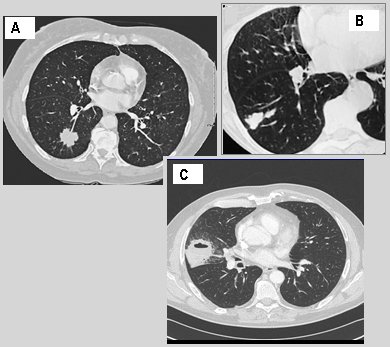 Figura 5. A: n¾dulo pulmonar espiculado. B: lobulado. C: n¾dulo pulmonar con ōcolaö.
Figura 5. A: n¾dulo pulmonar espiculado. B: lobulado. C: n¾dulo pulmonar con ōcolaö.

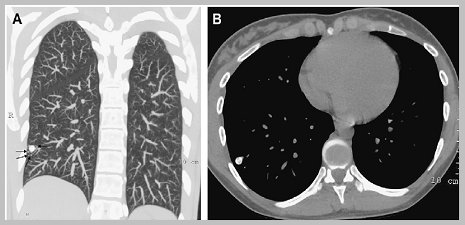 Figura 6. N¾dulo con lesiones satķlites: imagen muy sugerente de granulomas.
Figura 6. N¾dulo con lesiones satķlites: imagen muy sugerente de granulomas.

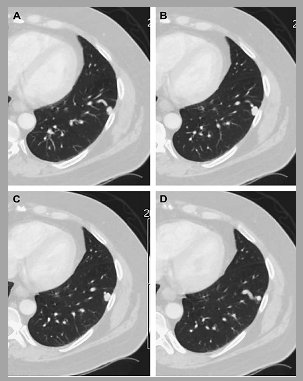 Figura 7. La identificaci¾n de vasos que alimentan al n¾dulo sugiere MAV.
Figura 7. La identificaci¾n de vasos que alimentan al n¾dulo sugiere MAV.

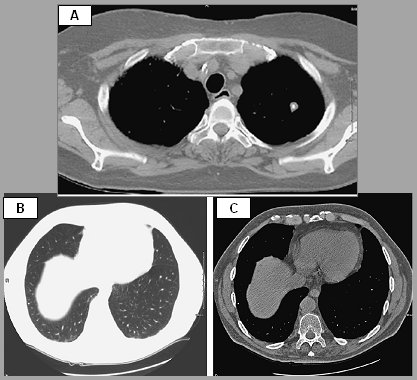 Figura 8. A: Calcificaci¾n total o central es altamente sugerente de lesi¾n benigna. B y C: N¾dulo con densidad igual o mayor de 200 UH, indica que estß calcificado.
Figura 8. A: Calcificaci¾n total o central es altamente sugerente de lesi¾n benigna. B y C: N¾dulo con densidad igual o mayor de 200 UH, indica que estß calcificado.

 Figura 9. A: Calcificaciones granulares (pop corn) indican hamartoma. B: Calcificaciones excķntricas o distr¾ficas pueden enmascarar una lesi¾n maligna.
Figura 9. A: Calcificaciones granulares (pop corn) indican hamartoma. B: Calcificaciones excķntricas o distr¾ficas pueden enmascarar una lesi¾n maligna.

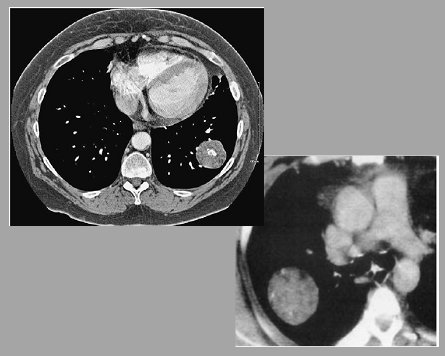 Figura 10. N¾dulo con densidades compatibles con grasa son muy sugerentes de hamartoma.
Figura 10. N¾dulo con densidades compatibles con grasa son muy sugerentes de hamartoma.

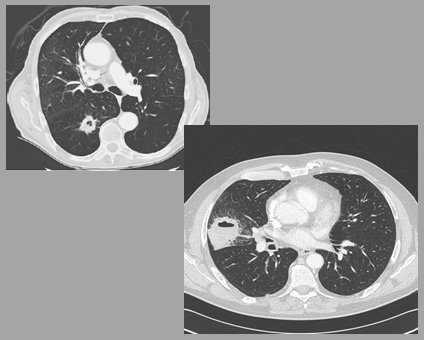 Figura 11. La cavitaci¾n puede estar presente en lesiones benignas y malignas, no obstante el grosor de la pared de 15 mm o mayor sugiere malignidad.
Figura 11. La cavitaci¾n puede estar presente en lesiones benignas y malignas, no obstante el grosor de la pared de 15 mm o mayor sugiere malignidad.

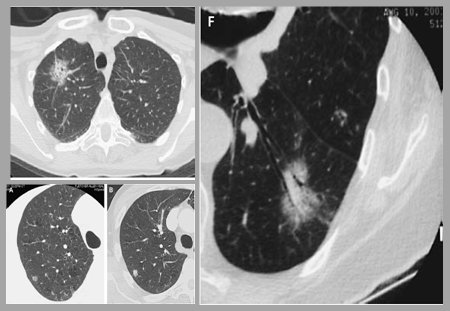 Figura 12. Los n¾dulos heterogķneos que contienen broncograma aķreo o vidrio esmerilado pueden ser malignos hasta en 60% de los casos.
Figura 12. Los n¾dulos heterogķneos que contienen broncograma aķreo o vidrio esmerilado pueden ser malignos hasta en 60% de los casos.

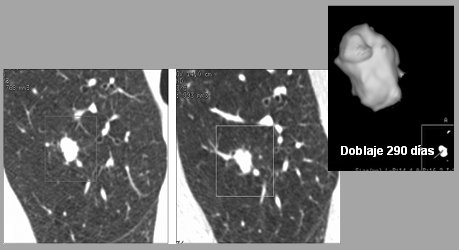 Figura 13. Determinaci¾n del tiempo de doblaje de un n¾dulo pulmonar.
Figura 13. Determinaci¾n del tiempo de doblaje de un n¾dulo pulmonar.

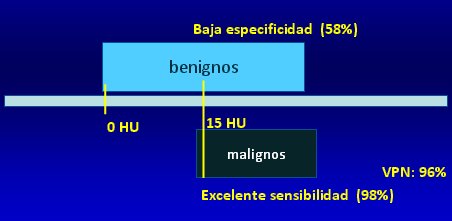 Figura 14. Estudios complementarios: evaluaci¾n del n¾dulo con contraste.
Figura 14. Estudios complementarios: evaluaci¾n del n¾dulo con contraste.

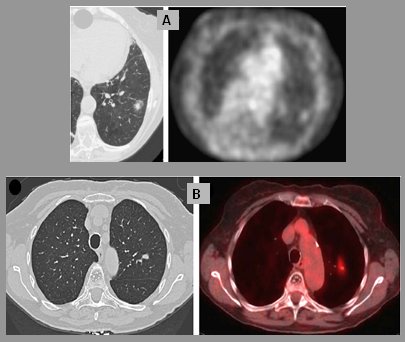 Figura 15. A: PET negativo, adenocarcinoma. B: PET falso positivo, granuloma tuberculoso.
Figura 15. A: PET negativo, adenocarcinoma. B: PET falso positivo, granuloma tuberculoso.

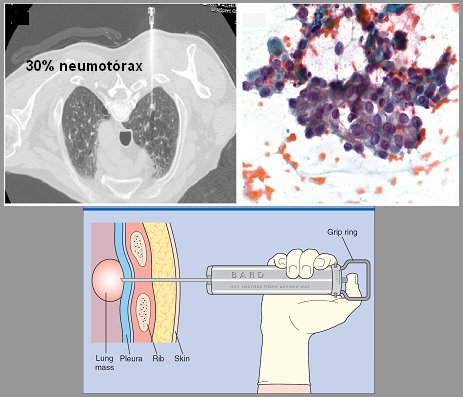 Figura 16. Punci¾n percutßnea guiada por TAC.
Figura 16. Punci¾n percutßnea guiada por TAC.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en reuni¾n clĒnica del Departamento de Medicina, Hospital ClĒnico Universidad de Chile. La publicaci¾n de estas actas ha sido posible gracias a una colaboraci¾n editorial entre Medwave y el Departamento de Medicina del Hospital ClĒnico Universidad de Chile. El director del Departamento de Medicina es el Dr. Alejandro Cotera.
 Autor:
Mauricio Ruiz[1]
Autor:
Mauricio Ruiz[1]

Citaci¾n: Ruiz M. Solitary pulmonary nodule. Medwave 2009 Jul;9(7):e4042 doi: 10.5867/medwave.2009.07.4042
Fecha de publicaci¾n: 1/7/2009

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Swensen SJ, Jett JR, Hartman TE, Midthun DE, Mandrekar SJ, Hillman SL, et al. CT screening for lung cancer: five-year prospective experience. Radiology. 2005 Apr;235(1):259-65. Epub 2005 Feb 4. | CrossRef | PubMed |
Swensen SJ, Jett JR, Hartman TE, Midthun DE, Mandrekar SJ, Hillman SL, et al. CT screening for lung cancer: five-year prospective experience. Radiology. 2005 Apr;235(1):259-65. Epub 2005 Feb 4. | CrossRef | PubMed | Ost D, Fein AM, Feinsilver SH. Clinical practice. The solitary pulmonary nodule. N Engl J Med. 2003 Jun 19;348(25):2535-42. | CrossRef | PubMed |
Ost D, Fein AM, Feinsilver SH. Clinical practice. The solitary pulmonary nodule. N Engl J Med. 2003 Jun 19;348(25):2535-42. | CrossRef | PubMed | International Early Lung Cancer Action Program Investigators, Henschke CI, Yankelevitz DF, Libby DM, Pasmantier MW, Smith JP, et al. Survival of patients with stage I lung cancer detected on CT screening. N Engl J Med. 2006 Oct 26;355(17):1763-71. | CrossRef | PubMed |
International Early Lung Cancer Action Program Investigators, Henschke CI, Yankelevitz DF, Libby DM, Pasmantier MW, Smith JP, et al. Survival of patients with stage I lung cancer detected on CT screening. N Engl J Med. 2006 Oct 26;355(17):1763-71. | CrossRef | PubMed | Klein JS, Braff S. Imaging evaluation of the solitary pulmonary nodule. Clin Chest Med. 2008 Mar;29(1):15-38, v. | CrossRef | PubMed |
Klein JS, Braff S. Imaging evaluation of the solitary pulmonary nodule. Clin Chest Med. 2008 Mar;29(1):15-38, v. | CrossRef | PubMed | Takashima S, Sone S, Li F, Maruyama Y, Hasegawa M, Matsushita T, et al. Small solitary pulmonary nodules (< or =1 cm) detected at population-based CT screening for lung cancer: Reliable high-resolution CT features of benign lesions. AJR Am J Roentgenol. 2003 Apr;180(4):955-64. | PubMed |
Takashima S, Sone S, Li F, Maruyama Y, Hasegawa M, Matsushita T, et al. Small solitary pulmonary nodules (< or =1 cm) detected at population-based CT screening for lung cancer: Reliable high-resolution CT features of benign lesions. AJR Am J Roentgenol. 2003 Apr;180(4):955-64. | PubMed | Gould MK, Ananth L, Barnett PG; Veterans Affairs SNAP Cooperative Study Group. A clinical model to estimate the pretest probability of lung cancer in patients with solitary pulmonary nodules. Chest. 2007 Feb;131(2):383-8. | CrossRef | PubMed | PMC |
Gould MK, Ananth L, Barnett PG; Veterans Affairs SNAP Cooperative Study Group. A clinical model to estimate the pretest probability of lung cancer in patients with solitary pulmonary nodules. Chest. 2007 Feb;131(2):383-8. | CrossRef | PubMed | PMC | MacMahon H, Austin JH, Gamsu G, Herold CJ, Jett JR, Naidich DP, et al. Guidelines for management of small pulmonary nodules detected on CT scans: a statement from the Fleischner Society. Radiology. 2005 Nov;237(2):395-400. | CrossRef | PubMed |
MacMahon H, Austin JH, Gamsu G, Herold CJ, Jett JR, Naidich DP, et al. Guidelines for management of small pulmonary nodules detected on CT scans: a statement from the Fleischner Society. Radiology. 2005 Nov;237(2):395-400. | CrossRef | PubMed | Revel MP, Merlin A, Peyrard S, Triki R, Couchon S, Chatellier G, et al. Software volumetric evaluation of doubling times for differentiating benign versus malignant pulmonary nodules. AJR Am J Roentgenol. 2006 Jul;187(1):135-42. | CrossRef | PubMed |
Revel MP, Merlin A, Peyrard S, Triki R, Couchon S, Chatellier G, et al. Software volumetric evaluation of doubling times for differentiating benign versus malignant pulmonary nodules. AJR Am J Roentgenol. 2006 Jul;187(1):135-42. | CrossRef | PubMed | Jennings SG, Winer-Muram HT, Tann M, Ying J, Dowdeswell I. Distribution of stage I lung cancer growth rates determined with serial volumetric CT measurements. Radiology. 2006 Nov;241(2):554-63. Epub 2006 Sep 27. | CrossRef | PubMed |
Jennings SG, Winer-Muram HT, Tann M, Ying J, Dowdeswell I. Distribution of stage I lung cancer growth rates determined with serial volumetric CT measurements. Radiology. 2006 Nov;241(2):554-63. Epub 2006 Sep 27. | CrossRef | PubMed | Swensen SJ, Viggiano RW, Midthun DE, M³ller NL, Sherrick A, Yamashita K, et al. Lung nodule enhancement at CT: multicenter study. Radiology. 2000 Jan;214(1):73-80. | PubMed |
Swensen SJ, Viggiano RW, Midthun DE, M³ller NL, Sherrick A, Yamashita K, et al. Lung nodule enhancement at CT: multicenter study. Radiology. 2000 Jan;214(1):73-80. | PubMed |