 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada durante el Simposio Sevoflurano organizado por Abbott Laboratories durante el XXX Congreso Chileno de AnestesiologĒa y VI Simposio Latinoamericano de Anestesia Regional, en noviembre de 2002.
Sevoflurano es un anestķsico de baja solubilidad sangre/gas lo que ha demostrado, desde el inicio de su uso en clĒnica, que se asocia con recuperaci¾n rßpida, mayor que la de cualquier agente endovenoso. La experiencia acumulada y la continua investigaci¾n clĒnica y de laboratorio ense±an hoy dĒa otras ventajas del agente. De este modo, un conocimiento actualizado de los anestķsicos lleva a la necesidad de familiarizarse con la particular farmacocinķtica de este agente y las ventajas que puede entregar en clĒnica; se revisarß entonces el concepto y la aplicaci¾n del bolo inhalatorio. Igualmente, resulta necesario conocer aspectos novedosos de la farmacodinamia del agente. Por este motivo, se verßn los efectos de sevoflurano en hemodinamia cerebral y las evidencias que se han conocido sobre su efecto citoprotector y el concepto de preacondicionamiento.
Es importante conocer el efecto farmacol¾gico de los anestķsicos en el flujo sanguĒneo cerebral. Se ha demostrado que con sevoflurano este flujo se mantiene constante; en cambio, con desflurano aumenta, lo mismo que la frecuencia cardĒaca y la presi¾n arterial. Tambiķn se ha visto que la pķrdida de la autorregulaci¾n cerebral se produce con menores concentraciones, en relaci¾n a lo que ocurre con sevoflurano (Figura 1).
El halotano se utiliza mucho todavĒa, debido al buen efecto que tiene en la vĒa aķrea; sin embargo, produce mayor depresi¾n cardiovascular que otros agentes disponibles. Esto se ha demostrado en varios estudios; en uno de ellos se analiz¾ la evoluci¾n de la presi¾n arterial sist¾lica y se observ¾ que el grupo con halotano presentaba menor frecuencia cardĒaca y menor presi¾n arterial que el de sevoflurano. Lo anterior tiene particular importancia en ni±os; a ellos no se les puede administrar grandes dosis de halotano, porque se producirĒa un importante descenso de la presi¾n arterial.
Este tema es nuevo en la farmacologĒa de los agentes anestķsicos volßtiles. En animales de laboratorio, se habla de preacondicionamiento isquķmico cuando se inducen breves perĒodos de isquemia, con el fin de aumentar la capacidad del miocardio para resistir episodios mßs prolongados. El preacondicionamiento se asocia con una menor cantidad de miocardio infartado, menor disfunci¾n mecßnica y menor incidencia de anomalĒas ultraestructurales despuķs de la reperfusi¾n, o sea, despuķs de desaparecer la isquemia.
El preacondicionamiento con anestķsicos volßtiles (APC) es un fen¾meno similar, pero en este caso se utiliza un anestķsico en vez de un episodio isquķmico. Se cree que ambos tipos de preacondicionamiento (anestķsico e isquķmico) se deben a la activaci¾n de canales de potasio, ATP dependientes, de modo que las drogas que afectan estos canales tambiķn act·an sobre el fen¾meno protector.
Muchos estudios demuestran la utilidad del preacondicionamiento anestķsico en animales. En seres humanos s¾lo hay informaci¾n preliminar debida a un trabajo muy reciente que se realiz¾ en 20 pacientes con indicaci¾n de by-pass coronario. Se dividieron en dos grupos: uno recibi¾ infusi¾n continua de propofol, en dosis de 2 a 4 mg/ml y el otro sevoflurano al 8%, ajustado para inducci¾n y, posteriormente, para mantenimiento. Ambos grupos recibieron remifentanilo en un bolo y luego en infusi¾n. Los grupos fueron similares en cuanto a la fracci¾n de eyecci¾n preoperatoria, la duraci¾n de la cirugĒa, el cross clamp quir·rgico y el tiempo de by-pass (2).
Se monitoriz¾ la presi¾n de la arteria pulmonar, el gasto cardiaco y la respuesta del ventrĒculo izquierdo a la elevaci¾n de las extremidades inferiores, maniobra que lleva la sangre hacia el sistema circulatorio central. La frecuencia cardĒaca se mantuvo constante con un marcapaso.
Despuķs del by-pass, se observ¾ que en el grupo con propofol las cifras de presi¾n arterial media, fracci¾n de eyecci¾n y presi¾n mßxima del ventrĒculo izquierdo, que reflejan el estado de la funci¾n cardĒaca, fueron siempre inferiores a las cifras basales, o sea, la funci¾n qued¾ da±ada por el by-pass realizado en el grupo con este medicamento. En cambio, en el grupo con sevoflurano el da±o fue menor, ya que la presi¾n arterial, la fracci¾n de eyecci¾n y la presi¾n generada fueron mayores y la contractilidad estuvo casi en rango normal. Este resultado fue significativamente mejor que el observado con propofol.
Tambiķn se midi¾ la troponina cardĒaca durante 36 horas en el postoperatorio, como un indicador de da±o cardĒaco. En el grupo con propofol, todos los pacientes tuvieron valores elevados a las horas medidas (12, 24, 36 horas) y alcanzaron el mayor nivel a las 24 horas. El grupo con sevoflurano tuvo, en todo momento, valores menores. Esto quiere decir que el acondicionamiento sĒ ocurrirĒa, aunque no con propofol, ya que es un efecto propio de los anestķsicos volßtiles; en este grupo, todos los pacientes tuvieron concentraciones de troponina por sobre el punto de corte de 2 ng/ml (Figura 2).
El sevoflurano es una droga de baja solubilidad en sangre. Resulta de interķs conocer los estudios que, de manera mßs cientĒfica, eval·an la acci¾n farmacol¾gica y la farmacodinamia de los agentes volßtiles y su impacto en el manejo clĒnico.
Los anestķsicos deben actuar en dos lugares: en la mķdula espinal, que tiene relaci¾n con la percepci¾n del dolor y con la motilidad, y en el cerebro, por su relaci¾n con el ciclo de vigilia/somnolencia (Figura 3).
Figura 3. Sitios de acci¾n de los anestķsicos volßtiles.
Generalmente, la profundidad anestķsica se eval·a mediante la MAC, (minimum alveolar concentration), aunque no estß claro lo que este parßmetro refleja. En estudios recientes se han descrito cambios en ciertos parßmetros electroencefalogrßficos como el SEF90 (spectral edge frequency 90) y lentitud de ondas cerebrales en respuesta a los anestķsicos volßtiles.
La evaluaci¾n del ritmo mßs lento del EEG permite calcular el tiempo medio de llegada al sitio afectado, o sea, el tiempo que tarda el fßrmaco en llegar al cerebro propiamente tal. El gas espirado se mide en la vĒa aķrea, pero la acci¾n del anestķsico no se produce en ella sino en el sistema nervioso central. El tiempo medio de equilibrio del sevoflurano es de 2,4 minutos y en todos los agentes volßtiles es de dos a tres minutos. Esto significa que un cambio instantßneo de la concentraci¾n de sevoflurano en la vĒa aķrea causarß, 2,4 minutos mßs tarde, un cambio en la concentraci¾n de sevoflurano en el cerebro (3).
El tiempo de respuesta del sevoflurano es graduable. Se recomienda titular la concentraci¾n de las drogas volßtiles y endovenosas, logrando una sobrepresi¾n alveolar, entregando mßs de lo necesario, de modo que el efecto total se obtendrß a los 2,4 minutos, pero se iniciarß antes. El promedio de la poblaci¾n para que el EEG sea mßs lento se denomina AC-50 y se correlaciona con el Ēndice MAC al despertar, que es de 0,6 con sevoflurano y 0,4 con isoflurano.
El MAC al despertar o MAC en la pķrdida de conciencia es la concentraci¾n que se debe alcanzar en el cerebro para que el paciente pase de despierto a dormido o de dormido a despierto. Si se aumenta la concentraci¾n de sevoflurano, deberßn pasar 2,4 minutos para que el sevoflurano al 8% llegue al cerebro, pero el paciente se dormirß cuando en el cerebro se alcance en promedio 0,6% MAC, es decir 1,2%. Esto explica por quķ se quedan dormidos tan rßpidamente.
En un estudio en el que se compar¾ la inducci¾n inhalatoria a capacidad vital con sevoflurano con inducci¾n endovenosa con propofol, los pacientes fueron asignados al azar para recibir 8% de sevoflurano en 75% de N2O/O2 desde un circuito preparado (32 pacientes) o propofol en un bolo de 2 mg/kg (24 pacientes). Se observ¾ que los pacientes que inspiraron un gran bolo de sevoflurano al 8% perdieron la conciencia en 40 segundos, que es el tiempo tĒpico. Los pacientes que tomaron dos a tres inspiraciones se durmieron poco despuķs de transcurrido un minuto. El tiempo promedio de pķrdida de conciencia fue de 50 segundos en el grupo con sevoflurano y mßs largo en el grupo con propofol, debido, por una parte, a que el efecto de ķste depende de la velocidad del goteo endovenoso y, por otra, a la sobrepresi¾n lograda con el inhalatorio(4) (Figura 4).
El sevoflurano se puede administrar sin problemas a cuatro MAC, o sea, a cuatro veces la concentraci¾n anestķsica, pero si se hace lo mismo con propofol y se aumenta la dosis a 8 mg/kg, el paciente se dormirß muy rßpidamente, pero con una severa repercusi¾n hemodinßmica.
Es la aplicaci¾n prßctica del tiempo medio de efecto y de la cinķtica farmacol¾gica. Con respecto a la aplicaci¾n prßctica del Ēndice MAC al despertar y los tiempos medios de la recuperaci¾n; al comparar sevoflurano e isoflurano se pudo ver que, despuķs de una hora de anestesia, los tiempos de despertar (apertura de ojos, respuesta a instrucciones) son mßs lentos con la droga mßs soluble y la diferencia persiste despuķs de una hora, pues los pacientes del grupo isoflurano tardaron mßs en sentarse sin nßuseas ni mareos.(5) (Figura 5).
Otro concepto errado es que los agentes de baja solubilidad se necesitan s¾lo en casos de cirugĒa de corta duraci¾n. En casos mßs largos, con MAC de 2,5 horas, el tiempo de salida es de 10 minutos. Cuanto mßs larga la operaci¾n o mßs prolongada la anestesia, mßs importante es usar agentes de baja solubilidad para el despertar del paciente.
El propofol es popular por varias razones, pero, igual que todas las demßs drogas, no es una droga perfecta. Uno de sus problemas es que la recuperaci¾n no es muy buena, salvo si se utiliza en peque±a cantidad.
En un estudio dise±ado para comparar la recuperaci¾n con agentes volßtiles nuevos (sevoflurano, desflurano) y la infusi¾n de propofol para mantenimiento, mediante el puntaje de recuperaci¾n modificado de Aldrete, se comprob¾ que, despuķs de una hora de anestesia, en el grupo con propofol la recuperaci¾n fue mßs lenta para despertar, lograr orientaci¾n y alcanzar un mayor puntaje de recuperaci¾n. Ademßs, el propofol disminuy¾ las nßuseas y v¾mitos, pero no los elimin¾ y se encontr¾ una incidencia de 10%. La diferencia entre sevoflurano (20%) y desflurano (30%) no fue significativa, pero casi todos los estudios demuestran que con este ·ltimo se producen mßs v¾mitos, seguramente por activaci¾n simpßtica (6).
El propofol no es un agente de acci¾n corta, como se cree por lo general. Esto queda claro al analizar el tiempo medio sensible al contexto de opioides e hipn¾ticos; se ubica en el eje vertical el tiempo necesario para que disminuya la concentraci¾n sanguĒnea y, en el eje horizontal, la duraci¾n de la infusi¾n. El tiempo medio sensible al contexto indica que la recuperaci¾n depende no s¾lo de la profundidad de la anestesia, sino tambiķn de su duraci¾n, es decir, del tiempo de exposici¾n (Figura 6).
Se sabe que la infusi¾n de fentanilo no es satisfactoria, especialmente en las cirugĒas ambulatorias, porque la recuperaci¾n puede alargarse mucho. Sin embargo, la curva de propofol es idķntica a la de sufentanilo y, a pesar de eso, los colegas, en su mayorĒa, no utilizarĒan una infusi¾n de sufentanilo como anestesia principal en una cirugĒa ambulatoria, porque saben que la recuperaci¾n es muy lenta. Lo que ocurre es que, cuando se administra una cantidad peque±a de propofol, el efecto desaparece rßpidamente por redistribuci¾n, pero, si se utilizan dosis mayores o por mßs tiempo, el efecto pasa a depender del metabolismo farmacol¾gico, que con propofol no es muy bueno. Se desprende, pues, que este medicamento es bueno en dosis bajas, por tiempos cortos, pero no para usos prolongados (7).
En un estudio realizado en pacientes ambulatorios, evaluamos la combinaci¾n de remifentanilo con propofol o alfentanilo con propofol, que es el ·nico opioide que se puede usar en infusi¾n, y observamos que el remifentanilo es muy bueno para obtener una anestesia estable. El problema de este anestķsico es el control del dolor, porque le queda poco efecto narc¾tico restante para el dolor postoperatorio, de modo que se debe aplicar otro tipo de manejo del dolor antes de que el paciente despierte. Nosotros no lo hicimos asĒ, porque nuestra agencia reguladora nos pidi¾ que no lo hiciķramos. Estos pacientes no recibieron anestesia de reemplazo y se necesit¾ medicaci¾n para el dolor muy pronto, lo que prolong¾ la estadĒa en la sala de recuperaci¾n durante 20 minutos mßs para obtener buen control del dolor. Por lo tanto, para asegurar una buena recuperaci¾n con remifentanilo es necesario tomar en cuenta el manejo del dolor.

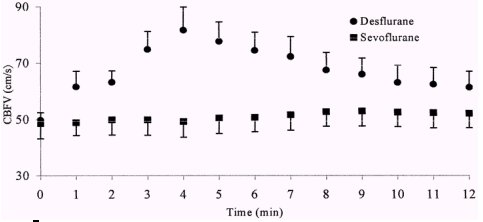 Figura 1. Velocidad Flujo Sanguineo Cerebral (CBFV) luego de la introducci¾n de desflurano y sevoflurano al Tiempo 0 (Nive l concentraci¾n alveolar mĒnima (MAC) y el aumento al Tiempo 2 P < 0,01. From: Bedforth: Anesth Analg, Volume 91(1). July 2000.1
Figura 1. Velocidad Flujo Sanguineo Cerebral (CBFV) luego de la introducci¾n de desflurano y sevoflurano al Tiempo 0 (Nive l concentraci¾n alveolar mĒnima (MAC) y el aumento al Tiempo 2 P < 0,01. From: Bedforth: Anesth Analg, Volume 91(1). July 2000.1

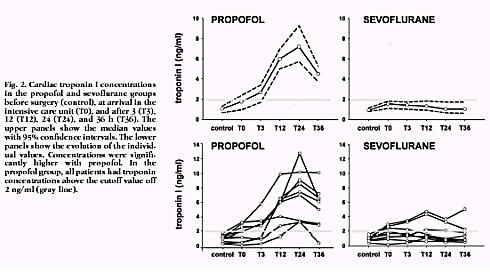 Figura 2. Concentraciones de troponina 1 en los grupos de propofol y sevoflurano antes de la cirugĒa (control), a la llegada a la unidad de cuidados intensivos (T0), y despuķs de 3 (T3), 12 (T12), 24 (T24) y 36 horas(T36). Las imßgenes superiores mues
Figura 2. Concentraciones de troponina 1 en los grupos de propofol y sevoflurano antes de la cirugĒa (control), a la llegada a la unidad de cuidados intensivos (T0), y despuķs de 3 (T3), 12 (T12), 24 (T24) y 36 horas(T36). Las imßgenes superiores mues

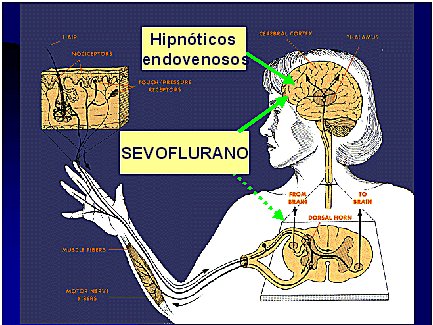 Figura 3. Sitios de acci¾n de los anestķsicos volßtiles.
Figura 3. Sitios de acci¾n de los anestķsicos volßtiles.

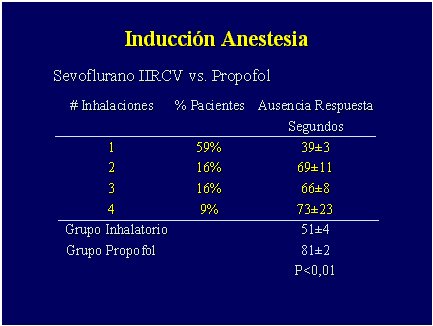 Figura 4.
Figura 4.

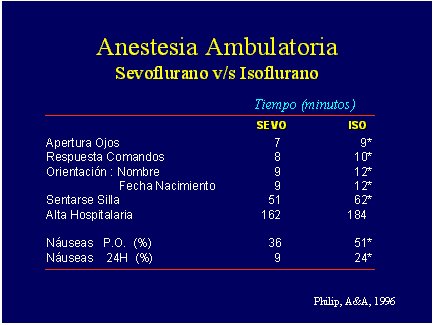 Figura 5.
Figura 5.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada durante el Simposio Sevoflurano organizado por Abbott Laboratories durante el XXX Congreso Chileno de AnestesiologĒa y VI Simposio Latinoamericano de Anestesia Regional, en noviembre de 2002.
 Expositora:
Beverly Philip[1]
Expositora:
Beverly Philip[1]

Citaci¾n: Philip B. Sevoflurane Symposium I. Medwave 2003 Ene;3(1):e1670 doi: 10.5867/medwave.2003.01.1670
Fecha de publicaci¾n: 1/1/2003

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Bedforth NM, Hardman JG, Nathanson MH. Cerebral Hemodynamic Response to the Introduction of Desflurane: A Comparison with Sevoflurane. Anesth Analg. 2000 Jul;91(1):152-5. | PubMed |
Bedforth NM, Hardman JG, Nathanson MH. Cerebral Hemodynamic Response to the Introduction of Desflurane: A Comparison with Sevoflurane. Anesth Analg. 2000 Jul;91(1):152-5. | PubMed | De Hert SG, ten Broecke PW, Mertens E, Van Sommeren EW, De Blier IG, Stockman BA,et al Sevoflurane but not Propofol Preserves Myocardial Function in Coronary Surgery Patients. Anesthesiology 2002 Jul;97(1):42-9. | CrossRef | PubMed |
De Hert SG, ten Broecke PW, Mertens E, Van Sommeren EW, De Blier IG, Stockman BA,et al Sevoflurane but not Propofol Preserves Myocardial Function in Coronary Surgery Patients. Anesthesiology 2002 Jul;97(1):42-9. | CrossRef | PubMed | Bailey J. Context-Sensitive Half-Times and Other Decrement Times of Inhaled Anesthetics. Anesth Analg. 1997 Sep;85(3):681-6. | PubMed |
Bailey J. Context-Sensitive Half-Times and Other Decrement Times of Inhaled Anesthetics. Anesth Analg. 1997 Sep;85(3):681-6. | PubMed | Philip BK, Lombard LL, Roaf ER, Drager LR, Calalang I, Philip JH. Comparison of Vital Capacity Induction with Sevoflurane to Intravenous Induction with Propofol for Adult Ambulatory Anesthesia. Anesth Analg 1999 Sep;89(3):623-7. | PubMed |
Philip BK, Lombard LL, Roaf ER, Drager LR, Calalang I, Philip JH. Comparison of Vital Capacity Induction with Sevoflurane to Intravenous Induction with Propofol for Adult Ambulatory Anesthesia. Anesth Analg 1999 Sep;89(3):623-7. | PubMed | Philip BK, Kallar SK, Bogetz MS, Scheller MS, Wetchler BV. A Multicenter Comparison of Maintenance and Recovery with Sevoflurane or Isoflurane for Adult Ambulatory Anesthesia. Anesth Analg. 1996 Aug;83(2):314-9. | PubMed |
Philip BK, Kallar SK, Bogetz MS, Scheller MS, Wetchler BV. A Multicenter Comparison of Maintenance and Recovery with Sevoflurane or Isoflurane for Adult Ambulatory Anesthesia. Anesth Analg. 1996 Aug;83(2):314-9. | PubMed | Song D, Joshi GP, White PF. Fast-track Elegibility after Ambulatory Anesthesia: a Comparison of Desflurane, Sevoflurane and Propofol. Anesth Analg. 1998 Feb;86(2):267-73. | PubMed |
Song D, Joshi GP, White PF. Fast-track Elegibility after Ambulatory Anesthesia: a Comparison of Desflurane, Sevoflurane and Propofol. Anesth Analg. 1998 Feb;86(2):267-73. | PubMed |