 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Palabras clave: vaccine, chickenpox, varicella, Epistemonikos, GRADE.
INTRODUCCIėN
La varicela es una enfermedad infectocontagiosa producida por el virus varicela-z¾ster. Para su prevenci¾n, convencionalmente se utiliza la vacuna varicela, cuya administraci¾n busca disminuir la aparici¾n de enfermedad y sus complicaciones. Sin embargo, a·n existe controversia sobre la efectividad.
M╔TODOS
Realizamos una b·squeda en Epistemonikos, la mayor base de datos de revisiones sistemßticas en salud, la cual es mantenida mediante el cribado de m·ltiples fuentes de informaci¾n, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, analizamos los datos de los estudios primarios, realizamos un metanßlisis y preparamos una tabla de resumen de los resultados utilizando el mķtodo GRADE.
RESULTADOS Y CONCLUSIONES
Se identificaron dos revisiones sistemßticas que en conjunto incluyeron 16 estudios primarios, de los cuales, tres corresponden a ensayos aleatorizados. Concluimos que la vacunaci¾n contra la varicela disminuye el riesgo de contraer la enfermedad a largo plazo en pacientes sanos sin exposici¾n previa y que probablemente disminuye el riesgo de contraer la enfermedad a corto plazo. Sin embargo, aumenta la reacci¾n local 48 horas posterior a su administraci¾n y probablemente aumenta la aparici¾n de fiebre y varicela-like rash.
La varicela es una enfermedad infectocontagiosa producida por el virus varicela-zóster. La mayoría de los casos ocurren en la niñez (menores de 14 años), siendo una causa importante de ausentismo escolar y generando gastos importantes a la comunidad [1], [2]. El diagnóstico de la varicela es clínico, caracterizándose por presentar exantema vesicular polimorfo céfalo-caudal pruriginoso, con compromiso de cuero cabelludo, asociándose a fiebre en la mayoría de los casos.
Para su prevención convencionalmente se utiliza la vacuna varicela, la cual es de tipo virus vivo atenuado que induce respuesta inmune humoral. Su administración permitiría prevenir la aparición de enfermedad y sus complicaciones. Sin embargo, aún existe controversia sobre la efectividad de la vacuna para disminuir la incidencia de la enfermedad a corto y largo plazo.
|
Mensajes clave
|
|
Cuál es la evidencia |
Se encontraron dos revisiones sistemáticas [3], [4], que incluyeron 16 estudios primarios reportados en 17 referencias [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16], [17], [18], [19], [20], [21], de los cuales dos corresponden a ensayos aleatorizados reportados en tres referencias [19], [20], [21]. Esta tabla y el resumen en general se basan en estos últimos, dado que los estudios observacionales no aumentaban la certeza de la evidencia existente, ni entregaban información adicional relevante. |
|
Qué tipo de pacientes incluyeron los estudios* |
En todos los ensayos se incluyeron pacientes sanos, sin historia de varicela ni vacunación contra la enfermedad. Un ensayo incluyó pacientes entre uno y 14 años de edad [20], mientras que el otro ensayo incluyó pacientes de 10 a 30 meses [21]. |
|
Qué tipo de intervenciones incluyeron los estudios* |
En todos los ensayos se administró una dosis de vacuna varicela de la cepa Oka [20],[21]. Ambos ensayos evaluaron vacuna varicela en comparación a grupo control no vacunado [20], [21]. Además, uno de los ensayos incluyó una comparación sin seguimiento del grupo control [20], por lo que en este resumen los autores decidieron evaluarlo asumiendo el peor de los casos (worst-case scenario), es decir, que ningún paciente no vacunado desarrolle varicela en los años de seguimiento. |
|
Qué tipo de desenlaces midieron |
Los ensayos reportaron múltiples desenlaces, los cuales fueron agrupados por las revisiones sistemáticas de la siguiente manera:
|
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario
La información sobre los efectos de vacuna varicela está basada en dos ensayos aleatorizados que incluyeron 1449 pacientes.
Dos ensayos midieron los desenlaces contraer varicela a corto plazo y varicela-like rash (1407 pacientes) [20], [21]. Uno de los ensayos midió los desenlaces contraer varicela a largo plazo, fiebre y reacción local (914 pacientes) [20]. Ningún ensayo reportó el desenlace varicela severa o complicada.
El resumen de los resultados es el siguiente:
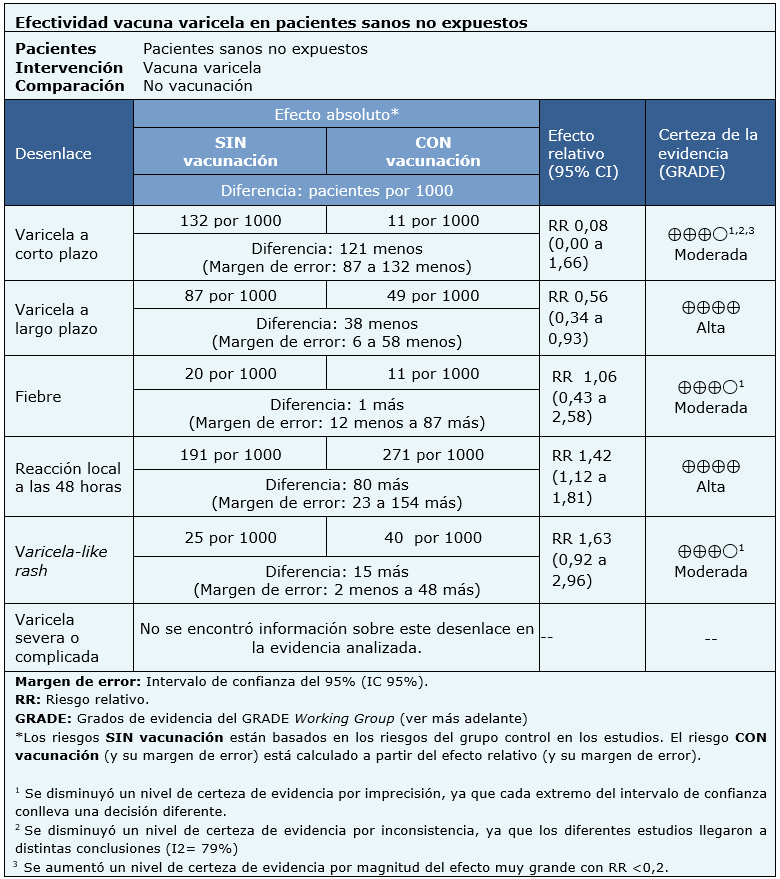
| Siga el enlace para acceder a la versión interactiva de esta tabla (Interactive Summary of Findings - iSoF) |
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés la presentamos en una matriz de evidencia.

Siga el enlace para acceder a la versión interactiva: Efectividad vacuna varicela en pacientes sanos no expuestos.
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículos.
Las conclusiones de este resumen son aplicables a niños y adultos mayores, y se considera que también pueden ser extrapolables a la población general.
La evidencia presentada en este resumen no debería extrapolarse a participantes alérgicos a componentes de la vacuna contra influenza.
Estas conclusiones pueden aplicarse a cualquier tipo de recordatorios enviados más de una vez, en distintos tiempos, combinados o no con una postal.
La evidencia presentada se aplica a niños y adolescentes sanos no expuestos a la enfermedad varicela.
No se aplica a pacientes expuestos o inmunosuprimidos, con exclusión directa de éstos en los ensayos clínicos. Estos pacientes podrían presentar desenlaces clínicos distintos a los descritos, lo cual estaría determinado por variaciones en la respuesta inmune generada por su organismo ante la vacuna.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

INTRODUCTION
Chickenpox is an infectious disease caused by varicella-zoster virus. Varicella vaccine is conventionally used for its prevention, and its administration seeks to reduce the onset of the disease and complications associated. However, there is still controversy about its effectiveness.
METHODS
We searched in Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified two systematic reviews including 16 studies overall, of which three were randomized trials. We concluded that the varicella vaccine decreases the risk of contracting the disease in the long term and probably reduces the risk of developing the disease in the short term in healthy unexposed patients. Nevertheless, the vaccination increases the occurrence of local reactions 48 hours after its administration and probably increases the presence of fever and chickenpox-like rash.
 Autores:
MarĒa Catalina Castro[1,2], Pamela Rojas[2,3]
Autores:
MarĒa Catalina Castro[1,2], Pamela Rojas[2,3]

Citaci¾n: Castro M, Rojas P. Preventive effectiveness of varicella vaccine in healthy unexposed patients. Medwave 2020;20(06):e7982 doi: 10.5867/medwave.2020.06.7982
Fecha de envĒo: 23/5/2019
Fecha de aceptaci¾n: 28/11/2019
Fecha de publicaci¾n: 30/7/2020
Origen: Este artĒculo es producto del Epistemonikos Evidence Synthesis Project de la Fundaci¾n Epistemonikos, en colaboraci¾n con Medwave para su publicaci¾n.
Tipo de revisi¾n: Con revisi¾n por pares sin ciego por parte del equipo metodol¾gico del Centro Evidencia UC en colaboraci¾n con Epistemonikos Evidence Synthesis Project.

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Choo P, Donahue J, Manson J, Platt R. The Epidemiology of Varicella and Its Complications. Journal of Infectious Diseases. 1995;172(3):706-712.
Choo P, Donahue J, Manson J, Platt R. The Epidemiology of Varicella and Its Complications. Journal of Infectious Diseases. 1995;172(3):706-712.  Yawn B, Yawn R, Lydick E. Community impact of childhood varicella infections. The Journal of Pediatrics. 1997;130(5):759-765.
Yawn B, Yawn R, Lydick E. Community impact of childhood varicella infections. The Journal of Pediatrics. 1997;130(5):759-765.  Bayer O, Heininger U, Heiligensetzer C, von Kries R. Metaanalysis of vaccine effectiveness in varicella outbreaks. Vaccine. 2007;25(37-38):6655-60.
Bayer O, Heininger U, Heiligensetzer C, von Kries R. Metaanalysis of vaccine effectiveness in varicella outbreaks. Vaccine. 2007;25(37-38):6655-60.  Skull SA, Wang EE. Varicella vaccination--a critical review of the evidence. Archives of disease in childhood. 2001;85(2):83-90.
Skull SA, Wang EE. Varicella vaccination--a critical review of the evidence. Archives of disease in childhood. 2001;85(2):83-90.  Galil K, Fair E, Mountcastle N, Britz P, Seward J. Younger age at vaccination may increase risk of varicella vaccine failure. The Journal of infectious diseases. 2002;186(1):102-5.
Galil K, Fair E, Mountcastle N, Britz P, Seward J. Younger age at vaccination may increase risk of varicella vaccine failure. The Journal of infectious diseases. 2002;186(1):102-5.  Dworkin MS, Jennings CE, Roth-Thomas J, Lang JE, Stukenberg C, Lumpkin JR. An Outbreak of Varicella among children attending preschool and elementary school in Illinois. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 2002;35(1):102-4.
Dworkin MS, Jennings CE, Roth-Thomas J, Lang JE, Stukenberg C, Lumpkin JR. An Outbreak of Varicella among children attending preschool and elementary school in Illinois. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 2002;35(1):102-4.  Miron D, Lavi I, Kitov R, Hendler A. Vaccine effectiveness and severity of varicella among previously vaccinated children during outbreaks in day-care centers with low vaccination coverage. The Pediatric infectious disease journal. 2005;24(3):233-6.
Miron D, Lavi I, Kitov R, Hendler A. Vaccine effectiveness and severity of varicella among previously vaccinated children during outbreaks in day-care centers with low vaccination coverage. The Pediatric infectious disease journal. 2005;24(3):233-6.  Lopez AS, Guris D, Zimmerman L, et al.. One dose of varicella vaccine does not prevent school outbreaks: is it time for a second dose?. Pediatrics. 2006;117(6)(Available at: www. pediatrics. org/ cgi/ content/ full/ 117/ 6/ e1070).
Lopez AS, Guris D, Zimmerman L, et al.. One dose of varicella vaccine does not prevent school outbreaks: is it time for a second dose?. Pediatrics. 2006;117(6)(Available at: www. pediatrics. org/ cgi/ content/ full/ 117/ 6/ e1070).  Centers for Disease Control and Prevention (CDC). Outbreak of varicella among vaccinated children--Michigan, 2003. MMWR. Morbidity and mortality weekly report. 2004;53(18):389-92.
Centers for Disease Control and Prevention (CDC). Outbreak of varicella among vaccinated children--Michigan, 2003. MMWR. Morbidity and mortality weekly report. 2004;53(18):389-92.  Centers for Disease Control and Prevention (CDC). Varicella outbreak among vaccinated childrenŚ Nebraska, 2004. MMWR Morb Mortal Wkly. 2006;55(27):749¢752.
Centers for Disease Control and Prevention (CDC). Varicella outbreak among vaccinated childrenŚ Nebraska, 2004. MMWR Morb Mortal Wkly. 2006;55(27):749¢752.  Galil K, Lee B, Strine T, Carraher C, Baughman AL, Eaton M, Montero J, Seward J. Outbreak of varicella at a day-care center despite vaccination. The New England journal of medicine. 2002;347(24):1909-15.
Galil K, Lee B, Strine T, Carraher C, Baughman AL, Eaton M, Montero J, Seward J. Outbreak of varicella at a day-care center despite vaccination. The New England journal of medicine. 2002;347(24):1909-15.  Tugwell BD, Lee LE, Gillette H, Lorber EM, Hedberg K, Cieslak PR. Chickenpox outbreak in a highly vaccinated school population. Pediatrics. 2004;113(3 Pt 1):455-9.
Tugwell BD, Lee LE, Gillette H, Lorber EM, Hedberg K, Cieslak PR. Chickenpox outbreak in a highly vaccinated school population. Pediatrics. 2004;113(3 Pt 1):455-9.  Arnedo-Pena A, Puig-BarberÓ J, Aznar-Orenga MA, Ballester-Albiol M, Pardo-Serrano F, Bellido-Blasco JB, Romeu-GarcĒa MA. Varicella vaccine effectiveness during an outbreak in a partially vaccinated population in Spain. The Pediatric infectious disease journal. 2006;25(9):774-8.
Arnedo-Pena A, Puig-BarberÓ J, Aznar-Orenga MA, Ballester-Albiol M, Pardo-Serrano F, Bellido-Blasco JB, Romeu-GarcĒa MA. Varicella vaccine effectiveness during an outbreak in a partially vaccinated population in Spain. The Pediatric infectious disease journal. 2006;25(9):774-8.  Izurieta HS, Strebel PM, Blake PA. Postlicensure effectiveness of varicella vaccine during an outbreak in a child care center. JAMA. 1997;278(18):1495-9.
Izurieta HS, Strebel PM, Blake PA. Postlicensure effectiveness of varicella vaccine during an outbreak in a child care center. JAMA. 1997;278(18):1495-9.  Buchholz U, Moolenaar R, Peterson C, Mascola L. Varicella outbreaks after vaccine licensure: should they make you chicken?. Pediatrics. 1999;104(3 Pt 1):561-3.
Buchholz U, Moolenaar R, Peterson C, Mascola L. Varicella outbreaks after vaccine licensure: should they make you chicken?. Pediatrics. 1999;104(3 Pt 1):561-3.  Marin M, Nguyen HQ, Keen J, Jumaan AO, Mellen PM, Hayes EB, Gensheimer KF, Gunderman-King J, Seward JF. Importance of catch-up vaccination: experience from a varicella outbreak, Maine, 2002-2003. Pediatrics. 2005;115(4):900-5.
Marin M, Nguyen HQ, Keen J, Jumaan AO, Mellen PM, Hayes EB, Gensheimer KF, Gunderman-King J, Seward JF. Importance of catch-up vaccination: experience from a varicella outbreak, Maine, 2002-2003. Pediatrics. 2005;115(4):900-5.  Lee BR, Feaver SL, Miller CA, Hedberg CW, Ehresmann KR. An elementary school outbreak of varicella attributed to vaccine failure: policy implications. The Journal of infectious diseases. 2004;190(3):477-83.
Lee BR, Feaver SL, Miller CA, Hedberg CW, Ehresmann KR. An elementary school outbreak of varicella attributed to vaccine failure: policy implications. The Journal of infectious diseases. 2004;190(3):477-83.  Haddad MB, Hill MB, Pavia AT, Green CE, Jumaan AO, De AK, Rolfs RT. Vaccine effectiveness during a varicella outbreak among schoolchildren: Utah, 2002-2003. Pediatrics. 2005;115(6):1488-93.
Haddad MB, Hill MB, Pavia AT, Green CE, Jumaan AO, De AK, Rolfs RT. Vaccine effectiveness during a varicella outbreak among schoolchildren: Utah, 2002-2003. Pediatrics. 2005;115(6):1488-93.  Kuter BJ, Weibel RE, Guess HA, Matthews H, Morton DH, Neff BJ, Provost PJ, Watson BA, Starr SE, Plotkin SA. Oka/Merck varicella vaccine in healthy children: final report of a 2-year efficacy study and 7-year follow-up studies. Vaccine. 1991;9(9):643-7.
Kuter BJ, Weibel RE, Guess HA, Matthews H, Morton DH, Neff BJ, Provost PJ, Watson BA, Starr SE, Plotkin SA. Oka/Merck varicella vaccine in healthy children: final report of a 2-year efficacy study and 7-year follow-up studies. Vaccine. 1991;9(9):643-7.  Weibel RE, Neff BJ, Kuter BJ, Guess HA, Rothenberger CA, Fitzgerald AJ, Connor KA, McLean AA, Hilleman MR, Buynak EB. Live attenuated varicella virus vaccine. Efficacy trial in healthy children. The New England journal of medicine. 1984;310(22):1409-15.
Weibel RE, Neff BJ, Kuter BJ, Guess HA, Rothenberger CA, Fitzgerald AJ, Connor KA, McLean AA, Hilleman MR, Buynak EB. Live attenuated varicella virus vaccine. Efficacy trial in healthy children. The New England journal of medicine. 1984;310(22):1409-15.  Varis T, Vesikari T. Efficacy of high-titer live attenuated varicella vaccine in healthy young children. The Journal of infectious diseases. 1996;174 Suppl 3:S330-4.
Varis T, Vesikari T. Efficacy of high-titer live attenuated varicella vaccine in healthy young children. The Journal of infectious diseases. 1996;174 Suppl 3:S330-4.  Cortķs I, Pķrez-Camarero S, Del Llano J, Pe±a LM, Hidalgo-Vega A. Systematic review of economic evaluation analyses of available vaccines in Spain from 1990 to 2012. Vaccine. 2013;31(35):3473-84.
Cortķs I, Pķrez-Camarero S, Del Llano J, Pe±a LM, Hidalgo-Vega A. Systematic review of economic evaluation analyses of available vaccines in Spain from 1990 to 2012. Vaccine. 2013;31(35):3473-84.  Unim B, Saulle R, Boccalini S, Taddei C, Ceccherini V, Boccia A, Bonanni P, La Torre G. Economic evaluation of Varicella vaccination: results of a systematic review. Human vaccines & immunotherapeutics. 2013;9(9):1932-42.
Unim B, Saulle R, Boccalini S, Taddei C, Ceccherini V, Boccia A, Bonanni P, La Torre G. Economic evaluation of Varicella vaccination: results of a systematic review. Human vaccines & immunotherapeutics. 2013;9(9):1932-42.  Prevention of Varicella: Recommendations of the Advisory Committee on Immunization Practices (ACIP) [Internet]. Cdc.gov. 2019 [cited 22 March 2019]. | Link |
Prevention of Varicella: Recommendations of the Advisory Committee on Immunization Practices (ACIP) [Internet]. Cdc.gov. 2019 [cited 22 March 2019]. | Link |