 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
INTRODUCCIėN
La artritis psorißsica es una artritis inflamatoria sin una clara etiologĒa, con el tratamiento biol¾gico como un pilar fundamental en pacientes mßs complejos. Existen varias alternativas para tratamiento biol¾gico, debido a su alto costo, es importante evaluar la real efectividad de estos para un buen tratamiento.
M╔TODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemßticas en salud a nivel mundial, la cual es mantenida mediante b·squedas en m·ltiples fuentes de informaci¾n, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios, realizamos un metanßlisis y preparamos una tabla de resumen de los resultados utilizando el mķtodo GRADE.
RESULTADOS Y CONCLUSIONES
Identificamos 12 revisiones sistemßticas que en conjunto incluyen tres ensayos aleatorizados. Concluimos que el ustekinumab logra una mejorĒa clĒnica en pacientes con psoriasis, y probablemente no se asocia a efectos adversos graves.
La artritis psoriásica es una artritis inflamatoria sin etiología clara, asociada al diagnóstico de psoriasis, donde la mayoría de los pacientes son seronegativos para el factor reumatoideo. Actualmente existen algunas alternativas para su tratamiento, principalmente en base a medicamentos probados para artritis reumatoide. En el último tiempo se ha estudiado con mayor profundidad la eficacia de nuevos medicamentos en pacientes con artritis psoriásica, en especial para aquellos que son resistentes al tratamiento inicial, ya sea con antiinflamatorios no esteroidales, fármacos modificadores de enfermedad tradicionales (por ej. metotrexato), o fármacos biológicos (por ej. inhibidores de TNF). Dentro de estas nuevas alternativas se encuentra el ustekinumab, un inhibidor de IL-12 e IL-23.
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y reanalizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia |
Encontramos 12 revisiones sistemáticas [1],[2],[3],[4],[5],[6],[7],[8],[9],[10],[11],[12], que incluyen tres estudios primarios en seis referencias [13],[14],[15],[16],[17],[18], de los cuales todos son ensayos controlados aleatorizados. Esta tabla y el resumen en general se basan en estos últimos. |
|
Qué tipo de pacientes incluyeron los estudios* |
Todos los ensayos incluyeron pacientes adultos con diagnóstico clínico de artritis psoriásica con enfermedad activa (tres o más articulaciones inflamadas o dolorosas, además de proteína C reactiva de 3 mg/L [13],[14] o 15 mg/L [15]) y respuesta inadecuada o mala tolerancia al uso de antiinflamatorios no esteroidales o fármacos modificadores de enfermedad, además de psoriasis cutánea con lesión activa o historia previa de enfermedad. En un ensayo [13] se excluyeron pacientes con uso previo de anti-TNF. Por el contrario, los otros dos ensayos [14],[15] si incluyeron a pacientes con inadecuada respuesta o mala tolerancia al uso de terapias biológicas. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Dos ensayos [13],[14] incluyeron ustekinumab subcutáneo 45 mg o 90 mg al inicio, luego a la semana 4, luego cada 12 semanas. Un ensayo [15] no reportó la dosis ni el esquema de administración. Todos los ensayos compararon contra placebo. |
|
Qué tipo de desenlaces midieron |
Los ensayos evaluaron múltiples desenlaces, los cuales fueron agrupados por las revisiones sistemáticas de la siguiente forma:
|
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
Cuál es la evidencia
La información sobre los efectos de ustekinumab está basada en tres ensayos aleatorizados que incluyen 1073 pacientes [13],[14],[15]. Dos ensayos reportaron los desenlaces ACR 20 HAQ-DI, PASI 75, DAS-28 [13],[14]. Tres ensayos reportaron eventos adversos graves [13],[14],[15].
El resumen de los resultados es el siguiente:
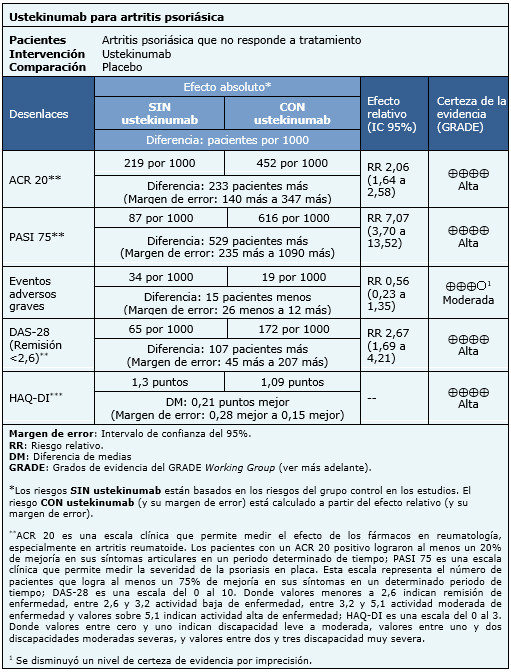
| Siga el enlace para acceder a la versión interactiva de esta tabla (Interactive Summary of Findings - iSoF) |
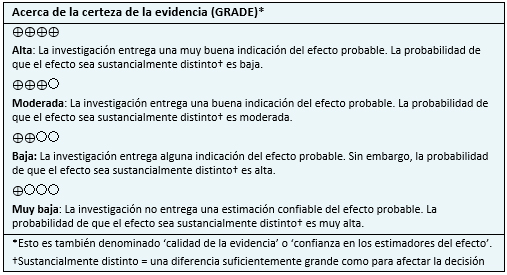
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
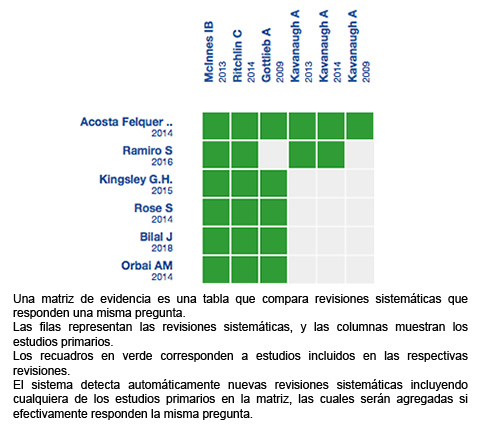
Siga el enlace para acceder a la versión interactiva: Ustekinumab para artritis psoriásica
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

INTRODUCTION
Psoriatic arthritis is an inflammatory arthritis without a clear etiology. Biological therapy is key for its treatment, especially in more complex patients. There are several alternatives for biological treatment, but due to its high cost, it is important to evaluate their real effectiveness.
METHODS
To answer this question we used Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, conducted a meta-analysis and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified 12 systematic reviews including three randomized trials overall. We concluded ustekinumab leads to clinical improvement in psoriatic arthritis, and probably is not associated to severe adverse effects.
 Autores:
Soledad Venegas-Iribarren[1,2], Romina Andino-Navarrete[2,3]
Autores:
Soledad Venegas-Iribarren[1,2], Romina Andino-Navarrete[2,3]

Citaci¾n: Venegas-Iribarren S, Andino-Navarrete R. Is ustekinumab effective for psoriatic arthritis with insufficient response to initial treatment?. Medwave 2018 Mar-Abr;18(2):e7173 doi: 10.5867/medwave.2018.02.7173
Fecha de envĒo: 23/11/2017
Fecha de aceptaci¾n: 4/12/2017
Fecha de publicaci¾n: 8/3/2018
Origen: Este artĒculo es producto del Epistemonikos Evidence Synthesis Project de la Fundaci¾n Epistemonikos, en colaboraci¾n con Medwave para su publicaci¾n.
Tipo de revisi¾n: Con revisi¾n por pares sin ciego por parte del equipo metodol¾gico del Epistemonikos Evidence Synthesis Project.

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Acosta Felquer ML, Coates LC, Soriano ER, Ranza R, Espinoza LR, Helliwell PS, FitzGerald O, McHugh N, Roussou E, Mease PJ. Drug therapies for peripheral joint disease in psoriatic arthritis: a systematic review. J Rheumatol. 2014 Nov;41(11):2277-85. | CrossRef | PubMed |
Acosta Felquer ML, Coates LC, Soriano ER, Ranza R, Espinoza LR, Helliwell PS, FitzGerald O, McHugh N, Roussou E, Mease PJ. Drug therapies for peripheral joint disease in psoriatic arthritis: a systematic review. J Rheumatol. 2014 Nov;41(11):2277-85. | CrossRef | PubMed | Bilal J, Riaz IB, Kamal MU, Elyan M, Sudano D, Khan MA. A Systematic Review and Meta-analysis of Efficacy and Safety of Novel Interleukin Inhibitors in the Management of Psoriatic Arthritis. J Clin Rheumatol. 2017 Sep 19. | CrossRef | PubMed |
Bilal J, Riaz IB, Kamal MU, Elyan M, Sudano D, Khan MA. A Systematic Review and Meta-analysis of Efficacy and Safety of Novel Interleukin Inhibitors in the Management of Psoriatic Arthritis. J Clin Rheumatol. 2017 Sep 19. | CrossRef | PubMed | Boehncke WH, Alvarez Martinez D, Solomon JA, Gottlieb AB. Safety and efficacy of therapies for skin symptoms of psoriasis in patients with psoriatic arthritis: a systematic review. J Rheumatol. 2014 Nov;41(11):2301-5. | CrossRef | PubMed |
Boehncke WH, Alvarez Martinez D, Solomon JA, Gottlieb AB. Safety and efficacy of therapies for skin symptoms of psoriasis in patients with psoriatic arthritis: a systematic review. J Rheumatol. 2014 Nov;41(11):2301-5. | CrossRef | PubMed | Kingsley G.H., Scott D.L.. Assessing the effectiveness of synthetic and biologic disease-modifying antirheumatic drugs in psoriatic arthritis - A systematic review. Psoriasis: Targets and Therapy. 2015;5:71-81.
Kingsley G.H., Scott D.L.. Assessing the effectiveness of synthetic and biologic disease-modifying antirheumatic drugs in psoriatic arthritis - A systematic review. Psoriasis: Targets and Therapy. 2015;5:71-81.  Ramiro S, Smolen JS, Landewķ R, van der Heijde D, Dougados M, Emery P, de Wit M, Cutolo M, Oliver S, Gossec L. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis. 2016 Mar;75(3):490-8. | CrossRef | PubMed |
Ramiro S, Smolen JS, Landewķ R, van der Heijde D, Dougados M, Emery P, de Wit M, Cutolo M, Oliver S, Gossec L. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis. 2016 Mar;75(3):490-8. | CrossRef | PubMed | Rose S, Toloza S, Bautista-Molano W, Helliwell PS; GRAPPA Dactylitis Study Group. Comprehensive treatment of dactylitis in psoriatic arthritis. J Rheumatol. 2014 Nov;41(11):2295-300. | CrossRef | PubMed |
Rose S, Toloza S, Bautista-Molano W, Helliwell PS; GRAPPA Dactylitis Study Group. Comprehensive treatment of dactylitis in psoriatic arthritis. J Rheumatol. 2014 Nov;41(11):2295-300. | CrossRef | PubMed | Ungprasert P, Thongprayoon C, Davis JM 3rd. Indirect comparisons of the efficacy of subsequent biological agents in patients with psoriatic arthritis with an inadequate response to tumor necrosis factor inhibitors: a meta-analysis. Clin Rheumatol. 2016 Jul;35(7):1795-803. | CrossRef | PubMed |
Ungprasert P, Thongprayoon C, Davis JM 3rd. Indirect comparisons of the efficacy of subsequent biological agents in patients with psoriatic arthritis with an inadequate response to tumor necrosis factor inhibitors: a meta-analysis. Clin Rheumatol. 2016 Jul;35(7):1795-803. | CrossRef | PubMed | Ungprasert P, Thongprayoon C, Davis JM 3rd. Indirect comparisons of the efficacy of biological agents in patients with psoriatic arthritis with an inadequate response to traditional disease-modifying anti-rheumatic drugs or to non-steroidal anti-inflammatory drugs: A meta-analysis. Semin Arthritis Rheum. 2016 Feb;45(4):428-38. | CrossRef | PubMed |
Ungprasert P, Thongprayoon C, Davis JM 3rd. Indirect comparisons of the efficacy of biological agents in patients with psoriatic arthritis with an inadequate response to traditional disease-modifying anti-rheumatic drugs or to non-steroidal anti-inflammatory drugs: A meta-analysis. Semin Arthritis Rheum. 2016 Feb;45(4):428-38. | CrossRef | PubMed | Wu Y, Chen J, Li YH, Ma GZ, Chen JZ, Gao XH, Chen HD. Treatment of psoriasis with interleukin-12/23 monoclonal antibody: a systematic review. Eur J Dermatol. 2012 Jan-Feb;22(1):72-82. | CrossRef | PubMed |
Wu Y, Chen J, Li YH, Ma GZ, Chen JZ, Gao XH, Chen HD. Treatment of psoriasis with interleukin-12/23 monoclonal antibody: a systematic review. Eur J Dermatol. 2012 Jan-Feb;22(1):72-82. | CrossRef | PubMed | Ustekinumab (Stelara) Injection [Internet]. Ottawa (ON): Canadian Agency for Drugs and Technologies in Health; 2016 Nov. | PubMed | Link |
Ustekinumab (Stelara) Injection [Internet]. Ottawa (ON): Canadian Agency for Drugs and Technologies in Health; 2016 Nov. | PubMed | Link | Song GG, Lee YH. Relative efficacy and safety of apremilast, secukinumab, and
ustekinumab for the treatment of psoriatic arthritis. Z Rheumatol. 2017 Aug 8. | CrossRef | PubMed |
Song GG, Lee YH. Relative efficacy and safety of apremilast, secukinumab, and
ustekinumab for the treatment of psoriatic arthritis. Z Rheumatol. 2017 Aug 8. | CrossRef | PubMed | Orbai AM, Weitz J, Siegel EL, Siebert S, Savage LJ, Aydin SZ, Luime JJ, Elkayam O, Neerinckx B, Urbancek S, de Vlam K, Ritchlin CT; GRAPPA Enthesitis Working Group. Systematic review of treatment effectiveness and outcome measures for enthesitis in psoriatic arthritis. J Rheumatol. 2014 Nov;41(11):2290-4. | CrossRef | PubMed |
Orbai AM, Weitz J, Siegel EL, Siebert S, Savage LJ, Aydin SZ, Luime JJ, Elkayam O, Neerinckx B, Urbancek S, de Vlam K, Ritchlin CT; GRAPPA Enthesitis Working Group. Systematic review of treatment effectiveness and outcome measures for enthesitis in psoriatic arthritis. J Rheumatol. 2014 Nov;41(11):2290-4. | CrossRef | PubMed | McInnes IB, Kavanaugh A, Gottlieb AB, Puig L, Rahman P, Ritchlin C, Brodmerkel C, Li S, Wang Y, Mendelsohn AM, Doyle MK; PSUMMIT 1 Study Group. Efficacy and safety of ustekinumab in patients with active psoriatic arthritis: 1 year results of the phase 3, multicentre, double-blind, placebo-controlled PSUMMIT 1 trial. Lancet. 2013 Aug 31;382(9894):780-9. | CrossRef | PubMed |
McInnes IB, Kavanaugh A, Gottlieb AB, Puig L, Rahman P, Ritchlin C, Brodmerkel C, Li S, Wang Y, Mendelsohn AM, Doyle MK; PSUMMIT 1 Study Group. Efficacy and safety of ustekinumab in patients with active psoriatic arthritis: 1 year results of the phase 3, multicentre, double-blind, placebo-controlled PSUMMIT 1 trial. Lancet. 2013 Aug 31;382(9894):780-9. | CrossRef | PubMed | Ritchlin C, Rahman P, Kavanaugh A, McInnes IB, Puig L, Li S, Wang Y, Shen YK, Doyle MK, Mendelsohn AM, Gottlieb AB; PSUMMIT 2 Study Group. Efficacy and safety of the anti-IL-12/23 p40 monoclonal antibody, ustekinumab, in patients with active psoriatic arthritis despite conventional non-biological and biological anti-tumour necrosis factor therapy: 6-month and 1-year results of the phase 3, multicentre, double-blind, placebo-controlled, randomised PSUMMIT 2 trial. Ann Rheum Dis. 2014 Jun;73(6):990-9. | CrossRef | PubMed | PMC |
Ritchlin C, Rahman P, Kavanaugh A, McInnes IB, Puig L, Li S, Wang Y, Shen YK, Doyle MK, Mendelsohn AM, Gottlieb AB; PSUMMIT 2 Study Group. Efficacy and safety of the anti-IL-12/23 p40 monoclonal antibody, ustekinumab, in patients with active psoriatic arthritis despite conventional non-biological and biological anti-tumour necrosis factor therapy: 6-month and 1-year results of the phase 3, multicentre, double-blind, placebo-controlled, randomised PSUMMIT 2 trial. Ann Rheum Dis. 2014 Jun;73(6):990-9. | CrossRef | PubMed | PMC | Gottlieb A, Menter A, Mendelsohn A, Shen YK, Li S, Guzzo C, Fretzin S, Kunynetz R, Kavanaugh A. Ustekinumab, a human interleukin 12/23 monoclonal antibody, for psoriatic arthritis: randomised, double-blind, placebo-controlled, crossover trial. Lancet. 2009 Feb 21;373(9664):633-40. Erratum in: Lancet. 2009 Apr 18;373(9672):1340. Lancet. 2010 Nov 6;376(9752):1542. | CrossRef | PubMed |
Gottlieb A, Menter A, Mendelsohn A, Shen YK, Li S, Guzzo C, Fretzin S, Kunynetz R, Kavanaugh A. Ustekinumab, a human interleukin 12/23 monoclonal antibody, for psoriatic arthritis: randomised, double-blind, placebo-controlled, crossover trial. Lancet. 2009 Feb 21;373(9664):633-40. Erratum in: Lancet. 2009 Apr 18;373(9672):1340. Lancet. 2010 Nov 6;376(9752):1542. | CrossRef | PubMed | Kavanaugh A. The efficacy of ustekinumab on the articular and dermatologic manifestations of psoriatic arthritis. Curr Rheumatol Rep. 2009 Aug;11(4):233-4. | PubMed |
Kavanaugh A. The efficacy of ustekinumab on the articular and dermatologic manifestations of psoriatic arthritis. Curr Rheumatol Rep. 2009 Aug;11(4):233-4. | PubMed | Kavanaugh A, Ritchlin C, Rahman P, Puig L, Gottlieb AB, Li S, Wang Y, Noonan L, Brodmerkel C, Song M, Mendelsohn AM, McInnes IB; PSUMMIT-1 and 2 Study Groups. Ustekinumab, an anti-IL-12/23 p40 monoclonal antibody, inhibits radiographic progression in patients with active psoriatic arthritis: results of an integrated analysis of radiographic data from the phase 3, multicentre, randomised, double-blind, placebo-controlled PSUMMIT-1 and PSUMMIT-2 trials. Ann Rheum Dis.
2014 Jun;73(6):1000-6. | CrossRef | PubMed | PMC |
Kavanaugh A, Ritchlin C, Rahman P, Puig L, Gottlieb AB, Li S, Wang Y, Noonan L, Brodmerkel C, Song M, Mendelsohn AM, McInnes IB; PSUMMIT-1 and 2 Study Groups. Ustekinumab, an anti-IL-12/23 p40 monoclonal antibody, inhibits radiographic progression in patients with active psoriatic arthritis: results of an integrated analysis of radiographic data from the phase 3, multicentre, randomised, double-blind, placebo-controlled PSUMMIT-1 and PSUMMIT-2 trials. Ann Rheum Dis.
2014 Jun;73(6):1000-6. | CrossRef | PubMed | PMC | Kavanaugh A, Puig L, Gottlieb AB. Efficacy and Safety of Ustekinumab in Patients with Active Psoriatic Arthritis: 2-Year Results from a Phase 3, Multicenter, Double-Blind, Placebo-Controlled Study. Arthritis Rheum. 2013;65(Supple 10):L10.
Kavanaugh A, Puig L, Gottlieb AB. Efficacy and Safety of Ustekinumab in Patients with Active Psoriatic Arthritis: 2-Year Results from a Phase 3, Multicenter, Double-Blind, Placebo-Controlled Study. Arthritis Rheum. 2013;65(Supple 10):L10.  American Academy of Dermatology Work Group, Menter A, Korman NJ, Elmets CA, Feldman SR, Gelfand JM, Gordon KB, Gottlieb A, Koo JY, Lebwohl M, Leonardi CL, Lim HW, Van Voorhees AS, Beutner KR, Ryan C, Bhushan R. Guidelines of care for the management of psoriasis and psoriatic arthritis: section 6. Guidelines of care for the treatment of psoriasis and psoriatic arthritis: case-based presentations and evidence-based conclusions. J Am Acad Dermatol. 2011 Jul;65(1):137-74. | CrossRef | PubMed |
American Academy of Dermatology Work Group, Menter A, Korman NJ, Elmets CA, Feldman SR, Gelfand JM, Gordon KB, Gottlieb A, Koo JY, Lebwohl M, Leonardi CL, Lim HW, Van Voorhees AS, Beutner KR, Ryan C, Bhushan R. Guidelines of care for the management of psoriasis and psoriatic arthritis: section 6. Guidelines of care for the treatment of psoriasis and psoriatic arthritis: case-based presentations and evidence-based conclusions. J Am Acad Dermatol. 2011 Jul;65(1):137-74. | CrossRef | PubMed | Smith CH, Anstey AV, Barker JN, Burden AD, Chalmers RJ, Chandler DA, Finlay AY, Griffiths CE, Jackson K, McHugh NJ, McKenna KE, Reynolds NJ, Ormerod AD; (Chair of Guideline Group). British Association of Dermatologists' guidelines for biologic interventions for psoriasis 2009. Br J Dermatol. 2009 Nov;161(5):987-1019. | CrossRef | PubMed |
Smith CH, Anstey AV, Barker JN, Burden AD, Chalmers RJ, Chandler DA, Finlay AY, Griffiths CE, Jackson K, McHugh NJ, McKenna KE, Reynolds NJ, Ormerod AD; (Chair of Guideline Group). British Association of Dermatologists' guidelines for biologic interventions for psoriasis 2009. Br J Dermatol. 2009 Nov;161(5):987-1019. | CrossRef | PubMed | Daudķn E, Puig L, Ferrßndiz C, Sßnchez-Carazo JL, Hernanz-Hermosa JM; Spanish Psoriasis Group of the Spanish Academy of Dermatology and Venereology. Consensus document on the evaluation and treatment of moderate-to-severe psoriasis: Psoriasis Group of the Spanish Academy of Dermatology and Venereology. J Eur Acad Dermatol Venereol. 2016 Mar;30 Suppl 2:1-18. | CrossRef | PubMed |
Daudķn E, Puig L, Ferrßndiz C, Sßnchez-Carazo JL, Hernanz-Hermosa JM; Spanish Psoriasis Group of the Spanish Academy of Dermatology and Venereology. Consensus document on the evaluation and treatment of moderate-to-severe psoriasis: Psoriasis Group of the Spanish Academy of Dermatology and Venereology. J Eur Acad Dermatol Venereol. 2016 Mar;30 Suppl 2:1-18. | CrossRef | PubMed | Gossec L, Smolen JS, Ramiro S, de Wit M, Cutolo M, Dougados M, Emery P, Landewķ R, Oliver S, Aletaha D, Betteridge N, Braun J, Burmester G, Ca±ete JD, Damjanov N, FitzGerald O, Haglund E, Helliwell P, Kvien TK, Lories R, Luger T, Maccarone M, Marzo-Ortega H, McGonagle D, McInnes IB, Olivieri I, Pavelka K, Schett G, Sieper J, van den Bosch F, Veale DJ, Wollenhaupt J, Zink A, van der Heijde D. European League Against Rheumatism (EULAR) recommendations for the management of psoriatic arthritis with pharmacological therapies: 2015 update. Ann Rheum Dis. 2016 Mar;75(3):499-510. | CrossRef | PubMed |
Gossec L, Smolen JS, Ramiro S, de Wit M, Cutolo M, Dougados M, Emery P, Landewķ R, Oliver S, Aletaha D, Betteridge N, Braun J, Burmester G, Ca±ete JD, Damjanov N, FitzGerald O, Haglund E, Helliwell P, Kvien TK, Lories R, Luger T, Maccarone M, Marzo-Ortega H, McGonagle D, McInnes IB, Olivieri I, Pavelka K, Schett G, Sieper J, van den Bosch F, Veale DJ, Wollenhaupt J, Zink A, van der Heijde D. European League Against Rheumatism (EULAR) recommendations for the management of psoriatic arthritis with pharmacological therapies: 2015 update. Ann Rheum Dis. 2016 Mar;75(3):499-510. | CrossRef | PubMed |