 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
INTRODUCCIÓN
La caquexia y la anorexia se encuentran dentro de los síntomas más frecuentes en los pacientes oncológicos. Los cannabinoides han sido propuestos para su manejo en los pacientes con cáncer avanzado, sin embargo, su rol es controvertido.
MÉTODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud a nivel mundial, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios y preparamos una tabla de resumen de los resultados utilizando el método GRADE.
RESULTADOS Y CONCLUSIONES
Identificamos diez revisiones sistemáticas, que en conjunto incluyen tres estudios, entre ellos dos ensayos aleatorizados. Concluimos que no está claro si los cannabinoides logran o no un aumento de peso en pacientes con anorexia-caquexia porque la certeza de la evidencia es muy baja, podrían no tener tampoco efecto sobre el apetito, y probablemente se asocian a efectos adversos frecuentes.
El síndrome anorexia-caquexia corresponde a un estado hipercatabólico caracterizado por ausencia de deseo de comer y baja de peso involuntario asociado a una pérdida de masa muscular. Este fenómeno se observa hasta en un 80% de los pacientes con cáncer y en porcentajes variables en pacientes con otras enfermedades no oncológicas [1].
En pacientes con cáncer, la anorexia, es decir, la pérdida de apetito ocurre por una variedad de causas (disfagia, sequedad bucal, náuseas, depresión, etc.), que determinan una disminución de la ingesta y de la disponibilidad de nutrientes, y como consecuencia una baja de peso. En pacientes con anorexia aislada, el aumento de la ingesta y de la disponibilidad de nutrientes permite revertir la baja de peso. Si bien la anorexia por sí sola no explica el deterioro que se observa en los pacientes con cáncer, es un factor que contribuye a la baja de peso y es considerada un parámetro relevante de calidad de vida [2].
La caquexia corresponde a un síndrome multifactorial caracterizado por la pérdida de masa del músculo esquelético, con o sin pérdida de masa grasa, lo que conduce a un deterioro funcional progresivo [3]. Se encuentra entre los síntomas más comunes en pacientes oncológicos, con una prevalencia de 50% al momento del diagnóstico y 80% en etapa de fin de vida. Se asocia a un descenso en la calidad de vida y sobrevida (pudiendo ser la causa directa de un 20% de los fallecimientos por esta enfermedad) y a otros síntomas tales como anorexia (hasta 90% en pacientes oncológicos), fatiga, astenia, debilidad, saciedad precoz, entre otros [4]. Se sabe que la fisiopatología de la caquexia es multifactorial; por ejemplo, el crecimiento tumoral está asociado con profundas alteraciones metabólicas y neuroquímicas, como la producción de una serie de citoquinas pro inflamatorias, incluyendo TNF-alfa, IL-1 e IL-6, que favorecen un estado hipercatabólico y dificultan la utilización de los nutrientes disponibles.
Se han propuestos diversas intervenciones enfocadas en estos mecanismos particulares, dentro de las cuales encontramos progestágenos, corticoides y cannabinoides [5]. Estos últimos buscarían mejorar el apetito a través de la activación de los receptores CB 1 (sistema nervioso central) y CB 2 (células inmunes) del sistema endocannabidiol [6], y disminuir la baja de peso a través de un efecto de inmunomodulación de citoquinas [7]. Sin embargo, existen dudas sobre si esto se traduce realmente en un efecto en la práctica clínica.
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y reanalizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, tablas de resumen de resultados con el método GRADE, y tabla de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia |
Encontramos 10 revisiones sistemáticas [8],[9],[10],[11],[12],[13],[14],[15],[16],[17] que incluyen tres estudios primarios pertinentes a la pregunta [18],[19],[20], de los cuales dos corresponden a ensayos aleatorizados [18],[19]. Esta tabla y el resumen en general se basan en estos últimos. |
|
Qué tipo de pacientes incluyeron los estudios* |
Ambos ensayos incluyeron pacientes adultos (mayores de 18 años), de ambos sexos con cáncer sólido o hematológico en estadio IV. Un ensayo estableció como criterio de inclusión la baja de peso en los últimos 2 a 6 meses y también seleccionó por ECOG menor a 2 [18]. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Ambos ensayos evaluaron delta-9-tetrahydrocannabinol (THC) oral. Un ensayo [18] utilizó THC oral (5 mg/día) y cannabidiol (2 mg/ día) por seis semanas versus placebo. El otro ensayo [19] utilizó sólo THC oral en tres dosis día (0,1 mg/kg/día) por dos semanas versus placebo. |
|
Qué tipo de desenlaces midieron |
Los estudios midieron múltiples desenlaces, pero las revisiones sistemáticas identificadas los agruparon de la siguiente manera:
|
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
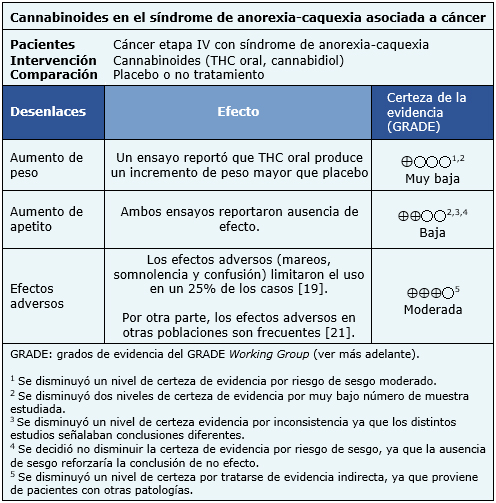
La información sobre los efectos de los cannabinoides para el síndrome anorexia-caquexia en pacientes con cáncer avanzado está basada en dos ensayos aleatorizados que incluyen 218 pacientes.
Un ensayo [18] reportó el desenlace aumento de peso (164 pacientes). Ambos ensayos [18],[19] reportaron los desenlaces aumento de apetito (218 pacientes).
El resumen de los resultados es el siguiente:
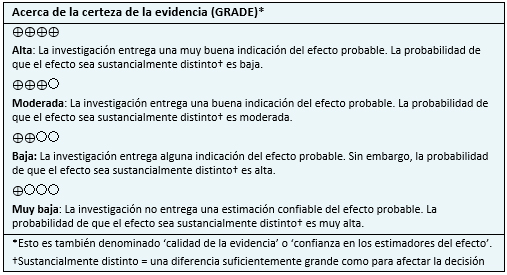
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
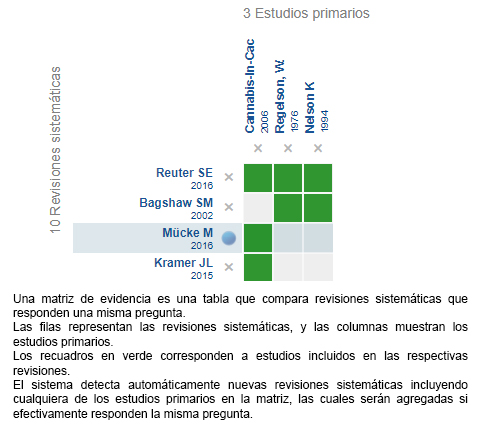
Siga el enlace para acceder a la versión interactiva: Cannabinoides versus placebo para caquexia- anorexia en pacientes con cáncer
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

INTRODUCTION
Cachexia and anorexia are among the most frequent symptoms in patients with cancer. Cannabinoids have been used in patients with advanced cancer; however, their role is still controversial.
METHODS
To answer this question we used Epistemonikos, the largest database of systematic reviews in health, which is maintained by screening multiple information sources, including MEDLINE, EMBASE, Cochrane, among others. We extracted data from the systematic reviews, reanalyzed data of primary studies, and generated a summary of findings table using the GRADE approach.
RESULTS AND CONCLUSIONS
We identified ten systematic reviews including three studies overall, of which two were randomized trials. We concluded it is not clear whether cannabinoids have any positive effect on increasing weight because the certainty of the evidence is very low. They might not have any effect on appetite, and are probably associated to frequent adverse effects.
 Autores:
Claudia Cabeza[1,3], Oscar Corsi[2,3], Pedro Pérez-Cruz[2,3,4]
Autores:
Claudia Cabeza[1,3], Oscar Corsi[2,3], Pedro Pérez-Cruz[2,3,4]

Citación: Cabeza C, Corsi O, Pérez-Cruz PE. Are cannabinoids an alternative for cachexia-anorexia syndrome in patients with advanced cancer?. Medwave 2017 Nov-Dic;17(9):e7130 doi: 10.5867/medwave.2017.09.7130
Fecha de envío: 17/11/2017
Fecha de aceptación: 20/12/2017
Fecha de publicación: 29/12/2017
Origen: Este artículo es producto del Epistemonikos Evidence Synthesis Project de la Fundación Epistemonikos, en colaboración con Medwave para su publicación.
Tipo de revisión: Con revisión por pares sin ciego por parte del equipo metodológico del Epistemonikos Evidence Synthesis Project.

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Del Fabbro E, Dalal S, Bruera E. Symptom control in palliative care--Part II: cachexia/anorexia and fatigue. J Palliat Med. 2006 Apr;9(2):409-21. | PubMed |
Del Fabbro E, Dalal S, Bruera E. Symptom control in palliative care--Part II: cachexia/anorexia and fatigue. J Palliat Med. 2006 Apr;9(2):409-21. | PubMed | Bruera E. ABC of palliative care. Anorexia, cachexia, and nutrition. BMJ. 1997 Nov 8;315(7117):1219-22 | PubMed | PMC |
Bruera E. ABC of palliative care. Anorexia, cachexia, and nutrition. BMJ. 1997 Nov 8;315(7117):1219-22 | PubMed | PMC | Fearon K, Strasser F, Anker SD, Bosaeus I, Bruera E, Fainsinger RL, Jatoi A, Loprinzi C, MacDonald N, Mantovani G, Davis M, Muscaritoli M, Ottery F, Radbruch L, Ravasco P, Walsh D, Wilcock A, Kaasa S, Baracos VE. Definition and classification of cancer cachexia: an international consensus. Lancet Oncol. 2011 May;12(5):489-95. | CrossRef | PubMed |
Fearon K, Strasser F, Anker SD, Bosaeus I, Bruera E, Fainsinger RL, Jatoi A, Loprinzi C, MacDonald N, Mantovani G, Davis M, Muscaritoli M, Ottery F, Radbruch L, Ravasco P, Walsh D, Wilcock A, Kaasa S, Baracos VE. Definition and classification of cancer cachexia: an international consensus. Lancet Oncol. 2011 May;12(5):489-95. | CrossRef | PubMed | Laviano A, Meguid MM, Inui A, Muscaritoli M, Rossi-Fanelli F. Therapy insight: Cancer anorexia-cachexia syndrome--when all you can eat is yourself. Nat Clin Pract Oncol. 2005 Mar;2(3):158-65. | PubMed |
Laviano A, Meguid MM, Inui A, Muscaritoli M, Rossi-Fanelli F. Therapy insight: Cancer anorexia-cachexia syndrome--when all you can eat is yourself. Nat Clin Pract Oncol. 2005 Mar;2(3):158-65. | PubMed | Aapro M, Arends J, Bozzetti F, Fearon K, Grunberg SM, Herrstedt J, Hopkinson J, Jacquelin-Ravel N, Jatoi A, Kaasa S, Strasser F; ESMO (European School of Medical Oncology).. Early recognition of malnutrition and cachexia in the cancer patient: a position paper of a European School of Oncology Task Force. Ann Oncol. 2014 Aug;25(8):1492-9. | CrossRef | PubMed |
Aapro M, Arends J, Bozzetti F, Fearon K, Grunberg SM, Herrstedt J, Hopkinson J, Jacquelin-Ravel N, Jatoi A, Kaasa S, Strasser F; ESMO (European School of Medical Oncology).. Early recognition of malnutrition and cachexia in the cancer patient: a position paper of a European School of Oncology Task Force. Ann Oncol. 2014 Aug;25(8):1492-9. | CrossRef | PubMed | Mechoulam R, Parker LA. The endocannabinoid system and the brain. Annu Rev Psychol. 2013;64:21-47. | CrossRef | PubMed |
Mechoulam R, Parker LA. The endocannabinoid system and the brain. Annu Rev Psychol. 2013;64:21-47. | CrossRef | PubMed | Massa F, Marsicano G, Hermann H, Cannich A, Monory K, Cravatt BF, Ferri GL, Sibaev A, Storr M, Lutz B. The endogenous cannabinoid system protects against colonic inflammation. J Clin Invest. 2004 Apr;113(8):1202-9. | PubMed | PMC |
Massa F, Marsicano G, Hermann H, Cannich A, Monory K, Cravatt BF, Ferri GL, Sibaev A, Storr M, Lutz B. The endogenous cannabinoid system protects against colonic inflammation. J Clin Invest. 2004 Apr;113(8):1202-9. | PubMed | PMC | Amato L, Davoli M, Minozzi S, Mitrova Z, Parmelli E, Saulle R, Vecchi S. Systematic reviews on therapeutic efficacy and safety of Cannabis (including extracts and tinctures) for patients with multiple sclerosis, chronic neuropathic pain, dementia and Tourette syndrome, HIV/AIDS, and cancer receiving chemotherapy. Departament of Epidemiology Lazio Regional Healty Service. 2016.
Amato L, Davoli M, Minozzi S, Mitrova Z, Parmelli E, Saulle R, Vecchi S. Systematic reviews on therapeutic efficacy and safety of Cannabis (including extracts and tinctures) for patients with multiple sclerosis, chronic neuropathic pain, dementia and Tourette syndrome, HIV/AIDS, and cancer receiving chemotherapy. Departament of Epidemiology Lazio Regional Healty Service. 2016.  Bagshaw SM, Hagen NA. Medical efficacy of cannabinoids and marijuana: a comprehensive review of the literature. Journal of palliative care. 2002;18(2):111-22.
Bagshaw SM, Hagen NA. Medical efficacy of cannabinoids and marijuana: a comprehensive review of the literature. Journal of palliative care. 2002;18(2):111-22.  Ben Amar M. Cannabinoids in medicine: A review of their therapeutic potential. J Ethnopharmacol. 2006 Apr 21;105(1-2):1-25. | PubMed |
Ben Amar M. Cannabinoids in medicine: A review of their therapeutic potential. J Ethnopharmacol. 2006 Apr 21;105(1-2):1-25. | PubMed | Goldenberg M, Reid MW, IsHak WW, Danovitch I. The impact of cannabis and cannabinoids for medical conditions on health-related quality of life: A systematic review and meta-analysis. Drug Alcohol Depend. 2017 May 1;174:80-90. | CrossRef | PubMed |
Goldenberg M, Reid MW, IsHak WW, Danovitch I. The impact of cannabis and cannabinoids for medical conditions on health-related quality of life: A systematic review and meta-analysis. Drug Alcohol Depend. 2017 May 1;174:80-90. | CrossRef | PubMed | Hazekamp A, Grotenhermen F. Review on clinical studies with cannabis and cannabinoids 2005–2009. Cannabinoids. 2010 Feb 13; 5(special): 1–21. | Link |
Hazekamp A, Grotenhermen F. Review on clinical studies with cannabis and cannabinoids 2005–2009. Cannabinoids. 2010 Feb 13; 5(special): 1–21. | Link | Kairuz MJF. Systematic review of clinical studies on cannabis use for therapeutic purposes between 2005-2015. 2015.
Kairuz MJF. Systematic review of clinical studies on cannabis use for therapeutic purposes between 2005-2015. 2015.  Kramer JL. Medical marijuana for cancer. CA Cancer J Clin. 2015 Mar;65(2):109-22. | CrossRef | PubMed |
Kramer JL. Medical marijuana for cancer. CA Cancer J Clin. 2015 Mar;65(2):109-22. | CrossRef | PubMed | Mücke M, Carter C, Cuhls H, Prüß M, Radbruch L, Häuser W. [Cannabinoids in palliative care: Systematic review and meta-analysis of efficacy, tolerability and safety]. Schmerz. 2016 Feb;30(1):25-36. | CrossRef | PubMed |
Mücke M, Carter C, Cuhls H, Prüß M, Radbruch L, Häuser W. [Cannabinoids in palliative care: Systematic review and meta-analysis of efficacy, tolerability and safety]. Schmerz. 2016 Feb;30(1):25-36. | CrossRef | PubMed | Reuter SE, Martin JH. Pharmacokinetics of Cannabis in Cancer Cachexia-Anorexia Syndrome. Clin Pharmacokinet. 2016 Jul;55(7):807-12. | CrossRef | PubMed |
Reuter SE, Martin JH. Pharmacokinetics of Cannabis in Cancer Cachexia-Anorexia Syndrome. Clin Pharmacokinet. 2016 Jul;55(7):807-12. | CrossRef | PubMed | Zhornitsky S, Potvin S. Cannabidiol in humans-the quest for therapeutic targets. Pharmaceuticals (Basel). 2012 May 21;5(5):529-52. | CrossRef | PubMed | PMC |
Zhornitsky S, Potvin S. Cannabidiol in humans-the quest for therapeutic targets. Pharmaceuticals (Basel). 2012 May 21;5(5):529-52. | CrossRef | PubMed | PMC | Cannabis-In-Cachexia-Study-Group., Strasser F, Luftner D, Possinger K, Ernst G, Ruhstaller T, Meissner W, Ko YD, Schnelle M, Reif M, Cerny T. Comparison of orally administered cannabis extract and delta-9-tetrahydrocannabinol in treating patients with cancer-related anorexia-cachexia syndrome: a multicenter, phase III, randomized, double-blind, placebo-controlled clinical trial from the Cannabis-In-Cachexia-Study-Group. J Clin Oncol. 2006 Jul 20;24(21):3394-400. | PubMed |
Cannabis-In-Cachexia-Study-Group., Strasser F, Luftner D, Possinger K, Ernst G, Ruhstaller T, Meissner W, Ko YD, Schnelle M, Reif M, Cerny T. Comparison of orally administered cannabis extract and delta-9-tetrahydrocannabinol in treating patients with cancer-related anorexia-cachexia syndrome: a multicenter, phase III, randomized, double-blind, placebo-controlled clinical trial from the Cannabis-In-Cachexia-Study-Group. J Clin Oncol. 2006 Jul 20;24(21):3394-400. | PubMed | Regelson W, Butler JR, Schulz J, Kirk T, Peek L, Green ML, Zalis MO. Delta-9-tetrahydrocannabinol as an effective antidepressant and appetite-stimulating agent in advanced cancer patients. In: Braude MC, Szara S. (Eds.). The Pharmacology of Marihuana. 1976. Raven Press, New York. pp. 763–776.
Regelson W, Butler JR, Schulz J, Kirk T, Peek L, Green ML, Zalis MO. Delta-9-tetrahydrocannabinol as an effective antidepressant and appetite-stimulating agent in advanced cancer patients. In: Braude MC, Szara S. (Eds.). The Pharmacology of Marihuana. 1976. Raven Press, New York. pp. 763–776.  Nelson K, Walsh D, Deeter P, Sheehan F. A phase II study of delta-9-tetrahydrocannabinol for appetite stimulation in cancer-associated anorexia. J Palliat Care. 1994 Spring;10(1):14-8. | PubMed |
Nelson K, Walsh D, Deeter P, Sheehan F. A phase II study of delta-9-tetrahydrocannabinol for appetite stimulation in cancer-associated anorexia. J Palliat Care. 1994 Spring;10(1):14-8. | PubMed | Whiting PF, Wolff RF, Deshpande S, Di Nisio M, Duffy S, Hernandez AV, Keurentjes JC, Lang S, et al. Cannabinoids for Medical Use: A Systematic Review and Meta-analysis. JAMA. 2015 Jun 23-30;313 (24):2456-73.
Whiting PF, Wolff RF, Deshpande S, Di Nisio M, Duffy S, Hernandez AV, Keurentjes JC, Lang S, et al. Cannabinoids for Medical Use: A Systematic Review and Meta-analysis. JAMA. 2015 Jun 23-30;313 (24):2456-73.  National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Palliative Care 1.2017 [cited May 18, 2017] | Link |
National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Palliative Care 1.2017 [cited May 18, 2017] | Link |