 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Los pacientes con insuficiencia renal crónica poseen riesgo cardiovascular mayor que la población general, algo que ha sido relacionado con niveles altos de homocisteína. El uso de ácido fólico se ha propuesto como una medida que podría disminuir la hiperhomocisteinemia, y por esta vía disminuir los eventos cardiovasculares. Sin embargo, existe controversia sobre la verdadera utilidad de esta medida. Utilizando la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en 30 bases de datos, identificamos seis revisiones sistemáticas que en conjunto incluyen 13 estudios aleatorizados que responden la pregunta de interés. Realizamos un metanálisis y tablas de resumen de los resultados utilizando el método GRADE. Concluimos que la suplementación con ácido fólico no disminuye el riesgo de infarto agudo al miocardio ni de accidente vascular encefálico en pacientes con insuficiencia renal crónica, y que podría no tener efecto sobre la mortalidad.
Está claramente identificado que los pacientes con insuficiencia renal crónica poseen riesgo cardiovascular mayor que la población general. No obstante, pese al control de los factores de riesgo clásicos (diabetes, hipertensión arterial, dislipidemia, tabaco, entre otros) aún existe una diferencia sobre la población con estas patologías sin insuficiencia renal crónica. Paralelamente, se ha observado que los niveles de homocisteína se encuentran elevados en insuficiencia renal crónica y existe correlación con los eventos cardiovasculares y la respectiva mortalidad.
Debido a esto, se ha propuesto el uso de ácido fólico como terapia para reducir el riesgo cardiovascular y su mortalidad asociada, fundamentado en el mecanismo fisiopatológico de reducción de niveles de homocisteína.
Sin embargo, la evidencia sobre si esto realmente se traduce en algún beneficio clínico aún es controvertida.
Utilizamos la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en 30 bases de datos, para identificar revisiones sistemáticas y sus estudios primarios incluidos. Con esta información generamos un resumen estructurado, siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios, tablas de resumen de resultados con el método GRADE, y tabla de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
|
Cuál es la evidencia. |
Encontramos seis revisiones sistemáticas [1],[2],[3],[4], [5],[6] que incluyen 13 estudios controlados aleatorizados, reportados en 24 referencias [7],[8],[9],[10],[11],[12], |
|
Qué tipo de pacientes incluyeron los estudios |
Características generales: El promedio de edad de los pacientes de los estudios fue de 58,7 años. El porcentaje promedio de hombres fue 66%. Caracterizando tipo de nefropatía y su etapa:Tres estudios [23],[30],[32] incluyeron pacientes en cualquier etapa de insuficiencia renal, cuatro estudios [7],[24],[27],[29] en etapa previa a diálisis, cinco en diálisis [22],[25],[26], [28],[31] y uno en trasplantados [9]. Diez estudios [9],[22],[23],[25],[26],[27],[28],[29],[31], [32] incluyeron cualquier tipo de nefropatía, dos estudios [7],[30] incluyeron sólo nefropatía diabética y un estudio [24] incluyó nefropatía diabética o vascular. Respecto a los antecedentes de los pacientes incluidos: El porcentaje promedio de pacientes con antecedente de infarto agudo al miocardio correspondió al 40,9%, con un estudio que tenía este antecedente como criterio de inclusión [27]. El porcentaje promedio de pacientes diabéticos fue de 40,9%, con dos estudios con criterio de inclusión correspondiente a este antecedente [7],[30]. |
|
Qué tipo de intervenciones incluyeron los estudios |
Cinco estudios [25],[28],[30],[31],[32] evaluaron la intervención de ácido fólico como monoterapia, ocho estudios [7],[9],[22],[23],[24],[26],[27],[29] en combinación con vitamina B6 y B12. La dosis utilizada de ácido fólico en promedio fue 8,8 mg/día, con rango entre 2-40 mg/día. Ocho estudios [7],[23],[24],[27],[28],[29], [30],[32] compararon contra placebo, dos estudios [25], [26] compararon contra cuidado habitual, un estudio [9] contra vitamina B y dos estudios [22],[31] contra dosis menores de ácido fólico con o sin complemento de vitamina B. |
|
Qué tipo de desenlaces midieron |
Las diferentes revisiones sistemáticas agruparon los desenlaces de la siguiente manera:
|
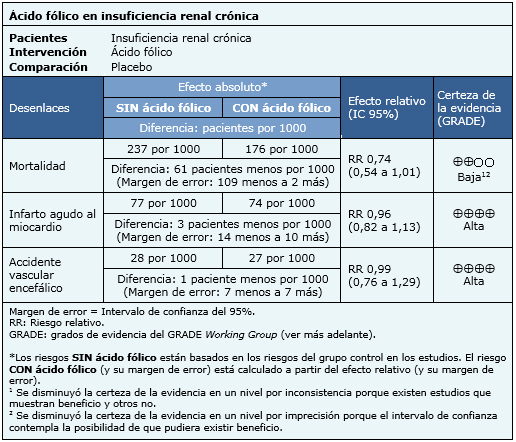
La información sobre los efectos del ácido fólico en pacientes con insuficiencia renal crónica está basada en trece estudios aleatorizados que incluyen 11 049 pacientes.
Nueve estudios (8500 pacientes) midieron el desenlace de mortalidad general [7],[9],[22],[23],[24],[26],[28],[31],[32], siete estudios (7718 pacientes) midieron infarto agudo al miocardio [7],[9],[22], [23],[26],[31],[32] y siete estudios (8536 pacientes) midieron el desenlace accidente vascular encefálico [9],[22],[23],[24],[26],[31],[32].
El resumen de los resultados es el siguiente:

|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Qué piensan los pacientes y sus tratantes |
|
| Consideraciones de recursos |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
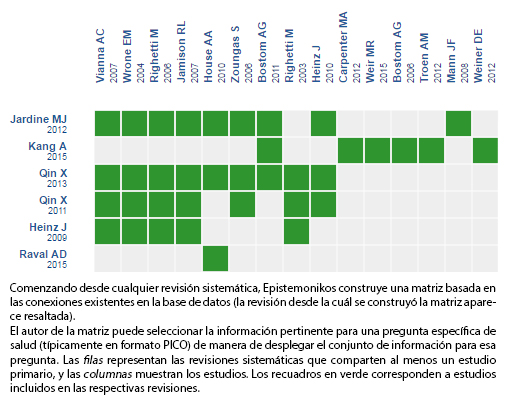
Siga el enlace para acceder a la versión interactiva: Suplementación con ácido fólico para la insuficiencia renal crónica
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más rápida.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta. El detalle de los métodos para elaborar este resumen están descritos aquí: http://dx.doi.org/10.5867/medwave.2014.06.5997.
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Los resúmenes de evidencia siguen un riguroso proceso de revisión por pares interno.
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Patients with chronic kidney disease have higher cardiovascular risk than general population, a fact that has been linked to high homocysteine levels. Folic acid supplementation can reduce homocysteine levels, which would reduce cardiovascular events. However, there is controversy about the clinical effects of this measure. Searching in Epistemonikos database, which is maintained by screening 30 databases, we identified six systematic reviews comprising 13 trials addressing the question of this article. We combined the evidence using meta-analysis and generated a summary of findings following the GRADE approach. We concluded folic acid supplementation does not reduce the risk of myocardial infarction or stroke in patients with chronic kidney disease, and might have no effect on mortality.
 Autores:
Gonzalo A. Bravo-Soto[1,2], Trinidad Madrid[2,3]
Autores:
Gonzalo A. Bravo-Soto[1,2], Trinidad Madrid[2,3]

Citación: Bravo-Soto GA, Madrid T. Is folic acid supplementation useful for chronic kidney disease?. Medwave 2016;16(Suppl 5):e6591 doi: 10.5867/medwave.2016.6591
Fecha de publicación: 7/11/2016

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Heinz J, Kropf S, Domröse U, Westphal S, Borucki K, Luley C, Neumann KH, et al. B vitamins and the risk of total mortality and cardiovascular disease in end-stage renal disease: results of a randomized controlled trial. Circulation. 2010 Mar 30;121(12):1432-8. | CrossRef | PubMed |
Heinz J, Kropf S, Domröse U, Westphal S, Borucki K, Luley C, Neumann KH, et al. B vitamins and the risk of total mortality and cardiovascular disease in end-stage renal disease: results of a randomized controlled trial. Circulation. 2010 Mar 30;121(12):1432-8. | CrossRef | PubMed | Jardine MJ, Kang A, Zoungas S, Navaneethan SD, Ninomiya T, Nigwekar SU, et al. The effect of folic acid based homocysteine lowering on cardiovascular events in people with kidney disease: systematic review and meta-analysis. BMJ. 2012 Jun 13;344:e3533. | CrossRef | PubMed |
Jardine MJ, Kang A, Zoungas S, Navaneethan SD, Ninomiya T, Nigwekar SU, et al. The effect of folic acid based homocysteine lowering on cardiovascular events in people with kidney disease: systematic review and meta-analysis. BMJ. 2012 Jun 13;344:e3533. | CrossRef | PubMed | Kang A, Nigwekar SU, Perkovic V, Kulshrestha S, Zoungas S, Navaneethan SD, et al. Interventions for lowering plasma homocysteine levels in kidney transplant recipients. Cochrane Database Syst Rev. 2015 May 4;(5):CD007910. | CrossRef | PubMed |
Kang A, Nigwekar SU, Perkovic V, Kulshrestha S, Zoungas S, Navaneethan SD, et al. Interventions for lowering plasma homocysteine levels in kidney transplant recipients. Cochrane Database Syst Rev. 2015 May 4;(5):CD007910. | CrossRef | PubMed | Qin X, Huo Y, Langman CB, Hou F, Chen Y, Matossian D, et al. Folic acid therapy and cardiovascular disease in ESRD or advanced chronic kidney disease: a meta-analysis. Clin J Am Soc Nephrol. 2011 Mar;6(3):482-8. | CrossRef | PubMed |
Qin X, Huo Y, Langman CB, Hou F, Chen Y, Matossian D, et al. Folic acid therapy and cardiovascular disease in ESRD or advanced chronic kidney disease: a meta-analysis. Clin J Am Soc Nephrol. 2011 Mar;6(3):482-8. | CrossRef | PubMed | Qin X, Huo Y, Xie D, Hou F, Xu X, Wang X. Homocysteine-lowering therapy with folic acid is effective in cardiovascular disease prevention in patients with kidney disease: a meta-analysis of randomized controlled trials. Clin Nutr. 2013 Oct;32(5):722-7. | CrossRef | PubMed |
Qin X, Huo Y, Xie D, Hou F, Xu X, Wang X. Homocysteine-lowering therapy with folic acid is effective in cardiovascular disease prevention in patients with kidney disease: a meta-analysis of randomized controlled trials. Clin Nutr. 2013 Oct;32(5):722-7. | CrossRef | PubMed | Raval AD, Thakker D, Rangoonwala AN, Gor D, Walia R. Vitamin B and its derivatives for diabetic kidney disease. Cochrane Database Syst Rev. 2015 Jan 12;1:CD009403. | CrossRef | PubMed |
Raval AD, Thakker D, Rangoonwala AN, Gor D, Walia R. Vitamin B and its derivatives for diabetic kidney disease. Cochrane Database Syst Rev. 2015 Jan 12;1:CD009403. | CrossRef | PubMed | House AA, Eliasziw M, Cattran DC, Churchill DN, Oliver MJ, Fine A, et al. Effect of B-vitamin therapy on progression of diabetic nephropathy: a randomized controlled trial. JAMA. 2010 Apr 28;303(16):1603-9. | CrossRef | PubMed |
House AA, Eliasziw M, Cattran DC, Churchill DN, Oliver MJ, Fine A, et al. Effect of B-vitamin therapy on progression of diabetic nephropathy: a randomized controlled trial. JAMA. 2010 Apr 28;303(16):1603-9. | CrossRef | PubMed | House AA, Ehasziw M, Cattran DC, Churchill DN, Oliver MJ, Fine A, et al. Vitamin therapy for homocysteine accelerates loss of renal function in diabetic kidney disease. Journal of the American Society of Nephrology. 2009;20:80A. | Link |
House AA, Ehasziw M, Cattran DC, Churchill DN, Oliver MJ, Fine A, et al. Vitamin therapy for homocysteine accelerates loss of renal function in diabetic kidney disease. Journal of the American Society of Nephrology. 2009;20:80A. | Link | Carpenter MA, John A, Weir MR, Smith SR, Hunsicker L, Kasiske BL, et al. BP, cardiovascular disease, and death in the Folic Acid for Vascular Outcome Reduction in Transplantation trial. J Am Soc Nephrol. 2014 Jul;25(7):1554-62. | CrossRef | PubMed |
Carpenter MA, John A, Weir MR, Smith SR, Hunsicker L, Kasiske BL, et al. BP, cardiovascular disease, and death in the Folic Acid for Vascular Outcome Reduction in Transplantation trial. J Am Soc Nephrol. 2014 Jul;25(7):1554-62. | CrossRef | PubMed | Bostom AG, Carpenter M, Kusek J. Baseline characteristics of the folic acid for vascular outcome reduction in transplantation (FAVOURIT) trial. Journal of the American Society of Nephrology 2008;19(Abstracts Issue):883A. | Link |
Bostom AG, Carpenter M, Kusek J. Baseline characteristics of the folic acid for vascular outcome reduction in transplantation (FAVOURIT) trial. Journal of the American Society of Nephrology 2008;19(Abstracts Issue):883A. | Link | Bostom AG, Carpenter MA, Hunsicker L, Jacques PF, Kusek JW, Levey AS. Baseline characteristics of participants in the folic acid for vascular outcome reduction in transplantation (FAVORIT) trial. American Journal of Transplantation 2009;9(Suppl 2):429. | Link |
Bostom AG, Carpenter MA, Hunsicker L, Jacques PF, Kusek JW, Levey AS. Baseline characteristics of participants in the folic acid for vascular outcome reduction in transplantation (FAVORIT) trial. American Journal of Transplantation 2009;9(Suppl 2):429. | Link | Bostom AG, Carpenter MA, Hunsicker L, Jacques PF, Kusek JW, Levey AS, et al. Baseline characteristics of participants in the Folic Acid for Vascular Outcome Reduction in Transplantation (FAVORIT) Trial. Am J Kidney Dis. 2009 Jan;53(1):121-8. | CrossRef | PubMed |
Bostom AG, Carpenter MA, Hunsicker L, Jacques PF, Kusek JW, Levey AS, et al. Baseline characteristics of participants in the Folic Acid for Vascular Outcome Reduction in Transplantation (FAVORIT) Trial. Am J Kidney Dis. 2009 Jan;53(1):121-8. | CrossRef | PubMed | Bostom AG, Carpenter MA, Kusek JW, Hunsicker LG, Jacques P, Levey AS, et al. Homocysteine-lowering in chronic stable renal transplant recipients: the FAVORIT Trial. American Society of Nephrology Renal Week; 2009 Oct 27-Nov 1; San Diego, CA. 2009. | Link |
Bostom AG, Carpenter MA, Kusek JW, Hunsicker LG, Jacques P, Levey AS, et al. Homocysteine-lowering in chronic stable renal transplant recipients: the FAVORIT Trial. American Society of Nephrology Renal Week; 2009 Oct 27-Nov 1; San Diego, CA. 2009. | Link | Bostom AG, Carpenter MA, Kusek JW, Hunsicker LG, Pfeffer MA, Levey AS, et al. Rationale and design of the Folic Acid for Vascular Outcome Reduction In Transplantation (FAVORIT) trial. Am Heart J. 2006 Sep;152(3):448.e1-7. | PubMed |
Bostom AG, Carpenter MA, Kusek JW, Hunsicker LG, Pfeffer MA, Levey AS, et al. Rationale and design of the Folic Acid for Vascular Outcome Reduction In Transplantation (FAVORIT) trial. Am Heart J. 2006 Sep;152(3):448.e1-7. | PubMed | Bostom AG, Carpenter MA, Kusek JW, Levey AS, Hunsicker L, Pfeffer MA, et al. Homocysteine-lowering and cardiovascular disease outcomes in kidney transplant recipients: primary results from the Folic Acid for Vascular Outcome Reduction in Transplantation trial. Circulation. 2011 Apr 26;123(16):1763-70. | CrossRef | PubMed |
Bostom AG, Carpenter MA, Kusek JW, Levey AS, Hunsicker L, Pfeffer MA, et al. Homocysteine-lowering and cardiovascular disease outcomes in kidney transplant recipients: primary results from the Folic Acid for Vascular Outcome Reduction in Transplantation trial. Circulation. 2011 Apr 26;123(16):1763-70. | CrossRef | PubMed | Carpenter M, Bostom A, Hunsicker L, Ivanova A, Kasiske B, Kusek J, et al. Higher systolic blood pressure is associated with increased cardiovascular risk in patients with hypertension in the Folic Acid for Vascular Outcome Reduction in Transplantation trial fficacy of Folic Acid Therapy on the Progression of Chronic Kidney Disease. American Journal of Transplantation 2011;11(Suppl 2):375.
Carpenter M, Bostom A, Hunsicker L, Ivanova A, Kasiske B, Kusek J, et al. Higher systolic blood pressure is associated with increased cardiovascular risk in patients with hypertension in the Folic Acid for Vascular Outcome Reduction in Transplantation trial fficacy of Folic Acid Therapy on the Progression of Chronic Kidney Disease. American Journal of Transplantation 2011;11(Suppl 2):375.  Carpenter MA, Bostom A, Kusek J, Adey D, Cole E, House A, et al. Untreated CVD risk factors in chronic, stable kidney transplant recipients at baseline in the folic acid for vascular outcome reduction (FAVORIT) study. Journal of the American Society of Nephrology 2009;20:888A.
Carpenter MA, Bostom A, Kusek J, Adey D, Cole E, House A, et al. Untreated CVD risk factors in chronic, stable kidney transplant recipients at baseline in the folic acid for vascular outcome reduction (FAVORIT) study. Journal of the American Society of Nephrology 2009;20:888A.  Carpenter MA, Weir MR, Adey DB, House AA, Bostom AG, Kusek JW. Inadequacy of cardiovascular risk factor management in chronic kidney transplantation - evidence from the FAVORIT study. Clin Transplant. 2012 Jul-Aug;26(4):E438-46. | CrossRef | PubMed |
Carpenter MA, Weir MR, Adey DB, House AA, Bostom AG, Kusek JW. Inadequacy of cardiovascular risk factor management in chronic kidney transplantation - evidence from the FAVORIT study. Clin Transplant. 2012 Jul-Aug;26(4):E438-46. | CrossRef | PubMed | Troen AM, Scott TM, D'Anci KE, Moorthy D, Dobson B, Rogers G, et al. Cognitive dysfunction and depression in adult kidney transplant recipients: baseline findings from the FAVORIT Ancillary Cognitive Trial (FACT). J Ren Nutr. 2012 Mar;22(2):268-76.e1-3. | CrossRef | PubMed |
Troen AM, Scott TM, D'Anci KE, Moorthy D, Dobson B, Rogers G, et al. Cognitive dysfunction and depression in adult kidney transplant recipients: baseline findings from the FAVORIT Ancillary Cognitive Trial (FACT). J Ren Nutr. 2012 Mar;22(2):268-76.e1-3. | CrossRef | PubMed | Weiner DE, Carpenter MA, Levey AS, Ivanova A, Cole EH, Hunsicker L, et al. Kidney function and risk of cardiovascular disease and mortality in kidney transplant recipients: the FAVORIT trial. Am J Transplant. 2012 Sep;12(9):2437-45. | CrossRef | PubMed |
Weiner DE, Carpenter MA, Levey AS, Ivanova A, Cole EH, Hunsicker L, et al. Kidney function and risk of cardiovascular disease and mortality in kidney transplant recipients: the FAVORIT trial. Am J Transplant. 2012 Sep;12(9):2437-45. | CrossRef | PubMed | Weir MR, Gravens-Muller L, Costa N, Ivanova A, Manitpisitkul W, Bostom AG, et al. Safety events in kidney transplant recipients: results from the folic Acid for vascular outcome reduction in transplant trial. Transplantation. 2015 May;99(5):1003-8. | CrossRef | PubMed |
Weir MR, Gravens-Muller L, Costa N, Ivanova A, Manitpisitkul W, Bostom AG, et al. Safety events in kidney transplant recipients: results from the folic Acid for vascular outcome reduction in transplant trial. Transplantation. 2015 May;99(5):1003-8. | CrossRef | PubMed | Heinz J, Kropf S, Luley C, Dierkes J. Homocysteine as a risk factor for cardiovascular disease in patients treated by dialysis: a meta-analysis. Am J Kidney Dis. 2009 Sep;54(3):478-89. | CrossRef | PubMed |
Heinz J, Kropf S, Luley C, Dierkes J. Homocysteine as a risk factor for cardiovascular disease in patients treated by dialysis: a meta-analysis. Am J Kidney Dis. 2009 Sep;54(3):478-89. | CrossRef | PubMed | Jamison RL, Hartigan P, Kaufman JS, Goldfarb DS, Warren SR, Guarino PD, et al. Effect of homocysteine lowering on mortality and vascular disease in advanced chronic kidney disease and end-stage renal disease: a randomized controlled trial. JAMA. 2007 Sep 12;298(10):1163-70. | CrossRef | PubMed |
Jamison RL, Hartigan P, Kaufman JS, Goldfarb DS, Warren SR, Guarino PD, et al. Effect of homocysteine lowering on mortality and vascular disease in advanced chronic kidney disease and end-stage renal disease: a randomized controlled trial. JAMA. 2007 Sep 12;298(10):1163-70. | CrossRef | PubMed | Mann JF, Sheridan P, McQueen MJ, Held C, Arnold JM, Fodor G, et al. Homocysteine lowering with folic acid and B vitamins in people with chronic kidney disease--results of the renal Hope-2 study. Nephrol Dial Transplant. 2008 Feb;23(2):645-53. | PubMed |
Mann JF, Sheridan P, McQueen MJ, Held C, Arnold JM, Fodor G, et al. Homocysteine lowering with folic acid and B vitamins in people with chronic kidney disease--results of the renal Hope-2 study. Nephrol Dial Transplant. 2008 Feb;23(2):645-53. | PubMed | Righetti M, Ferrario GM, Milani S, Serbelloni P, La Rosa L, Uccellini M, et al. Effects of folic acid treatment on homocysteine levels and vascular disease in hemodialysis patients. Med Sci Monit. 2003 Apr;9(4):PI19-24. | PubMed |
Righetti M, Ferrario GM, Milani S, Serbelloni P, La Rosa L, Uccellini M, et al. Effects of folic acid treatment on homocysteine levels and vascular disease in hemodialysis patients. Med Sci Monit. 2003 Apr;9(4):PI19-24. | PubMed | Righetti M, Serbelloni P, Milani S, Ferrario G. Homocysteine-lowering vitamin B treatment decreases cardiovascular events in hemodialysis patients. Blood Purif. 2006;24(4):379-86. | PubMed |
Righetti M, Serbelloni P, Milani S, Ferrario G. Homocysteine-lowering vitamin B treatment decreases cardiovascular events in hemodialysis patients. Blood Purif. 2006;24(4):379-86. | PubMed | Armitage JM, Bowman L, Clarke RJ, Wallendszus K, Bulbulia R, Rahimi K, et al. Effects of homocysteine-lowering with folic acid plus vitamin B12 vs placebo on mortality and major morbidity in myocardial infarction survivors: a randomized trial. JAMA. 2010 Jun 23;303(24):2486-94. | CrossRef | PubMed |
Armitage JM, Bowman L, Clarke RJ, Wallendszus K, Bulbulia R, Rahimi K, et al. Effects of homocysteine-lowering with folic acid plus vitamin B12 vs placebo on mortality and major morbidity in myocardial infarction survivors: a randomized trial. JAMA. 2010 Jun 23;303(24):2486-94. | CrossRef | PubMed | Vianna AC, Mocelin AJ, Matsuo T, Morais-Filho D, Largura A, Delfino VA, et al. Uremic hyperhomocysteinemia: a randomized trial of folate treatment for the prevention of cardiovascular events. Hemodial Int. 2007 Apr;11(2):210-6. | PubMed |
Vianna AC, Mocelin AJ, Matsuo T, Morais-Filho D, Largura A, Delfino VA, et al. Uremic hyperhomocysteinemia: a randomized trial of folate treatment for the prevention of cardiovascular events. Hemodial Int. 2007 Apr;11(2):210-6. | PubMed | VITATOPS Trial Study Group. B vitamins in patients with recent transient ischaemic attack or stroke in the VITAmins TO Prevent Stroke (VITATOPS) trial: a randomised, double-blind, parallel, placebo-controlled trial. Lancet Neurol. 2010 Sep;9(9):855-65. | CrossRef | PubMed |
VITATOPS Trial Study Group. B vitamins in patients with recent transient ischaemic attack or stroke in the VITAmins TO Prevent Stroke (VITATOPS) trial: a randomised, double-blind, parallel, placebo-controlled trial. Lancet Neurol. 2010 Sep;9(9):855-65. | CrossRef | PubMed | Wotherspoon F, Laight DW, Turner C, Meeking DR, Allard SE, Munday LJ, et al. The effect of oral folic acid upon plasma homocysteine, endothelial function and oxidative stress in patients with type 1 diabetes and microalbuminuria. Int J Clin Pract. 2008 Apr;62(4):569-74. | CrossRef | PubMed |
Wotherspoon F, Laight DW, Turner C, Meeking DR, Allard SE, Munday LJ, et al. The effect of oral folic acid upon plasma homocysteine, endothelial function and oxidative stress in patients with type 1 diabetes and microalbuminuria. Int J Clin Pract. 2008 Apr;62(4):569-74. | CrossRef | PubMed | Wrone EM, Hornberger JM, Zehnder JL, McCann LM, Coplon NS, Fortmann SP. Randomized trial of folic acid for prevention of cardiovascular events in end-stage renal disease. J Am Soc Nephrol. 2004 Feb;15(2):420-6. | PubMed |
Wrone EM, Hornberger JM, Zehnder JL, McCann LM, Coplon NS, Fortmann SP. Randomized trial of folic acid for prevention of cardiovascular events in end-stage renal disease. J Am Soc Nephrol. 2004 Feb;15(2):420-6. | PubMed | Zoungas S, McGrath BP, Branley P, Kerr PG, Muske C, Wolfe R, et al. Cardiovascular morbidity and mortality in the Atherosclerosis and Folic Acid Supplementation Trial (ASFAST) in chronic renal failure: a multicenter, randomized, controlled trial. J Am Coll Cardiol. 2006 Mar 21;47(6):1108-16. | PubMed |
Zoungas S, McGrath BP, Branley P, Kerr PG, Muske C, Wolfe R, et al. Cardiovascular morbidity and mortality in the Atherosclerosis and Folic Acid Supplementation Trial (ASFAST) in chronic renal failure: a multicenter, randomized, controlled trial. J Am Coll Cardiol. 2006 Mar 21;47(6):1108-16. | PubMed | Eknoyan G, Lameire N, Eckardt KU, Kasiske BL, Wheeler DC, Levin A, et al. KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int. 2013. 3:5-14.
Eknoyan G, Lameire N, Eckardt KU, Kasiske BL, Wheeler DC, Levin A, et al. KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int. 2013. 3:5-14.  Kopple JD. National kidney foundation K/DOQI clinical practice guidelines for nutrition in chronic renal failure. Am J Kidney Dis. 2001 Jan;37(1 Suppl 2):S66-70. | PubMed |
Kopple JD. National kidney foundation K/DOQI clinical practice guidelines for nutrition in chronic renal failure. Am J Kidney Dis. 2001 Jan;37(1 Suppl 2):S66-70. | PubMed |