Este texto completo es la transcripción editada y revisada de una conferencia dictada en las Jornadas Latinoamericanas de Cáncer de Mama 2002, organizadas por la Escuela Latinoamericana de Mastología, la Federación Latinoamericana de Mastología y la Sociedad Chilena de Mastología.
Editor Científico: Dr. Hernando Paredes.
Introducción
El objetivo primario de la mamografía es detectar los cánceres clínicamente ocultos, en un estado precoz de su crecimiento, con la esperanza de interrumpir la historia natural de la enfermedad antes de que haya dado metástasis.
Está demostrado que el uso masivo de mamografía reduce la mortalidad por cáncer de mama en forma significativa. El último análisis publicado del screening sueco demuestra una reducción de la mortalidad por cáncer mamario en 50% (1).
La detección precoz exige el screening de mujeres asintomáticas, aparentemente sanas, y un radiólogo experto que no deje pasar cambios sutiles en una mamografía.
Estudios recientes demuestran que entre 15% y 56% de los cánceres que se detectan en screenig mamario corresponden a cánceres in situ, clínicamente ocultos (2).
Además de reducir la mortalidad por cáncer mamario, el diagnóstico precoz permite el uso de tratamientos menos agresivos.
Las lesiones no palpables se pueden presentar como :
I.- Lesiones Circulares u Ovaladas (nódulos).
II.- Microcalcificaciones.
III.- Asimetrías de Densidad.
Constituyen un problema de diagnóstico diferencial más que de percepción. Necesitan un estudio cuidadoso, ya que generalmente no es necesario hacer una biopsia quirúrgica.
Criterios diagnósticos:
A) Análisis del contorno:
B) Análisis de densidad:
Los tumores malignos infiltran el tejido circundante, lo que determina la indefinición de los bordes.
Generalmente, los nódulos bien delimitados son benignos, pero hay cánceres que se manifiestan también como nódulos bien delimitados, por ejemplo: carcinoma medular, coloideo, sarcoma, tumores intraquísticos, metástasis. Por lo tanto, siempre se debe hacer un estudio con métodos diagnósticos suplementarios, como ecotomografía y biopsia percutánea. Por otra parte, suele haber lesiones benignas que se presentan con contornos mal definidos; en estos casos, es importante evaluar la densidad de la lesión y usar otros métodos diagnósticos antes de llegar a una biopsia quirúrgica.
En orden de frecuencia decreciente, los tumores malignos que se presentan como lesiones circulares u ovaladas en la mamografía son:
El principal valor de encontrar microcalcificaciones en la mamografía es diagnosticar cáncer ductal in situ (CDIS).
Criterios diagnósticos: para diferenciar benigno de maligno.
I - Criterios primarios: nos dan una idea del tipo de cavidad en la que se formaron.
II - Criterio secundario: densidad (subjetivo, varía con la técnica y el tipo constitucional de la mama).
De acuerdo al sitio de origen de las microcalcificaciones, éstas se pueden localizar:
Pueden deberse a enfermedad maligna o benigna.
Microcalcificaciones malignas: son de gran valor para el diagnóstico radiológico del CDIS; 84% de los CDIS se presentan a la mamografía con microcalcificaciones, con o sin masa asociada.
El CDIS se divide en dos tipos:
1. CDIS de alto grado (tipo comedo o mal diferenciado); más agresivo, recurre más y más rápido, mayor asociación con microinvasión y progresa a invasivo más rápidamente. Crece más rápido que su suministro sanguíneo, por lo que se produce necrosis central y calcificaciones. En 94% de los casos, los CDIS de alto grado se calcifican.
Hay:
En las calcificaciones de alto grado, hay una estrecha relación entre las calcificaciones y las células malignas, lo que tiene importancia práctica al momento de decidir una biopsia percutánea.
2. CDIS de grado intermedio y bajo (no comedo, bien diferenciado); la necrosis es rara en el intermedio y no ocurre en los de bajo grado, la microinvasión es infrecuente y la recurrencia es más escasa. En 53% de los casos, estas lesiones se calcifican. Las calcificaciones más típicas son en puntatas, granulares, agrupadas, las que varían en tamańo, forma y densidad. No se deben a necrosis, sino por depósito de calcio en material secretorio de los conductos neoplásicos. Cuando las calcificaciones pasan de 15, generalmente hay polimorfismo.
En este tipo de cáncer, las calcificaciones no representan la extensión de la enfermedad. Es decir las células malignas se extienden más allá de las calcificaciones detectables en la mamografía; de ahí la importancia de la radiografía de la pieza operatoria y del estudio posterior de los márgenes por el patólogo.
Con gran frecuencia, los CDIS tienen componentes mixtos, lo que produce distintos tipos de microcalcificaciones; por otra parte, mientras más numerosas sean las microcalcificaciones, mayor probabilidad habrá de polimorfismo.
Las calcificaciones ductales benignas son: en secreciones retenidas, con o sin proliferación epitelial, o con galactoforitis (mastitis de células plasmáticas). Fibroadenomas o papilomas intraductales esclerosados y hialinizados.
Aunque estas calcificaciones pueden estar asociadas con malignidad, la mayoría representa procesos benignos. El diagnóstico diferencial puede ser difícil.
En el caso del carcinoma lobular in situ (CLIS), las microcalcificaciones no constituyen un hallazgo específico. El CLIS es un hallazgo de biopsia por otros motivos.
El carcinoma lobulillar invasivo constituye 3%-6% de los cánceres de mama. Sólo 10% presentarían microcalcificaciones.
Las calcificaciones lobulares benignas se deben principalmente:
Adenosis microquística: dilatación quística de los acinos. Las calcificaciones pueden estar en grupos, generalmente, de 5 mm o dispersas (cuando afecta lóbulos completos de una o las dos mamas).
Las calcificaciones son granulares, toscas, distinguibles unas de otras, como “piedras quebradas” o facetadas. El grupo presenta un aspecto mora, con pequeńos tabiques (tejido conectivo interquístico), y contorno lobulado.
También pueden existir calcificaciones puntatas, pero monomorfas y de tamańo uniforme, raras veces agrupadas.
Adenosis esclerosante: hay proliferación del tejido fibroso y mioepitelio que rodea el acino, la que causa compresión del lumen del lóbulo. Se asocia con microquistes. Presenta microcalcificaciones, estructura radial y la combinación de ambas. Las microcalcificaciones presentan gran polimorfismo determinado por quistes con calcio, que son distorsionados por la proliferación del mioepitelio y tejido fibroso. Los pequeńos quistes con calcio están deformados y las calcificaciones pueden verse lineales, curvadas o en forma de V, por lo que pueden verse como carcinoma intraductal. En casos difíciles, la solución es biopsia percutánea con aguja gruesa (core, mammotome) o biopsia quirúrgica.
Enfermedad microquística: en este caso, la dilatación de los acinos es mucho mayor. En la mamografía los quistes con calcio y cuerpos de psammoma se ven redondos, de 1-2 mm., en las dos placas o, como manchas de 2-5 mm, en la placa craneocaudal; en la placa lateral se ven con un nivel en “taza de té”, por la formación de un sedimento del calcio y cuerpos de psammoma que ocupan la parte inferior. Los grupos de estos quistes son redondeados o amorfos. Estos quistes se encuentran en asociación con quistes grandes. Muy frecuentemente coexiste con los otros dos tipos de adenosis.
Otras causas de calcificaciones lobulares son: papiloma parcialmente calcificado, fibroadenoma.
Criterios primarios
La escuela estaadounidense de radiología usa el sistema BIRADS.
De acuerdo a la forma: la escuela estadounidense de radiología las clasifica como sigue:
De acuerdo a la distribución, la escuela estadounidense de radiología las clasifica como sigue:
Son un problema de detección, más que de diagnóstico diferencial. Encontrar estas lesiones, cuando son pequeńas (menores de 1 cm), es un verdadero desafío. Aunque el diagnóstico mamográfico es bastante preciso, una vez detectada la lesión, el diagnóstico definitivo se hace sólo con examen microscópico.
La asimetría de densidad puede tener diversas causas:
1.-Asimetría causada por Parénquima Normal: está compuesta de tejido glandular y grasa. El diagnóstico se realiza con compresión localizada y magnificación si es necesario. Generalmente corresponden a:
2.-Asimetrías no específicas:
3.-Lesión definitiva:
1.-Lesión estrellada:
Cuando se encuentra una lesión estrellada que se mantiene con las compresiones localizadas, el paso siguiente es determinar si se trata de una “estrella blanca“ (carcinoma ductal invasor) o de una “estrella negra” (cicatriz radiada, necrosis grasa post traumática y a veces carcinoma lobular invasor). Esto exige una cuidadosa evaluación clínica, radiológica y microscópica.
Hay que preguntar si la paciente tiene historia de cirugía previa o de algún otro trauma, se debe examinar a la paciente para ver si el hallazgo mamográfico corresponde a una masa palpable (en las cicatrices radiadas no hay lesión palpable). Si se encuentra una masa palpable, la lesión se hace muy sospechosa de cáncer, por lo que se necesita biopsia aunque exista el antecedente de trauma.
En el análisis mamográfico de estas lesiones, lo más importante es que, en los tumores, la longitud de las espiculaciones está directamente relacionada con el tamańo de la lesión central, no así en las cicatrices radiadas. En los tumores va a haber poca variación de la apariencia mamográfica en las diferentes proyecciones.
En la mayoría de los casos, el diagnóstico de cicatriz postquirúrgica o necrosis grasa se puede hacer combinando la historia clínica con el análisis mamográfico. Habitualmente es necesario realizar biopsia.
Si el diagnóstico radiológico indica cicatriz radiada, es preferible hacer biopsia quirúrgica, ya que la biopsia percutánea puede subestimar el diagnóstico. En 20% a 30% de los casos, las cicatrices radiadas se asocian con malignidad.
1. Punción con aguja fina:
La punción con aguja fina tendría algunas ventajas sobre la aguja gruesa, como, por ejemplo, menos probabilidades de provocar complicaciones como hematoma o, rara vez, neumotórax.
Sin embargo, el uso clínico de este método ha sido cuestionado por la variabilidad de los resultados comunicados (4).
Cuando se excluyen del análisis las muestras insuficientes, el rango de sensibilidad es de 58,3% a 100% y el de especificidad es de 55% a 100%; el VPN es de 46,6% a 98,6%.
El procedimiento depende mucho del operador y, en especial, del citólogo que interpreta los frotis.
Los porcentajes de material insuficiente son muy altos y van de 0% a 34%, lo que ha reducido la aceptación de este método.
2. Biopsia percutánea con guía ultrasonográfica o estereotáxica:
La biopsia core (aguja de 14 G) con guía estereotáxica fue descrita por primera vez en 1990, por Parker, y la biopsia core guiada por ultrasonido, en 1993.
El desarrollo de estos métodos se vio potenciado por el gran número de biopsias quirúrgicas con resultados benignos y por la presión para bajar los costos.
La biopsia percutánea tiene varias ventajas sobre la biopsia radioquirúrgica en el diagnóstico de las lesiones mamarias sospechosas no palpables; por ejemplo, es un procedimiento ambulatorio, no deja cicatriz, necesita sólo anestesia local, es de menor costo (aproximadamente 1/3) y permite programar el tratamiento antes de la cirugía, lo que evita muchas veces un segundo acto quirúrgico (5) (6) (8).
La sensibilidad de la biopsia core con aguja 14 G se evaluó comparándola con la biopsia radioquirúrgica posterior. Los falsos negativos alcanzaron un promedio de 4,4% (5). La subestimación diagnóstica de hiperplasia ductal atípica (HDA) es de 31% a 88%, en distintas series; de CDIS es de 15% a 36%.
Las biopsias percutáneas con guía ultrasonográfica o estereotáxica también se pueden realizar con aguja de 11 G y sistema de vacío (Mammotome). Las ventajas de este último son que la muestra que se obtiene es más grande (97 mg. contra 17 mg. del core) y que la subestimación es menor, del orden de 18% (7).
3. Biopsia radioquirúrgica:
Se introdujo en 1965 y poco a poco se transformó en el método normal para resecar lesiones no palpables detectadas en mamografía. Hay diversos métodos de localización.
El fracaso parcial o total en la extirpación de la lesión se ha reportado entre 0% y 18% de los casos en los diferentes grupos (9).
Las causas de los fracasos, según las distintas publicaciones, son de diversos tipos. Se han seńalado factores mamográficos, de la propia localización, factores quirúrgicos o histológicos.
Para obtener buenos resultados es fundamental el trabajo en equipo y el rigor en el procedimiento, el que debe incluir siempre radiografía o ultrasonido de la pieza quirúrgica.
La localización se puede realizar con guía mamográfica, ultrasonográfica o estereotáxica y se usan agujas especiales diseńadas para el efecto.
En nuestro país la biopsia radioquirúrgica se usa ampliamente, ya que, en la mayoría de los casos, las pacientes tienen dificultades para acceder a la biopsia estereotáxica.
A continuación se proponen alternativas de trabajo para el manejo de las lesiones no palpables:
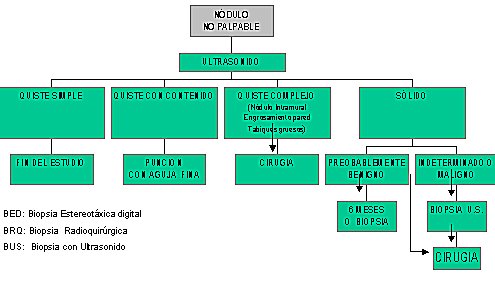
Algoritmo No. 1
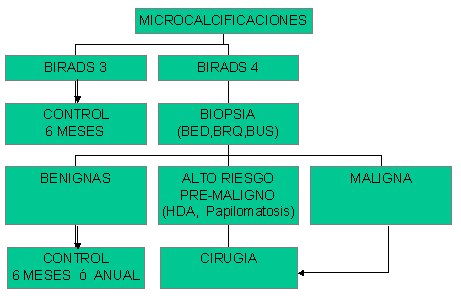
Algoritmo No. 2
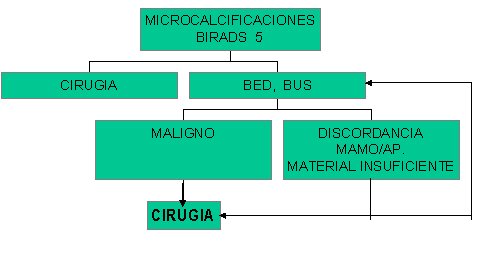
Algoritmo No. 3
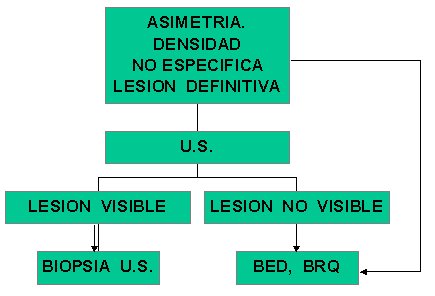
Algoritmo No. 4




 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de una conferencia dictada en las Jornadas Latinoamericanas de Cáncer de Mama 2002, organizadas por la Escuela Latinoamericana de Mastología, la Federación Latinoamericana de Mastología y la Sociedad Chilena de Mastología.
Editor Científico: Dr. Hernando Paredes.
 Expositora:
Dravna Razmilic[1]
Expositora:
Dravna Razmilic[1]

Citación: Razmilic D. Nonpalpable breast lesions. Medwave 2003 Jun;3(5):e3574 doi: 10.5867/medwave.2003.05.3574
Fecha de publicación: 1/6/2003

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión