Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso Internacional de Diabetes del Ni±o y del Adolescente, organizado por la Asociaci¾n Latinoamericana de Diabetes entre los dĒas 19 al 21 de abril de 2006. Directora: Dra. Gloria L¾pez.
La diabetes mellitus tipo 2 (DM 2) se comenz¾ a manejar hace diez a±os en el Hospital General de Ni±os Pedro de Elizalde, que se encuentra ubicado al sur de Buenos Aires y atiende a ni±os de bajos recursos de ese sector (Fig. 1). A continuaci¾n se presentarß la experiencia acumulada hasta la fecha en este establecimiento.
Figura 1. Frontis del Hospital General de Ni±os Pedro de Elizalde, Montes de Oca 40, Buenos Aires, Argentina
Las clasificaciones de la diabetes mellitus son cada vez mßs complicadas, pero el concepto bßsico establece que es un grupo de trastornos metab¾licos de diversas etiologĒas; que se caracteriza por la hiperglicemia cr¾nica; que ķsta acompa±a o es la causa de una alteraci¾n del metabolismo de los hidratos de carbono, grasas y proteĒnas; y que a corto o a largo plazo termina con trastornos micro y macrovasculares. La clasificaci¾n etiol¾gica que se utiliza en este momento es la de la ADA (American Diabetes Association), la que cataloga la diabetes tipo 1 autoinmune e idiopßtica; la diabetes mellitus tipo 2; otros tipos de diabetes, como la MODY y la diabetes transitoria del RNn, entre otras; y la diabetes mellitus gestacional.
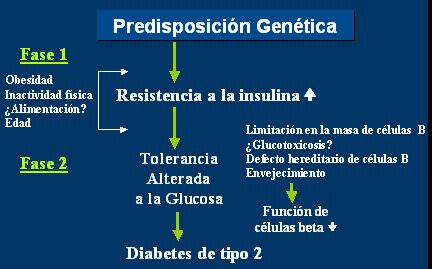
En cuanto a la historia natural de la diabetes tipo 2, siempre hay una predisposici¾n genķtica que se manifiesta por un aumento de la resistencia a la insulina o una disminuci¾n de la sensibilidad a la insulina, y que, en presencia de algunos factores como la obesidad, la inactividad fĒsica, la alimentaci¾n y la edad, va a provocar alteraciones en el metabolismo de la glucosa, que hoy se conocen como prediabetes o tolerancia alterada a la glucosa. Si este cuadro progresa, terminarß en diabetes tipo 2, con alteraciones de la funci¾n de la cķlula beta y, por tanto, insulinopenia (Fig. 2).
Figura 2. Historia natural de la diabetes mellitus tipo 2
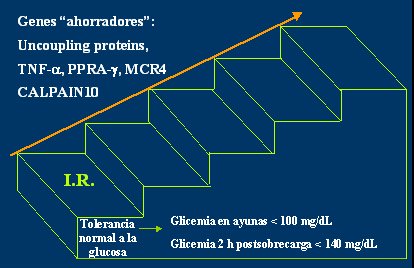
En la Figura 3 se ilustra la evoluci¾n de la enfermedad, en forma de una escalera cuyo primer escal¾n representa la insulinorresistencia, que estß determinada en forma genķtica, se relaciona con ciertos genes ahorradores y estß presente con tolerancia normal a la glucosa. Para hablar de diabetes debe haber hiperglicemia; no basta con la clĒnica, el valor de la glicemia es lo que hace el diagn¾stico. Si a esta persona, ni±o o adolescente ubicado en este primer escal¾n de insulinorresistencia, se le hace una glicemia en ayunas o a las 2 horas de recibir una sobrecarga de glucosa de 1,75 g/kg, con un mßximo de 75 g, diluida en agua o tķ al 20%, sus valores serßn normales, es decir, tendrß una glicemia en ayunas menor de 100 mg/dL o una glicemia dos horas post sobrecarga, menor de 140 mg/dL.
Figura 3. Influencia de la genķtica en el paso de insulinorresistencia a diabetes mellitus tipo 2 (J Clin Endocrinol Metab 2004)
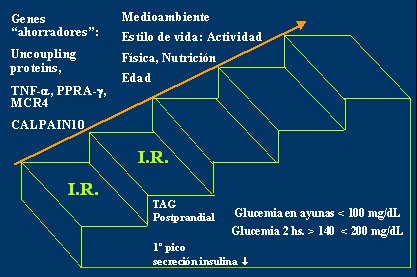
Posteriormente, debido a factores del medio ambiente debidos por el nuevo estilo de vida, que se caracterizan por menor actividad fĒsica, mayor ingesta cal¾rica y edad, en el adolescente generalmente aparece una tolerancia a la glucosa postprandial alterada; es decir, cuando se sobrecarga al individuo, se mantiene la glicemia de ayuno postprandial normal, menor de 100, pero la glicemia a las 2 horas post sobrecarga estß entre 140 y 200 mg/dl y la primera punta de secreci¾n de insulina es dķbil (Fig. 4).
Figura 4. Influencia del medio ambiente en la progresi¾n desde insulinorresistencia a diabetes mellitus tipo 2 (J Clin Endocrinol Metab 2004)
La insulinorresistencia, o disminuci¾n de la sensibilidad a la insulina, se define como la incapacidad de la insulina, en concentraciones normales, a) para adecuar la disponibilidad perifķrica de la glucosa; b) para suprimir la glucogenolisis hepßtica, se hace incapaz de sostener la glucogķnesis hepßtica; y c) para inhibir la producci¾n de lipoproteĒnas de muy baja densidad. La incapacidad para adecuar la disponibilidad perifķrica refleja que se estß perdiendo la homeostasis, ya que el organismo, en situaci¾n normal, se las arregla para mantenerse entre 100 y 140 ml/dl; en cambio, ahora, la insulina es incapaz de cumplir estas condiciones.
La insulinorresistencia va a dar origen a una hiperinsulinemia. Todos tenemos insulinemias en ayuno normales, hasta que entra este factor que origina una insulinemia mayor de 15 uU/ml y mayor de 75 uU/ml post sobrecarga a las 2 horas, con una punta mayor de 150 uU/ml (Reaven GM J Clin Endocrinol Metab 1993). El HOMA es un Ēndice que se calcula mediante la f¾rmula glicemia (mg/dL/18) por insulinemia basal (uU/ml), dividido por 22,5 y que, seg·n Matthews, se considera normal si resulta un valor menor de 3,8. Por lo tanto, la medici¾n de la homeostasis de la glicemia relaciona la glicemia en ayunas con la insulinemia en ayunas.
Todos los seres humanos podrĒan desarrollar insulinorresistencia, pero esto ocurre s¾lo en algunos que son los individuos que presentan factores como antecedentes familiares (Goran MI. J Clin End Metab 2003); genķtica y peso al nacer (Kolterman OG. J Clin Invest 1980); sexo: las mujeres son mßs insulinorresistentes (Travers SH J Clin End Metab 1995); raza (The Bogalusa Heart Study. Arslanian S. J Clin Metab 2003); y pubertad (Arslanian SA., Diabetes 1994; Goran MI, Diabetes 2001).
Entre los factores que determinan la insulinorresistencia, los antecedentes familiares son fundamentales: el factor de predisposici¾n bßsico es el de los genes relacionados con la secreci¾n de insulina; en los estudios familiares se encuentra historia de DM 2 en el primer y segundo grado de parentesco, en 74% a 100% de los casos; y en los indios pima menores de 25 a±os de edad, se ha descrito la DM 2 exclusivamente en individuos con al menos uno de los padres con DM 2 (Kapriel Danadian, Diabetes Care, 1999; Goran Diabetes Care, 2002.
En cuanto a la genķtica, la hip¾tesis del fenotipo ahorrador establece que tienen mayor riesgo los ni±os que nacen con bajo peso para la edad gestacional (hecho frecuente en las poblaciones latinoamericanas) y que experimentan una ganancia brusca de peso en el perĒodo postnatal. Este hecho se debe a que, frente a un medio ambiente agresivo, estos ni±os se adaptan para sobrevivir mediante una respuesta que luego va a actuar en su contra, porque va a contribuir al desarrollo de DM 2, insulinorresistencia y enfermedades metab¾licas, fen¾meno descrito por Barker (Diabetologia 1992; 35: 595).
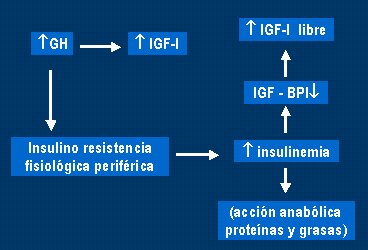
Respecto a la raza, se ha comprobado que los ni±os afroamericanos sanos tienen mßs hiperinsulinemia e insulinorresistencia, y menos sensibilidad que sus pares blancos, ya sean pre p·beres o p·beres (Kapriel Danadian, Diabetes Care, 1999); Arslanian SA, Diabetes, 2002). En los mexicanos tambiķn ocurre lo mismo. En la pubertad, la insulinorresistencia fisiol¾gica puede causar aumento de la insulinemia, que tiene una acci¾n anab¾lica de proteĒnas y grasas (Fig. 5).
Figura 5. Insulinorresistencia fisiol¾gica de la pubertad
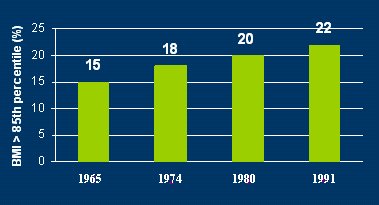
La genķtica, igual que en la diabetes mellitus tipo 1, por ahora no se puede evitar, pero sĒ es posible evitar la DM 2, porque entre los mecanismos que la causan hay varios que se pueden controlar, como la obesidad, el sedentarismo y, seg·n algunos autores, el tipo de alimentaci¾n. La obesidad se puede definir, en forma simplificada, como un ac·mulo excesivo de grasa corporal. Se habla de riesgo de obesidad cuando el peso del individuo estß sobre el percentil 85, el Ēndice de masa corporal (MC) es mayor de 25 y el z score estß entre 2 y 2,5; y se entiende por obesidad que el peso estķ sobre el percentil 95, el IMC sea mayor de 30 y el z score, mayor de 2,5. En los ·ltimos a±os, la prevalencia de la obesidad, estimada por los valores medios de IMC, ha ido en aumento en todo el mundo (Fig. 6).
Figura 6. Prevalencia de obesidad en ni±os de 6 a 11 a±os en Estados Unidos, seg·n valores medios de IMC (NHANES)
El sedentarismo tambiķn ha aumentado notablemente. Todos los ni±os ven televisi¾n y juegan con videojuegos, y, debido a los peligros de la calle, los padres prefieren mantener a los ni±os dentro del hogar, aun a costa de reducir su actividad fĒsica espontßnea. Se ha demostrado que en ciertos grupos ķtnicos la prevalencia de DM 2 en personas inactivas es dos a tres veces mayor que en sujetos activos de la misma poblaci¾n (Kryska AM, La Porte RE. Diabetologia 1993; 35: 863) y que, en individuos con tolerancia a la glucosa alterada, la incidencia de DM 2 disminuye gracias al ejercicio (Pan XR, Li GW Diabetes Care 1997; 20: 537). En cuanto a la alimentaci¾n, algunos autores afirman que el problema no estß solamente en el aumento del valor cal¾rico total, sino tambiķn en el aumento de las grasas e hidratos de carbono refinados, asĒ como el menor contenido de fibras vegetales.
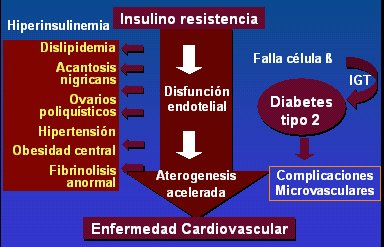
La insulinorresistencia produce hiperinsulinemia, dislipidemia, acantosis nigricans, ovario poliquĒstico, hipertensi¾n arterial, obesidad central y, en el ßmbito cardiovascular, disfunci¾n endotelial, aterogķnesis acelerada, fibrinolisis anormal y enfermedad cardiovascular (Fig. 7).
Figura 7. Consecuencias de la insulinorresistencia
Entre estas consecuencias, se debe recordar que, para el National Cholesterol Education Panel, la concentraci¾n deseable de colesterol total es menos de 170 mg/dl; de LDL, menos de 110 mg/dl; de HDL, mßs de 45 mg/dl; de triglicķridos en menores de 10 a±os, menos de 75 mg/dl, y menos de 90 mg/dl en ni±os de 10 a 19 a±os. En cuanto a la acantosis, que tanto preocupa a las adolescentes, es una papilomatosis e hiperqueratosis que se correlaciona con el grado de insulinorresistencia y que se presenta, en general, en las zonas de roce: axila, nuca, pliegue cubital, ingle, ombligo, codos, surco submamario, etc. En lo que se refiere al sĒndrome de ovario poliquĒstico, es importante recordar que afecta a entre 4% y 12 % de las mujeres en edad reproductiva y que se debe sospechar en las adolescentes con hiperandrogenismo. Por ·ltimo, la hiperinsulinemia puede provocar aumento de la presi¾n arterial mediante la reabsorci¾n de sodio y la activaci¾n del sistema simpßtico, y debido a que los ßcidos grasos libres inducen la sensibilidad adrenķrgica y antagonizan la vasodilataci¾n mediada por oxido nĒtrico.
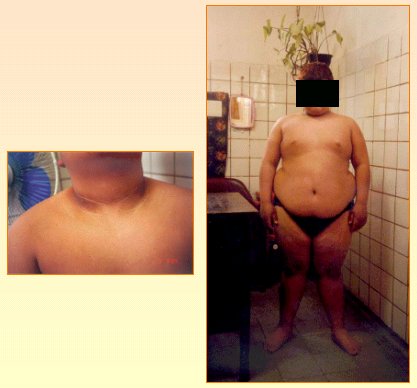
En el esquema de los escalones, en el primer escal¾n estß la tolerancia anormal a la glucosa en ayunas, es decir, valores entre 100 y 126, con glicemia a las 2 horas post sobrecarga entre 140 y 200. En el caso de un paciente de 12 a±os de edad (Fig. 8) con antecedentes de DM 2 en los padres y en los abuelos, acantosis nigricans marcada, presi¾n arterial de 130/85, IMC de 31 y glicemia de 116mg/dL, o sea que es intolerante, pero la insulina es de 28 uU/ml (mayor de 15 uU/ml y el HOMA estß en 8,13. A los 30 minutos post sobrecarga, la glicemia sube a 160mg/dl y la insulina a 135 uU/ml, pero logra manejarlo y llega a los 120 minutos con una glicemia de 74 mg/dl y una insulina de 16 uU/ml.
Figura 8. Caso clĒnico de intolerancia a la glucosa (detalle en el texto)
Los valores normales, como ya se dijo, son 100 mg/dL o menor para la glicemia en ayunas y 140 mg/dL o menor a las 2 horas post sobrecarga; y la tolerancia alterada se define por la glicemia en ayunas entre 100 y 126 mg/dL y la de 2 horas post sobrecarga, mayor de 140 y menor de 200 mg/dL. AsĒ se llega al cuarto escal¾n, donde ya estß presente la DM 2 y luego al quinto escal¾n, en el que se agrega insulinopenia (Fig. 9). AquĒ ya se manifiesta la clĒnica de la DM 2, con polidipsia, poliuria, polifagia, pķrdida de peso y cambio de carßcter en los ni±os, mßs una glicemia casual igual o mayor de 200 mg/dl; glicemia en ayunas de 126 mg/dl o mßs, o una glicemia a las 2 horas post sobrecarga de 200 mg/dl o mßs.
Figura 9. Evoluci¾n de insulinorresistencia a prediabetes y DM2
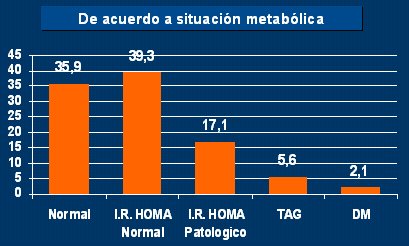
En nuestro servicio se hizo un estudio en 235 pacientes que consultaron entre enero y diciembre de 2004, con edad media de 11,4 a±os e IMC mayor del percentil 95, en quienes se hizo prueba de tolerancia oral a la glucosa (PTOG), glicemia e insulinemia basal y a los 120 minutos. El HOMA (Fig.10) fue normal en 35,9% de los pacientes; 56% de ellos tuvieron insulinorresistencia; la mayorĒa tenĒan HOMA normal; otros, HOMA alterado; 5,6% tenĒan tolerancia alterada a la glucosa y 2%, diabetes.
Figura 10. HOMA, TAG Y DM en pacientes obesos que concurrieron durante 2004 al Servicio Nutrici¾n y Diabetes del Hospital Pedro de Elizalde (ME. Andres, M. Ferraro, P. Duran, O. Ramos)
En el mundo, se prevķ que el n·mero de personas con DM 2 aumentarß a 121 millones en 2010 y a 300 millones en 2025. En los ni±os, la DM 2 se describi¾ en 1992 en Jap¾n; en 1993 en China; en 1996 en Libia, Estados Unidos y Australia; en 1997 en Bangladesh; en 1999 en Nueva Zelanda y en 2000 en Gran Breta±a. En nuestro servicio no existĒa este problema antes de 1994, pero desde entonces han aparecido mßs casos cada a±o. Se debe estudiar a todos los ni±os que tengan sobrepeso (IMC sobre el percentil 85 seg·n edad y sexo); historia familiar de DM 2 en primer o segundo grado; insulinorresistencia o condiciones asociadas como acantosis nigricans, hipertensi¾n, dislipidemia y ovario poliquĒstico; ademßs de la edad de inicio desde los 10 a±os. El estudio consiste en examen clĒnico, con ķnfasis en la presi¾n arterial; glicemia de ayuno y a las 2 horas post sobrecarga; PTOG; glicemia e insulinemia; perfil lipĒdico (colesterol total, HDL, LDL y triglicķridos); y HbA1c.
Los pacientes con insulinorresistencia solamente necesitan terapia nutricional y ejercicio, lo que significa que deben consultar a la psic¾loga y a la nutricionista; los pacientes que tienen hiperglicemia necesitan dieta, ejercicio y, si es necesario, hipoglicemiantes orales. Hoy se suelen indicar estos fßrmacos apenas se detecta la insulinorresistencia, pero el sentido com·n indica que primero se debe tratar de lograr que el paciente modifique su estilo de vida. Aquellos pacientes que entran en cetoacidosis, que prßcticamente siempre es cetosis, es decir, el pH es superior a 7,30 y el bicarbonato es superior a 15, se deben hospitalizar para recibir el tratamiento habitual, con el cual la glicemia bajarß rßpidamente. Despuķs de iniciar el tratamiento con insulina, algunos pacientes se mantienen equilibrados con dieta y ejercicio, pero algunos necesitan hipoglicemiantes orales.
El ni±o que no baja de peso y no mejora con la dieta y el ejercicio tiene mal pron¾stico, como ocurri¾ con un paciente que acudi¾ en noviembre de 1999 con hiperglicemia, glucosuria y cetonuria, a pesar de lo cual, su perfil lipĒdico era casi normal. La Hb glicosilada era de 9,6 %. En este paciente el tratamiento empez¾ con insulina NPH 10 U a.d. y 4 U a.c, mßs correcciones con insulina corriente, seg·n necesidad. Pesaba 69,5 kilos y lleg¾ como mßximo a 37 unidades, es decir, media unidad por kilo. Todo esto, junto con un plan alimentario hipocal¾rico. Luego de 45 dĒas de tratamiento se suspendi¾ la insulina y la glicemia baj¾ progresivamente hasta llegar a lo normal, a los 2 a±os y medio, con un IMC de 24 y una Hb glicosilada de 4,5. La acantosis desapareci¾ y, en la curva de tolerancia, la glicemia basal fue de 83 mg/dl; a los 30 minutos, 130 mg/dl; a los 60 minutos, 108 mg/dl; y a las 2 horas, 63 mg/dl. La curva de insulina tenĒa un nivel basal de 6,6 UI/mL; a los 30 minutos fue de 35,5 UI/mL; a los 60 minutos, de 49,2 UI/mL; y a los 120 minutos, de 16,9 UI/mL.
Pero no siempre se logran estos resultados. Otro paciente desapareci¾ despuķs del tratamiento con plan de alimentaci¾n hipocal¾rico, actividad fĒsica e insulina, y volvi¾ despuķs de seis a siete meses, otra vez obeso, por lo que necesit¾ metformina. Y en otro caso, a·n peor, el paciente tambiķn lleg¾ con cetosis, hipertensi¾n y dislipidemia. Por lo tanto, pacientes con el mismo cuadro clĒnico tienen distinto grado de adhesi¾n al tratamiento; por eso se debe iniciar el tratamiento con insulina, porque para la familia esto significa riesgo y enfermedad en cambio, si se indica s¾lo ejercicio, la familia no le da mayor importancia. El tratamiento con dieta y ejercicio se considera un ķxito cuando el paciente frena la ganancia de peso, crece en el percentil adecuado y mantiene la glicemia en ayunas en menos de 126 mg/dL y laHbA1c en menos de 7%. Sin embargo, aunque el tratamiento tenga ķxito, se deben realizar evaluaciones peri¾dicas a intervalos de no mßs de dos meses, para reforzar la modalidad de tratamiento y revisar la automonitorizaci¾n de la glicemia, glucosuria y cetonuria. El paciente debe mantener contacto casi permanente con el equipo multidisciplinario. Cuando el tratamiento no tiene ķxito, se debe tratar como una diabetes mellitus tipo 1.
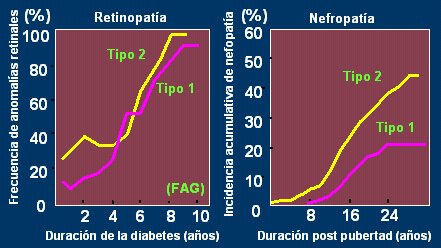
En Jap¾n (Fig. 11), los ni±os con diabetes tipo 2 llegan a retinopatĒa y nefropatĒa en mayor porcentaje que los diabķticos tipo 1, con el mismo tiempo de evoluci¾n, lo que significa que no es una enfermedad banal: al contrario, el paciente con diabetes tipo 2 tambiķn va a tener complicaciones y en forma temprana.
Figura 11. Complicaciones en ni±os japoneses con diabetes tipo 1 y tipo 2. A: frecuencia de anomalĒas retinales seg·n duraci¾n de la diabetes (Yamamoto T. et al J. Jpn Soc Opthalmol 1979). B: incidencia acumulativa de nefropatĒa seg·n duraci¾n de la enfermedad post pubertad (Yokoyama H. 2000)
La investigaci¾n de la diabetes tipo 2 en la edad escolar parte con la determinaci¾n de glucosuria matinal: si es positiva, se debe hacer una curva simplificada de tolerancia a la glucosa y si ķsta es positiva, se hace la curva regular de tolerancia oral a la glucosa con insulinemia, ademßs de la Hb glicosilada y un estudio de lĒpidos.
El Bogalusa Heart Study demostr¾ que la obesidad y el sedentarismo en el ni±o y el adolescente son los mejores predictores de riesgo de desarrollar una constelaci¾n de des¾rdenes metab¾licos y hemodinßmicos, entre ellos la DM 2 y las enfermedades cardiovasculares. En consecuencia, la obesidad, cuya tendencia secular mundial va en aumento, se debe considerar como un problema de Salud P·blica. La prevenci¾n y la intervenci¾n precoz, para evitar el aumento de peso en las primeras etapas de la vida, debe ser la base de una de las polĒticas sanitarias de mßxima importancia y los mķdicos pediatras, que son los ·ltimos mķdicos de familia, cumplen un papel fundamental en la tarea de impedir que un ni±o de dos a±os de edad, con buenos hßbitos alimentarios y buen peso, se convierta en los a±os siguientes en un paciente obeso.













 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso Internacional de Diabetes del Ni±o y del Adolescente, organizado por la Asociaci¾n Latinoamericana de Diabetes entre los dĒas 19 al 21 de abril de 2006. Directora: Dra. Gloria L¾pez.
 Expositora:
Olga Ramos[1]
Expositora:
Olga Ramos[1]

Citaci¾n: Ramos O. Type 2 diabetes mellitus in children and adolescents. Medwave 2006 Sep;6(8):e3421 doi: 10.5867/medwave.2006.08.3421
Fecha de publicaci¾n: 1/9/2006

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n