Este texto completo es la transcripciůn editada y revisada de una conferencia dictada en el curso Realidad Nacional en el Uso de Terapia Biolůgica en Enfermedad Inflamatoria Intestinal, organizado por la Agrupaciůn Chilena de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa de la Sociedad Chilena de GatroenterologŪa, el dŪa 14 de diciembre de 2006. Moderador: Dr. Roque Saenz.
Antes de exponer las recomendaciones actuales sobre el uso de infliximab en Colitis Ulcerosa (CU), es importante seŮalar que, al aŮo de una crisis, aproximadamente 25% de los pacientes serŠn dependientes de esteroides y que, de los pacientes que responden a esteroides, alrededor de 30% necesitarŠn cirugŪa al aŮo de evoluciůn (1). Por otra parte, el uso de inmunosupresores como estrategia terapťutica en pacientes con Enfermedades Inflamatorias Intestinales (EII) ha ido aumentando, como lo demuestra un estudio publicado en 2005, en el cual se observů que la probabilidad de utilizar azatioprina fue de 0,13 en 1978 y de 0,56 en 2002. Pese a este aumento, el riesgo de necesitar cirugŪa no cambiů en forma significativa durante este perŪodo, manteniťndose en alrededor de 0,35 (2). Por lo tanto, se puede concluir que aunque los inmunosupresores (azatioprina, metrotexato entre otros) son una terapia vŠlida en el tratamiento de las EII, en ningķn caso son la estrategia ideal para estos pacientes.
El conocimiento de la patogťnesis de la EII ha mostrado importantes avances en el ķltimo tiempo: hoy se sabe que el factor genťtico juega un rol importante en la patogťnesis de las EII. Como ejemplo estŠ el polimorfismo en el gen NOD2/CARD15, localizado en el cromosoma 16. Este gen posee un importante rol en el reconocimiento de ciertas componentes de bacterias ubicadas en el intestino; las mutaciones en este gen han sido descritas principalmente en pacientes con Enfermedad de Crohn (EC). Tambiťn se han demostrado alteraciones inmunolůgicas locales a nivel de la respuesta innata. Estudios han seŮalado que pacientes con EII presentan alteraciones inmunolůgicas a nivel de las cťlulas de Paneth, de las alfa-defensinas y de la barrera epitelial. Por ķltimo, ha habido interesantes avances en el estudio de las bacterias y el efecto de los probiůticos, prebiůticos y simbiůticos en la evoluciůn de estos pacientes (3). Sin embargo, la fisiopatologŪa de la EII aķn permanece incierta. De hecho, publicaciones del aŮo 2006 hablan de la importancia del linfocito T-17 y de la interleuquina- 23 en la EII, lo que indica que es probable que en los průximos aŮos existan nuevos avances en la patogťnesis y tratamiento de las EII (4) (Fig.1).
Figura 1. FisiopatologŪa de la enfermedad inflamatoria intestinal (3).
Al analizar el efecto de infliximab en las EII hay que tener presente el tipo de enfermedad inflamatoria que se estŠ evaluando. Por ejemplo, existe bastante evidencia sobre el papel que cumple el infliximab en el tratamiento de la EC. A continuaciůn analizaremos la evidencia del efecto de infliximab en CU, la evoluciůn de los pacientes tratados con infliximab y, por ķltimo, los efectos adversos del fŠrmaco en este grupo especŪfico de pacientes con EII.
Primero se debe mencionar el rol del factor de necrosis tumoral alfa (TNF-alfa) en la CU. Los primeros estudios mostraron que pacientes con CU no presentaban niveles elevados de este factor; sin embargo, un estudio realizado por Komatsu demostrů que pacientes con CU presentaban niveles de TNF-alfa muy cercanos a los de pacientes con EC (Fig. 2) (5). Sin duda que los niveles de TNF-alfa dependerŠn de la severidad del cuadro clŪnico, endoscůpico e histolůgico. Se ha demostrado que en pacientes con CU grave, los niveles de TNF-alfa son significativamente mŠs elevados que en los individuos sin colitis y en los pacientes con CU en etapa de remisiůn o con actividad leve a moderada (6).
Figura 2. TNF-alfa y colitis ulcerosa (5).
Aunque las primeras evidencias sobre el efecto de infliximab en pacientes con CU aparecieron en 2001, el nķmero de pacientes incluidos en estos trabajos era demasiado pequeŮo para poder sacar conclusiones definitivas. AdemŠs, la metodologŪa utilizada en los estudios era muy diferente, tanto desde el punto de vista clŪnico como endoscůpico. Sůlo a partir del aŮo 2005, con los estudios de Rutgeerts y Sandborn, se pudieron obtener conclusiones sobre el papel de Infliximab en el tratamiento de la CU (Tabla I).
En lo que se refiere a estudios abiertos, hay al menos tres trabajos interesantes. El primero se publiců en Am J Gastroenterol en 2002 y, aunque se incluyeron sůlo 27 pacientes, los resultados fueron bastante claros; la tasa de respuesta fue elevada: 44% de los casos presentaron remisiůn completa y en 22% hubo respuesta parcial, lo que significa una mejorŪa importante en el pronůstico de los pacientes con CU (7) (Tabla II).
Tabla II. Respuesta clŪnica a tratamiento con infliximab (7).
El 2006 apareciů en J Clin Gastroenterol un pequeŮo estudio, realizado en 12 pacientes hospitalizados por CU severa, de los cuales 9 (75%) no respondieron a la terapia con infliximab y tuvieron que ir a cirugŪa (colectomŪa); los 3 pacientes que respondieron pudieron abandonar los esteroides (8). Esto indica que se requieren mŠs estudios para poder determinar cuŠl es el grupo de pacientes con CU que mŠs se beneficia (Fig. 3).
Figura 3. Respuesta a infliximab (8).
En cuanto a estudios controlados, en 2004 se publiců un estudio con 13 pacientes con respuesta a tratamiento esteroidal, en los que se evaluů la respuesta a infliximab o prednisolona y se comprobů que la respuesta en ambas estrategias fue similar, de modo que infliximab permanece como una propuesta interesante (9). Por otra parte, en un estudio publicado el 2004, efectuado en 20 pacientes dependientes de esteroides, los autores comprobaron que infliximab fue al menos tan efectivo como los esteroides en pacientes con CU grave a moderada dependiente de esteroides, evitando los efectos adversos y complicaciones secundarias a los corticoides (10).
En un estudio realizado por Probert en el aŮo 2003 en pacientes refractarios a tratamiento esteroidal, no se encontrů un efecto positivo; solamente se evaluů la evoluciůn a las seis semanas, al cabo de las cuales hubo 30% de mejorŪa en los que usaron placebo y aproximadamente 40% en los que usaron infliximab. La diferencia no fue significativa (p< 0,76), probablemente porque el nķmero de pacientes incluidos fue de sůlo 45 pacientes (11). Posteriormente, en el Gastroenterology de diciembre de 2005 apareciů alguna evidencia de que infliximab podrŪa ser una estrategia ķtil en pacientes con CU refractaria. En ese estudio se incluyeron 45 pacientes; 17 pacientes entre 24 (71%) que usaron infliximab y 7 pacientes entre 21 (33%) que recibieron placebo, no necesitaron cirugŪa en el plazo de un mes. A los tres meses, que fue el punto de corte de los casos, 70% de los pacientes con infliximab necesitaron sůlo manejo mťdico, versus 33% de los que recibieron placebo, lo que sugiere que este fŠrmaco permitirŪa ofrecer a los pacientes una mejorŪa nutricional y evitar las complicaciones y los efectos adversos de otros fŠrmacos, como los esteroides (Fig. 4). Hay que tener en consideraciůn que los autores afirmaron categůricamente que no hubo diferencia entre usar infliximab o placebo en pacientes con CU fulminante; esto es importante tenerlo presente al momento de evaluar quť pacientes con CU pueden ser candidatos a este medicamento (12).
Figura 4. Efecto de infliximab en pacientes refractarios a tratamiento esteroidal endovenoso (12).
En la revista NEJM de diciembre del 2005 se publiců el diseŮo de dos estudios, cada uno realizado con 364 pacientes con CU. En el ACT 1 (Active Ulcerative Colitis Trial 1), los pacientes se asignaron en forma aleatoria a tres grupos de tratamiento: uno con placebo y dos con infliximab, en dosis de 5 mg ů 10 mg a las 0, 2 y 6 semanas, y luego cada 8 semanas hasta la semana 46, con evaluaciůn a la semana 54. En el segundo grupo o estudio ACT 2 (Active Ulcerative Colitis Trial 2), compuesto por 364 pacientes, se hizo lo mismo, con la diferencia de que se administrů infliximab por un perŪodo mucho mŠs corto, a las 0, 2, 6, 14 y 22 semanas, con evaluaciůn a la semana 30. La otra diferencia fue que en el estudio ACT2 se incluyů a pacientes que no respondieron o que desarrollaron tolerancia al uso de mezalazina o 5-ASA derivados (13). Los resultados mostraron que la respuesta a infliximab, en cualquiera de las dos dosis, fue mejor que la respuesta a placebo a las 8 semanas, y que la tendencia se mantuvo a las 52-54 semanas; por lo tanto, se puede decir que hubo una respuesta, desde el punto clŪnico, endoscůpico e histolůgico (Tabla III) (14). En relaciůn con la remisiůn y con el hecho de abandonar el uso crůnico de esteroides, que es uno de los objetivos que se persigue con las nuevas terapias, en solamente 25% de los pacientes que lograron remisiůn se pudo suspender los esteroides, por lo que infliximab no alcanzů este objetivo. En el ACT 2, a la semana 8 tambiťn hubo una diferencia significativa entre infliximab 5 ů 10 mg y placebo, pero, igual que en el ACT 1, el grupo de pacientes que entraron en remisiůn y se mantuvieron sin esteroides tambiťn fue escaso.
Tabla III. Resultados de los estudios ACT (Active Ulcerative Colitis Trial) (14).
El tercer estudio fue publicado en enero de este aŮo en el Alimentary Pharmacology Therapeutics. Se trata de un metaanŠlisis de 34 estudios aleatorios en los que se comparů infliximab con placebo o esteroides y se concluyů que 53% de los pacientes que usaron infliximab tuvieron respuesta positiva a largo plazo, versus 24% en los tratados con placebo. …ste es el primer artŪculo que determina el nķmero de pacientes que hay que tratar para lograr una mejorŪa o efecto positivo con el tratamiento, nķmero que es de 3 a 5. AdemŠs, 40% de los pacientes alcanzaron remisiůn clŪnica a los 9 meses de seguimiento (15).
Hay pocos estudios en pacientes con CU en quienes se eligiů la cirugŪa como opciůn terapťutica y que evolucionaron con crisis post cirugŪa. En un trabajo publicado en el Alimentary Pharmacology Therapeutic de 2003 se muestra que, de 7 pacientes con pouchitis y fistulas tratados con infliximab, 6 presentaron respuesta clŪnica a las diez semanas de seguimiento y en 5 se logrů cerrar completamente la fŪstula. Los autores explican que los pacientes incluidos tenŪan claramente una CU, desde el punto de vista endoscůpico, histolůgico y radiolůgico (16).
En los estudios ACT, los efectos adversos fueron mŠs frecuentes con infliximab (85%) que con placebo (73%), pero, desde el punto de vista de la infecciůn, los tres grupos de pacientes, tratados con placebo, 5 mg ů 10 mg de infliximab, no mostraron diferencias significativas. En relaciůn con el compromiso neurolůgico, hay que tener claro que infliximab conlleva cierto riesgo de neuritis ůptica y neuropatŪa motora multifocal. En cuanto al desarrollo de procesos linfoproliferativos, no hay datos disponibles hasta el momento, dado el pequeŮo nķmero de pacientes tratados. En relaciůn con la presencia de anticuerpos, hasta 17% de los pacientes con CU tratados con infliximab desarrollaron anticuerpos (13).
En una revisiůn de la base de datos Cochrane sobre el papel de los bloqueadores del TNF-alfa en la inducciůn de remisiůn en CU, los autores concluyen que en pacientes con CU moderada a grave, refractaria a tratamiento convencional con corticoides o agentes inmunosupresores, infliximab induce efectivamente la remisiůn, induce respuesta clŪnica, promueve la curaciůn de la mucosa y reduce la necesidad de colectomŪa, al menos en el corto plazo. Los efectos adversos atribuibles a infliximab no son frecuentes, aunque los mťdicos deben estar atentos a la apariciůn de reacciones anafilŠcticas e infecciones (17).
En diciembre de 2006, en Gastroenterol Clin N Am se seŮala que la FDA aprobů recientemente el uso de infliximab en CU activa, moderada o grave, cuando la respuesta a agentes convencionales es inadecuada (18); segķn la revisiůn descrita, infliximab es mŠs eficaz que placebo, con un nķmero necesario de 3 a 5 pacientes que tratar, y permite lograr la remisiůn clŪnica a los 9 meses de seguimiento, en alrededor de 40% de los pacientes. No estŠ demostrado con estudios que el efecto se mantenga por mŠs tiempo.
Infliximab se presenta como una nueva opciůn terapťutica, que se agrega a las ya disponibles: mezalazina (5-ASA), esteroides, AZA/6-mercaptopurina, ciclosporina y tacrolimus. EstarŪa indicado para inducir remisiůn en CU moderada a grave refractaria o intolerante a 5-ASA o inmunomoduladores; en CU moderada a grave refractaria a esteroides vŪa oral; y en CU dependiente de esteroides, refractaria o intolerante a inmunomoduladores. Tambiťn estarŪa indicado para mantener la remisiůn en los pacientes en quienes han fracasado 5-ASA y los inmunomoduladores, aun con dosis ůptimas y adecuadas de estas estrategias terapťuticas; y como alternativa a la ciclosporina, en pacientes hospitalizados con crisis moderada o grave. No se debe utilizar infliximab en pacientes con CU fulminante, dado que su vida media es demasiado larga y en este caso no hay tiempo para esperar los resultados; y no hay evidencia que avale su uso como tratamiento de primera lŪnea en pacientes con crisis leve a moderada.

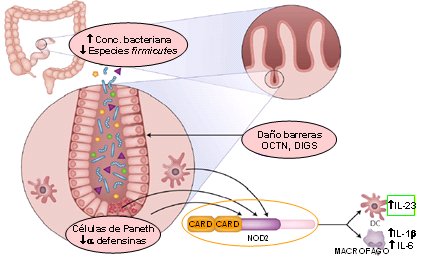 Figura 1. FisiopatologŪa de la enfermedad inflamatoria intestinal (3).
Figura 1. FisiopatologŪa de la enfermedad inflamatoria intestinal (3).

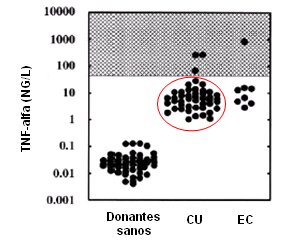 Figura 2. TNF-alfa y colitis ulcerosa (5).
Figura 2. TNF-alfa y colitis ulcerosa (5).

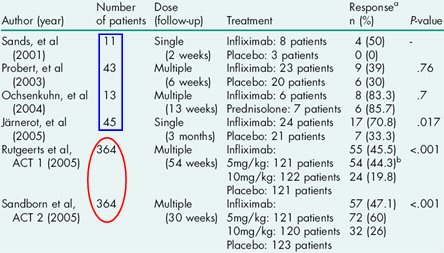 Tabla I: Estudios aleatorios y controlados sobre el efecto de infliximab en pacientes con colitis ulcerosa.
Tabla I: Estudios aleatorios y controlados sobre el efecto de infliximab en pacientes con colitis ulcerosa.

 Tabla II. Respuesta clŪnica a tratamiento con infliximab (7).
Tabla II. Respuesta clŪnica a tratamiento con infliximab (7).

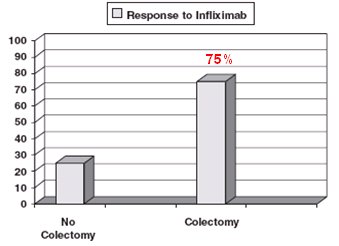 Figura 3. Respuesta a infliximab (8).
Figura 3. Respuesta a infliximab (8).

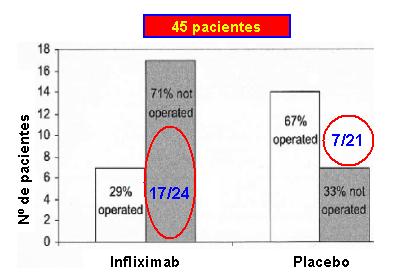 Figura 4. Efecto de infliximab en pacientes refractarios a tratamiento esteroidal endovenoso (12).
Figura 4. Efecto de infliximab en pacientes refractarios a tratamiento esteroidal endovenoso (12).

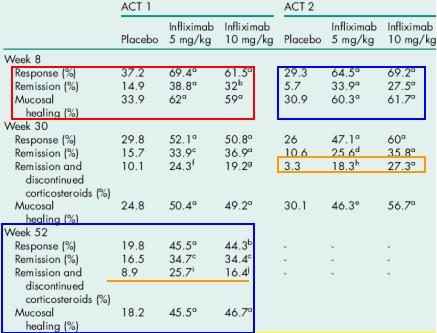 Tabla III. Resultados de los estudios ACT (Active Ulcerative Colitis Trial) (14).
Tabla III. Resultados de los estudios ACT (Active Ulcerative Colitis Trial) (14).
 Esta obra de Medwave estŠ bajo una licencia Creative Commons Atribuciůn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciůn y reproducciůn del artŪculo en cualquier medio, siempre y cuando se otorgue el crťdito correspondiente al autor del artŪculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estŠ bajo una licencia Creative Commons Atribuciůn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciůn y reproducciůn del artŪculo en cualquier medio, siempre y cuando se otorgue el crťdito correspondiente al autor del artŪculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripciůn editada y revisada de una conferencia dictada en el curso Realidad Nacional en el Uso de Terapia Biolůgica en Enfermedad Inflamatoria Intestinal, organizado por la Agrupaciůn Chilena de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa de la Sociedad Chilena de GatroenterologŪa, el dŪa 14 de diciembre de 2006. Moderador: Dr. Roque Saenz.
 Expositor:
Rodrigo Quera[1]
Expositor:
Rodrigo Quera[1]

Citaciůn: Quera R. Current treatment recommendations on use of infliximab in ulcerative colitis. Medwave 2007 Mar;7(2):e3306 doi: 10.5867/medwave.2007.02.3306
Fecha de publicaciůn: 1/3/2007

Nos complace que usted tenga interťs en comentar uno de nuestros artŪculos. Su comentario serŠ publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcciůn editorial considera que su comentario es: ofensivo en algķn sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polŪticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisiůn por pares.
Aķn no hay comentarios en este artŪculo.
Para comentar debe iniciar sesiůn