Este texto completo es la transcripción editada y revisada de una conferencia dictada en el curso Realidad Nacyonal en el Uso de Terapia Biológica en Enfermedad Inflamatoria Intestinal, organizado por la Agrupación Chilena de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa de la Sociedad Chilena de Gastroenterología, el día 14 de diciembre de 2006. Moderador: Dr. Roque Saenz.
A continuación se tratará la evidencia disponible sobre la utilidad de infliximab en el tratamiento de la enfermedad de Crohn (EC), sobre cuya base la FDA (Food and Drug Administration, Estados Unidos) estableció las recomendaciones actuales relativas a dosis y forma de administración.
El infliximab es un anticuerpo IgG1 monoclonal quimérico, es decir, tiene una parte humana (75%) y una parte de ratón, lo que explica algunas de las complicaciones y dificultades que surgen durante su administración. Tiene la capacidad de unirse al factor de necrosis tumoral (TNF), tanto al soluble como al que está en los tejidos transmembrana, característica que aumenta su potencialidad, a diferencia de otros anti TNF, que no tienen esa cualidad; impide la unión de TNF con receptores celulares y así detienen la lisis celular mediada por citotoxicidad y fijación de complemento. Fue el primer anticuerpo monoclonal que aprobó la FDA, primero en artritis reumatoide (AR) y luego en EC.
Los principales problemas del infliximab provienen del hecho de ser quimérico, por lo que es muy inmunogénico y genera anticuerpos anti-infliximab; si tal efecto no se impide, puede ocasionar reacciones alérgicas graves y pérdida de respuesta. Más adelante se analizará cómo evitarlo; en general, se debe efectuar terapia inmunosupresora concomitante y preferir terapia de mantención y no episódica. En una comparación (Fig. 1) de la composición de los anticuerpos anti TNF disponibles, la primera molécula es el infliximab; la parte verde es la parte de ratón, la que se ha ido modificando en nuevas moléculas, pero ellas aún no están aceptadas en el tratamiento de la EC.
Figura 1. Comparación de anticuerpos quimérico, humanizado y humano.
Los anticuerpos quiméricos, como infliximab, son 75% humanos; los humanizados, como CDP571, tienen 95% de proteína humana; y adalimumab es completamente humano.
La primera publicación al respecto fue revolucionaria: en 1995, Van Dullemen describió 10 casos de EC tratados con infliximab, 8 de los cuales tuvieron mejoría rápida y dramática, tanto clínica como endoscópica. Este resultado fue el inicio de todo lo que se expone a continuación (1). Después apareció el trabajo clásico de Targan (2), que se publicó en NEJM y fue el primer trabajo aleatorio y controlado con placebo que se hizo para evaluar la inducción de remisión, que era el objetivo inicial en EC. Dicho estudio se hizo en 108 pacientes, que recibieron una dosis única de infliximab, de 5, 10 ó 20 m/kg, y se midió la respuesta a las cuatro semanas. Hubo una gran diferencia (Fig. 2) entre el grupo placebo, representado por la curva inferior, y todos los demás grupos; el de 5 mg/kg fue significativamente mejor. A las cuatro semanas hubo diferencias significativas, en cuanto a respuesta (gráfico A), definida como la disminución significativa de los índices de actividad; y en cuanto a remisión completa (gráfico B), también con porcentaje mayor de remisión en el grupo de 5 mg/kg. Los detalles son los siguientes: porcentaje de respuesta de 81% en el grupo de 5 mg/kg; en cambio, en los grupos de 10 y 15 mg/kg fue de 50% y 64% respectivamente, frente a 17% del grupo placebo; 33% del total de pacientes remitieron, versus 4% de los del grupo placebo; la respuesta clínica (remisión) se mantuvo a las 12 semanas en 41% de los pacientes, independiente de la terapia asociada y la localización de la EC, es decir, hubo un efecto residual relativamente importante; el grupo de 5 mg/kg mostró los mejores resultados.
Figura 2: Infliximab en pacientes con enfermedad de Crohn activa (2).
En cuanto a la mantención de la remisión, Rutgeers publicó los resultados del primer estudio aleatorio, doble ciego, controlado con placebo y multicéntrico que se realizó en 73 pacientes, quienes habían tenido buena respuesta a las cuatro semanas y recibieron tratamiento de mantención de la remisión; este tratamiento consistió en cuatro infusiones repetidas cada ocho semanas, es decir, a la semana 12, 20, 28 y 36, con un último control en la semana 44, es decir, 8 semanas después de última infusión. En dicho control, 52,9 % del grupo tratado estaba en remisión, frente a sólo 20% del grupo placebo, o sea, de los que respondieron a la primera dosis y continuaron el tratamiento, la mitad se mantuvo en remisión, a pesar de que era un grupo resistente a terapias habituales (3).
Los estudios más extensos que se han hecho sobre infliximab son los ACCENT I y II (A Crohn’s disease Clinical trial Evaluating infliximab in a New long-term Treatment regimen), de los cuales se ha extraído la mayor parte de la información disponible actualmente. En el primero se estudió a 580 pacientes con EC activa e índice de actividad elevado (CDAI sobre 220). Los criterios fueron estrictos: los pacientes debían estar recibiendo dosis estables de inmunosupresores y otros antiinflamatorios, y se excluyó a pacientes que hubieran recibido previamente infliximab o se hubieran tratado en otros estudios. Los respondedores se asignaron en forma aleatoria a una dosis única de 5 mg/kg a las dos semanas y los que respondieron a dicha dosis se asignaron a tres grupos: I) grupo placebo, II) de 5 mg/kg y III), de 10 mg/kg. Los pacientes recibieron infliximab o placebo en la semana 2 y 6, y después cada 8 semanas hasta la semana 46. Las tasas de remisión clínica y de respuesta clínica (Fig. 3), pero sin remisión completa, a las 30 semanas; muestran una clara diferencia entre el grupo I o placebo y los grupos II, de 5 mg/kg y III, de 10 mg/kg. En la semana 54 se mantienen más o menos las mismas proporciones (4).
Figura 3. ACCENT I: Mantención de remisión con infliximab (4).
En el mismo trabajo se evaluó la necesidad del uso de esteroides; es uno de los problemas graves de estos pacientes: que son dependientes de esteroides, con las complicaciones consiguientes. Desde las semanas 6 a 10 en adelante (Fig. 4), en ambos grupos tratados prácticamente no hubo necesidad de utilizar esteroides; en el grupo placebo se mantuvo esa necesidad hasta las 54 semanas.
Figura 4. ACCENT I: Necesidad de corticoides durante el tratamiento con infliximab en EC (4).
Se han hecho varias publicaciones a partir de los datos del ACCENT I; en la primera de ellas se describió que infliximab fue superior al placebo en mantener la remisión a las 30 y 54 semanas; se necesitaron menos esteroides y la inducción con 3 dosis a las 0, 2 y 6 semanas fue muy superior a la que se observó con la dosis única que se utilizó en el trabajo inicial de Targan. Como el grupo placebo no recibió esa dosis, se pudo comparar muy bien la efectividad de la inducción de remisión con tres dosis y con una. Esta información, que se extrajo de dicho trabajo, fue la base de las indicaciones que se manejan en la actualidad.
Más adelante se evaluó la diferencia entre mantener un esquema de remisión permanente o efectuar tratamiento episódico, cuando el paciente presenta reactivación, en un trabajo que agrupó a 573 pacientes; todos ellos recibieron 5 mg/kg en fase de inducción, desde la semana cero, y luego se asignaron en forma aleatoria a tres grupos: placebo, 5 mg/kg y 10 mg/kg, cada 8 semanas. El porcentaje de pacientes en remisión fue mucho mayor en los pacientes tratados con esquema que en el grupo que recibió tratamiento episódico (Fig. 5)
La necesidad de cirugía (Fig. 6) es otro parámetro importante en el seguimiento de los pacientes con EC y se considera un control de calidad. Los pacientes que recibieron tratamiento episódico tuvieron mayor necesidad de cirugía que los que se trataron con 5 ó 10 mg/kg. La necesidad de hospitalización también fue mucho mayor en el grupo que recibió terapia episódica.
En resumen, la respuesta al tratamiento por esquema fue significativamente mayor que en el tratamiento episódico, tanto en actividad clínica como en curación endoscópica. La producción de anticuerpos antiinfliximab (ATI) fue muy superior en el grupo episódico, así como la tasa de cirugía y hospitalización, aunque en los tres grupos las tasas de complicaciones generales fueron semejantes. Los niveles de ATI se relacionan con mayor frecuencia de reacciones adversas y menor respuesta, o pérdida de respuesta, a infliximab, de modo que, con el tiempo, el grupo de pacientes cuyas tasas de anticuerpos eran mayores fue perdiendo la respuesta a infliximab. La estrategia para disminuir los niveles de ATI es el uso de inmunomoduladores concomitantes. La terapia de mantención por esquema también se asocia con menores tasas de producción de ATI, en comparación con el tratamiento episódico.
En el ACCENT II se analizó específicamente lo que pasaba en pacientes con EC fistulizante, quienes recibieron la misma terapia que ya se mencionó, a las 0, 2 y 6 semanas de inducción; se obtuvo respuesta en 69% de los pacientes, a los que se inició tratamiento de mantención de la remisión con infliximab o placebo cada 8 semanas, en el mismo esquema que en el ACCENT I. La diferencia fue significativa entre el grupo placebo y el grupo de mantención con infliximab (Fig.7). La remisión completa también fue mucho mayor en el grupo con infliximab que en el grupo placebo, de acuerdo con el índice de actividad; en el ACCENT II, este índice fue el cierre de la fístula y, en el ACCENT I, la caída del CDAI más de 70 puntos, lo que se considera una disminución significativa de la actividad. Se estimó con remisión completa a los pacientes con CDAI bajo 150.
Figura 7. Infliximab y Crohn fistulizante. Respuesta completa: todas las fístulas cerradas (6).
En cuanto a infliximab en el mantenimiento de EC fistulizante, también dentro del ACCENT II, Sands, en un trabajo con 94 pacientes con EC, con fístula perianal, enterocutánea o rectovaginal, observó que la respuesta en el grupo tratado con infliximab fue significativamente mayor que en el grupo con placebo (7). En cuanto a las complicaciones extraintestinales, no hay una recomendación aprobada por la FDA, pero en múltiples comunicaciones se describe buena respuesta en casos de pioderma gangrenoso refractario y fenómenos articulares secundarios.
Las recomendaciones generales son las siguientes: la dosis inicial recomendada para cualquier grupo es de 5 mg/kg, que se administra en infusión intravenosa, en 2 horas, y se repite a las semanas 2 y 6. Se debe administrar terapia de mantención de la remisión, con la misma dosis cada 8 semanas. En caso de pérdida de respuesta, si el paciente se activa antes de las 8 semanas, se puede adelantar las dosis, pero nunca a menos de 4 semanas; si con eso no basta, se recomienda aumentar la dosis a 10 mg/kg.
Tratamiento de la EC con actividad moderada a grave (grado A):
En pacientes resistentes a terapia médica convencional o intolerantes: terapia de inducción con tres dosis de 5 mg/kg a las semanas 0, 2 y 6; no insistir si no hubo respuesta. Apoyado por evidencia sólida grado A. El tratamiento con esteroides o inmunomoduladores (AZA, 6-MP o MTX) antes, o junto con infliximab, reduce la formación de ATI. Entre el tratamiento episódico y el esquema no habría diferencias significativas en cuanto a toxicidad, pero sí las hay en cuanto a pérdida de respuesta; en estos casos, la recomendación, como ya se seńaló, es ir acortando el intervalo y aumentar las dosis si se llega a menos de 4 semanas.
Tratamiento de la EC fistulizante sin respuesta a terapia convencional:
Se debe administrar antibióticos y efectuar drenaje quirúrgico con examen bajo anestesia o inmunomoduladores, con evidencia grado A. Las dosis de inducción son las mismas que en la EC inflamatoria: 3 dosis de 5 mg/kg en las semanas 0, 2 y 6. Si no hay respuesta se debe suspender. Seguir con mantención cada 8 semanas. Antes de iniciar infliximab es esencial descartar la presencia de abscesos en el trayecto fistuloso; esto se hace mediante un examen clínico acucioso, idealmente en conjunto con el proctólogo, bajo anestesia y guiado por endosonografia o RNM pélvica, que son excelentes exámenes para descartar colecciones. Si se han instalado drenajes tipo Seton, que son hilos que se ponen a través del trayecto fistuloso, se deben retirar antes de la segunda infusión de infliximab, para asegurar el cierre de la fístula.
Tratamiento de las manifestaciones extraintestinales con infliximab:
Con evidencia grado C, sólo se realiza en casos de enfermedad refractaria, pero hay múltiples comunicaciones sobre la utilidad de infliximab en todas ellas: pioderma, eritema nodoso, Crohn metastásico, uveítis, epiescleritis y artropatía, tanto axial como periférica.

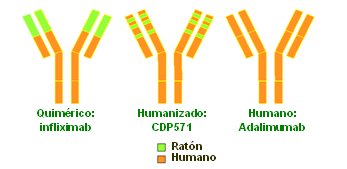 Figura 1. Comparación de anticuerpos quimérico, humanizado y humano.
Figura 1. Comparación de anticuerpos quimérico, humanizado y humano.

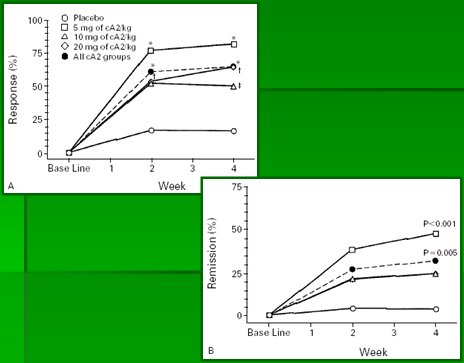 Figura 2: Infliximab en pacientes con enfermedad de Crohn activa (2).
Figura 2: Infliximab en pacientes con enfermedad de Crohn activa (2).

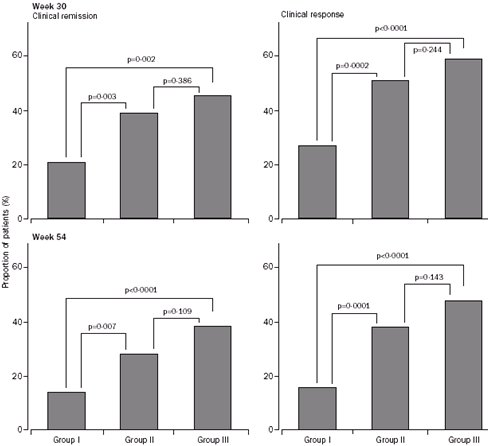 Figura 3. ACCENT I: Mantención de remisión con infliximab (4).
Figura 3. ACCENT I: Mantención de remisión con infliximab (4).

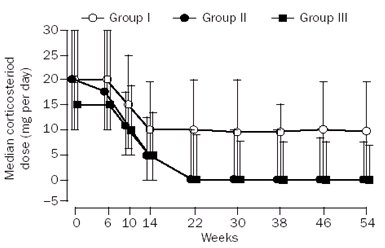 Figura 4. ACCENT I: Necesidad de corticoides durante el tratamiento con infliximab en EC (4).
Figura 4. ACCENT I: Necesidad de corticoides durante el tratamiento con infliximab en EC (4).

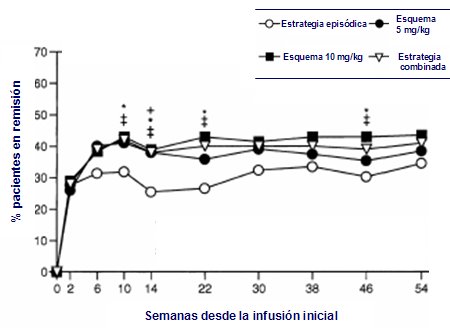 Figura 5. Porcentaje de pacientes en remisión según tipo de tratamiento: episódico o por esquema (5).
Figura 5. Porcentaje de pacientes en remisión según tipo de tratamiento: episódico o por esquema (5).

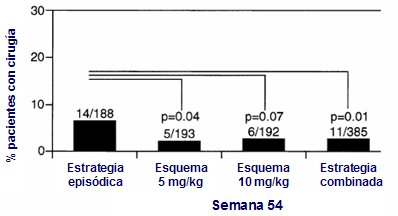 Figura 6. Porcentaje de pacientes con cirugía según tipo de tratamiento: episódico o por esquema (5).
Figura 6. Porcentaje de pacientes con cirugía según tipo de tratamiento: episódico o por esquema (5).

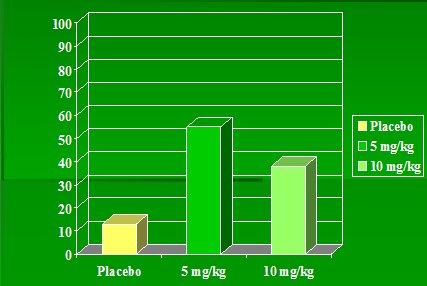 Figura 7. Infliximab y Crohn fistulizante. Respuesta completa: todas las fístulas cerradas (6).
Figura 7. Infliximab y Crohn fistulizante. Respuesta completa: todas las fístulas cerradas (6).
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de una conferencia dictada en el curso Realidad Nacyonal en el Uso de Terapia Biológica en Enfermedad Inflamatoria Intestinal, organizado por la Agrupación Chilena de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa de la Sociedad Chilena de Gastroenterología, el día 14 de diciembre de 2006. Moderador: Dr. Roque Saenz.
 Expositor:
Jaime Lubascher Correa[1]
Expositor:
Jaime Lubascher Correa[1]

Citación: Lubascher J. Infliximab and Crohn's disease. Medwave 2007 Mar;7(2):e3305 doi: 10.5867/medwave.2007.02.3305
Fecha de publicación: 1/3/2007

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión