Este texto completo es la transcripción editada y revisada de una conferencia dictada en el curso Lesiones Tumorales y Pseudotumorales del Sistema Musculoesquelético, organizado en Santiago por el Departamento de Ortopedia y Traumatología de la Universidad de Chile del 12 al 16 de mayo de 2003.
Director: Dr. Miguel Sepulveda H.
Introducción
Los pacientes que tienen este tipo de lesión tumoral refieren dolor, aumento de volumen e impotencia funcional, síntomas que comparten con las lesiones tumorales óseas.
Se denomina tejido blando a todo el tejido extraesquelético no epitelial del cuerpo, concepto que incluye los músculos voluntarios, la grasa, el tejido fibroso y los vasos sanguíneos.
Además se agrega al sistema nervioso periférico, único elemento que no forma parte de los tejidos blandos, como una manera de evaluar e integrar mejor esta patología, ya que también puede generar una lesión tumoral.
La proporción entre tumores benignos y malignos es de 100:1; es decir, la gran mayoría de los tumores de partes blandas son benignos. La variedad maligna es poco frecuente y corresponde a 1% de todos los tumores malignos.
Con frecuencia se desconoce si el tumor es maligno o benigno, y los cirujanos generales suelen extraer la lesión tumoral de partes blandas sin enviarla a estudio histológico.
A modo de anécdota, un médico del Instituto Traumatológico tuvo un aumento de volumen en una pierna, que se extirpó y se desechó la pieza operatoria. A los pocos meses reapareció la lesión y hubo que reintervenir. Esta vez se solicitó biopsia de la pieza quirúrgica y resultó que era un sarcoma de bajo grado.
En conclusión, por muy pequeńa que sea la lesión, siempre se debe enviar a biopsia, a pesar de la baja frecuencia de los tumores malignos.
Se denomina así el tumor maligno de partes blandas que se asocia en alta proporción con patologías como la enfermedad de Von Recklinhausen, el síndrome de Gardner, la esclerosis tuberosa, la poliposis familiar y el síndrome de Li-Fraumeni, patología muy infrecuente, de origen genético; es la que presenta la mayor incidencia de sarcomas, por lo que se utiliza como prototipo para su estudio e investigación.
Etiología
Se desconocen las causas de este sarcoma, pero puede haber una predisposición genética o puede ser secundario a radiación, linfedema crónico y exposición química.
Métodos de estudio
Como métodos de estudio se utilizan la citometría de flujo, para ver morfología y tamańo celular; los marcadores tumorales, de los cuales se usan en forma habitual el Ki67 y el P53; y la citogenética, que permite determinar translocaciones características de algunas entidades, tales como T(12;16)(q13-p11) en el liposarcoma y T(x;18) (p11;q11.2) en el sarcoma sinovial.
Por tanto, el sarcoma actualmente es una patología de estudio fácil, si se dispone de los medios para realizar los tres métodos mencionados.
Clínica y epidemiología
Con respecto a su localización, 20% de ellos se ubican en la extremidad superior y 40% en la inferior; las demás localizaciones (tronco 30 %, cabeza y cuello 10 %) no llegan a manos de los traumatólogos.
El sarcoma de partes blandas se presenta con dolor, aumento de volumen, impotencia funcional y aparición de ganglios linfáticos regionales, en algunos tipos. El motivo de consulta más frecuente es el aumento de volumen.
Los tipos de sarcoma más frecuentes son: el rabdomiosarcoma, que deriva de la musculatura estriada, el fibrohistiocitoma maligno, que proviene del tejido conectivo, el sarcoma sinovial y el sarcoma epiteloídeo.
Además, estos sarcomas son los que con mayor frecuencia afectan ganglios linfáticos regionales.
Con respecto a la edad de presentación, se pueden ver en todas las edades, siendo más frecuentes entre los 20 y los 60 ańos, rango que acumula 45 % de los casos, 11% de éstos en menores de 20 ańos. No hay diferencia de frecuencia según sexo.
La distribución de cada tipo de sarcoma, según grupo etario, es la siguiente:
Los tres tipos más importantes son el rabdomiosarcoma, el liposarcoma y el fibrohistiocitoma maligno.
Las metástasis habitualmente se originan por diseminación hematógena hacia pulmón, que es la localización más importante, pero también puede comprometer hueso, hígado y ganglios linfáticos.
Factores pronósticos
Los principales factores que inciden en el pronóstico de esta lesión son:
Estudio
Dentro del estudio clínico, se debe realizar anamnesis, examen físico, exámenes de laboratorio, radiografía local y de tórax (posteroanterior y lateral), cintigrama óseo, tomografía axial computarizada (TC) local y de tórax, y resonancia nuclear magnética (RM), que cumple un papel esencial en el estudio de esta patología.
Biopsia
En cuanto a la biopsia, las técnicas empleadas para efectuarla pueden ser cerradas (aspiración, tru-cut) o abiertas (incisional, excisional). Lo que se usa habitualmente es la biopsia incisional, es decir, sólo se extrae una parte del tumor, no su totalidad. Si aparentemente se logra resecar todo el tumor, entonces se trata de una biopsia excisional.
Por esta razón, cuando se opera a un paciente con sarcoma, sea óseo o de partes blandas, sin lograr extraerlo con margen adecuado, se habla de biopsia incisional.
La importancia de la técnica incisional quedó demostrada en un metaanálisis realizado en más de 4000 casos, en el que se observó que la biopsia incisional era más precisa para catalogar una lesión como benigna o maligna, y para determinar su grado y tipo histológico, se concluyó que la única biopsia segura es la incisional. Los resultados se pueden ver en detalle en la tabla I.
Tabla I. Positividad de los resultados según tipo de biopsia.
La biopsia congelada o rápida se debe realizar siguiendo algunas técnicas para lograr 94% de apoyo cuando se utilizan bordes libres en lesión tumoral, que es su uso más importante. La técnica de tru-cut es adecuada en cuanto a sacar tejido, pero no es mejor que la incisional.
La biopsia es una intervención quirúrgica con características particulares. La incisión que se efectúa debe ser pequeńa y, si se trata de una extremidad, debe seguir la longitud de ésta.
Durante la biopsia se debe realizar una hemostasia prolija, porque, en un procedimiento de este tipo, la hemorragia puede determinar diseminación tumoral. Por otra parte, no se puede usar drenaje, porque si éste se retira por un sitio distinto al de la lesión, se pueden contaminar zonas alejadas.
El tamańo de la biopsia debe ser adecuado. La medida se determinó en un trabajo protocolizado y cooperativo en el que se vio que las lesiones que medían más de 5 cm tenían peor pronóstico que las de menor tamańo, y que cuanto mayor era el tamańo del tumor era más probable que éste fuese maligno.
Con estos datos se estableció que, si la lesión medía más de 5 cm, la biopsia debía ser incisional y que, si medía menos de 5 cm, debía ser excisional.
En el ańo 2000 este límite se bajó a 3 cm como una manera de obligar al cirujano a realizar biopsias incisionales.
Clasificación
La clasificación antigua del American Joint Comittee (AJC) de 1998 utiliza grado histológico, tamańo tumoral, presencia de ganglios linfáticos y metástasis, asignándoles las denominaciones siguientes:
Grado histológico
G1: bien diferenciado.
G2: moderadamente diferenciado.
G3: poco diferenciado.
Tumor
T1: menor de 5cms.
T2: mayor de 5 cms.
Ganglios linfáticos
N0: negativo
N1: positivo
Metástasis
M0: negativo
M1: positivo
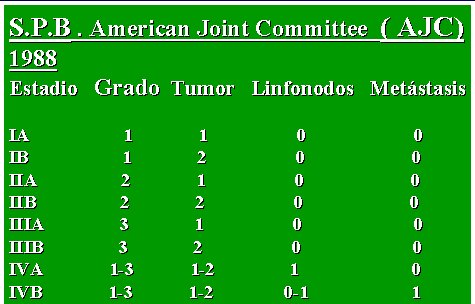
Estos cuatro parámetros determinan la etapificación de la lesión que se ve en la tabla II, que considera cuatro etapas, de IA a IVB, de bajo a alto grado. En la etapa IV, lo que importa es la presencia o no de metástasis, no el grado histológico.
Tabla II. Clasificación del sarcoma de partes blandas. American Joint Committee ( AJC) 1988.
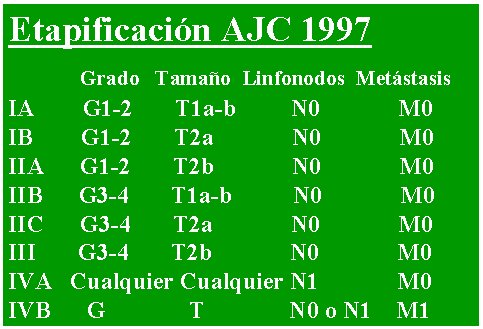
La actual clasificación del AJC, de 1997, que se puede ver en la tabla III, mantiene los altos y bajos grados e incorpora las letras a y b minúsculas, las cuales indican superficial y profundo respectivamente, y el resto se mantiene igual.
Tabla III. Etapificación AJC 1997.
El tratamiento se caracteriza por ser multidisciplinario y multicéntrico, y por su alta eficacia en el control local de la enfermedad, no así en el control a distancia.
El objetivo es que el paciente quede con la mejor funcionalidad posible, ya que la sobrevida sigue siendo igual que hace 20 ańos; en lo que hay diferencia es en el control local de la enfermedad.
Los tratamientos de elección son la cirugía y la radioterapia. La utilidad de la quimioterapia es dudosa, ya que en un metaanálisis realizado en más de 2000 pacientes estudiados no se encontró una diferencia en los resultados con o sin su uso.
En la actualidad el tratamiento incluye cirugía conservadora, radioterapia (pre o postoperatoria) y quimioterapia (pre o postoperatoria).
Nuestro protocolo comprende cirugía conservadora, es decir, conservando la extremidad, radioterapia preoperatoria, quimioterapia monodosis preoperatoria y poliquimioterapia postoperatoria en el caso de sarcomas de alto grado.
En sarcomas de bajo grado está indicada solamente la resección quirúrgica.
Cirugía
La cirugía puede ser de tipo intracapsular, marginal, amplia y radical (compartimental, ablación); el ideal es hacer una cirugía amplia, con bordes libres de tumor.
Los resultados evaluados con metaanálisis (4700 casos) demuestran que si se realiza sólo enucleación del tumor hay un 90 % de recidiva local; en otras palabras, al extraer en forma total el tumor, lo que se ejecuta finalmente es una biopsia incisional.
Un concepto importante es que el plano de clivaje de estos tumores no es el límite tumoral. De hecho, los estudios histológicos muestran que existe una mayor proporción de mitosis en el tejido que quedó en el paciente que en el que fue extraído.
Si el tumor recidiva en forma local, el paciente presenta mortalidad en forma precoz. Con la amputación o desarticulación la recidiva local es de un 15 a 20 %, y cuando se efectuaba cirugía y radioterapia la recidiva era de un 10 a 20 %, o sea, el porcentaje de recidiva con amputación o con cirugía conservadora es el mismo, por lo tanto no existe indicación de amputar.
En los últimos estudios se ha agregado poliquimioterapia a la cirugía y a la radioterapia, con lo que la recidiva local baja a 5 a 10 %. Es decir, la quimioterapia ayuda en el control local, pero no en cuanto al control a distancia.




 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de una conferencia dictada en el curso Lesiones Tumorales y Pseudotumorales del Sistema Musculoesquelético, organizado en Santiago por el Departamento de Ortopedia y Traumatología de la Universidad de Chile del 12 al 16 de mayo de 2003.
Director: Dr. Miguel Sepulveda H.
 Expositor:
Miguel Sepúlveda H.[1]
Expositor:
Miguel Sepúlveda H.[1]

Citación: Sepúlveda M. General considerations and clinical manifestations of soft tissue sarcoma. Medwave 2004 Abr;4(3):e3284 doi: 10.5867/medwave.2004.03.3284
Fecha de publicación: 1/4/2004

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión