Este texto completo es la transcripciůn editada y revisada de una conferencia dictada en el curso Lesiones Tumorales y Pseudotumorales del Sistema Musculoesquelťtico, organizado en Santiago por el Departamento de Ortopedia y TraumatologŪa de la Universidad de Chile del 12 al 16 de mayo de 2003.
Director: Dr. Miguel Sepulveda H.
Antiguamente, la presencia de un tumor de cťlulas gigantes era sinůnimo de amputaciůn. Hoy, los principios bŠsicos del tratamiento son los siguientes:
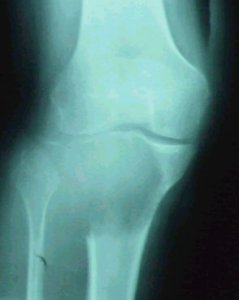
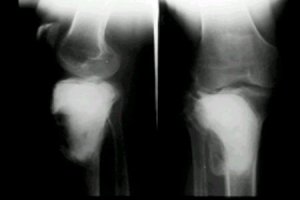
En la figura 1 se ve un tumor en etapa III de la clasificaciůn de Campanacci, con destrucciůn de la epŪfisis, por lo que no se va hacer un curetaje, sino una resecciůn tumoral completa guiada por la TC y la RM. Posteriormente, se rellenarŠ el sitio de la resecciůn.
Figura 1. RadiografŪa de rodilla, tumor en etapa III.
El tratamiento es quirķrgico. Se puede realizar curetaje, resecciůn, amputaciůn primaria o secundaria, o desarticulaciůn en los casos mŠs graves.
Curetaje
Es un tratamiento intralesional. Con este procedimiento se dejan cťlulas tumorales, por lo que se necesita una terapia de adyuvancia y es preciso contar con una gran ventana ůsea, para poder introducirse en el tumor y visualizar toda la epŪfisis. El curetaje debe ser prolijo y lo mŠs amplio posible, hasta que no queden rastros macrosocůpicos del tumor, porque se estŠ trabajando con un paciente que tiene isquemia. A continuaciůn se hace un fresado de la cavidad y se cauteriza el lecho.
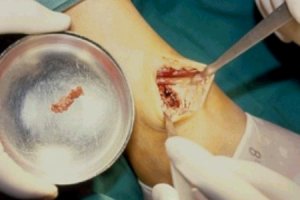
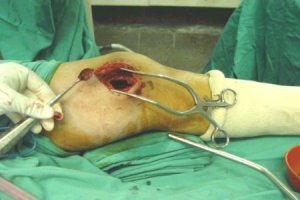
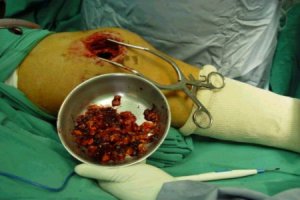
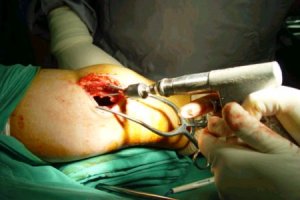
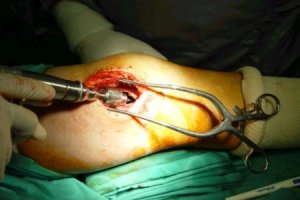
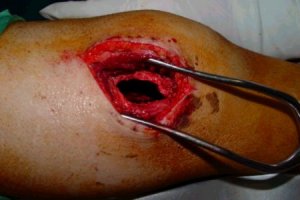
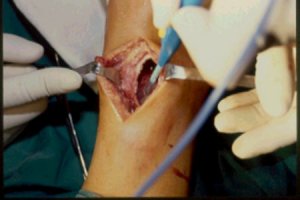
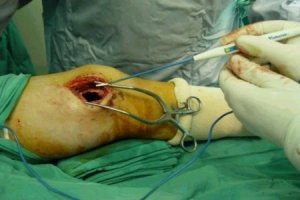
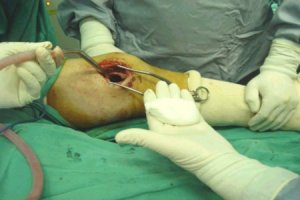
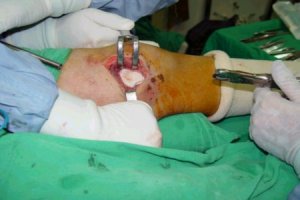
La siguiente secuencia de imŠgenes ilustra el procedimiento quirķrgico. Se abre una ventana ůsea; se ve la epŪfisis distal y el material (cucharilla); se saca todo el tumor hasta que se vea todo limpio y luego se realiza un fresado de la cavidad, procedimiento que elimina las cťlulas tumorales que quedan en las espŪculas ůseas, en las crestas del hueso. El fresado se efectķa en distintas direcciones. Despuťs del fresado se lava de nuevo y el lecho queda relativamente limpio. Se aspira y se verifica que las criptas estťn limpias; luego se aplica un electrocauterio de punta fina o larga y se llega a las zonas que la fresa no alcanza, para cauterizar todo el lecho hasta que la zona queda quemada. A continuaciůn se realiza un nuevo curetaje de la zona (Figuras 2 a 9).
Figuras 2 a 9. Secuencia de curetaje.
Adyuvancia
Este tipo de tumor tiende a recidivar, pero, con el concepto de adyuvancia, ha disminuido el porcentaje de recidivas. Este procedimiento elimina los focos residuales de tumor y trata las crestas ůseas mediante un efecto tťrmico (que se puede obtener por calor o por frŪo) o un efecto quŪmico agregado, con lo que se obtiene una necrosis tumoral agregada.
En resumen, al efecto del curetaje y del fresado se agrega una electrocauterizaciůn o una crioterapia que induce una necrosis tumoral agregada, que es lo que se define como adyuvancia. Su propůsito es disminuir las recidivas a menos de 50%, con un tratamiento menos agresivo que la resecciůn.
Los elementos que se emplean para la adyuvancia son: el fenol, que tiene el inconveniente de que daŮa las partes blandas y produce necrosis de la piel y los mķsculos; el nitrůgeno lŪquido, con el que tambiťn se debe tener cuidado; el lŠser carbůnico; el perůxido de hidrůgeno; y el cemento quirķrgico, que es el que utilizamos nosotros por sus propiedades especiales.
El curetaje consiste en cauterizar el lecho y colocar el cemento ůseo, aunque tambiťn se puede utilizar el injerto biolůgico.
CaracterŪsticas del cemento quirķrgico
Agrega una necrosis ůsea de 1 mm y da una estabilidad inmediata, por lo que no es necesario agregar osteosŪntesis ni otros elementos. Tambiťn permite una detecciůn temprana de la recidiva. Si se coloca hueso, no se ve ninguna interfase entre el injerto ůseo y el hueso propio, de modo que la recidiva no se pesquisa hasta que se produce una lesiůn clŪnica tardŪa. En cambio, con el cemento ůseo se produce normalmente una radiolucidez de alrededor de 1 mm. Cuando ťsta sobrepasa los 5 mm, se cataloga de recidiva y se procede a efectuar una biopsia y un nuevo curetaje o una resecciůn. Otra caracterŪstica del cemento es que se puede repetir la cementaciůn.
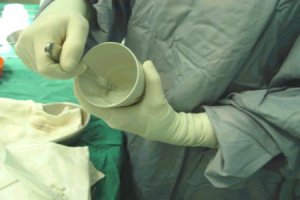
La siguiente secuencia de imŠgenes muestra la preparaciůn del cemento, cůmo se coloca y comprime una vez realizada la ventana ůsea y la imagen de radiolucidez que origina la zona cementada (Figuras 10 a 13).
Figuras 10 a 13. Colocaciůn de cemento quirķrgico e imagen radiogrŠfica posterior.
La radioterapia se utiliza sůlo en lesiones inaccesibles. Como tratamiento, es de uso excepcional, aunque algunos radioterapeutas la preconizan. Yo recomiendo usarla como radioterapia convencional en algunos sitios inaccesibles.
Recidiva
Con el curetaje simple se produce alrededor de 50% a 70% de recidiva; cuando se agrega adyuvancia, la recidiva disminuye a menos de 20%. Por ejemplo, con fenol, crio o termoterapia, baja a menos de 10%; incluso, los ķltimos estudios muestran una recidiva de alrededor de 5% con crioterapia. La resecciůn da una recidiva inferior a 10%.
Resecciůn
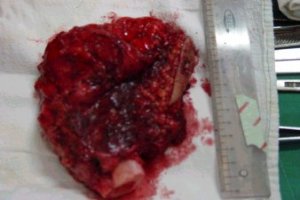
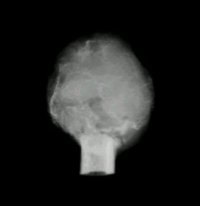
Se debe realizar con criterio oncolůgico, lo que significa que la resecciůn debe tener borde libre y sin tumor, pero esto obliga a ejecutar una gran reconstrucciůn. La siguiente es una pieza resecada en la que se ve un borde bastante amplio, para mayor seguridad (Figuras 14 y 15).
Figura 14. Muestra macroscůpica de pieza resecada.
Figura 15. RadiografŪa A-P de pieza resecada.
Si el hueso es dispensable, como el caso de la ulna distal, no es obligatorio reconstruir; asŪ, si el tumor es muy grande, se puede eliminar todo en una sola intervenciůn, con poca limitaciůn funcional, escasa morbilidad secundaria y un tiempo operatorio mucho mŠs corto; habitualmente, si una resecciůn dura dos horas y media, con la sustituciůn se alarga a cuatro horas.
Reconstrucciůn
Para la reconstrucciůn se utiliza aloinjerto estructural y průtesis de reconstrucciůn. Antes se usaba mŠs la artrodesis, porque no habŪa posibilidad de utilizar aloinjertos y las průtesis eran prŠcticamente inalcanzables. La artrodesis es de bajo costo para el paciente, pero ťste debe aceptar que su articulaciůn no va a quedar funcional.
Complicaciones
Los aloinjertos y las průtesis tienen alrededor de 50% de complicaciones. Con la průtesis, la recuperaciůn es mŠs rŠpida que con el aloinjerto, pero la průtesis de reconstrucciůn tiene una sobrevida limitada.
Tťcnica
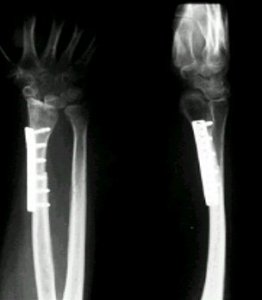
Se toma la biopsia, se elimina el tumor, se hace el curetaje y se toma muestra del canal distal y proximal, para ver si hay tumor. Se revisa el lecho y los elementos vasculares. Luego se coloca el material de osteosŪntesis y se reconstruye y sutura la rodilla. Todo el procedimiento dura alrededor de dos horas y media. En la figura 16 se ve el control radiogrŠfico realizado despuťs del procedimiento descrito.
Figura 16. Resultado radiogrŠfico de una tťcnica de reconstrucciůn.
MetŠstasis
La resecciůn de las metŠstasis no modifica el pronůstico. Es mŠs probable que el paciente fallezca por una insuficiencia respiratoria que por una metŠstasis.
















 Esta obra de Medwave estŠ bajo una licencia Creative Commons Atribuciůn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciůn y reproducciůn del artŪculo en cualquier medio, siempre y cuando se otorgue el crťdito correspondiente al autor del artŪculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estŠ bajo una licencia Creative Commons Atribuciůn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciůn y reproducciůn del artŪculo en cualquier medio, siempre y cuando se otorgue el crťdito correspondiente al autor del artŪculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripciůn editada y revisada de una conferencia dictada en el curso Lesiones Tumorales y Pseudotumorales del Sistema Musculoesquelťtico, organizado en Santiago por el Departamento de Ortopedia y TraumatologŪa de la Universidad de Chile del 12 al 16 de mayo de 2003.
Director: Dr. Miguel Sepulveda H.
 Expositor:
William Hofer[1]
Expositor:
William Hofer[1]

Citaciůn: Hofer W. Giant cell tumor: treatment. Medwave 2003 Dic;3(11):e3281 doi: 10.5867/medwave.2003.11.3281
Fecha de publicaciůn: 1/12/2003

Nos complace que usted tenga interťs en comentar uno de nuestros artŪculos. Su comentario serŠ publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcciůn editorial considera que su comentario es: ofensivo en algķn sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polŪticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisiůn por pares.
Aķn no hay comentarios en este artŪculo.
Para comentar debe iniciar sesiůn