Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso DesafĒos y Oportunidades en GastroenterologĒa y Nutrici¾n, organizado por la Sociedad Chilena de PediatrĒa durante los dĒas 3, 4 y 5 de mayo de 2007. Directores: Dra. Sylvia Cruchet y Dr. Francisco Moraga.
La oferta de probi¾ticos por parte de la industria farmacķutica y alimentaria aumenta dĒa a dĒa, por lo que es importante saber quķ requisitos debe cumplir un microorganismo para que se considere como probi¾tico. En este contexto se debe recordar las caracterĒsticas de la flora intestinal, porque los probi¾ticos tienen como objetivo intervenir sobre ella.
La flora intestinal del ser humano estß constituida por mßs de 400 especies diferentes, la mayorĒa de ellas anaerobias estrictas, que establecen una relaci¾n simbi¾tica con el ser humano a nivel intestinal. Cada bacteria que se instala en el intestino humano lo hace en una zona definida y estable, en la cual se queda en forma permanente, desarrollando una asociaci¾n Ēntima con el epitelio de la mucosa; esto se relaciona con las funciones que cumplirß a lo largo de la vida, seg·n el segmento en que se ubique cada especie. Esta flora mantiene un equilibrio estricto, regulado por factores de secreci¾n, presi¾n de oxĒgeno, gradiente de nutrientes y peristaltismo, los que en conjunto determinan los cambios que va sufriendo la flora, en la cual coexisten bacterias aut¾ctonas y transitorias.
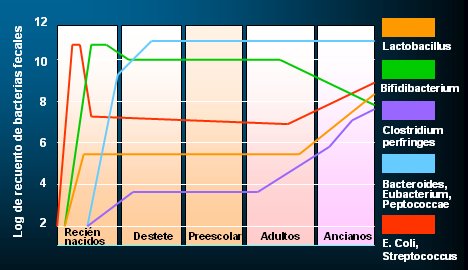
El feto in utero tiene un aparato digestivo prßcticamente estķril. La flora intestinal se comienza a establecer desde el nacimiento, incluso desde los primeros momentos del parto y en su desarrollo influyen varios factores. Entre ellos estß el tipo de parto, ya que los ni±os que nacen por parto vaginal tienen una flora mucho mßs rica en bifidobacterias, que son las que interesa tener en gran cantidad, que los ni±os que nacen por cesßrea. Tambiķn influye el tipo de alimentaci¾n del reciķn nacido: el ni±o alimentado al pecho recibe el beneficio de los efectos biogķnicos de la leche materna, que por su contenido en lactosa favorece el crecimiento de las bifidobacterias beneficiosas para la salud, a diferencia de los ni±os que reciben f¾rmula desde el primer momento de la vida; hoy en dĒa se han agregado microorganismos a muchas f¾rmulas, en un intento de desarrollar una flora similar a la que se consigue con la lactancia materna, pero hasta ahora ķsta es irremplazable. Otro factor importante es la edad del destete y la edad en que se incorporan los s¾lidos y las f¾rmulas y, finalmente, la alimentaci¾n del adulto puede modificar levemente la flora, siendo mßs beneficiosa, por ejemplo, la de los individuos que se atienen a una dieta vegetariana estricta.
Figura 1. Evoluci¾n de la microbiota intestinal con la edad.
Cada vez que se lanza al mercado un probi¾tico, que cumple determinada funci¾n, se debe demostrar que posee las caracterĒsticas descritas mediante estudios in vivo que demuestren la sobrevida en las deposiciones. Despuķs de la ingesta de un probi¾tico, su eliminaci¾n en las deposiciones sigue curva exponencial, llegando a ser indetectable entre los 5 y los 9 dĒas, como mßximo a los 14 dĒas. Se ha definido el criterio de actividad del probi¾tico como una concentraci¾n de 10 elevado a siete unidades formadoras de colonias (UFC) por gramo de deposiciones, que es la cantidad mĒnima que debe estar presente para obtener una respuesta; sin embargo, algunas bacterias sobreviven mßs tiempo adheridas a la pared del intestino, especialmente del colon y por lo tanto no aparecen en las deposiciones, de modo que los estudios sobre este aspecto son invasivos, ya que se requiere la intubaci¾n de los pacientes.
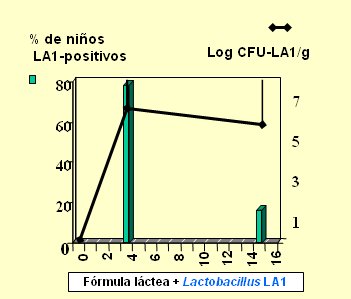
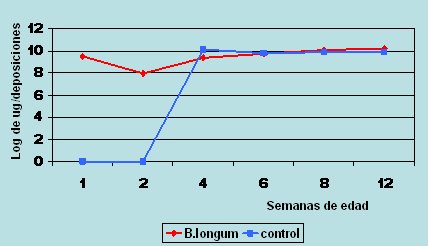
Antes de que las bacterias probi¾ticas se utilicen en un estudio clĒnico, se debe demostrar que se eliminan vivas por las deposiciones. En la Fig. 2 se resumen los resultados de un estudio efectuado en el INTA; se observa que, cuando se agrega Lactobacillus LA1 a una f¾rmula lßctea, el germen comienza a aparecer en las deposiciones de los lactantes, con una diferencia significativa con respecto a controles o placebo. Cuando se suspende la ingesta los gķrmenes empiezan a disminuir en forma progresiva, hasta desaparecer en todos los pacientes despuķs de 14 dĒas.
Figura 2. Permanencia del probi¾tico en el tubo digestivo tras administrar f¾rmula lßctea + Lactobacillus LA1 en lactantes (Brunser et al., 2004).
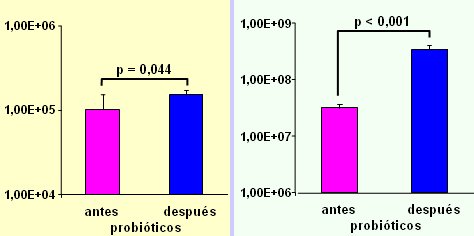
En otro estudio, en que se analiz¾ el efecto de Lactobacillus y bifidobacterias sobre algunos aspectos de la inmunidad, tambiķn hubo que partir por demostrar que ambos tipos de bacterias aumentaban despuķs del consumo de probi¾ticos, respecto al grupo control (Fig. 3).
Figura 3. Conteos bacterianos por gramo de deposici¾n (de Vrese et al, Clin Nutr 2005 (24) 481.
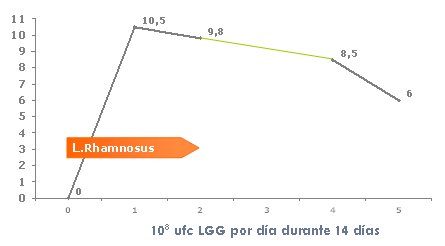
En la Fig. 4 se muestra el resultado de un estudio efectuado con Lactobacillus rhamnosus GG, un probi¾tico que se utiliza mucho, especialmente en pediatrĒa, que en este caso se administr¾ durante 14 dĒas, en dosis de 10 elevado a 8 UFC. La excreci¾n en las deposiciones aument¾ rßpidamente y comenz¾ a disminuir dos semanas despuķs de que se suspendi¾ la ingesta. En la Fig. 5, el grßfico resume un estudio efectuado en reciķn nacidos de pretķrmino, en el que se demostr¾ que las bifidobacterias eran eliminadas vivas por las deposiciones.
Figura 4. Aparici¾n de L. rhamnosus GG en las heces de lactantes de pretķrmino
(Millar M et al. Arch Dis Child 1993;69:483)
Figura 5. Colonizaci¾n de reciķn nacidos de pretķrmino por bifidobacterias. Recuento de deposiciones (Akiyama K et al Acta Neonatol Jap 1994; 30:25)
Gran cantidad de microorganismos se han postulado como probi¾ticos. Los principales son los microorganismos lßcteos de los grupos Lactobacillus sp y Bifidobacterium sp, aunque tambiķn hay algunos microorganismos no lßcteos, todos ellos considerados ōGRASö (general regarding as safe), lo que significa que la FDA ha declarado que su uso es sano y saludable para los seres humanos. Es muy importante recordar que no todos los lactobacilos ni todas las bifidobacterias son iguales; por eso, cuando se habla de Lactobacillus se debe aclarar de quķ especie se estß hablando y quķ uso tiene o va a tener, seg·n la evidencia: para la diarrea, para evitar reacciones adversas a antibi¾ticos, para la fibrosis quĒstica o para prevenir alguna patologĒa.
En la actualidad, los probi¾ticos se encuentran en el mercado: principalmente en productos lßcteos fermentados, como yogur, leches fermentadas y cultivadas y quesos; en algunos productos vegetales fermentados, como aceitunas, chucrut, soya y cereales; en algunas carnes o pescados fermentados y salchichas; en bebidas alcoh¾licas, como vino, cerveza, sidra y otras bebidas, por lo general artesanales; y en el gran grupo de los liofilizados, sea como medicamentos o como suplementos nutricionales.
En este momento existen varias cepas probi¾ticas disponibles en alimentos y productos farmacķuticos, cuyo uso estß permitido en los claims (beneficio que se atribuye a un producto o servicio a la hora de realizar su publicidad) y existen dieciocho mensajes saludables aceptados por el Ministerio de Salud para que sean utilizados por las empresas. Entre ellos estß el uso de probi¾ticos y prebi¾ticos, por lo que es importante conocer los microorganismos que cumplen esta funci¾n, con nombre y apellido, porque lo importante es la especie (Tabla I)
Tabla I. Ejemplo de cepas probi¾ticas disponibles en alimentos o productos farmacķuticos autorizadaos para ser usados en claims
La seguridad del uso de los probi¾ticos que se han desarrollado hasta este momento es excelente, ya que no se han descrito casos de efectos adversos graves. Se han descrito algunas infecciones por lactobacilo, bifidobacteria y Saccharomyces boulardii en forma ocasional, pero s¾lo se han aislado lactobacilos o bifidobacterias en pacientes con sepsis, sin que se haya podido demostrar que fueran causantes de ķsta. Tambiķn se han descrito casos de infecciones de catķter por Saccharomyces boulardii liofilizado, pero en esos casos se manipul¾ el producto al lado de pacientes de alto riesgo en una unidad de tratamiento intensivo. Por lo tanto, por una parte se debe tener precauci¾n, pero tambiķn se debe emplear estos productos en forma mßs intensiva, ya que no se ha demostrado que tengan efectos adversos graves.
Algunos de estos productos desencadenan una actividad metab¾lica excesiva en la mucosa intestinal, pudiendo producir degradaci¾n de ķsta, lo que potencialmente podrĒa tener un efecto negativo en salud, pero tampoco se ha observado este tipo de problema, excepto en un trabajo que no ha podido ser replicado. La inmunomodulaci¾n excesiva tambiķn podrĒa ser un efecto adverso, en especial en casos de enfermedad inflamatoria intestinal, en las cuales el exceso de estimulaci¾n podrĒa actuar como factor activante. Finalmente, se habla de la posibilidad de que ocurra una transferencia genķtica, especĒficamente de resistencia a antibi¾ticos; por el momento no existe evidencia de que ello suceda, pero los estudios a·n son insuficientes, de modo que en este momento se estßn desarrollando varias investigaciones sobre este aspecto.
En resumen, los probi¾ticos tienen un efecto positivo sobre la salud del ser humano cuando cumplen con ciertas caracterĒsticas, que se describieron en esta presentaci¾n; y ejercen este efecto actuando sobre la microflora intestinal, en forma directa o a travķs de la modulaci¾n del sistema inmune.







 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso DesafĒos y Oportunidades en GastroenterologĒa y Nutrici¾n, organizado por la Sociedad Chilena de PediatrĒa durante los dĒas 3, 4 y 5 de mayo de 2007. Directores: Dra. Sylvia Cruchet y Dr. Francisco Moraga.
 Expositora:
Silvia Cruchet[1]
Expositora:
Silvia Cruchet[1]

Citaci¾n: Cruchet S. When is an organism considered to be a probiotic?. Medwave 2007 Jun;7(5):e3253 doi: 10.5867/medwave.2007.05.3253
Fecha de publicaci¾n: 1/6/2007

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n