Resumen
Este texto completo es la transcripción editada y revisada de una conferencia dictada en el Curso Desafíos y Oportunidades en Gastroenterología y Nutrición, organizado por la Sociedad Chilena de Pediatría durante los días 3, 4 y 5 de mayo de 2007. Directores: Dra. Sylvia Cruchet y Dr. Francisco Moraga.
Introducción
El síndrome de intestino corto corresponde a una patología conocida desde hace ańos, sin que a la fecha se hayan postulado cambios respecto a su fisiopatología, pero sí en relación con su manejo clínico.
Hay al menos tres definiciones, que se refieren a tres situaciones relacionadas, una, con la necesidad de nutrición parenteral; otra, con la resección intestinal; y otra, con la mala absorción de nutrientes:
- paciente que requiere más de 42 días o más de 3 meses de nutrición parenteral;
- intestino residual de más de 25% o resección mayor del 75% de lo previsto para un paciente pequeńo para la edad gestacional;
- mala absorción global de nutrientes con posterioridad a una resección intestinal.
Entre sus causas, las más frecuentes son la enterocolitis necrotizante y la invaginación intestinal; menos frecuentes, la atresia o estenosis duodenal, de yeyuno o íleon; la malrotación intestinal; los vólvulos o duplicaciones intestinales; los divertículos y las hernias. Su frecuencia no es del todo conocida, pero claramente es más frecuente en los menores de 37 semanas de edad gestacional. En el momento de hacer las estadísticas se toman aquellos nińos que están en alimentación parenteral, pero no se consideran los casos que ya no la necesitan, por lo que la frecuencia estimada dependerá de cómo se tome el número de pacientes.
Como consecuencias de la resección intestinal, se presenta disminución de la superficie de absorción intestinal, pérdida de agua y electrolitos y mala absorción de nutrientes: hidratos de carbono, lípidos, vitaminas hidro y liposolubles, proteínas, hierro, folatos, calcio, fósforo, etc. Otro aspecto importante es que al resecar un segmento intestinal se pierden factores que intervienen en la digestión y absorción de nutrientes: sales biliares, enzimas pancreáticas, enzimas de la mucosa intestinal, hormonas gastrointestinales y elementos del sistema inmune.
El pronóstico está dado por el estado de la absorción intestinal después de la resección, la que depende de: la extensión y sitio de ésta; la conservación o remoción de la válvula ileocecal; la función hepática, intestinal, del colon y páncreas; los cambios adaptativos que ocurran en el intestino delgado; la presencia de enfermedad residual del intestino delgado; la presencia de complicaciones quirúrgicas o compromiso hepático. Los factores mencionados se conocen desde hace muchos ańos, pero su ponderación ha ido variando en el tiempo; hoy se considera que lo que ocurra con la válvula ileocecal es más importante que las alteraciones funcionales del colon. Por otra parte, los tamańos de intestino remanente han ido disminuyendo; actualmente hay individuos que viven con intestinos hasta de 15 cm, pero todo depende del estado de los demás elementos que determinan el pronóstico.
En la evolución clínica, la primera etapa es bastante complicada: es importante mantener el equilibrio hidroelectrolítico mediante el uso de soluciones con concentraciones relativamente altas de sodio y haciendo todo lo posible por reducir las pérdidas por vía digestiva. La segunda etapa corresponde a la alimentación por boca, que es la vía fisiológica, lo que permite mejorar la respuesta adaptativa del tracto gastrointestinal; se ha demostrado que la infusión continua tiene mayor utilidad que los bolos y la concentración de nutrientes y su complejidad dependerán de la tolerancia digestiva y edad del paciente. Existe la posibilidad de utilizar la alimentación con fórmulas parenterales, pero se debe hacer por el tiempo más breve posible, para reducir el riesgo de dańo hepático y muerte secundaria.
El dańo causado dependerá del sitio de la resección:
- Si se trata del duodeno, habrá mala absorción de hierro, folato, calcio y zinc, además de alteración de la mezcla de las sales biliares con la secreción pancreática y, derivado de esto, mala absorción de lípidos y vitaminas liposolubles.
- Si el segmento resecado es el yeyuno, el íleon y colon intactos se adaptan a la absorción de nutrientes, agua y electrolitos; por lo tanto, el pronóstico de una resección yeyunal es bastante mejor si el íleon y colon están intactos.
- Por otra parte, al resecar el yeyuno disminuye la secreción de hormonas gastrointestinales, cuya importancia se reconoce cada vez más, ya que actúan no sólo a nivel del tubo digestivo, sino también en otros tejidos y además hay pérdida de células y enzimas inmunológicas.
- Al resecar un segmento de ileon, lo más importante que ocurre es que se pierde la absorción de sales biliares y se producen ácidos biliares hepatotóxicos, dańo que puede ser irreversible. Otro de los efectos en este caso es la alteración de la producción de vitamina B12.
- Cuando se pierde la válvula ileocecal, se acelera el tránsito intestinal y hay ascenso de la flora microbiana, lo que determina sus propias complicaciones.
- Al resecar el colon derecho ocurre mayor pérdida de agua y de electrolitos y, en segundo lugar, se pierde el salvataje colónico de hidratos de carbono no digeridos ni absorbidos. Estas dos funciones que desempeńa el colon son vitales, en especial por la mitad más proximal. A su vez, el colon derecho es capaz de modular respuestas de adaptación.
Adaptación intestinal frente a una resección
La adaptación intestinal consiste en una mejoría de la morfología del intestino delgado, lo que permite mejorar la absorción de nutrientes, proceso que se habían dańado por causa de la resección. Esta adaptación depende de una serie de factores: en primer lugar, los nutrientes mismos constituyen un factor muy importante y mientras antes lleguen al intestino proximal, mejor será la adaptación. Junto con los nutrientes también son importantes los combustibles endógenos, dentro de los cuales la glutamina y los ácidos grasos de cadena corta son de gran relevancia como combustibles, en especial de las células colónicas. Las secreciones biliopancreáticas y el punto donde se realice la conexión de la vía biliopancreática con el intestino también son importantes, ya que desde ese punto hacia distal se produce mayor proliferación de células e hipertrofia del intestino, lo que causa una mejoría evidente. Respecto a los moduladores intracelulares, en los que se tenía mucha esperanza, su papel no está muy claro aún y, en relación con las prostaglandinas, se sabe que prolongan la vida de los enterocitos, impidiendo la apoptosis de las células intestinales en las vellosidades, en especial la E2. Por último, las poliaminas, sintetizadas a partir de la decarboxilación de la ornitina, son muy importantes, ya que guardan relación con la síntesis de DNA y RNA en el tracto gastrointestinal, tanto en el intestino delgado como en el grueso.
De lo anterior se puede deducir que hay una serie de elementos que se pueden intervenir para mejorar la evolución de estos enfermos. Entre las hormonas conocidas están la hormona del crecimiento, T3 y T4, gastrina, CCK, secretina, enteroglucagón y prolactina. El octiotride, derivado de la somatostatina, es excelente como inhibidor de las secreciones intestinales y, por lo mismo, de gran utilidad en los nińos con secreción elevada. La investigación acerca de estas hormonas y factores está en pleno desarrollo y se ha realizado muchos estudios en animales, los que aún no se han extendido al ser humano, excepto en algunos casos, como el de GLP-2 y leptina. En la actualidad se cree que los cambios de óxido-reducción en el intestino distal podrían causar una clara estimulación de la reparación intestinal, especialmente en las células del intestino delgado, pero trabajos recientes no han logrado demostrarlo.
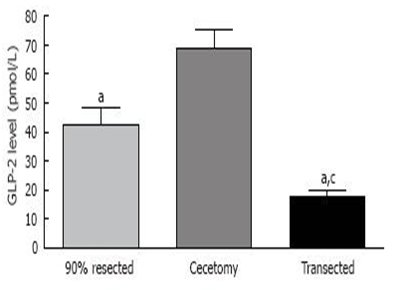
En la Fig. 1, el gráfico muestra los cambios en los niveles del péptido GLP-2, en un experimento realizado en ratas. A un grupo de animales se les resecó 90% de intestino delgado proximal, dejando un remanente de íleon equivalente a 10%; a otro grupo se le practicó una cecostomía y se removió todo el yeyuno, excepto los últimos 20 cm, que se anastomosaron al colon ascendente; y a un tercer grupo se le resecó 90% del intestino proximal, quedando un remanente de 10% de íleon y se alimentó a los animales por vía enteral. En el caso de una resección importante, como la del primer grupo, aumenta la secreción del GLP-2; si se incluye el colon, la respuesta es mayor. Esto demostró que este péptido es importante para la reparación del intestino luego de una resección intestinal e impulsó el desarrollo de homólogos de GLP-2, que se están utilizando en trabajos experimentales en individuos con resección del intestino delgado.
Figura 1. Variación en los niveles de GLP-2 en ratas con diferentes resecciones intestinales (World J Gastroenterology. 2006; 12: 4117-29)
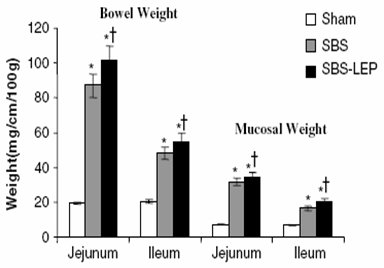
En otro trabajo experimental realizado en ratas se evaluó el efecto de la resección en la secreción de leptinas (Fig. 2). En este caso se observó un aumento de peso del intestino en las ratas a las que se efectuó resección intestinal y se administró leptina; y no sólo aumentó el peso macroscópico, sino que también se observó aumento del DNA y de las proteínas de la mucosa, con cambios bastante significativos. Es decir, cuando el intestino es corto aumenta la cantidad de proteínas en el intestino y, microscópicamente, se observa aumento de la reproducción celular, objetivada mediante el aumento del peso, lo que mejora aún más al agregar leptina. Algo similar se observa a la microscopía óptica, que muestra que la altura de las vellosidades crece significativamente en los casos en que se agrega leptina y también mejora la profundidad de las criptas. De acuerdo con lo anterior, la leptina sería bastante prometedora en estos casos, pero la experiencia y la investigación actual están en etapas muy iniciales.
Figura 2. Efecto de la resección intestinal y del uso de leptina parenteral en el aspecto macroscópico del intestino delgado remanente (Pediatric Surgery Int. 2006; 22: 9-15)
Consecuencias clínicas
La primera consecuencia es la
hipersecreción gástrica que ocurre luego de haber sacado un trozo de intestino productor de hormonas que frenan la secreción gástrica; esta hipersecreción, si bien cesa luego de un ańo, puede producir úlceras y acrecienta la peristalsis intestinal, por aumento del volumen descargado al intestino. Asimismo, el ácido clorhídrico produce un medio intestinal desfavorable para la función de las enzimas pancreáticas y altera la digestión de los nutrientes.
Otra consecuencia es que se producen
cálculos biliares, debido a disminución del
pool de sales biliares y a que se produce bilis litogénica, por lo que 12% de los enfermos con resección intestinal requieren colecistectomía; los
cálculos renales son más bien raros y se deben a mala absorción de las grasas y presencia de oxalatos en circulación; otro problema del que se habla mucho, pero se sabe poco, es la
acidosis láctica; además puede ocurrir
sepsis, habitualmente por infección del catéter, como consecuencia de la sobrepoblación bacteriana y es uno de los peligros más graves a los que se expone el nińo que recibe alimentación parenteral; también puede haber
sobrepoblación bacteriana con cepas más invasivas, lo que obliga a utilizar antibióticos y mezclas de ellos, en tratamientos con dosis bajas y rotación de fármacos, para evitar aparición de resistencia.
La
enfermedad hepática por alimentación parenteral prolongada se ha tratado muchas veces con ácido ursodeoxicólico, pero éste sólo sería eficaz a corto plazo; las bases en que se sustenta este hecho son débiles, pero la experiencia clínica lo avala. La colilsarcosina es un aporte novedoso; algunos trabajos demuestran que este ácido biliar es resistente a la acción bacteriana, de modo que no se re-conjuga, lo que evita que se produzcan ácidos biliares tóxicos para el hígado y le permite ejercer su papel de sal biliar en la absorción de lípidos y vitaminas liposolubles. Los efectos benéficos de esta sustancia están demostrados, pero aún no está al alcance de todas las personas, lo que resulta dramático, porque 10 a 15% de los enfermos trasplantados por este tipo de enfermedad hepática mueren.
Manejo del síndrome de intestino corto
En lo referente a la
alimentación, la disminución de la alimentación parenteral dependerá de la disminución del volumen de las deposiciones o bien, de la salida por ostomía. Se considera que se puede avanzar en la alimentación enteral cuando la cantidad de estos volúmenes disminuye a razón de 40 a 50 ml/kg/día. El ideal es alimentar a estos pacientes con leche materna; si se usan fórmulas, éstas deben ser ricas en lípidos y pobres en hidratos de carbono, en el caso de los lactantes, ya que aquéllos podrían causar intolerancia; lo anterior siempre se debe investigar por medio de la determinación de pH y sustancias reductoras en las deposiciones.
En el nińo mayor de 2 ańos se recomiendan dietas ricas en hidratos de carbono complejos, en especial si hay colon, ya que se presentan todos los efectos positivos de esta dieta. El uso de hidratos de carbono complejos y de ácidos grasos de cadena larga se recomienda en nińos mayores de 2 ańos, junto con adición de vitaminas, minerales y un adecuado aporte de calorías, líquidos, electrolitos y micronutrientes. El objetivo final es moderar o evitar la insuficiencia intestinal. Al respecto, es importante definir cómo está la absorción intestinal, lo que se puede efectuar por medio de 2 marcadores: la citrulina, que se utiliza ampliamente y la 3-oxi-metil-glucosa, un marcador de absorción que también asociada a marcadores de la permeabilidad intestinal, pero que tiene un uso muy restringido.
La propia insuficiencia intestinal conducirá, por último, al trasplante intestinal. Para evitar esta situación está la rehabilitación intestinal, que tiene tres componentes terapéuticos: los propios de la rehabilitación intestinal, la mantención de la alimentación oral o parenteral y el trasplante intestinal.
Con respecto al tratamiento, hay que recalcar la importancia del trabajo en equipo, en que participen cirujano, pediatra, médico experto en nutrición, nutricionistas, enfermeras, kinesiólogos y psicólogos; todos ellos deben participar en el manejo del pacientes desde las primeras etapas, para evitar las complicaciones.

Esta
obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.


 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Expositor:
Julio Espinoza Madariaga[1]
Expositor:
Julio Espinoza Madariaga[1]

