Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del Congreso de Enfermedades Respiratorias 2007, realizado en Pucón los días 7 al 10 de noviembre de 2007. El evento fue organizado por la Sociedad Chilena de Enfermedades Respiratorias.
Presidente Sociedad Chilena de Enfermedades Respiratorias: Dr. Raúl Corrales.
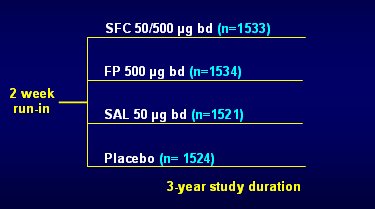
Figura 1. TORCH: diseńo del estudio
Se permitió a los pacientes continuar con todas las medicaciones por condiciones distintas de la EPOC durante el estudio y se permitió llevar a cabo tratamientos para dejar de fumar. Los medicamentos para EPOC permitidos fueron las teofilinas de larga y corta acción, los agentes anticolinérgicos de acción corta y los beta 2 agonistas de acción corta. Se proporcionó salbutamol para su uso como medicamento de rescate, durante todo el estudio. Se suspendió el uso de corticosteroides inhalados y broncodilatadores de acción prolongada, incluidos los beta 2 agonistas de acción prolongada y los agentes anticolinérgicos de acción prolongada en la visita 1 (antes del run-in) y se indicó a los sujetos que no iniciaran tratamiento con estos medicamentos, excepto los proporcionados por el estudio, durante el período de tratamiento. Se prohibió el uso de corticosteroides sistémicos a largo plazo, definido como uso crónico, continuo durante más de 6 semanas). Los sujetos podían tomar cursos cortos de corticosteroides sistémicos si era necesario para el tratamiento de una exacerbación; los cursos cortos de corticosteroides sistémicos separados por un período de menos de 7 días se consideraron como uso continuo. Durante el estudio, incluidos el run-in y el período de seguimiento, se permitieron cambios en la medicación EPOC, por ejemplo, para el tratamiento de las exacerbaciones.
La hipótesis de investigación de Glaxo planteaba que la fluticasona es la molécula que, por su efecto antiinflamatorio, disminuye la inflamación y por lo tanto, la mortalidad; y que la combinación con salmeterol magnifica este efecto. El control fue el placebo, que implica no administrar ninguna de estas dos medicaciones y, a pesar de que la comparación entre ambas no era el objetivo del estudio, se incluyó una rama con fluticasona y una rama con salmeterol, lo que quizás redujo la probabilidad de demostrar el impacto sobre la mortalidad, porque hubo cuatro ramas con 1500 pacientes en cada una, en lugar de dos ramas con 3000 pacientes. Sin embargo, esta base de datos de 1500 personas permitió investigar el efecto del salmeterol solo, lo cual fue positivo, ya que a raíz de los resultados del estudio SMART (The Salmeterol Multicenter Asthma Research Trial) corría el rumor de que el uso de salmeterol estaba asociado a mayor mortalidad.
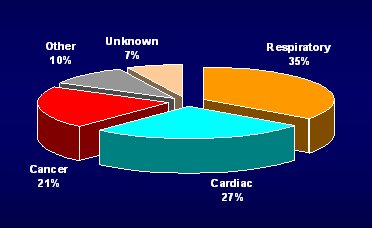
Figura 2. TORCH: Causas de muerte, determinadas según el comité de punto final clínico CEC (Clinical Endpoint Committee)
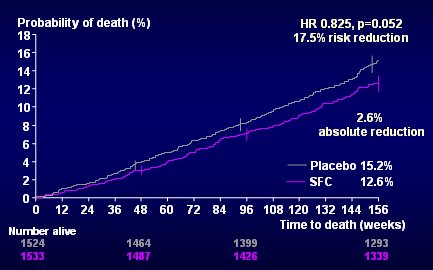
En la Fig. 3 se observa el placebo, en gris y la combinación de salmeterol y fluticasona, en morado: hubo una diferencia de 17% en la disminución del riesgo relativo; la reducción absoluta fue 2,6%. Hay dos formas de interpretar este resultado: se puede decir que el resultado fue negativo, porque el valor de p fue 0,052, aunque, si hubiera sido 0,048, se habría considerado positivo. Sin embargo, si bien este valor es negativo desde el punto de vista estadístico, también está indicando que hubo 5,2 chances en 100 de que el resultado que se observó se deba al azar. Esto puede tener dos explicaciones; en primer lugar, la mortalidad fue menor que lo que se esperaba, se hizo un análisis de probabilidades con base en una mortalidad de 17%, pero la cifra real fue 15%; en segundo lugar, muchos pacientes abandonaron el placebo y es muy probable que al menos la mitad de ellos se hayan tratado posteriormente con esteroides inhalados y salmeterol, pero en el análisis se siguieron considerando por la intención de tratamiento, como si estuvieran en el grupo placebo. Considerando estos elementos, la reducción del riesgo de mortalidad con la combinación cobra mayor importancia (3).
Figura 3. Mortalidad por todas las causas a tres ańos. Curva de placebo y SFC (3)
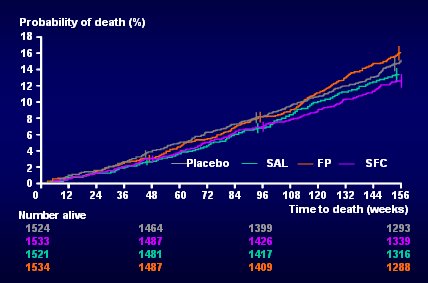
Las otras dos ramas son sumamente interesantes. En la Fig. 4 se muestra en verde el resultado de salmeterol, que fue muy bueno, ligeramente mejor que el placebo. En la rama de salmeterol no hubo muertes fuera de lo común ni dańos de ningún tipo, lo que, desde el punto de vista práctico, significa que un beta agonista de acción prolongada como el salmeterol es útil en pacientes con EPOC y además es bastante seguro. En cuanto a la rama de fluticasona, para quienes creen que la inflamación es el factor central en la EPOC el comportamiento del corticoide fue sorprendente, porque la probabilidad de muerte con fluticasona sola, aunque no fue diferente de placebo o de salmeterol, fue mayor que con la combinación, en forma estadísticamente significativa.
Con estos resultados, quien expone (Dr. Celli) plantea que los esteroides inhalados se deberían administrar siempre en combinación con un beta agonista de acción prolongada en la EPOC y que los patrones y guías de clínicas deberían incorporar estos cambios (3).
Figura 4. Mortalidad por todas las causas a tres ańos. Curvas de placebo, salmeterol, fluticasona y SFC (3)
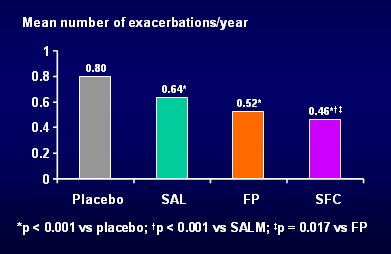
Figura 5. Tasa de exacerbaciones que requirieron corticosteroides sistémicos
La calidad de vida se midió con el SGRQ (St George's Respiratory Questionnaire). Los resultados se muestran en la Fig. 5: con el placebo todos tuvieron cierta mejoría al principio, pero después decayeron y al finalizar los tres ańos estaban peor que al comienzo; con el salmeterol el resultado fue un poco mejor; la curva de la fluticasona fue bastante parecida a la del salmeterol; y la combinación tuvo un resultado significativamente mejor, ya que los pacientes estaban mejor que en su estado basal al cumplir los tres ańos, en contraste con los que recibieron placebo, que estaban significativamente peor después de ese lapso.
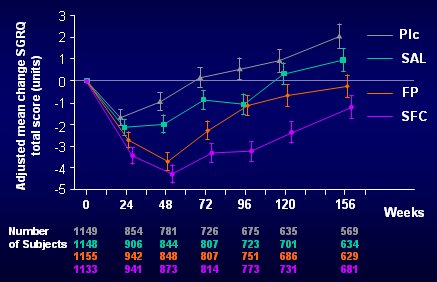
Figura 6. Score SGRQ total
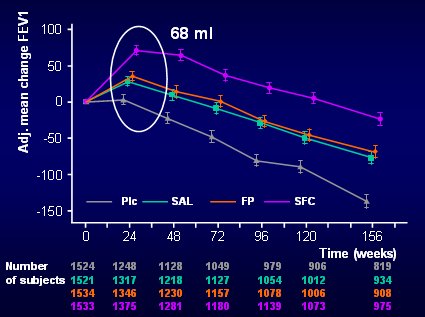
El VEF1 es un verdadero “santo grial” para todo el mundo: todos consideran que los tratamientos deben mejorar el VEF1 y que eso es lo único que importa en EPOC. Pues bien, los hallazgos del estudio TORCH en lo que se refiere al VEF1 fueron muy interesantes. Los pacientes del grupo placebo no mejoraron este parámetro a los seis meses, mientras que todos los demás grupos lo mejoraron, especialmente el grupo que recibió la combinación, en el cual el VEF1 era mayor que el del grupo placebo en 68 ml, como se ve en el gráfico de la Fig. 7.
Figura 7. VEF1 post broncodilatador (ml). Evaluación a los 6 meses
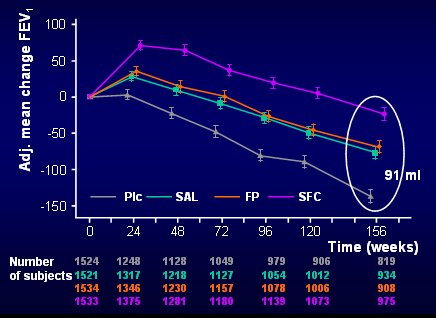
Al finalizar los tres ańos la diferencia entre la curva de SFC y placebo era de 91 ml, lo que significa que no sólo hubo un efecto broncodilatador, sino que a los tres ańos de tratamiento la caída del VEF1 fue mucho mayor en el grupo placebo que en los otros tres, a pesar de que 40% de los pacientes del grupo placebo dejaron de participar en el estudio y se sabe que fueron los que estaban peor (Fig. 8).
Figura 8. VEF1 post broncodilatador: evaluación a los 3 ańos
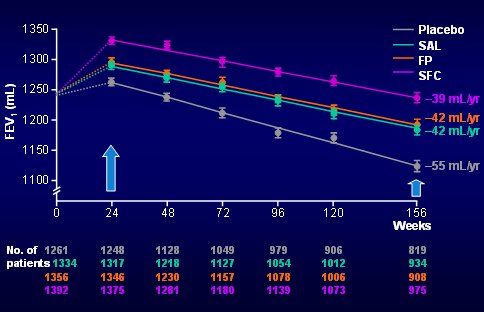
En el siguiente gráfico se observan las mismas curvas, pero en el eje de las “Y” está el VEF1, es decir, aquí no se comparó cada paciente con su principio, sino que se registró su volumen absoluto y se hizo un análisis de la pendiente entre los seis meses y los tres ańos para ver lo que pasó con la pendiente de broncodilatación máxima. La pendiente se identificó con los mismos colores. Se puede ver que hubo una diferencia significativa, de aproximadamente 16 ml, entre la curva de SFC y la de placebo; además hubo una diferencia de 13 ml entre la curva de SFC y las curvas de salmeterol y fluticasona solos. El primer resultado indica que el uso de SFC se asoció a una disminución de 36% en la pendiente de caída del VEF1, en comparación con placebo: es la primera vez que una farmacoterapia logra cambiar esta pendiente.
Figura 9. Tasa de declinación de la función pulmonar: efecto del tratamiento
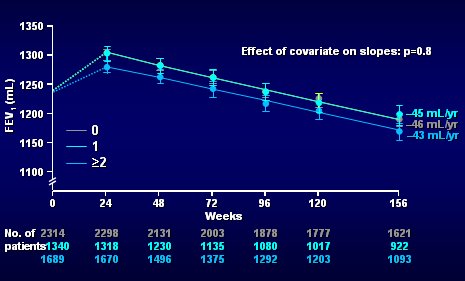
En la Fig. 10 se muestra el mismo gráfico, pero las curvas corresponden a los que presentaron 0, 1 ó 2 o más exacerbaciones en el ańo previo, según interrogatorio, al ingresar al estudio; se puede ver que el número de exacerbaciones en el ańo previo no influye sobre la pendiente de la caída del VEF1 (Fig. 10).
Figura 10. Declinación en el VEF1 según número de exacerbaciones en el ańo previo
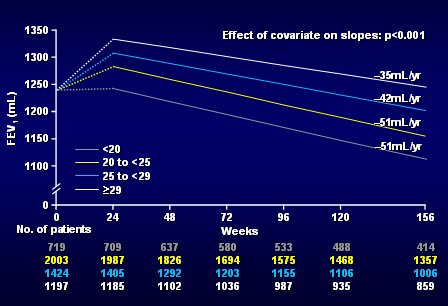
Sí hubo influencia del número de exacerbaciones durante el estudio: a mayor número de exacerbaciones, mayor fue la pérdida de función pulmonar, lo que no es nuevo. Lo novedoso fue la diferencia que se observó en la pérdida de función pulmonar según índice de masa corporal (IMC). Al comparar los individuos delgados, con IMC 20 a 25, con los individuos con IMC de 25 a 29 y con aquellos con IMC mayor de 29, se encontró que los más delgados tuvieron mayor pérdida de función pulmonar. Por lo tanto, para un individuo con EPOC el tener bajo peso es de muy mal pronóstico y esta característica podría ser un biomarcador (Fig. 11).
Figura 11. Declinación en el VEF1 según índice de masa corporal
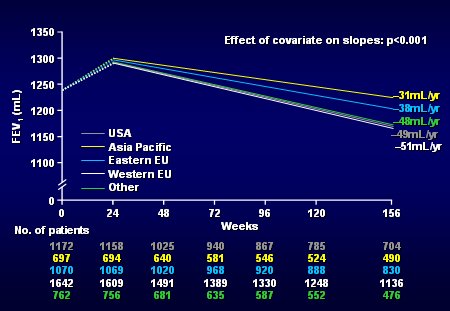
También se comparó la tasa de declinación del VEF1 en distintas regiones del mundo, como Estados Unidos, Asia, Europa Oriental, Europa Occidental, etc. y se encontró que los individuos de países más desarrollados, como Estados Unidos y Europa Occidental, perdieron más función pulmonar que los japoneses y los individuos de Europa Oriental, en forma estadísticamente significativa. La causa de esto no está clara, seguramente existen factores regionales que no se han explorado. Sería interesante ver si en Chile existen diferencias entre los habitantes de las distintas regiones (Fig. 12).
Figura 12. Declinación en el VEF1 según región
Finalmente, al analizar las diferencias por género corrigiendo por la talla, se encontró que la pérdida de función pulmonar fue similar en hombres y mujeres.
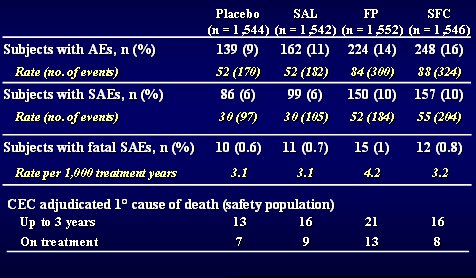
Tabla I. Reporte de neumonía (AE: adverse event; SAE = serious AE; CEC = Clinical Endpoint Committee)
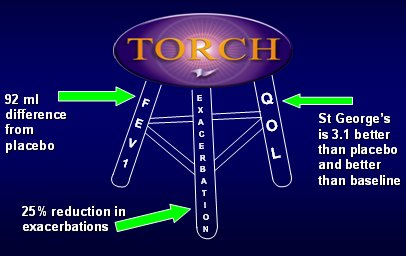
En la Fig. 14 se resumen los resultados del estudio TORCH: en VEF1, 92 ml de diferencia con placebo después de tres ańos, sin mencionar si ese cambio es o no significativo; 25% de reducción de exacerbaciones y hospitalizaciones y St George´s 3,1 unidades mejor que el placebo, al final de tres ańos. Esto, sumado a la baja carga de efectos colaterales, indica que la terapia que combina salmeterol y fluticasona es beneficiosa en pacientes con EPOC. Los datos disponibles sugieren que en los pacientes con EPOC cuyo VEF1 sea menor de 60%, se debería indicar esta medicación.
Figura 13. Resumen de resultados globales del estudio TORCH
La edición y publicación de esta conferencia han sido posibles gracias al auspicio de GlaxoSmithKline
Medwave. Ańo VIII, No. 3, Abril 2008. Derechos Reservados.














 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del Congreso de Enfermedades Respiratorias 2007, realizado en Pucón los días 7 al 10 de noviembre de 2007. El evento fue organizado por la Sociedad Chilena de Enfermedades Respiratorias.
Presidente Sociedad Chilena de Enfermedades Respiratorias: Dr. Raúl Corrales.
 Expositor:
Bartolomé R. Celli[1]
Expositor:
Bartolomé R. Celli[1]

Citación: Celli BR. TORCH study and mortality in COPD: a change in treatment paradigm?. Medwave 2008 Abr;8(3):e900 doi: 10.5867/medwave.2008.03.900
Fecha de publicación: 1/4/2008

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión