Resumen
Este texto completo es la transcripción editada y revisada de la conferencia dictada en el XXXIII Congreso Chileno de Gastroenterologķa, realizado en la ciudad de Vińa del Mar entre los dķas 22 al 24 de noviembre de 2006. El evento fue organizado por la Sociedad Chilena de Gastroenterologķa.
Presidente del Congreso: Dr. Zoltįn Berger Fleiszig.
Secretario Ejecutivo: Dr. Alex Navarro Reveco.
Introducción
A continuación se entregan algunos elementos para el abordaje de la masa pancreįtica inflamatoria, en relación con los antecedentes clķnicos y exįmenes necesarios para el diagnóstico diferencial.
Definición
La masa pancreįtica inflamatoria se define como un tumor sólido, localizado o difuso, cuya causa puede ser una inflamación primaria o secundaria del pįncreas; justamente, el interés fundamental para el clķnico y para el cirujano es determinar si la causa es primaria o secundaria.
Entre las inflamaciones primarias se encuentran la pancreatitis aguda, como la pancreatitis de origen biliar, que no tiene ningśn interés; y la pancreatitis crónica, que sķ tiene interés, porque se debe diferenciar de masas secundarias como el adenocarcinoma y el carcinoma neuroendocrino, que son los mįs frecuentes, y de cualquier tumor periampular.
Casos clķnicos
Se muestra la pieza de resección y la imagenologķa de un caso tķpico de masa secundaria a pancreatitits crónica: se observa litiasis, pequeńos quistes dentro de la cabeza del pįncreas y conductos pancreįticos dilatados: con estos hallazgos no hay ninguna dificultad diagnóstica. Se trata una persona con antecedentes de alcoholismo; la tomografķa muestra que la indicación quirśrgica es clara y la masa es resecable. Se muestra otro caso, de un paciente sin antecedente de alcoholismo: se observa una cabeza pancreįtica heterogénea, con dilatación del tronco de Henle; esta masa heterogénea empuja al duodeno. Un mes después se observa una masa inflamatoria de pancreatitis aguda sobre una pancreatitis crónica, es decir, ésta también puede originar una masa inflamatoria por una reacción aguda. Era una paciente de sexo femenino, de 56 ańos de edad, sin antecedentes de alcoholismo, que tenķa una masa neta en la cabeza del pįncreas que empujaba la arteria mesentérica izquierda y desplazaba al duodeno. Se realizaron tres punciones ecoendoscópicas, que fueron negativas. La paciente presentaba ictericia y distensión de la vesķcula, por lo que se puso un
stent endoscópico, se efectuó derivación biliodigestiva y pancreatoduodenectomķa. La pieza mostró que toda la masa inflamatoria estaba causada por un pequeńo carcinoma pancreįtico; o sea, se podrķa haber seguido puncionando esa masa durante ańos y jamįs se habrķa encontrado citologķa positiva.
Otro caso era el de una paciente de sexo femenino, de 49 ańos de edad, portadora de neurofibromatosis de Von Recklinghausen, que presentó dolor epigįstrico e hiperamilasemia. En la resonancia nuclear magnética se encontró una gran dilatación del conducto en la cabeza del pįncreas, con menor grado de dilatación en el resto del órgano; a nivel de la cabeza habķa una masa que comprimķa al duodeno. Se sabe que los neurofibromas de la enfermedad de Von Recklinghausen se asocian a tumores neuroendocrinos, por lo que se procedió a puncionar la masa dos veces por ecoendoscopķa, con resultados negativos. Al igual que en el caso anterior, se realizó una duodenopancreatectomķa y se demostró que detrįs de esta gran masa inflamatoria habķa un tumor neuroendocrino, con dos ganglios positivos tumorales. Esta paciente se tendrķa que haber operado cuatro o cinco meses antes. Lo anterior demuestra que la citologķa percutįnea y ecoendoscópica no tienen sentido.
Causas de duodenopancreatectomķa
En una revisión de las causas de duodenopancreatectomķa (DPC) en el Hospital Cosme Argerich entre 1993 y 2005, se analizaron 289 casos que tenķan todos los exįmenes disponibles, incluyendo resonancia nuclear magnética y tomografķa axial computarizada. En 181 casos se encontró patologķa maligna y en 108, patologķa benigna.
Para efectos de anįlisis, la patologķa benigna se clasificó en tres tipos: masa sólida; quiste de la cabeza, con o sin dilatación quķstica de los conductos, que son displasias quķsticas, sin mayor importancia; o dilatación de la vķa biliar sin masa, debida a afecciones a nivel papilar o suprapapilar.
De los 106 pacientes operados de DPC por patologķa benigna:
- 22 tenķan masa sólida, de los cuales 11 tenķan diagnóstico preoperatorio de pancreatitis crónica y los otros 11 tenķan diagnóstico preoperatorio dudoso, sin que se pudiera descartar adenocarcinoma (en esa época se operaban las pancreatitis crónicas);
- 64 tenķan neoplasia quķstica, con o sin dilatación quķstica de los conductos;
- 22 casos tenķan obstrucción ductal, con dilatación de la vķa biliar sin masa; entre ellos habķa tres casos de pancreatitis crónica: ésta a veces obstruye el conducto pancreįtico.
Masa pancreįtica: diagnóstico diferencial
El anįlisis de los casos demuestra que la realidad clķnica es que en algunos pacientes no se logra llegar a un diagnóstico claro, ni con exįmenes ni con citologķa, por lo que el diagnóstico diferencial se debe realizar considerando:
- Datos clķnicos: Antecedentes familiares; enfermedades asociadas, como otras neoplasias o enfermedades autoinmunes; sintomatologķa: anorexia y pérdida de peso, que son sķntomas caracterķsticos del adenocarcinoma.
- Radiologķa: Tomografķa axial computarizada, con fase arterial y venosa, que se utiliza siempre; ultrasonido convencional o, rara vez, endoscópico; pet-Scan (tomografķa por emisión de positrones); endoscopķa, siempre; colangiopancreatografķa retrógrada, en contados casos, cuando se sospecha patologķa autoinmune.
- Exįmenes de laboratorio: No sirven los antķgenos tumorales; los autoanticuerpos son śtiles cuando se sospecha pancreatitis crónica autoinmune, que es la entidad que causa mįs problemas de diagnóstico diferencial.
Con respecto a la sensibilidad y especificidad de los exįmenes para hacer el diagnóstico diferencial entre pancreatitis crónica y cįncer de pįncreas:
- La tomografķa axial computarizada tiene sensibilidad 75% y especificidad 70%.
- La resonancia nuclear magnética, 84% de sensibilidad y 81% de especificidad.
- La ecoendoscopķa, 82% y 79%, respectivamente.
- El Pet-Scan tuvo excelentes resultados al principio (99% y 100%), pero después esto no se confirmó. Es śtil cuando no hay inflamación asociada con el tumor, pero cuando hay un cįncer con una masa inflamatoria superpuesta el Pet-Scan darį un falso positivo para pancreatitis. Higashi demostró que no sirve para concluir en casos dudosos, ya que en su estudio obtuvo una sensibilidad de 65% y una especificidad de 93%.
- Algunos afirman que el pronóstico del cįncer pancreįtico no justifica el Pet-Scan, por razones de costo/beneficio, pero esto no es asķ: los cirujanos prefieren saber, en la forma mįs exacta posible, con qué tipo de tumor se van a encontrar. Su mayor utilidad es para medir la progresión de la enfermedad, definir si es difusa o localizada y para predecir la utilidad de la cirugķa.
- CA 19-9: no tiene ninguna utilidad.
- Citologķa preoperatoria: tiene 71% de sensibilidad si se efectśa con tomografķa computarizada y 78% con ecoendoscopķa, porque a veces se punciona la masa inflamatoria secundaria al tumor y no el tumor mismo. Un método con 20% de falsos negativos no puede ser utilizado en tumores de la cabeza del pįncreas.
- Histologķa previa: se utiliza cuando hay evidencia radiológica de irresecabilidad; cuando hay contraindicación para la cirugķa; en caso de sospecha de metįstasis o linfoma y en neoadyuvancia. Nunca se hace histologķa en un enfermo que se considera resecable.
Pancreatitis crónica autoinmune
La pancreatitis crónica autoinmune no siempre se puede distinguir del cįncer, ya que en la tomografķa computarizada se observa, en ambos casos, la misma imagen hipoecogénica, que puede ser difusa o localizada; y en ambos casos puede haber compromiso de la vķa biliar.
Se puede decir que en la pancreatitis crónica alcohólica el diagnóstico diferencial es fįcil y en la pancreatitis autoinmune, difķcil. La denominación de pancreatitis autoinmune tiene varios sinónimos, por ejemplo, el de pancreatitis ducto-obstructiva no alcohólica; pero el mejor nombre es el de pancreatitis esclerosante linfoplasmocitaria, porque tiene las siguientes caracterķsticas: en 30 a 40% de los casos se asocia a otras enfermedades autoinmunes; cursa con aumento de gammaglobulina y de IgG4; hay presencia de linfocitos T CD4+ con predominio del subtipo Th1, que son los que producen factor de necrosis tumoral, IL-2, etc; y se asocia a HLA-DR en los antķgenos leucocitarios.
La lista de enfermedades asociadas a la pancreatitis autoinmune es extensa: colangitis esclerosante primaria; enfermedad de Hashimoto; sķndrome de Sjöegren; cirrosis biliar primaria; lupus; fibrosis retroperitoneal primaria; colitis ulcerosa y enfermedad de Crohn.
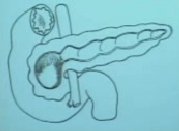
En nuestro centro ya no se utiliza la DPC en pancreatitis crónica alcohólica; ahora se saca la cabeza conservando el duodeno, técnica que tiene varios nombres, pero es mįs conocida como operación de Frey, que evita sacrificar el duodeno. Es la mejor solución para la masa inflamatoria por pancreatitis crónica alcohólica con conductos dilatados (Fig. 1).
Figura 1. Operación de Frey: resección de cabeza de pįncreas con conservación de duodeno
Conclusiones
- El diagnóstico diferencial entre masa pancreįtica maligna y benigna sigue siendo un problema no resuelto.
- En la “realidad clķnica” la duda se plantea hoy en 10% de los casos.
- La cirugķa resectiva se justifica, por la mortalidad actual de la cirugķa pancreįtica y porque es śtil en las masas benignas, con obstrucción ductal.
- En la masa pancreįtica inflamatoria, la resección conservadora, conservando el duodeno, es la mejor opción.

Esta
obra de Medwave estį bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artķculo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artķculo y al medio en que se publica, en este caso, Medwave.

 Esta obra de Medwave estį bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artķculo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artķculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estį bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artķculo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artķculo y al medio en que se publica, en este caso, Medwave.

 Expositor:
Alejandro Orķa[1]
Expositor:
Alejandro Orķa[1]

