Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del II Congreso Chileno de Medicina Nuclear, realizado en Vińa del Mar entre los dķas 6 al 11 de noviembre de 2006. El evento fue organizado por la Sociedad Chilena de Medicina Nuclear.
Presidente de la Sociedad: Dr. Juan Carlos Quintana Fresno.
Presidente Comité Cientķfico: Dra . Teresa Masssardo Vega.
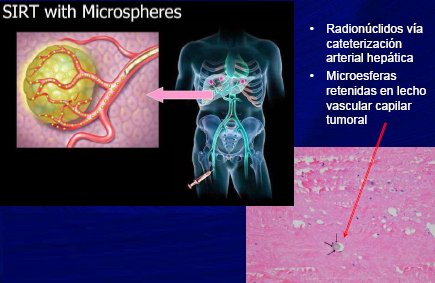
Figura 1. Radio-embolización de tumores hepįticos primarios y secundarios
La radioembolización, igual que la radioterapia dirigida, permite preservar parénquima
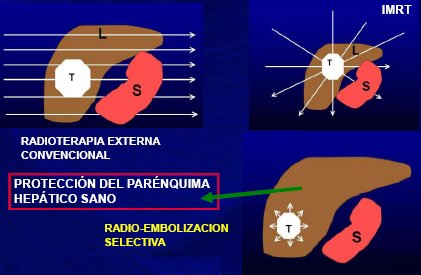
sano y evitar la irradiación masiva que ocurre, por ejemplo, con la radioterapia externa convencional; asimismo, evita el dańo hepįtico difuso debido a la quimioterapia sistémica. Por lo tanto, una de las grandes ventajas de la terapia por radioembolización es que permite entregar una alta dosis de radiación en el tumor y preservar el tejido vecino sano (Fig. 2).
Figura 2. La radio-embolización de tumores hepįticos preserva el tejido sano
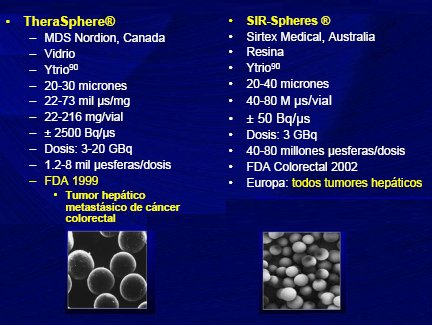
Para la radio-embolización hepįtica se dispone de dos productos comerciales: TheraSphere y SIR-Spheres. El primero es un producto fabricado por MDFS Nordion, de Canadį; son microesferas de vidrio marcadas con itrio 90, cuyo diįmetro es de 20 a 30 micrones y presentan alrededor de 2500 Bq de actividad radionucleidica por microesfera; se administra una dosis de 3 a 20 GBecquerel. La FDA lo aprobó en 1999 para tumores hepįticos metastįticos de cįncer de colon y recto. SIR-Spheres es un producto de Sirtex Medical, Australia; son microesferas de resina marcadas con itrio 90, cuyo diįmetro es de 20 a 40 micrones; entregan aproximadamente 50 Bq por microesfera, una dosis bastante inferior. La FDA lo aprobó en 2002 para cįncer de colon y recto, y en Europa estį aprobado para el tratamiento de todos los tumores hepįticos malignos, tanto primarios como secundarios (Fig. 3).
Figura 3. Radioembolización de tumores hepįticos primarios y secundarios (IRT: Internal Radiation Therapy). Técnicas disponibles
En cuanto a las ventajas y limitaciones de ambos productos: TheraSphere tiene una vida śtil de siete dķas; no produce embolización; su toxicidad es mķnima; la administración es independiente de la masa tumoral; se utilizan pocas esferas por dosis (aproximadamente 12 a 8000 microesferas). Las esferas no son visibles a la radiologķa convencional, lo que limita el control de la administración, y el sistema de administración es bastante engorroso. SIR-Spheres entrega de 40 a 80 millones de microesferas por dosis; su vida media es mįs corta, de 24 horas; su tamańo les permite traspasar el lecho capilar hepįtico y causar embolización sistémica. Los cįlculos dosimétricos son bastante complejos, debido a la difusión sistémica y dependen del volumen tumoral. El riesgo principal de este producto es que, al traspasar el lecho capilar hepįtico, si hay un cortocircuito pulmonar se podrķa producir una embolķa en la circulación cerebral (Fig. 4).
Figura 4. Radio-embolización de tumores hepįticos
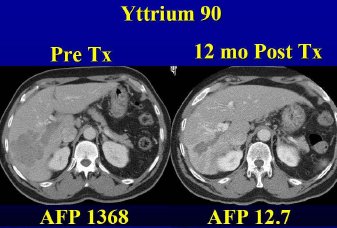
Figura 5. Radio-embolización de tumores hepįticos: control tomogrįfico después de la administración de microesferas
El paciente debe permanecer premedicado con bloqueadores H2 hasta un mes después de la terapia y puede presentar un estado febril o subfebril hasta una semana posterior a ella, sin mayor trascendencia. Se debe controlar las pruebas de función hepįtica y los marcadores tumorales que estuvieran previamente alterados, para observar el efecto terapéutico y se debe hacer un control de imįgenes, con resonancia magnética o escįner, cada dos a cuatro meses. La mįxima respuesta a las microesferas se prevé entre 80 y 90 dķas desde su administración, momento en que se puede programar una segunda dosis si se cumplen los criterios de inclusión (Fig. 6).
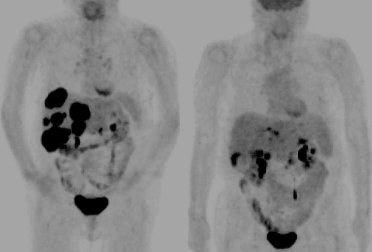
Figura 6. Radio-embolización de tumores hepįticos: control pre y post PET-FDG







 Esta obra de Medwave estį bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artķculo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artķculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estį bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artķculo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artķculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripción editada y revisada de la conferencia dictada en el marco del II Congreso Chileno de Medicina Nuclear, realizado en Vińa del Mar entre los dķas 6 al 11 de noviembre de 2006. El evento fue organizado por la Sociedad Chilena de Medicina Nuclear.
Presidente de la Sociedad: Dr. Juan Carlos Quintana Fresno.
Presidente Comité Cientķfico: Dra . Teresa Masssardo Vega.
 Expositor:
José Canessa[1]
Expositor:
José Canessa[1]

Citación: Canessa J. Nuclear medicine and treatment options I: liver malignancies. Medwave 2007 Oct;7(9):e580 doi: 10.5867/medwave.2007.09.580
Fecha de publicación: 1/10/2007

Nos complace que usted tenga interés en comentar uno de nuestros artķculos. Su comentario serį publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algśn sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polķticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aśn no hay comentarios en este artķculo.
Para comentar debe iniciar sesión