 Para Descargar PDF debe Abrir sesiˇn.
Para Descargar PDF debe Abrir sesiˇn.
Este texto completo es una transcripciˇn editada y revisada de una conferencia que se dictˇ en el Congreso Conjunto de NefrologÝa, Hipertensiˇn y Trasplante realizado en Pucˇn entre el 26 y el 29 de septiembre de 2007. El congreso fue organizado por las Sociedades Chilenas de NefrologÝa, Hipertensiˇn y Trasplante. El presidente de la Sociedad Chilena de NefrologÝa fue el Dr. Alejandro Cotera, la secretaria ejecutiva fue la Dra. MarÝa Eugenia Sanhueza y la directora del curso precongreso fue la Dra. Gloria ValdÚs.
En Chile, la preeclampsia (PE) estß incluida en el Plan AUGE (Atenciˇn Universal con GarantÝas ExplÝcitas), ya que es una de las principales entidades etiolˇgicas de la prematurez. La medicina materno fetal, que es una subespecialidad de la obstetricia, tiene entre sus objetivos reducir las tasas de mortalidad y morbilidad por malformaciones congÚnitas (MC), parto prematuro (PP) e insuficiencia placentaria (IP). Esta charla se enfocarß sobre la IP.
La tasa de mortalidad materna se ha reducido en forma notable entre 1960, en que la cifra era de 299/100.000 nacidos vivos, y el a˝o 2004, en que llegˇ a 17,3. Lo mismo ha ocurrido con la mortalidad infantil, que bajˇ de 120,3 a 8,4/1000 nacidos vivos en el mismo lapso. Seg˙n la proyecciˇn del Ministerio de Salud, se espera que en el a˝o 2010 la mortalidad materna llegue a 12/100.000 y la mortalidad infantil, a 7,5/1000, es decir, en el nivel actual cuesta mucho mßs lograr modificaciones significativas en estos indicadores y para ello se requieren conocimientos mucho mßs especÝficos y acabados de las condiciones que provocan dichas muertes.
Actualmente, la principal causa de mortalidad materna es la PE; 60% de las muertes infantiles estßn dadas por condiciones perinatales; dentro de estas condiciones, el PP es una de las principales causas de morbimortalidad; y 50% de los PP son causados por PE de presentaciˇn grave y precoz durante la gestaciˇn. Por lo tanto, la PE en sÝ misma es una de las principales causas de muerte, tanto materna como infantil y cualquier estrategia de prevenciˇn que se pueda desarrollar serß ˙til para lograr el objetivo sanitario del Ministerio de Salud.
Se define como PP a aquÚl que se produce antes de las 37 semanas de gestaciˇn, pero el que interesa desde el punto de vista de la salud p˙blica es el que se produce antes de las 34 semanas, porque concentra el 70% de la morbimortalidad. De las causas que producen el PP antes de las 34 semanas, alrededor de 50% son condiciones iatrogÚnicas, en que el parto se induce por enfermedad de la madre (PE) o del feto (restricciˇn de crecimiento fetal, RCF). Por lo tanto, la mitad de los PP bajo 34 semanas que ocurren en Chile se debe a PE o RCF y ambas condiciones expresan la presencia de disfunciˇn placentaria. Las cifras del Hospital ClÝnico de la Universidad de Chile indican que 4% de los partos corresponde a partos bajo 34 semanas y dentro de ese 4%, aproximadamente 40% estß dado por disfunciones placentarias, es decir, alrededor de 50% de las causas de prematurez extrema estßn dadas por PE o RCF.
En la hipˇtesis de Redman sobre la fisiopatologÝa de la PE se re˙ne a todas las condiciones llamadas PE y se introduce el concepto de que se trata de un sÝndrome, ya que la etiopatogenia de estas condiciones es muy diversa. Seg˙n esta hipˇtesis, el sÝndrome de la PE estß dado por dos factores. Por una parte, toda mujer embarazada normal presenta una respuesta inflamatoria sistÚmica, cuya exacerbaciˇn conduce al desarrollo de PE; los factores que producen esta exacerbaciˇn, que se asocia a activaciˇn endotelial y de mastocitos y granulocitos, tienen relaciˇn con el tama˝o placentario, como lo sugiere el hecho de que la PE es mucho mßs com˙n hacia el final del embarazo y en mujeres con placentas mßs grandes, como aquÚllas con diabetes gestacional, embarazo gemelar o embarazo molar. Por otro lado, tambiÚn hay una asociaciˇn con placentas de menor tama˝o, que bßsicamente tienen una alteraciˇn de la invasiˇn del trofoblasto extravellositario hacia las arterias espiraladas, que son ramas de las arterias uterinas; cuando dicha invasiˇn, que habitualmente se lleva a cabo entre las 12 y 18 a 20 semanas de gestaciˇn, no se produce en forma fisiolˇgica, se desencadena un estrÚs oxidativo en estas placentas de peque˝o tama˝o, el que desencadena la activaciˇn del endotelio a travÚs de la sÝntesis de un factor a˙n desconocido (Fig. 1).
Figura 1. FisiopatologÝa de la Preeclampsia (1).
Existen distintas condiciones que pueden producir la activaciˇn del endotelio, que es el fenˇmeno fisiopatolˇgico com˙n en todas las mujeres con PE, pero el grupo que interesa detectar es el que tiene alteraciones en la placentaciˇn, porque ese peque˝o grupo, que representa alrededor de 30% de las mujeres que desarrollan PE, es el que sufre PE mßs graves, incluyendo la condiciˇn mßs extrema que es el sÝndrome de HELLP (H por hemˇlisis, EL por enzimas hepßticas elevadas y LP por plaquetas disminuidas), que presenta las mayores cifras de mortalidad materna y perinatal. En este grupo, las alteraciones en la placentaciˇn se pueden detectar precozmente a travÚs de una tÚcnica no invasiva, el doppler de arterias uterinas.
La PE de origen placentario se puede a su vez dividir en dos estadios; en el primero se manifiesta la hipoperfusiˇn del territorio ˙tero-placentario y de la placenta como producto de la alteraciˇn de la placentaciˇn, que consiste en la invasiˇn inadecuada del trofoblasto extravellositario hacia las arterias espiraladas. La isquemia placentaria, a travÚs de factores placentarios y de la respuesta adaptativa hemodinßmica sistÚmica, desencadena la disfunciˇn del endotelio, que es el segundo estadio de la PE, en el cual se reduce el flujo hacia los ˇrganos blanco y se producen las manifestaciones clÝnicas de la enfermedad: hipertensiˇn, proteinuria y alteraciones de la coagulaciˇn (Fig. 2).
Figura 2. Estadios de la preeclampsia.
Actualmente, en el Hospital ClÝnico de la Universidad de Chile, tal como se estß haciendo en todo el mundo, se detecta a las mujeres en riesgo de desarrollar esta condiciˇn del embarazo mediante la ecografÝa, una tÚcnica no invasiva que permite evaluar el flujo ˙tero-placentario y se realiza en dos perÝodos: entre las 11 y 14 semanas (tercer mes), para detectar a la vez defectos fetales, y entre las 22 y 25 semanas de gestaciˇn (quinto mes), para determinar riesgo de parto prematuro, RCF y PE.
La base del cribado en medicina materno-fetal es una combinaciˇn de elementos que se agrupan en factores clÝnicos, ecogrßficos y bioquÝmicos, cuya combinaciˇn permite llevar a cabo un buen programa.
Los elementos clÝnicos del cribado de la PE son aquellos antecedentes de la historia materna que son conocidos factores de riesgo para desarrollar esta condiciˇn, entre ellos: edad mayor de 35 a˝os, Ýndice de masa corporal (IMC) mayor de 30, etnia, que en Chile no es un factor significativo ya que el riesgo es mayor en poblaciˇn afro-caribe˝a, historia obstÚtrica previa, ya que el riesgo aumenta cuatro veces cuando ha habido PE en embarazos previos, y tabaquismo, que aparece como un factor protector para PE. Algunos estudios han relacionado el consumo de tabaco con mejorÝa de la vasculogÚnesis, pero por otra parte produce RCF. Si se utilizan sˇlo los elementos clÝnicos de la anamnesis, la sensibilidad para la detecciˇn de PE severa es de 30%, con 5% de falsos positivos.
El marcador ecogrßfico en la PE es el doppler de arteria uterina, que constituye una forma indirecta de evaluar el flujo ˙tero-placentario y, por lo tanto, del desarrollo de la invasiˇn del trofoblasto. Si Ústa fue inadecuada, el flujo ˙tero-placentario estarß disminuido y se observarß un aumento de la resistencia de la arteria uterina; en cambio, si esta invasiˇn se desarrollˇ en forma adecuada el flujo ˙tero-placentario tendrß muy baja resistencia. En un trabajo publicado en 2005, nuestro grupo de trabajo demostrˇ que la mediciˇn del flujo ˙tero-placentario por vÝa abdominal permite detectar 90% de las PE graves, es decir, con PP antes de las 34 semanas. Ese mismo trabajo se ha replicado haciendo las mediciones por vÝa transvaginal, lo que permite, en forma adicional, predecir el PP a travÚs de la mediciˇn de la longitud cervical. Por lo tanto, un solo examen, la ecografÝa transvaginal, sirve para evaluar el flujo ˙tero-placentario y el cuello uterino y permite predecir los PP, tanto espontßneos como iatrogÚnicos (2).
El doppler transvaginal demuestra que las mujeres que van a desarrollar PE meses despuÚs, a los 7 u 8 meses de embarazo, tienen flujo ˙tero-placentario alterado a las 23 semanas, tanto las que desarrollarßn PE como aquÚllas que desarrollarßn RCF. Pero lo que importa no es tanto observar la diferencia significativa en cuanto a resistencia de esos vasos ˙tero-placentarios, sino encontrar la utilidad clÝnica de esta herramienta. La sensibilidad de esta prueba para predecir PE en forma global, es decir, para todas las mujeres, tanto las que tuvieron el parto antes de las 34 semanas como las que lo tuvieron despuÚs de 37 semanas, es sˇlo 38% y para RCF, que es una definiciˇn a˙n mßs inespecÝfica, es sˇlo 26%. Sin embargo, cuando se analiza la predicciˇn y cribado sˇlo de las condiciones severas, es decir, las que producen mortalidad materna y perinatal, que son aquellas en que el ni˝o nace antes de las 34 semanas de gestaciˇn, la sensibilidad sube a 85% para PE y a 71% para RCF grave. Por lo tanto, el doppler de arteria uterina es ˙til para predecir PE y RCF severos, que tienen relaciˇn con la fisiopatologÝa mencionada, por el hecho de que 30% de las PE en su conjunto se asocian a alteraciˇn del flujo ˙tero-placentario. El doppler no es ˙til en la PE asociada a diabetes gestacional o embarazo gemelar, ya que en estos casos la condiciˇn se debe a una exacerbaciˇn de la respuesta inflamatoria sistÚmica, que lleva a la disfunciˇn endotelial (Fig. 3).
Se sabe que el doppler es ˙til a las 23 semanas de gestaciˇn, pero ese momento es tardÝo, porque el proceso que originˇ la enfermedad ya estß finalizando, aunque no se haya manifestado clÝnicamente; por lo tanto, el ideal es saber quÚ ocurre con esta misma evaluaciˇn entre las 11 y las 14 semanas, cuando el proceso estß reciÚn comenzando. Esto fue evaluado por un grupo inglÚs en el a˝o 2002, en un estudio en que se demostrˇ que el doppler de arteria uterina realizado en este perÝodo tambiÚn es una buena herramienta para la detecciˇn de condiciones severas, con 60% de sensibilidad. Nuestro grupo repitiˇ la experiencia en un proyecto que a˙n estß en curso y la sensibilidad para las condiciones graves fue de 30 a 40%, pero no superior a 50%. Por lo tanto, el doppler de arteria uterina en el primer trimestre no es tan bueno como el del quinto mes, lo cual es lˇgico, ya que esta condiciˇn reciÚn se estß manifestando en el primer trimestre de gestaciˇn y a˙n no ha terminado el proceso de placentaciˇn. Por lo tanto, a este marcador ecogrßfico se le debe adicionar otro marcador.
Los marcadores bioquÝmicos han sido estudiados por nuestro grupo desde el a˝o 2002, con el fin de encontrar alg˙n elemento que mejore la sensibilidad de la ecografÝa de 40% alrededor de las 12 semanas de gestaciˇn y 80% a las 22 semanas. Con base en la fisiopatologÝa de la enfermedad, se midiˇ una serie de parßmetros que, en forma directa o indirecta, representan a cada uno de los eventos fisiopatolˇgicos y se encontrˇ que en el quinto mes de embarazo aumentan los indicadores de estrÚs oxidativo, tales como el F2-isoprostano, marcador de la lipoperoxidaciˇn del ßcido araquidˇnico, en las mujeres que desarrollan PE semanas despuÚs. TambiÚn se comprobˇ que estas mujeres tenÝan una diferencia significativa en los Ýndices de disfunciˇn endotelial y de vasculogÚnesis en relaciˇn con las controles: el receptor soluble del factor de crecimiento vascular, y por lo tanto anti-angiogÚnico, sFlt1 (soluble fms-like tyrosine kinase 1) estaba francamente aumentado y el PlGF (placental growth factor), que es el sÝmil a nivel placentario del VEGF (vascular endothelial growth factor), estaba francamente disminuido en las mujeres que desarrollaron PE meses despuÚs, en comparaciˇn con el grupo control.
Un nuevo marcador de vasculogÚnesis descrito recientemente es la endoglina soluble, que act˙a como co-receptor del TGF y tiene relaciˇn con la vasculogÚnesis y con la placentaciˇn. Lo interesante de este co-receptor es que, unido a sFlt1, favorece especialmente la apariciˇn de alteraciones hepßticas y hematolˇgicas, las cuales se observan en mujeres con PE severa, especialmente en aquellas con HELLP, mucho mßs que sFlt1, el cual se asocia mßs bien con alteraciones renales, favoreciendo la proteinuria y la vasoconstricciˇn. La combinaciˇn de ambos factores, endoglina y sFlt1, podrÝa reflejar el cuadro completo de la condiciˇn preeclßmptica, con todas sus alteraciones patolˇgicas; de hecho, el mismo grupo que demostrˇ que sFlt1 estaba aumentado diez semanas antes de que apareciera esta enfermedad, que es el grupo de Levine y colaboradores, demostrˇ que la endoglina soluble tambiÚn aumenta significativamente diez semanas antes de que aparezca la enfermedad. Sin embargo, estos elementos serÝan mßs bien consecuencia de las alteraciones hipˇxicas de la placenta, mßs que factores predisponentes a esa condiciˇn.
El anßlisis de regresiˇn logÝstica univariado de los marcadores que se midieron en las mujeres a las 23 semanas de gestaciˇn, incluido el doppler de arteria uterina, dio como resultado que cuatro marcadores se asociaron en forma significativa con la apariciˇn de PE: el doppler de arteria uterina, la relaciˇn PAI-1/PAI-2, que es expresiˇn de disfunciˇn endotelial, el F-2 isoprostano, que expresa da˝o oxidativo y el PlGF, que es expresiˇn de la anti-vasculogÚnesis. Sin embargo, el anßlisis multivariado mostrˇ que el ˙nico factor que se asocia en forma significativa e independiente con la apariciˇn de PE es el doppler de arterias uterinas, es decir, el marcador hemodinßmico sigue siendo superior a cualquiera de estos marcadores bioquÝmicos, a las 23 semanas de gestaciˇn. Posteriormente apareciˇ otra revisiˇn en que se tratˇ de combinar todos los marcadores clÝnicos, ecogrßficos y bioquÝmicos; los autores encontraron que con esto se podÝa lograr 90% de sensibilidad, con 5% de falsos positivos, para la predicciˇn de PE severa a las 23 semanas de gestaciˇn. Es decir, a las 22 semanas de gestaciˇn se puede lograr hasta 90% de sensibilidad en la predicciˇn de PE severa, sea utilizando solamente el marcador hemodinßmico o asocißndolo con los marcadores clÝnicos y bioquÝmicos.
La pregunta que se debe responder en el futuro es si existe alg˙n marcador bioquÝmico que pueda ser ˙til para mejorar la sensibilidad actual en el primer trimestre de la gestaciˇn, ya que la prevenciˇn a este nivel serÝa mucho mejor que la que se aplica en el segundo trimestre. Se ha encontrado que la proteÝna placentaria 13, que se relaciona con la placentaciˇn, asociada a doppler de arteria uterina logra una sensibilidad de 80-90% para detectar PE a las 12 semanas, con sˇlo 10% de falsos positivos.
Nuestro grupo evaluˇ los mismos marcadores que se midieron a las 23 semanas y encontrˇ que el ˙nico marcador con una diferencia significativa respecto a lo que sucede en las mujeres controles fue el PlGF, que es un factor vasculogÚnico: las mujeres que desarrollaron PE meses despuÚs tuvieron una reducciˇn del PlGF en la muestra tomada a las 12 semanas de gestaciˇn. Los casos severos fueron sˇlo nueve, pero en ellos se encontraron elementos que se asociaron en forma significativa con la apariciˇn de la enfermedad meses despuÚs: el PlGF y su antagonista el sFlt1, que estaba significativamente aumentado en las mujeres que desarrollarÝan PE severa, en comparaciˇn con los controles. Por otra parte, la endoglina soluble, que apareciˇ como un elemento interesante a las 23 semanas, no tendrÝa mayor importancia a las 12 semanas. Lo interesante es que la combinaciˇn de doppler de arteria uterina con los marcadores bioquÝmicos que resultaron significativos para la predicciˇn de PE severa tiene una sensibilidad de 44%, con 5% de falsos positivos.
Asumiendo que es posible predecir la apariciˇn de preeclampsia, habrÝa que establecer las medidas de prevenciˇn que se deberÝan aplicar a las pacientes de riesgo; sin embargo, ning˙n elemento ha demostrado utilidad. Los metaanßlisis demuestran que la Aspirina disminuye hasta en 15% la incidencia de esta enfermedad, pero en los estudios controlados no se ha encontrado una diferencia significativa en la incidencia de PE en mujeres con doppler de arteria uterina alterado tratadas con Aspirina, en comparaciˇn con el grupo control; en cambio, en el grupo tratado aumentˇ la tasa de desprendimiento placentario, que subiˇ de 2 a 4%. Por otra parte, por ser una enfermedad que se caracteriza por aumento del estrÚs oxidativo se pensˇ que las vitaminas antioxidantes podrÝan jugar un rol en la prevenciˇn de la PE, pero en estudios realizados en pacientes de alto riesgo, asÝ como en otro estudio efectuado en pacientes de bajo riesgo, tampoco se encontraron diferencias significativas en la incidencia de PE y RCF en el grupo tratado con vitaminas antioxidantes, en comparaciˇn con placebo.
Actualmente estß en curso un estudio multicÚntrico nacional, en el que estßn participando las unidades de medicina materno fetal de los hospitales ClÝnico de la U. de Chile, San JosÚ, Barros Luco, San Borja Arriarßn y de los ┴ngeles, donde los resultados preliminares de un estudio piloto mostraron que en las pacientes con doppler de arterias uterinas alterado que recibÝan vitamina antioxidante, la tasa de PE y RCF severos bajaba de 19 a 10%.
Actualmente no existen medidas de prevenciˇn probadamente ˙tiles para las patologÝas asociadas a insuficiencia placentaria, pero estß en estudio la utilidad de los antioxidantes.

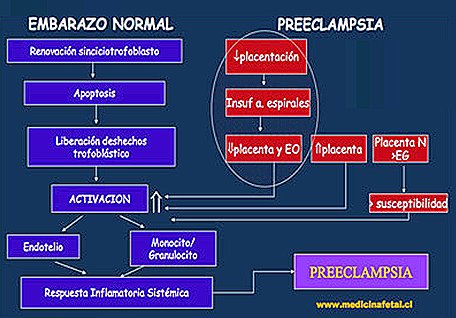 Figura 1. FisiopatologÝa de la Preeclampsia (1).
Figura 1. FisiopatologÝa de la Preeclampsia (1).

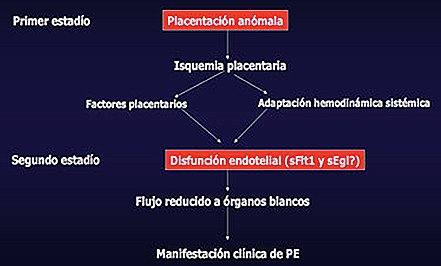 Figura 2. Estadios de la preeclampsia.
Figura 2. Estadios de la preeclampsia.

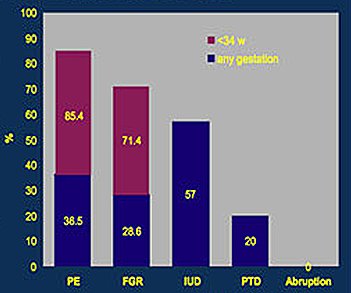 Figura 3. Tasa de detecciˇn de diferentes patologÝas usando doppler de arteria uterina a las 23 semanas.
Figura 3. Tasa de detecciˇn de diferentes patologÝas usando doppler de arteria uterina a las 23 semanas.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuciˇn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciˇn y reproducciˇn del artÝculo en cualquier medio, siempre y cuando se otorgue el crÚdito correspondiente al autor del artÝculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuciˇn-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuciˇn y reproducciˇn del artÝculo en cualquier medio, siempre y cuando se otorgue el crÚdito correspondiente al autor del artÝculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es una transcripciˇn editada y revisada de una conferencia que se dictˇ en el Congreso Conjunto de NefrologÝa, Hipertensiˇn y Trasplante realizado en Pucˇn entre el 26 y el 29 de septiembre de 2007. El congreso fue organizado por las Sociedades Chilenas de NefrologÝa, Hipertensiˇn y Trasplante. El presidente de la Sociedad Chilena de NefrologÝa fue el Dr. Alejandro Cotera, la secretaria ejecutiva fue la Dra. MarÝa Eugenia Sanhueza y la directora del curso precongreso fue la Dra. Gloria ValdÚs.
 Expositor:
Mauro Parra[1]
Expositor:
Mauro Parra[1]

Citaciˇn: Parra M. Prediction and prevention of placental dysfunction (preeclampsia and RCF). Medwave 2008 Ago;8(7):e555 doi: 10.5867/medwave.2008.07.555
Fecha de publicaciˇn: 1/8/2008

Nos complace que usted tenga interÚs en comentar uno de nuestros artÝculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcciˇn editorial considera que su comentario es: ofensivo en alg˙n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polÝticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisiˇn por pares.
A˙n no hay comentarios en este artÝculo.
Para comentar debe iniciar sesiˇn
 Medwave publica las vistas HTML y descargas PDF por artÝculo, junto con otras mÚtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artÝculo, junto con otras mÚtricas de redes sociales.