 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Este texto completo es una transcripci¾n editada de la conferencia que se dict¾ en el V Congreso de la Asociaci¾n Chilena de Nutrici¾n ClĒnica y Metabolismo realizado en Vi±a del Mar entre el 23 y el 26 de Abril de 2008. El congreso fue organizado por la Asociaci¾n Chilena de Nutrici¾n ClĒnica y Metabolismo, bajo la presidencia del Dr. Fernando Carrasco Naranjo.
En esta conferencia se hablarß en general acerca del metabolismo lipĒdico y se entregarß un resumen pragmßtico de los tratamientos que se pueden aplicar en los pacientes con trastornos lipĒdicos, los que para este efecto se clasifican en cinco grupos:
El colesterol LDL se considera elevado si se encuentra sobre 160, 130, 100 o 70 mg/dl, seg·n la categorĒa de riesgo de enfermedad coronaria; seg·n este criterio, un paciente con hipercolesterolemia es aquel que tiene valores mayores de 160 mg/dl sin haber recibido tratamiento. Seg·n las guĒas clĒnicas actuales del Tercer Reporte del Panel de Expertos en Detecci¾n, Evaluaci¾n y Tratamiento de la Hipercolesterolemia en Adultos (GuĒas clĒnicas ATP III), se considera como paciente con hipertrigliceridemia a aquel cuyos valores se encuentran sobre 150 mg/dl, pero ellos encontraron que el riesgo no se relaciona con los TG ni con el colesterol HDL bajo especĒficamente, sino con el nivel de colesterol no-HDL >190, >160,>130, o100 mg/dl, seg·n categorĒa de riesgo.
Se considera hiperlipidemia combinada, en el paciente no tratado, con colesterol LDL sobre 160 y TG sobre 150. El colesterol HDL bajo se considera factor de riesgo cuando su valor es inferior a 40, pero el sĒndrome metab¾lico tiene lugar cuando los niveles son de 50 para las mujeres y 40 para los hombres. Finalmente, la lipoproteĒna (a) se considera como un factor de riesgo independiente cuando se encuentra sobre 30 mg/dL, o la fracci¾n de colesterol unido a lipoproteĒna (a) es mayor de 10 mg/dL. Es importante saber que s¾lo 30% del peso de la molķcula de lipoproteĒna (a) corresponde a colesterol, de modo que se debe tener precauci¾n al analizar los exßmenes para evitar errores de interpretaci¾n (Tabla I).
Tabla I. El paciente con dislipidemia.
En el enfoque inicial del paciente dislipidķmico es importante prestar atenci¾n a las causas de dislipidemia adquirida. Es importante saber que dentro de las causas de dislipidemia se ha vuelto muy interesante el papel del factor genķtico, que en algunos pacientes es determinante en el desarrollo del problema; sin embargo se debe tratar a los pacientes por lo menos hasta la meta terapķutica. A continuaci¾n se mencionan los factores ambientales mßs importantes:
En el estudio MRFIT (Multiple Risk Factor Intervention Trial), que se realiz¾ en una poblaci¾n masculina, se analiz¾ la relaci¾n entre el colesterol total, entre otros factores de riesgo, y mortalidad por enfermedad cardiovascular (1). El autor, Stamler, tiene gran n·mero de publicaciones sobre la relaci¾n que existe entre el colesterol y la insuficiencia cardĒaca (Fig. 1).
En anßlisis de los estudios disponibles sobre el efecto de las estatinas en pacientes con riesgo de insuficiencia cardĒaca o con insuficiencia cardĒaca diagnosticada demuestra que los mayores niveles de LDL tienen una clara relaci¾n con mayor tasa de eventos cardiovasculares (Fig. 2).
Figura 2. Reducci¾n de colesterol LDL en estudios con estatinas.
Actualmente la evidencia sugiere que es mejor reducir el colesterol LDL por debajo de 70 mg/dl en lugar de 100 mg/dl, como se recomendaba en las guĒas clĒnicas del a±o 2001; de modo que es importante establecer nuevas metas y cambios de tratamiento en los pacientes con hipercolesterolemia o altos niveles de colesterol no HDL.
El estudio de Framingham se hizo en gente de raza blanca de clase media, pero se ha demostrado que se correlaciona con los valores de riesgo cardiovascular en el resto del mundo. La pr¾xima actualizaci¾n de las guĒas clĒnicas ATP III, que resultarß en la guĒa ATP IV, asĒ como las guĒas JNC 7 se convertirßn en las guĒas JNC 8 en la primavera de 2010, serß la primera actualizaci¾n que incluya guĒas clĒnicas de obesidad y sobrepeso ademßs del riesgo global en adultos. ┌ltimamente el panel de discusi¾n de expertos se ha reunido nuevamente para elaborar el riesgo global para ni±os, que estarß lista dentro de los pr¾ximos tres a±os.
Con los elementos descritos se define el riesgo como muy alto, moderadamente alto, moderado o bajo. Este ·ltimo se define por la presencia de uno o ning·n factor de riesgo y colesterol LDL < 160; en este caso se considera el tratamiento farmacol¾gico s¾lo cuando el colesterol LDL es superior a 190. El riesgo moderado implica que el paciente tiene un riesgo < 10% en los pr¾ximos diez a±os, con al menos dos factores de riesgo; en el riesgo moderado y moderadamente alto el paciente tiene un riesgo de 10% a 20% o > 20%, respectivamente, en los pr¾ximos diez a±os. La meta para los pacientes de riesgo moderadamente alto es menos de 130 de colesterol LDL y este paciente debe recibir tratamiento farmacol¾gico si su LDL supera ese nivel. En el caso de los pacientes con altos valores de riesgo la meta debe apuntar hacia valores inferiores a 100, pero no se puede considerar lograda si no se producen cambios en el estilo de vida. El nivel absoluto < 70 corresponde a la gente con enfermedad cardĒaca que tiene un riesgo excepcionalmente elevado, como los pacientes cardĒacos que contin·an fumando o los portadores de sĒndrome metab¾lico de causa genķtica no tratado (3) (Tabla II).
Tabla II. Metas para colesterol LDL revisadas (NCEP ATP III).
En cuanto a la dieta, es importante no descuidar las grasas trans en las comidas y recordar que hay otros tipos de grasas animales que no parecen tener el mismo efecto biol¾gico, pero se comportan como trans luego de la digesti¾n oral. Hoy se recomienda reducir las grasas saturadas a menos de 7% de las calorĒas ingeridas; las grasas trans, a cero; el colesterol, a menos de 200 mg diarios y aumentar la fibra dietķtica a mßs de 25 g diarios.
Las estatinas son los fßrmacos que mßs se utilizan para el tratamiento de los pacientes con riesgo de enfermedad cardiovascular o niveles altos de VLDL, incluso con buenos niveles de LDL, ya que logran una reducci¾n de 15 a 60%. En este contexto es importante recordar la regla del 6%, que indica que si se duplica la dosis de fßrmaco se consigue una reducci¾n de s¾lo 6% adicional en el colesterol de LDL. Ezetimiba es el fßrmaco de segunda elecci¾n, porque podrĒa favorecer la regresi¾n del proceso de aterosclerosis aunque reduce los niveles de LDL s¾lo entre 15 y 25%, seg·n los resultados del estudio ENHANCE (Ezetimibe and Simvastatin in Hypercholesterolemia Enhances Atherosclerosis Regression). En dicho estudio se incorpor¾ a pacientes con hipercolesterolemia familiar que habĒan recibido tratamiento previamente; sus valores de colesterol LDL de entrada eran superiores a 210 mg/dl (5,43 mmol/L) con colesterol total de entrada de 390 ml/dl, es decir eran personas con hipercolesterolemia severa. Se asignaron en forma aleatoria 720 pacientes con hipercolesterolemia familiar heterozigota, con valores de colesterol LDL superiores a 210 mg/dl, a tratamiento con simvastatina, 80 mg al dĒa o a la combinaci¾n de simvastatina 80 mg con ezetimiba 10 mg, durante 24 meses. Se observ¾ una reducci¾n de LDL 17% mayor en el grupo de terapia combinada que en el grupo de simvastatina sola (Fig. 3).
Figura 3. ENHANCE: colesterol LDL.
Los triglicķridos tambiķn disminuyeron mßs en el grupo que recibi¾ ezetimiba y ademßs, el colesterol HDL mejor¾ en el grupo que recibi¾ la terapia combinada, mientras que los pacientes tratados con simvastatina s¾lo presentaron reducci¾n en el colesterol LDL (4).
El anßlisis del cambio en el espesor Ēntima/media de la car¾tida (CIMT) no mostr¾ diferencias entre ambos grupos. Sin embargo, el significado de este parßmetro es dudoso; en primer lugar, la metodologĒa para obtenerlo difiere considerablemente en los diversos estudios, de modo que la reproducibilidad es un gran problema; el lugar en que se mide es muy variable, sin que se entregue ninguna raz¾n de porquķ se prefiera la car¾tida com·n, la interna o la externa. Por otra parte, la relaci¾n entre el CIMT y los eventos de insuficiencia cardĒaca cr¾nica es modesta, con 70% de sensibilidad, 50% de especificidad y valor predictivo negativo de alrededor de 80%. Finalmente, un elemento muy importante es que casi no existe evidencia de que el incremento en el CIMT pueda predecir la enfermedad cardiovascular; si asĒ fuera se esperarĒa que las estatinas redujeran los niveles y que en combinaci¾n los redujeran a·n mßs, pero la literatura no entrega ning·n tipo de informaci¾n sobre la composici¾n o la estabilidad de la placa.
No todos los estudios que demuestran los beneficios de la reducci¾n del colesterol para evitar las cardiopatĒas han utilizado estatinas; por ejemplo, el estudio de prevenci¾n coronaria primaria demuestra el beneficio de la colestiramina y se ha demostrado que la cirugĒa barißtrica se asocia a una gran reducci¾n del riesgo de patologĒa cardĒaca cr¾nica, lo que indica que existen otros factores de riesgo que se pueden modificar, ademßs del colesterol. Los secuestrantes de ßcidos biliares pueden reducir el colesterol LDL en 35%; aparentemente la colestiramina y el colestipol son mejores que el colesevelam (WelChol) para reducir el LDL, pero este ·ltimo tiene la ventaja de que se puede administrar conjuntamente con otros medicamentos, mientras que los dos primeros se deben administrar separados de otros fßrmacos para asegurarse de que no exista reacci¾n cruzada entre medicamentos. Este tratamiento es mejor que la ezetimiba en altas dosis, cuyos efectos colaterales pueden limitar su uso. Los esteroles vegetales tienen un efecto moderado y su combinaci¾n con WelChol no entrega efectos benķficos adicionales sobre los niveles de colesterol LDL. Cuando se estß cerca de la meta de reducci¾n la terapia con fibratos puede ofrecer una reducci¾n adicional de colesterol LDL en pacientes con dislipidemia combinada. Finalmente, la niacina es un fßrmaco dķbil en cuanto a su efecto sobre el colesterol LDL, no asĒ sobre los TG y el colesterol HDL.
En resumen, las prescripciones dirigidas a reducir el colesterol LDL tienen los siguientes resultados:
La terapia de afķresis de LDL se utiliza en pacientes con niveles muy altos de colesterol LDL que no han podido alcanzar sus metas terapķuticas mediante tratamiento farmacol¾gico. En la siguiente imagen se muestra el sistema Liposorber« que se utiliza en la afķresis: el paciente se encuentra consciente, su sangre es bombeada mediante una bomba de heparina y pasa a travķs de las columnas Liposorber, que contienen sulfato de dextrano, donde finalmente se remueven las lipoproteĒnas que contienen Apo B, es decir las proteĒnas que ligan el VLDL y el LDL, sin retener las lipoproteĒnas que contienen Apo A (Fig. 4).
Figura 4. Sistema Liposorber«.
La afķresis de LDL estß indicada en pacientes cuyo colesterol LDL es superior a 200 con patologĒa cardĒaca cr¾nica o pacientes con colesterol LDL superior a 300 a pesar de estar con dieta y tratamiento farmacol¾gico con dosis mßxima. En este tipo de paciente se efect·a este tratamiento cada dos semanas para retirar el colesterol LDL de su sangre, lo que permite reanudar en mejor forma su tratamiento (Fig. 5).
La experiencia mundial con el sistema Liposorber«, luego de mßs de 17 a±os de aplicaci¾n en mßs de 2.500 pacientes y mßs de 300.000 tratamientos y algunos estudios clĒnicos, demuestra que el mķtodo es beneficioso. En un estudio realizado en pacientes con hipercolesterolemia familiar y enfermedad coronaria, se hizo seguimiento durante seis a±os para medir la incidencia de eventos cardiovasculares en 43 pacientes que recibieron afķresis de LDL mßs medicaci¾n, con intervalos de catorce dĒas entre cada afķresis, y 87 pacientes que recibieron s¾lo medicaci¾n. Hubo 72% de reducci¾n de eventos cardiovasculares en el grupo de pacientes tratado con Liposorber« y medicamentos en comparaci¾n con los pacientes que se trataron s¾lo con medicamentos, lo que demuestra que el tratamiento con Liposorber« reduce el avance de la enfermedad cardiovascular (5) (Fig. 6).
En la siguiente imagen se resume el resultado de diversos estudios clĒnicos en cuanto al porcentaje de reducci¾n del riesgo cardiovascular; estß el Estudio Escandinavo de Sobrevivencia con Simvastatina (4S), el de Escocia Occidental (WOS), el de Cuidado del Coraz¾n (CARE) y el metaanßlisis CTT, entre otros, y se observa una diferencia de 69 a 78% en el riesgo residual (Fig. 7).
Figura 7. Reducci¾n del riesgo cardiovascular en estudios del efecto de estatinas sobre LDL.
El estudio de Framingham, asĒ como muchos otros que se ha realizado en el mundo, demuestra claramente la relaci¾n directa hipertrigliceridemia y riesgo cardiovascular. Asimismo, estß claro que la relaci¾n entre ambas variables es mßs fuerte en las mujeres al controlar por factores de riesgo (6) (Fig. 8).
Actualmente la evidencia se±ala que existen mejores predictores de riesgo que el colesterol LDL. Estudios observacionales, como el Quebec Cardiovascular Study, el de Moss et al (Circulation 1999), LIPID (placebo) y AMORIS, y estudios de intervenci¾n, como el AFCAPS/TexCAPS (lovastatina) y LIPID (pravastatina) apoyan este punto. La Apo B es superior a cualquiera de los Ēndices de colesterol para reconocer a aquellos pacientes con mayor riesgo de enfermedad vascular y para juzgar la adecuaci¾n de la terapia hipolipemiante; niveles < 90 mg/dl se asocian claramente a un aumento de dicho riesgo. La evidencia tambiķn indica que la relaci¾n Apo B/Apo A es superior a cualquiera de las razones convencionales entre tipos de colesterol en pacientes con enfermedad cardiovascular sintomßtica o diabetes, para evaluar el riesgo de enfermedad cardiovascular relacionado con lipoproteĒnas.
En el manejo de los TG elevados, lo primero es considerar como meta un nivel menor de 400, pero es probable que se deba comenzar a tratar al paciente con 150. Se debe: mejorar la glicemia; reducir el peso; aumentar la actividad fĒsica, aunque esta medida tiene un efecto modesto cuando se controla por otras variables que se pueden modificar con el ejercicio; indicar una dieta adecuada y decidir el uso de medicamentos.
El cuanto al tratamiento dietķtico de la hipertrigliceridemia, con niveles mayores de 1000 mg/dl se debe reducir la grasa de la dieta a menos de 10% y prohibir la ingesta de alcohol; es recomendable suspender todos los medicamentos. Con niveles entre 200 y 1000 mg/dl se debe restringir las grasas por debajo de 25-30%; si a pesar a esto los TG se mantienen elevados se debe reducir la ingesta de hidratos de carbono. No se puede permitir la ingesta de alcohol hasta que los TG bajen a menos de 300 mg/dl y se debe aumentar la ingesta de fibra por sobre 25 g diarios (7). El rango de reducci¾n de los triglicķridos con las drogas es: fibratos, 30-50%; ßcido nicotĒnico, 10-30%; estatinas, 0-35%; ßcidos grasos omega-3, 15-35%.
La gran pregunta es si la reducci¾n de TG realmente reduce el riesgo cardiovascular. El Helsinki Heart Study, un estudio abierto de seguimiento (8) sugiere que si los TG estßn sobre 180-200 mg/dl su reducci¾n reducirß el riesgo cardiovascular. En el estudio de prevenci¾n de infarto con bezafibrato (9) no hubo grandes cambios con la administraci¾n de este fßrmaco, y en el estudio VA-HIT no se encontr¾ relaci¾n entre la magnitud de la disminuci¾n de los TG y la reducci¾n del riesgo de patologĒa cardĒaca cr¾nica (10). Falta aclarar si existe alg·n mecanismo mediante el cual la reducci¾n de los TG pueda reducir el riesgo de enfermedad cardiovascular; se sabe que los fibratos tienen mecanismos por los cuales reducen los niveles de lĒpidos, tanto de los no ligados a proteĒnas como de los lĒpidos dependientes de lipoproteĒnas.
El colesterol HDL, conocido como ōbuenoö, tiene un impacto compuesto mßs que aditivo sobre el riesgo cardiovascular, en conjunto con la reducci¾n del colesterol LDL (estudio PROCAM, 177 eventos, 4.263 hombres de 40 a 65 a±os de edad). Se cree que podrĒa prevenir los accidentes de placa, la liberaci¾n de coßgulos a la circulaci¾n y los ataques cardĒacos, promoviendo las reacciones endoteliales que favorecen la salida de los LDL modificando el transporte de colesterol (Fig. 9).
Figura 9. Impacto de LDL y HDL sobre el riesgo de enfermedad cardiovascular.
La forma mßs apropiada de incrementar el colesterol HDL a travķs de la dieta es mediante la pķrdida de 10% del peso corporal; tres meses despuķs de mantener esta pķrdida se debe medir de nuevo el colesterol HDL. Las grasas saturadas tambiķn incrementan los valores de HDL, pero en ese caso los niveles de LDL tambiķn se incrementan. El alcohol no es considerado como un fßrmaco de prescripci¾n; en cambio el ejercicio aer¾bico es importante, porque permite perder grasa y cambiar la composici¾n corporal. En cuanto a medicamentos, la niacina es el fßrmaco de elecci¾n para incrementar el colesterol HDL, seguido por fibratos, estatinas y resinas, aunque el mejor efecto se ha observado luego de la administraci¾n de inhibidores de proteĒna transportadora de ķsteres de colesterol (CETP).
El efecto de los fßrmacos sobre los niveles de colesterol HDL tiene los siguientes rangos:
En cuanto a la evidencia disponible para sostener que el incremento del colesterol HDL reduce la cardiopatĒa, el estudio ARBITER-2 (Arterial Biology for the Investigation of the Treatment Effects of Reducing Colesterol) demostr¾ que la adici¾n de niacina al tratamiento de reducci¾n de las grasas con estatinas aumenta los niveles de colesterol HDL y reduce la progresi¾n de la patologĒa cardĒaca cr¾nica para el mismo valor de LDL (Fig. 10). Asimismo, en los pacientes con altos niveles de HDL tratados con niacina se observ¾ una reducci¾n del CIMT luego de tres meses (11).
El torcetrapib, fßrmaco prototipo dentro de los inhibidores de la proteĒna transportadora de ķsteres de colesterol (CETP), incrementa en gran magnitud los niveles de HDL; sin embargo, un estudio realizado para ver la relaci¾n entre los efectos favorables a nivel de lĒpidos y la reducci¾n de eventos cardiovasculares se tuvo que detener en forma prematura debido a que se produjo un aumento del riesgo de muerte y eventos cardĒacos en el grupo que estaba recibiendo el fßrmaco; luego de una inversi¾n de millones de d¾lares el medicamento fue discontinuado (12). Los autores del estudio descrito plantearon que los efectos adversos asociados a la terapia con torcetrapib se podrĒan explicar por un aumento importante de la presi¾n sanguĒnea. Existen otros dos o tres fßrmacos inhibidores de proteĒna transportadora que a·n no han llegado a la fase de pruebas clĒnicas. Por lo tanto, por ahora se debe enfocar el tratamiento en obtener la meta de reducci¾n de LDL; despuķs de conseguir esto se puede considerar aumentar el HDL.
En pacientes con sĒndrome metab¾lico, con o sin diabetes, la atorvastatina administrada en forma permanente despuķs del primer evento cardiovascular mayor redujo en forma significativa el riesgo de nuevos eventos y este efecto fue mayor con dosis de 80 mg que con dosis de 10 mg diarios (13). Otro elemento importante es la lipoproteĒna A o Apo (a), un precursor de LDL que se comporta como proteĒna ligando entre la superficie celular y este lĒpido. Ademßs estas lipoproteĒnas pueden promover la trombosis gracias a sus cadenas laterales, porque esta peque±a parte act·a como activador tisular plasmßtico provocando finalmente fibrinolisis. El estudio mßs reciente sobre la relaci¾n entre los niveles de Apo (a) y el riesgo de infarto de miocardio es el Copenhague City Heart Study, en el cual se observ¾ un aumento progresivo del riesgo a medida que aumenta la Apo (a); los niveles extremos de esta lipoproteĒna a una tasa de infartos 3 a 4 veces mayor en la poblaci¾n general (14).
En la prßctica, en el paciente con dislipidemia con Apo (a) superior a 30 mg/dl:

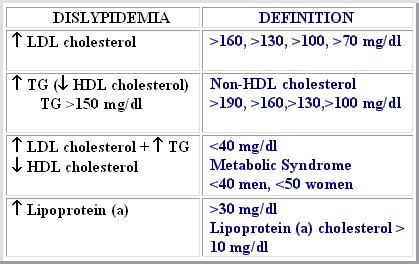 Tabla I. El paciente con dislipidemia.
Tabla I. El paciente con dislipidemia.

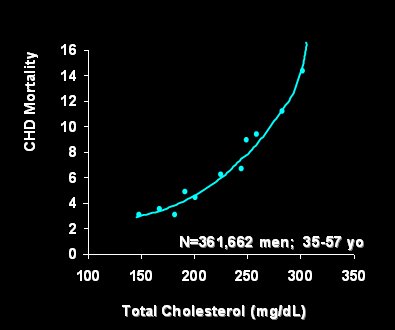 Figura 1. Estudio MRFIT: Mortalidad por enfermedad cardiovascular ajustada por edad (por 1.000 personas).
Figura 1. Estudio MRFIT: Mortalidad por enfermedad cardiovascular ajustada por edad (por 1.000 personas).

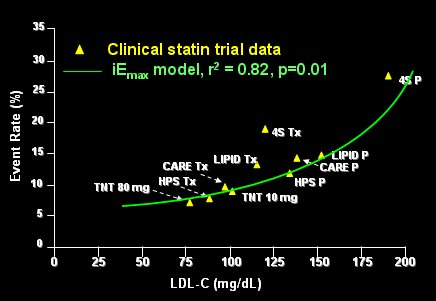 Figura 2. Reducci¾n de colesterol LDL en estudios con estatinas.
Figura 2. Reducci¾n de colesterol LDL en estudios con estatinas.

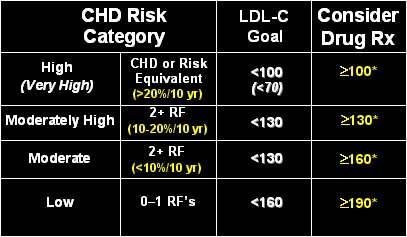 Tabla II. Metas para colesterol LDL revisadas (NCEP ATP III).
Tabla II. Metas para colesterol LDL revisadas (NCEP ATP III).

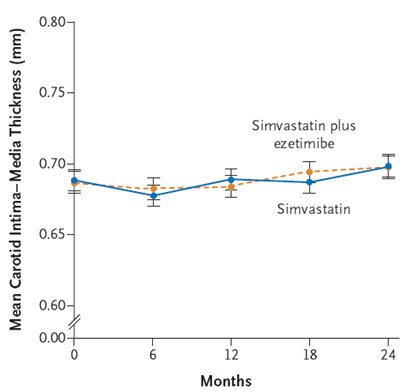 Figura 3. ENHANCE: colesterol LDL.
Figura 3. ENHANCE: colesterol LDL.

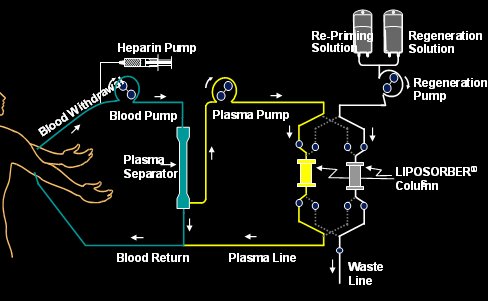 Figura 4. Sistema Liposorber«.
Figura 4. Sistema Liposorber«.

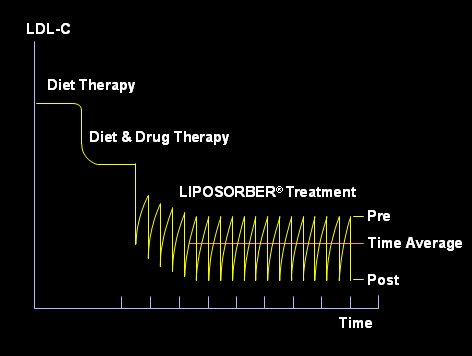 Figura 5. Afķresis de LDL.
Figura 5. Afķresis de LDL.

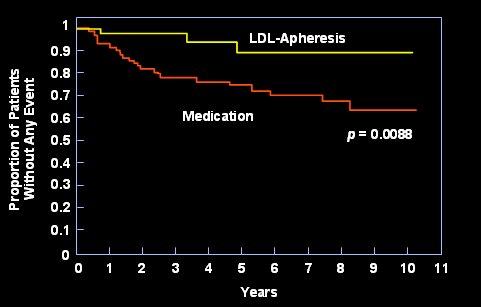 Figura 6. Curvas de Kaplan-Meier para pacientes con hipercolesterolemia familiar sin enfermedad cardiovascular.
Figura 6. Curvas de Kaplan-Meier para pacientes con hipercolesterolemia familiar sin enfermedad cardiovascular.

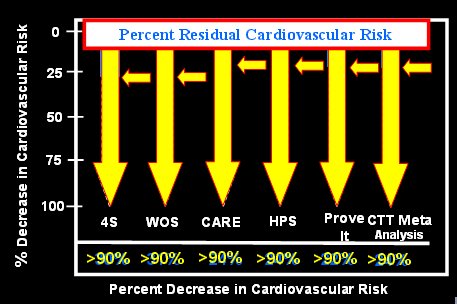 Figura 7. Reducci¾n del riesgo cardiovascular en estudios del efecto de estatinas sobre LDL.
Figura 7. Reducci¾n del riesgo cardiovascular en estudios del efecto de estatinas sobre LDL.

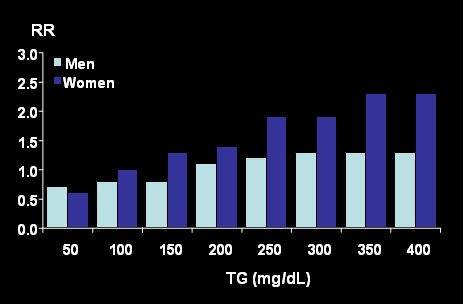 Figura 8. Impacto de los niveles de triglicķridos sobre el riesgo relativo de enfermedad cardiovascular: Framingham Heart Study.
Figura 8. Impacto de los niveles de triglicķridos sobre el riesgo relativo de enfermedad cardiovascular: Framingham Heart Study.

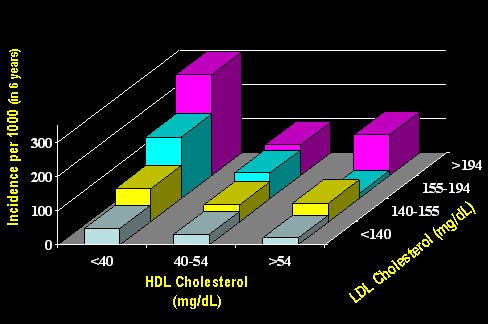 Figura 9. Impacto de LDL y HDL sobre el riesgo de enfermedad cardiovascular.
Figura 9. Impacto de LDL y HDL sobre el riesgo de enfermedad cardiovascular.

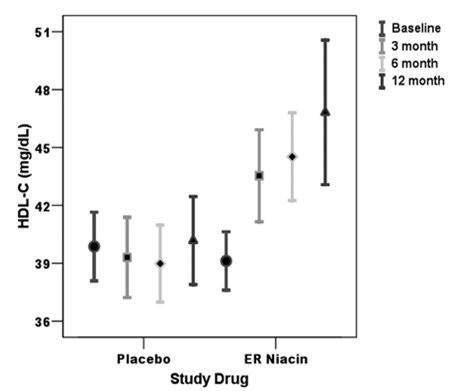 Figura 10. Arbiter 2: Cambios inducidos por niacina en el colesterol HDL, en pacientes tratados con estatinas.
Figura 10. Arbiter 2: Cambios inducidos por niacina en el colesterol HDL, en pacientes tratados con estatinas.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es una transcripci¾n editada de la conferencia que se dict¾ en el V Congreso de la Asociaci¾n Chilena de Nutrici¾n ClĒnica y Metabolismo realizado en Vi±a del Mar entre el 23 y el 26 de Abril de 2008. El congreso fue organizado por la Asociaci¾n Chilena de Nutrici¾n ClĒnica y Metabolismo, bajo la presidencia del Dr. Fernando Carrasco Naranjo.
 Autor:
Robert Eckel[1]
Autor:
Robert Eckel[1]

Citaci¾n: Eckel R. New drug options in dyslipidemias. Medwave 2009 May;9(5):e3915 doi: 10.5867/medwave.2009.05.3915
Fecha de publicaci¾n: 1/5/2009

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Stamler J, Wentworth D, Neaton JD. Is relationship between serum cholesterol and risk of premature death from coronary heart disease continuous and graded? Findings in 356,222 primary screenees of the Multiple Risk Factor Intervention Trial (MRFIT). JAMA. 1986 Nov 28;256(20):2823-8. | CrossRef | PubMed |
Stamler J, Wentworth D, Neaton JD. Is relationship between serum cholesterol and risk of premature death from coronary heart disease continuous and graded? Findings in 356,222 primary screenees of the Multiple Risk Factor Intervention Trial (MRFIT). JAMA. 1986 Nov 28;256(20):2823-8. | CrossRef | PubMed | Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA. 2001 May 16;285(19):2486-97. | CrossRef | PubMed |
Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA. 2001 May 16;285(19):2486-97. | CrossRef | PubMed | Grundy SM, Cleeman JI, Merz CN, Brewer HB Jr, Clark LT, Hunninghake DB, et al. Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines. Circulation. 2004 Jul 13;110(2):227-39. | CrossRef | PubMed |
Grundy SM, Cleeman JI, Merz CN, Brewer HB Jr, Clark LT, Hunninghake DB, et al. Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines. Circulation. 2004 Jul 13;110(2):227-39. | CrossRef | PubMed | Kastelein JJ, Akdim F, Stroes ES, Zwinderman AH, Bots ML, Stalenhoef AF, et al. Simvastatin with or without ezetimibe in familial hypercholesterolemia. N Engl J Med. 2008 Apr 3;358(14):1431-43. Epub 2008 Mar 30. | CrossRef | PubMed |
Kastelein JJ, Akdim F, Stroes ES, Zwinderman AH, Bots ML, Stalenhoef AF, et al. Simvastatin with or without ezetimibe in familial hypercholesterolemia. N Engl J Med. 2008 Apr 3;358(14):1431-43. Epub 2008 Mar 30. | CrossRef | PubMed | Mabuchi H, Koizumi J, Shimizu M, Kajinami K, Miyamoto S, Ueda K, et al. Long-term efficacy of low-density lipoprotein apheresis on coronary heart disease in familial hypercholesterolemia. Hokuriku-FH-LDL-Apheresis Study Group. Am J Cardiol. 1998 Dec 15;82(12):1489-95. | CrossRef | PubMed |
Mabuchi H, Koizumi J, Shimizu M, Kajinami K, Miyamoto S, Ueda K, et al. Long-term efficacy of low-density lipoprotein apheresis on coronary heart disease in familial hypercholesterolemia. Hokuriku-FH-LDL-Apheresis Study Group. Am J Cardiol. 1998 Dec 15;82(12):1489-95. | CrossRef | PubMed | Castelli WP. Cholesterol and lipids in the risk of coronary artery disease--the Framingham Heart Study. Can J Cardiol. 1988 Jul;4 Suppl A:5A-10A. | PubMed |
Castelli WP. Cholesterol and lipids in the risk of coronary artery disease--the Framingham Heart Study. Can J Cardiol. 1988 Jul;4 Suppl A:5A-10A. | PubMed | Capell WH, Eckel RH. Severe hypertriglyceridemia with a history of treatment failure. Nat Clin Pract Endocrinol Metab. 2005 Nov;1(1):53-8; quiz 59. | CrossRef | PubMed |
Capell WH, Eckel RH. Severe hypertriglyceridemia with a history of treatment failure. Nat Clin Pract Endocrinol Metab. 2005 Nov;1(1):53-8; quiz 59. | CrossRef | PubMed | Bloomfield HE. The role of fibrates in a statin world. Arch Intern Med. 2006 Apr 10;166(7):715-6. | CrossRef | PubMed |
Bloomfield HE. The role of fibrates in a statin world. Arch Intern Med. 2006 Apr 10;166(7):715-6. | CrossRef | PubMed | Secondary prevention by raising HDL cholesterol and reducing triglycerides in patients with coronary artery disease: the Bezafibrate Infarction Prevention (BIP) study. Circulation. 2000 Jul 4;102(1):21-7. | PubMed |
Secondary prevention by raising HDL cholesterol and reducing triglycerides in patients with coronary artery disease: the Bezafibrate Infarction Prevention (BIP) study. Circulation. 2000 Jul 4;102(1):21-7. | PubMed | Robins SJ, Rubins HB, Faas FH, Schaefer EJ, Elam MB, Anderson JW, et al. Insulin resistance and cardiovascular events with low HDL cholesterol: the Veterans Affairs HDL Intervention Trial (VA-HIT). Diabetes Care. 2003 May;26(5):1513-7. | CrossRef | PubMed |
Robins SJ, Rubins HB, Faas FH, Schaefer EJ, Elam MB, Anderson JW, et al. Insulin resistance and cardiovascular events with low HDL cholesterol: the Veterans Affairs HDL Intervention Trial (VA-HIT). Diabetes Care. 2003 May;26(5):1513-7. | CrossRef | PubMed | Taylor A, Sullenberger L, Lee H, Lee J, Grace K. Arterial biology for the investigation of the treatment effects of reducing cholesterol (ARBITER) 2: A double-blind, placebo-controlled study of extended-release niacin on atherosclerosis progression in secondary prevention patients treated with statins. Circulation. 2004; 110: 3512-7. | CrossRef | PubMed | Link |
Taylor A, Sullenberger L, Lee H, Lee J, Grace K. Arterial biology for the investigation of the treatment effects of reducing cholesterol (ARBITER) 2: A double-blind, placebo-controlled study of extended-release niacin on atherosclerosis progression in secondary prevention patients treated with statins. Circulation. 2004; 110: 3512-7. | CrossRef | PubMed | Link | Barter P, Gotto AM, LaRosa JC, Maroni J, Szarek M, Grundy SM, et al. HDL cholesterol, very low levels of LDL cholesterol, and cardiovascular events. N Engl J Med. 2007 Sep 27;357(13):1301-10. | CrossRef | PubMed |
Barter P, Gotto AM, LaRosa JC, Maroni J, Szarek M, Grundy SM, et al. HDL cholesterol, very low levels of LDL cholesterol, and cardiovascular events. N Engl J Med. 2007 Sep 27;357(13):1301-10. | CrossRef | PubMed |