 Para Descargar PDF debe Abrir sesi¾n.
Para Descargar PDF debe Abrir sesi¾n.
Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada en el marco del Congreso Conjunto de NefrologĒa, Hipertensi¾n y Trasplante 2007, realizado en Puc¾n entre los dĒas 26 al 29 de septiembre de 2007. El evento fue organizado por la Sociedad Chilena de NefrologĒa, Hipertensi¾n y Trasplante.
Presidente Sociedad Chilena de NefrologĒa: Dr. Alejandro Cotera.
Secretaria Ejecutiva: Dra. MarĒa Eugenia Sanhueza.
Directora Curso Precongreso: Dra. Gloria Valdķs.
texto
Desde que el blastocisto se implanta en el útero hasta que el niño nace ocurre una larga, progresiva y permanente demanda hemodinámica, que determina cambios hemodinámicos y humorales muy importantes. Entre los más significativos están los siguientes: la actividad de renina plasmática aumenta en 6,4 ng/ml/h, la aldosterona plasmática en 2.556 pmol/L, el índice cardíaco en 0,9 l/min/m2 y el volumen plasmático aumenta en 1.250 ml, mientras la masa globular sólo lo hace en 250 ml. La alteración independiente de varios de estos factores podría causar hipertensión arterial en una mujer no embarazada; así, si se alcanzan niveles similares a los de aldosterona en plasma por secreción de un tumor suprarrenal, la mujer desarrolla una hipertensión importante. En cambio, en el embarazo la presión arterial (PA) disminuye, principalmente en el segundo trimestre, la sistólica (PAS) en 3 mmHg y la diastólica (PAD) en 7 mmHg, lo que se debe una disminución de la resistencia vascular periférica (RVP) de 389 dyn/s/cm5.
Gant infundió angiotensina II (AT II) a embarazadas, y observó que las mujeres que cursaron embarazos normotensivos requerían a lo largo del embarazo una dosis significativamente mayor que la que requerían esas mismas mujeres en condiciones de no embarazo. Además, demostró que las mujeres que posteriormente desarrollaban un embarazo hipertensivo empezaban requerir dosis menores a partir de las 18 semanas, lo que se explica por mayor sensibilidad al vasoconstrictor (1). Esta intervención ha sido empleada para predecir los embarazos que se complicarán posteriormente con hipertensión. Lo anterior prueba que en el embarazo normal existe una disminución de la reactividad vascular, la que, en presencia del marcado aumento de factores presores, hay que atribuir a un estímulo de los sistemas vasodilatadores.
En la Fig. 1 se muestra el sistema calicreína-cinina contrapuesto al sistema vasoconstrictor por excelencia, el renina-angiotensina. Calicreína, actuando sobre el cininógeno, genera bradicinina que, además de ser un vasodilatador per se constituye un potente estímulo para la síntesis de óxido nítrico (NO) y de prostaciclina. Además, en los últimos años el grupo de Ferrario ha descrito una angiotensina vasodilatadora, angiotensina-(1-7), que forma parte de una red de vasodilatadores que se estimulan y potencian entre sí (en recuadros rojos se destacan los factores que han sido estudiados por nuestro grupo).
Figura 1. Principales sistemas vasoactivos
En la Fig. 2 se observa que la excreción urinaria de GMP-c, el segundo mensajero de NO, aumenta a lo largo del embarazo normal. En la preeclampsia, si bien hay una hay mayor dispersión de los valores, los promedios son iguales (2). Por otra parte, las mediciones de nitratos y nitritos durante el embarazo han dado resultados discordantes.
Figura 2. Excreci¾n urinaria de GMPc, segundo mensajero de NO, en el embarazo (2)
Estudios en que se han medido los metabolitos urinarios de prostaciclina y tromboxano en embarazo normal y preeclampsia, han demostrado que prostaciclina disminuye, y tromboxano aumenta, en mujeres que desarrollan preeclampsia, por lo que en ellas la relación entre prostaciclina y tromboxano está a favor de este último, que es un vasoconstrictor y agregante plaquetario (3). De estas experiencias, con prostaciclina y tromboxano circulante, urinario y placentario, fundamentalmente del grupo de Walsh, deriva el uso de aspirina en bajas dosis, con sus ventajas y limitaciones.
Nuestro grupo inició los estudios dirigidos a evaluar la excreción urinaria de calicreína, esperando que esta enzima que integra un sistema vasodilatador, fuera un sistema contrarregulador de los factores vasopresores. Sin embargo, al contraponer la curva de calicreína con la actividad de renina en el embarazo se encontró que calicreína excretada en orina, que refleja la síntesis renal, se eleva a al inicio del embarazo para descender posteriormente mientras la actividad de renina permanecía en valores elevados. La falta de concordancia entre los niveles del factor vasoconstrictor y el vasodilatador nos hizo dudar del rol contrarregulador de esteúltimo. Un estudio posterior, realizado en 10 mujeres que cursaron embarazos normotensivos, en las que obtuvimos muestras de orina en intervalos pequeños, demostramos que calicreína urinaria alcanza un peak entre las 8 y 12 semanas de gestación, etapa que corresponde al periodo de placentación, para luego descender. En estudios de Elebute y Mills se encontró que en embarazos hipertensivos la excreción promedio de calicreína promedio fue más bajo, aunque existía una sobreposición con los valores normales (Fig. 3) (4).
Figura 3. CalicreĒna urinaria a lo largo del ciclo, gestaci¾n normal y lactancia
En relación a angiotensina-(1-7), en un trabajo efectuado por nuestro grupo en conjunto con Brosnihan se observó un ascenso progresivo a lo largo del embarazo, lactancia y ciclo, en las mismas orinas empleadas en el estudio de calicreína. Es interesante contraponer los niveles de calicreína urinaria y los de angiotensina-(1-7), y constatar que mientras calicreína desciende angiotensina-(1-7), aumenta a medida que progresa la gestación (Fig. 4). Al comparar los niveles circulantes de angiotensina-(1-7) en mujeres con embarazo normal y con preeclampsia, el factor vasodilatador estaba disminuido significativamente en el segundo grupo (5).
Es muy posible que en un medio tan cambiante desde el punto de vista hormonal, en cuanto a niveles de hormona gonadotrófica, estrógenos y progesterona, los distintos vasodilatadores deben relevarse para mantener la vasodilatación a lo largo del embarazo.
Lo expuesto hasta ahora es lo que ocurre en la circulación o en la orina materna, pero la atención debiera estar puesta en el sitio en que se ha identificado el origen de la preeclampsia. Se ha analizado el estado de los factores vasodilatadores en relación con la hemodinamia materna, que requiere una importante adaptación para aumentar el flujo de la unidad feto-placentaria, pero la situación más crítica se presenta en la unión feto-placentaria. El feto necesita que el espacio intervelloso sea bañado por un abundante sangre materna, la que proviene de arterias uterinas transformadas de vasos cilíndricos con músculo liso en espacios saculares que han perdido su musculatura. Además, el feto debe asegurar su circulación e intercambio de nutrientes y desechos, vasodilatando los capilares de las vellosidades fetales.
En la Fig 6 se muestra la diferencia en la transformación de las arterias espirales entre un embarazo normal, en que se produce una invasión profunda, y un embarazo preeclámptico, en que la invasión es superficial. En el ambiente nefrológico vale la pena señalar que existe un modelo semejante a la placenta preeclámptica, que es el riñón de Goldblatt. Para recalcar la similitud entre el riñón y la placenta isquémicos he superpuesto sobre la arteria espiral el clamp usado por Goldblatt para generar hipertensión en sus perros. La placenta isquémica genera el cuadro sistémico materno, exportando hacia la circulación materna una serie de factores dañinos para el endotelio. En el centro de la figura se muestro que los vasodilatadores den actuar en el segmento comprendido entre la columna de anclaje (en la base de la vellosidad) y la arteria espiral. La hipótesis que expondré a continuación postula que los vasodilatadores tienen un importante rol en hacer receptivo el territorio materno a la penetración del trofoblasto.
En la Fig. 7 se muestra lo que sucede cuando este trofoblasto se acerca a una arteria de la decidua. Se observa expresión de angiotensina-(1-7) (B), receptor 2 de bradicinina (B2R en C), enzima de conversión 2 (ACE2 en D) que transforma angiotensina-I en angiotensina-(1-7), y la sintasa endotelial de óxido nitrico (eNOS en E). No existe tinción para calicreína (A), pero se sabe que en el trofoblasto invasor, y en el trofoblasto que ha llegado al vaso materno, se expresa el RNA mensajero para calicreína.
En la Fig 8 se observa una arteria espiral decidual invadida. Lo interesante es que el trofoblasto no sólo transformó al vaso e hizo desaparecer su capa muscular, sino que además, el trofoblasto transformado en endotelio sintetiza calicreína (se sabe que ahí también hay receptor de bradicinina), angiotensina (1-7), y ACE2, la enzima que la genera.
La expresión de vasodilatadores por el trofoblasto intravascular demuestra que la placentación adecuada o inadecuada, que va a originar un embarazo normal o una preeclampsia (y también un retardo de crecimiento intrauterino) está determinada no sólo por las arterias maternas, sino también por el citotrofoblasto, cuyo genotipo está determinado por los genes maternos y paternos. En cortes sagitales de vellosidades se encuentra una rica expresión de calicreína, sintasa de óxido nítrico endotelial, angiotensina-(1-7) y ACE2 en el sinciciotrofoblasto. Postulamos que podría haber una diferencia en estos factores entre el embarazo normal de término y la preeclampsia, pero no encontramos diferencia para calicreína ni para angiotensina-(1-7); sólo se observó una diferencia muy tenue para ACE2 (Fig. 9).
En la Fig. 10 se compara la expresión de calicreína, el receptor 2 de bradicinina y eNOS en embarazo normal de término, preeclampsia y placenta acreta. Esta última representa una condición de invasión exagerada, en que el trofoblasto llega hasta el músculo uterino. No se encontraron diferencias entre el embarazo normal y la preeclampsia, pero en la placenta acreta se observó aumento de la expresión de calicreína y de eNOS, lo que apoya la asociación de estos factores vasodilatadores a una mayor capacidad invasiva (7). En la parte inferior de la figura, la tinción con citoqueratina (CK) identifica al trofoblasto invasor.
A medida que ha pasado el tiempo, se han ido incorporando nuevos factores interrelacionados funcionalmente con el sistema calicreína-cinina , que contribuyen al proceso de construir la placenta. Uno de los avances más importantes de los últimos años ha sido la descripción del papel que cumple en placentación el factor angiogénico (VEGF), y el efecto de atrapar el VEGF con la fracción soluble de su receptor 1 (sFlt-1). Existe también el receptor 2 de VEGF, o KDR. Lo interesante es que el receptor de bradicinina es capaz de trasladar este receptor en su localización intracelular. El receptor de bradicinina actúa sobre eNOS y lo interesante es que el NO tiene efecto sobre el receptor angiogénico. A bradicinina se le ha descrito un rol angiogénico, que probablemente se realiza a través de la vía de VEGF. Es muy importante darse cuenta de que, en estado normal, la angiogénesis fisiológica es el sustrato para la construcción de la placenta, que es un territorio predominantemente vascular (Fig. 11).
Cuando se quiere estudiar otros factores, se deben utilizar modelos animales y entre estos la cobaya es una especie muy adecuada, pues su placentación requiere invasión de las arterias espirales, e incluso se extiende hacia las arterias mesometriales (Fig. 12). Esta ventaja es la que nos motivó a continuar nuestros estudios con la cobaya preñada.
Figura 12. Modelo animal de cobaya
En la placenta de cobaya, en primer trimestre, en el día 22 de una gestación que dura 60 días, se puede observar expresión del receptor 2 de bradicinina, eNOS, VEGF, Flt1y KDR en las mismas células; al término se pueden ubicar los factores mencionados en la misma localización dentro de la placenta, lo que supone una interacción funcional entre dichos factores. Si se observa la placenta laberíntina, donde se produce el intercambio entre la sangre materna y fetal, se observa la misma situación, en un tejido que se ha hecho más compacto. En la decidua se observa un tipo de trofoblasto invasor especial, que conforma digitaciones que van a buscar las arterias uterinas. En la Figura 13 se ve lo que ocurre con una arteria mesometrial que es invadida; las células citoqueratina positivas corresponden a trofoblasto y las actina positivas a músculo liso vascular; donde hay trofoblasto no hay presencia de tejido muscular, y en trofoblasto están expresados los receptores de bradicinina, eNOS, VEGF, Flt1 y KDR.
El espacio extracelular de la decidua, clave para la invasión trofoblástica, no es un espacio vacío, sino que contiene colágeno y proteoglicanos, que constituyen las proteínas de la matriz extracelular. Las células invasoras tienen que digerir dicha matriz para poder avanzando, y en este proceso desempeñan un papel muy importante las metaloproteinasas (MMP), en especial la MMP-2 y la MMP-9, que son las que digieren colágeno. Actualmente se sabe que la calicreína puede activar en especial a la MMP-9, que el NO puede activar metaloproteinasas y que el receptor de bradicinina estimula a eNOS (Fig. 14). Todos estos factores configuran un sistema vasodilatador que, potencialmente, puede participar en la angiogénesis y en la degradación de la matriz extracelular.
Figura 14. Papel de las metaloproteinasas sobre las proteinas de la matriz extracelular.
En un experimento realizado in vitro, en que se incubó proenzima MMP-2 y proenzima MMP-9, sin calicreína y con ella, se comprobó que, durante la incubación con calicreína, la fproenzima también tiene actividad gelatinolítica y sobre ella calicreína genera MMP-9. En cambio, sobre proMMP-2 calicreína no tiene acción (Fig. 15).
Lo importante es determinar si metaloproteinasas y calicreína co-localizan en las mismas células y tienen acciones autocrinas, o si los hacen en distintos tipos celulares y poseen funciones paracrinas. Al analizar la subplacenta de la cobaya, de la cual se constituyen los primeros brotes de la placenta, se encuentra MMP-2, MMP-9 y calicreína. Al analizar la placenta interlobar y la laberintina en los días 20, 40 y 60 de gestación, se encuentra que la expresión de estos factores vasodilatadores y antiagregantes va aumentando a medida que avanza la gestación. La expresión de MMP-2 es más intensa en la segunda etapa de la gestación en la subplacenta, y en las “digitaciones” que surgen de ella hay calicreína, MMP-9 y MMP-2 en los mismos tipos celulares. Por lo tanto, tiene sentido plantear que calicreína, como proteasa, participa en forma autocrina en la invasión de la matriz extracelular.
Si se observa el trofoblasto intravascular en una arteria mesometrial, en el día 40 no hay células citoqueratina positivas, por lo tanto no hay trofoblasto, sólo células músculares. Veinte días después se observa que el trofoblasto ha interrumpido la capa muscular, y expresa MMP- 2 y 9 y calicreína. Para determinar la relación entre la concentración de calicreína y de MMP-9, que es la que se activa, se realizaron western blots de homogeneizados de placenta de animales en días 20, 40 y 60 de gestación. Se encontró que en día 40 hay menos proMMP9 y mayor MMP-9 activa, coincidiendo con el peak de calicreína. Esto sólo es una asociación, y en esta etapa de nuestra investigación no podemos afirmar que ambas enzimas se expresan en forma sincrónica.
En este presentación se ha mostrado sólo el enfoque vascular que se inició con el estudio de los niveles de prostaciclina y tromboxano, que demostró el desequilibrio que favorece a tromboxano en el embarazo preeclamptico. Sin embargo, actualmente se sabe que existen otros sistemas vasodilatadores: la vía de L-arginina-oxido nítrico, el sistema calicreína-cinina, angiotensina-(1-7), el factor de crecimento vascular (VEGF) y sus receptores. Frente a estos se contraponen tromboxano, dimetil-arginina simétrica (ADMA), especies reactivas de oxígeno y el receptor soluble del receptor 1 de VEGF (sFlt1). El concepto es que todo este proceso se puede alterar debido al déficit de diferentes factores; por eso es que se obtiene un efecto escaso cuando se interviene con en este balance con aspirina, que sólo disminuye la síntesis de tromboxano.
Pero la situación en el embarazo es aún más compleja; no sólo está determinada por el balance vasoconstrictor-vasodilatador, sino que además ambos sistemas actúan sobre vasculaturas maternas que varían a lo largo de la vida de la mujer, la inmadura de la adolescente embarazada, la madura e intacta del periodo fértil entre los 20 y 35 años, y la vasculatura dañada de mujer mayor, de la hipertensa previa o de la diabética. Sabemos que la embarazada precoz, añosa, hipertensa y diabética tienen mayor riesgo de desarrollar preeclampsia
Se hace necesario considerar que además del punto de vista vascular, el flujo placentario también puede estar deteriorado por otros factores: una mayor respuesta inmunológica puede disminuir la invasión del trofoblasto y conducir a una placenta isquémica, y las trombofilias causan coagulación a nivel del lecho placentario. También se ha demostrado invasión defectuosa por falla de moléculas de adhesión (Fig. 16).
El alza de vasodilatadores en la gestación normal, tanto en plasma como en orina, y su déficit en preeclampsia, explica la mantención fisiológica de normotensión mientra que su déficit podría contribuir a la hipertensión asociada con el embarazo.
La distribución temporo-espacial de los sistemas vasodiladores interrelacionados, que además son pleiotrópicos en su función, apoya su rol en la placentación y en la mantención de su perfusión. Sin embargo, demostrar que su deficiencia representa una causa de preeclampsia requiere nuevas estrategias.
Es muy probable que el fenotipo que tiene menor capacidad de generar vasodilatadores y por lo tanto, mayor riesgo de generar preeclampsia, sea el mismo fenotipo que genera la enfermedad cardiovascular en el adulto. En un estudio escandinavo que realizó un seguimiento durante 25 años en más de 600.000 mujeres, las que presentaron preeclampsia y parto prematuro tuvieron significativamente menor sobrevida que las mujeres con preeclampsia sin parto prematuro, cuya sobrevida fue similar a la de la población normal (8). Un enfoque vasoactivo de la placentación y de la adaptación sistémica materna lleva a plantear que el binomio madre-hijo que desarrolla una placenta adecuada, que nace de término, con peso adecuado, tiene un fenotipo cardiovascular adecuado. En cambio, las mujeres que han dado a luz a un prematuro son deficitarias en factores vasodilatadores y antiagregantes, por lo que conforman, junto a sus hijos, un grupo de mayor riesgo, que necesita un seguimiento más cercano (Fig. 17).
Figura 17. Sobrevida a largo plazo en 626 272 primĒparas seguidas durante 25 a±os

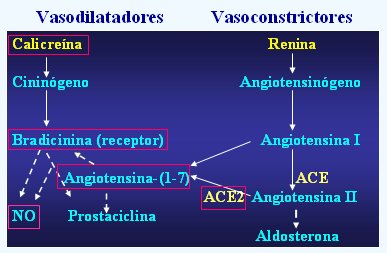 Figura 1. Principales sistemas vasoactivos
Figura 1. Principales sistemas vasoactivos

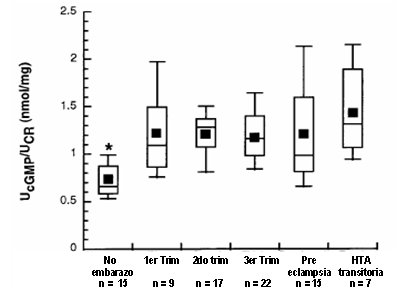 Figura 2. Excreci¾n urinaria de GMPc, segundo mensajero de NO, en el embarazo (2)
Figura 2. Excreci¾n urinaria de GMPc, segundo mensajero de NO, en el embarazo (2)

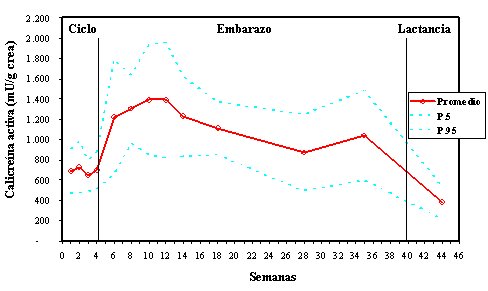 Figura 3. CalicreĒna urinaria a lo largo del ciclo, gestaci¾n normal y lactancia
Figura 3. CalicreĒna urinaria a lo largo del ciclo, gestaci¾n normal y lactancia

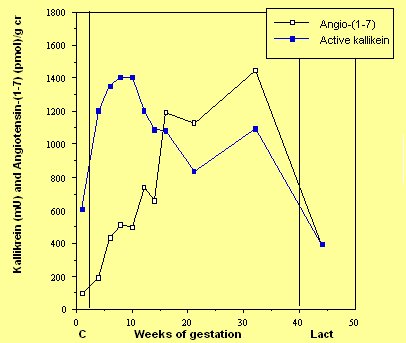 Figura 4. Excreci¾n urinaria de calicreĒna y angiotensina-(1-7) en ciclo, gestaci¾n normal y lactancia
Figura 4. Excreci¾n urinaria de calicreĒna y angiotensina-(1-7) en ciclo, gestaci¾n normal y lactancia

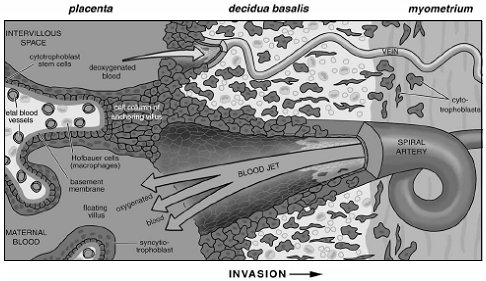 Figura 5. Placentaci¾n, dirigida a perfundir a alto flujo el espacio intervelloso mediante arterias espirales transformadas (6)
Figura 5. Placentaci¾n, dirigida a perfundir a alto flujo el espacio intervelloso mediante arterias espirales transformadas (6)

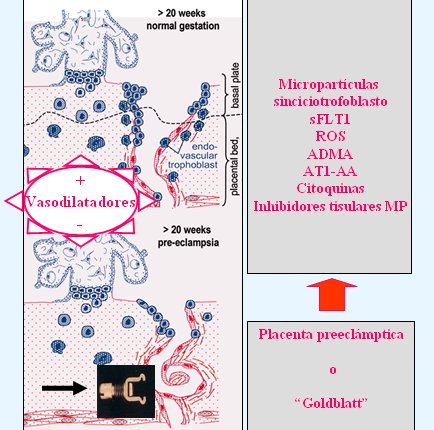 Figura 6. Invasi¾n trofoblßstica en embarazo normal y preeclampsia. Modelo de ōplacenta de Goldblattö. sFLT1=fracci¾n soluble del receptor Flt1 de VEGF, ROS=especies reactivas al oxĒgeno, ADMA=dimetilarginina asimķtrica, AT1-AA=anticuerpos cont
Figura 6. Invasi¾n trofoblßstica en embarazo normal y preeclampsia. Modelo de ōplacenta de Goldblattö. sFLT1=fracci¾n soluble del receptor Flt1 de VEGF, ROS=especies reactivas al oxĒgeno, ADMA=dimetilarginina asimķtrica, AT1-AA=anticuerpos cont

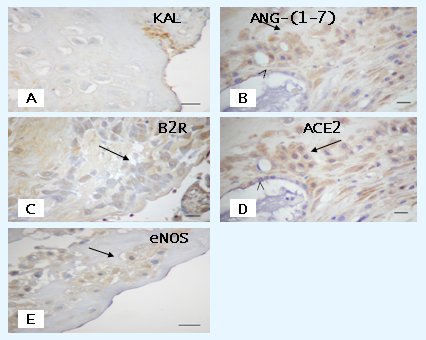 Figura 7. Invasi¾n trofoblßstica de la arteria decidual. A: calicreina (KAL). B: Angiotensina-(1-7) (Ang-(1-7). C: receptor 2 de bradicinina (B2R). D: ACE2. E: eNOS (5)
Figura 7. Invasi¾n trofoblßstica de la arteria decidual. A: calicreina (KAL). B: Angiotensina-(1-7) (Ang-(1-7). C: receptor 2 de bradicinina (B2R). D: ACE2. E: eNOS (5)

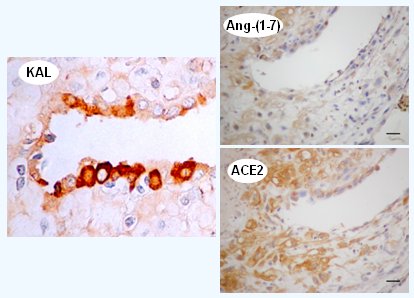 Figura 8. Expresi¾n de vasodilatadores en trofoblasto peri e intravascular. KAL=calicreina, Ang-(1-7)=Angiotensina-(1-7), ACE2=enzima de conversi¾n 2.
Figura 8. Expresi¾n de vasodilatadores en trofoblasto peri e intravascular. KAL=calicreina, Ang-(1-7)=Angiotensina-(1-7), ACE2=enzima de conversi¾n 2.

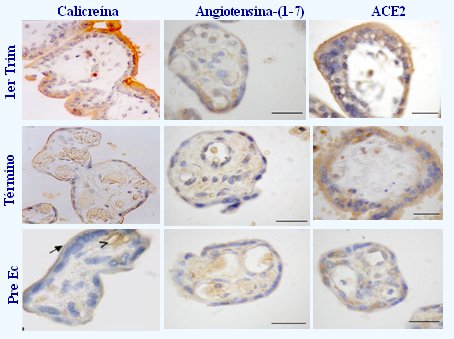 Figura 9. CalicreĒna, angiotensina-(1-7) y ACE2 en vellosidades placentarias de embarazo de primer trimestre, tķrmino y preeclampsia
Figura 9. CalicreĒna, angiotensina-(1-7) y ACE2 en vellosidades placentarias de embarazo de primer trimestre, tķrmino y preeclampsia

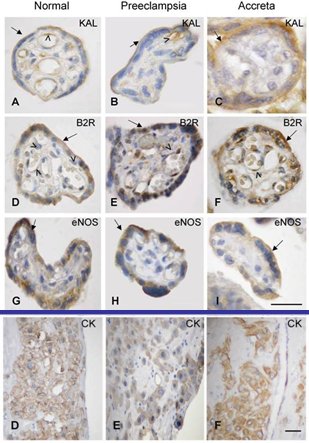 Figura 10. Expresi¾n de calicreĒna, receptor y eNOS en vellosidades placentarias de embarazo normal, preeclampsia y placenta acreta. En la parte inferior de la figura, la tinci¾n con citoqueratina (CK) identifica al trofoblasto invasor.
Figura 10. Expresi¾n de calicreĒna, receptor y eNOS en vellosidades placentarias de embarazo normal, preeclampsia y placenta acreta. En la parte inferior de la figura, la tinci¾n con citoqueratina (CK) identifica al trofoblasto invasor.

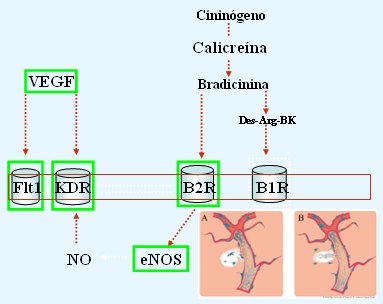 Figura 11. Rol del factor angiogķnico (VEGF) y de factores relacionados en el desarrollo de la vasculatura placentaria placentaria (en recuadrosverdes los factores estudiados por nuestro grupo).
Figura 11. Rol del factor angiogķnico (VEGF) y de factores relacionados en el desarrollo de la vasculatura placentaria placentaria (en recuadrosverdes los factores estudiados por nuestro grupo).

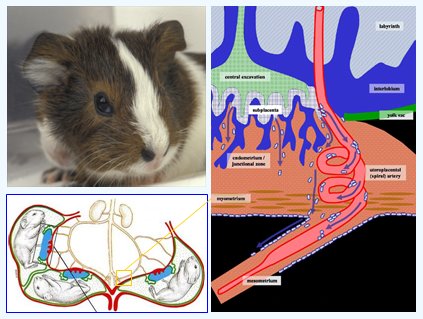 Figura 12. Modelo animal de cobaya
Figura 12. Modelo animal de cobaya

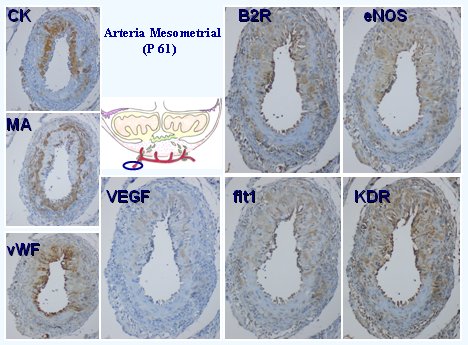 Figura 13. Arteria mesometrial invadida, y expresi¾n de citoqueratina, actina, B2R, enOS, VEGF y sus dos receptores (flt1 y KDR)
Figura 13. Arteria mesometrial invadida, y expresi¾n de citoqueratina, actina, B2R, enOS, VEGF y sus dos receptores (flt1 y KDR)

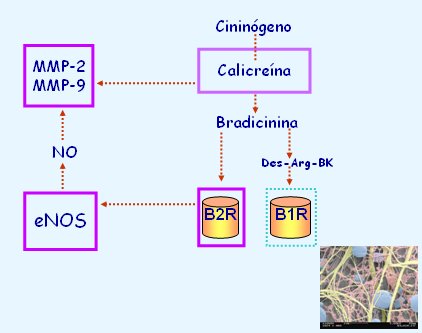 Figura 14. Papel de las metaloproteinasas sobre las proteinas de la matriz extracelular.
Figura 14. Papel de las metaloproteinasas sobre las proteinas de la matriz extracelular.

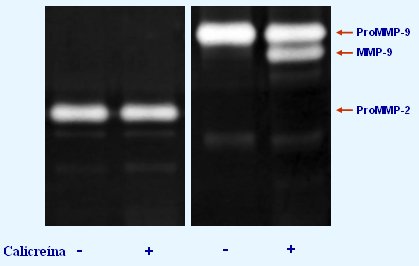 Figura 15. ZimografĒa que muestra la actividad gelatinolĒtica de calicreĒna sobre proMMP-2 y proMMP-9
Figura 15. ZimografĒa que muestra la actividad gelatinolĒtica de calicreĒna sobre proMMP-2 y proMMP-9

 Figura 16. Balance de factores funcionales y estructurales que favorecen o deterioran el flujo placentario
Figura 16. Balance de factores funcionales y estructurales que favorecen o deterioran el flujo placentario

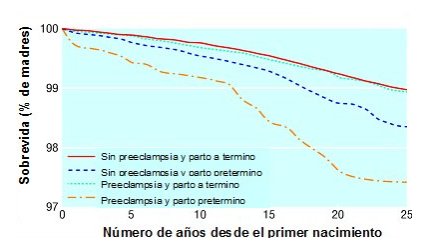 Figura 17. Sobrevida a largo plazo en 626 272 primĒparas seguidas durante 25 a±os
Figura 17. Sobrevida a largo plazo en 626 272 primĒparas seguidas durante 25 a±os
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada en el marco del Congreso Conjunto de NefrologĒa, Hipertensi¾n y Trasplante 2007, realizado en Puc¾n entre los dĒas 26 al 29 de septiembre de 2007. El evento fue organizado por la Sociedad Chilena de NefrologĒa, Hipertensi¾n y Trasplante.
Presidente Sociedad Chilena de NefrologĒa: Dr. Alejandro Cotera.
Secretaria Ejecutiva: Dra. MarĒa Eugenia Sanhueza.
Directora Curso Precongreso: Dra. Gloria Valdķs.
 Expositora:
Gloria Valdķs[1]
Expositora:
Gloria Valdķs[1]

Citaci¾n: Valdķs G. Role of vasodilators in the creation of the uteroplacental unit. Medwave 2008 Abr;8(3):e1386 doi: 10.5867/medwave.2008.03.1386
Fecha de publicaci¾n: 1/4/2008

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n
 Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artĒculo, junto con otras mķtricas de redes sociales.
 Gant NF, Daley GL, Chand S, Whalley PJ, MacDonald PC. A study of angiotensin II pressor response throughout primigravid pregnancy. J Clin Invest. 1973 Nov;52(11):2682-9. | CrossRef | PubMed |
Gant NF, Daley GL, Chand S, Whalley PJ, MacDonald PC. A study of angiotensin II pressor response throughout primigravid pregnancy. J Clin Invest. 1973 Nov;52(11):2682-9. | CrossRef | PubMed | Conrad KP, Kerchner LJ, Mosher MD. Plasma and 24-h NOx and cGMP during normal pregnancy and preeclampsia in women on a reduced NOx diet. Am J Physiol. 1999 Jul;277(1 Pt 2):F48-57. | PubMed |
Conrad KP, Kerchner LJ, Mosher MD. Plasma and 24-h NOx and cGMP during normal pregnancy and preeclampsia in women on a reduced NOx diet. Am J Physiol. 1999 Jul;277(1 Pt 2):F48-57. | PubMed | Mills JL, DerSimonian R, Raymond E, Morrow JD, Roberts LJ 2nd, Clemens JD, et al. Prostacyclin and thromboxane changes predating clinical onset of preeclampsia: A multicenter prospective study. JAMA. 1999 Jul 28;282(4):356-62. | CrossRef | PubMed |
Mills JL, DerSimonian R, Raymond E, Morrow JD, Roberts LJ 2nd, Clemens JD, et al. Prostacyclin and thromboxane changes predating clinical onset of preeclampsia: A multicenter prospective study. JAMA. 1999 Jul 28;282(4):356-62. | CrossRef | PubMed | Valdķs G, Corthorn J, Oyarz·n E, Berrios C, Foradori A, GermaĒn AM, Villarroel L. Urinary kallikrein excretion in the human menstrual cycle, normal pregnancy and lactation. Prenat Neonat Med 3: 474-81, 1998.
Valdķs G, Corthorn J, Oyarz·n E, Berrios C, Foradori A, GermaĒn AM, Villarroel L. Urinary kallikrein excretion in the human menstrual cycle, normal pregnancy and lactation. Prenat Neonat Med 3: 474-81, 1998.  Valdķs G, Germain AM, Corthorn J, Berrios C, Foradori AC, Ferrario CM, et al. Urinary vasodilator and vasoconstrictor angiotensins during menstrual cycle, pregnancy, and lactation. Endocrine. 2001 Nov;16(2):117-22. | CrossRef | PubMed |
Valdķs G, Germain AM, Corthorn J, Berrios C, Foradori AC, Ferrario CM, et al. Urinary vasodilator and vasoconstrictor angiotensins during menstrual cycle, pregnancy, and lactation. Endocrine. 2001 Nov;16(2):117-22. | CrossRef | PubMed | Zhou Y, Bellingard V, Feng KT, MacMaster M, Fisher SJ. Human cytotrophoblasts promote endothelial survival and vascular remodeling through secretion of Ang2, PlGF, and VEGF-C. Dev Biol. 2003 Nov 1;263(1):114-25. | CrossRef | PubMed |
Zhou Y, Bellingard V, Feng KT, MacMaster M, Fisher SJ. Human cytotrophoblasts promote endothelial survival and vascular remodeling through secretion of Ang2, PlGF, and VEGF-C. Dev Biol. 2003 Nov 1;263(1):114-25. | CrossRef | PubMed |