Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada en el marco del XVII Congreso Chileno de Nutrici¾n, realizado en Iquique entre los dĒas 29 de noviembre al 2 de diciembre de 2006. El evento fue organizado por la Sociedad Chilena de Nutrici¾n, BromatologĒa y ToxicologĒa.
Presidente: Dr. Francisco Mardones Santander.
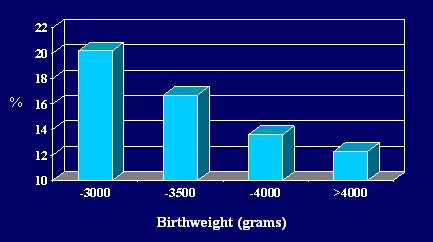
Figura 1. Incidencia acumulativa (%) de hipertensi¾n de acuerdo al peso al nacer
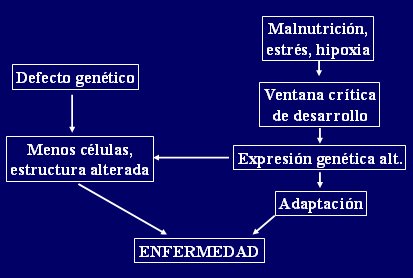
Figura 2. Relaci¾n entre genķtica, eventos adversos en perĒodos crĒticos y enfermedad
Los perĒodos crĒticos del desarrollo son parte de la vida: cada sistema u ¾rgano tiene un perĒodo, a veces breve, en el que ocurre su maduraci¾n. Los ri±ones maduran a las 34 semanas de gestaci¾n: el n·mero de unidades funcionales, los nefrones, que es de 1 a 3 millones, se determina seg·n el tama±o del cuerpo en ese momento y una a dos semanas despuķs ya no existen mßs posibilidades de fabricar nuevos nefrones. Por lo tanto, cada adulto adquiri¾ sus nefrones a las 34 semanas de gestaci¾n: ķse es el periodo crĒtico para el ri±¾n. Para el m·sculo, este perĒodo crĒtico es mßs precoz; el hĒgado tiene algunos perĒodos crĒticos despuķs del nacimiento y el coraz¾n tiene varios perĒodos crĒticos antes del nacimiento.
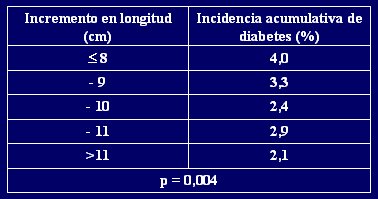
Es importante se±alar que no todos los adultos diabķticos tienen el antecedente de bajo peso al nacer, porque hay mßs de una vĒa para el desarrollo de la diabetes. Una de ellas la determina el bajo peso al nacer, pero hay una segunda vĒa que comienza con un reciķn nacido saludable, que no crece entre el nacimiento y los tres meses de vida. En la Tabla I se muestra c¾mo el aumento de la estatura entre el nacimiento y los tres meses se relaciona con la aparici¾n posterior de diabetes: a menor crecimiento, mayor incidencia de la enfermedad.
Tabla I. Incidencia acumulativa de diabetes tipo 2 en personas con peso al nacer mayor de 3,5 kg, seg·n el aumento de la longitud entre el nacimiento y los 3 meses de edad
El registro de la talla desde el nacimiento hasta los tres meses permite predecir la aparici¾n de diabetes 50 a±os mßs tarde. En ese perĒodo, tres ¾rganos pasan por perĒodos crĒticos del desarrollo: el m·sculo, en el cual se almacena la glucosa, el pßncreas endocrino, que fabrica la insulina, y el hĒgado. Los procesos que subyacen a este fen¾meno todavĒa son desconocidos, pero lo cierto es que hay ciertos carriles de crecimiento que conducen a enfermedades cr¾nicas y que algunos comienzan con un crecimiento pobre antes de nacer y otros comienzan con un crecimiento pobre en el periodo que va desde el nacimiento hasta cerca de un a±o de edad.
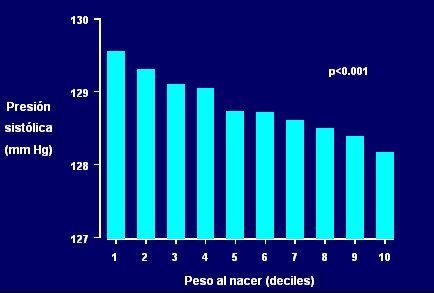
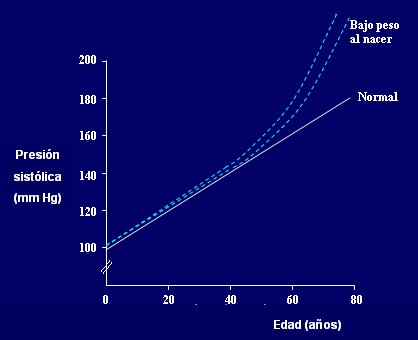
Figura 3. Relaci¾n entre la presi¾n sist¾lica y el peso al nacer en 149.378 hombres suecos de 18 a±os de edad
Las peque±as diferencias que se observan en las personas j¾venes contrastan con las grandes diferencias que se observan en edades mayores. Esto se explica de la siguiente manera: el individuo nace con alguna alteraci¾n que lo predispone a la hipertensi¾n, pero es capaz de compensar durante la mayor parte de su vida, hasta que llega un momento en que pierde esta capacidad de compensaci¾n, comienza a elevar sus cifras de presi¾n y, eventualmente, desarrolla la hipertensi¾n arterial. Si el individuo nace con menos nefrones, cada nefr¾n trabaja mßs y se desgasta mßs, de modo que sus nefrones morirßn en forma prematura; cuando los nefrones comienzan a morir, la presi¾n sanguĒnea comienza a subir; cuanto mßs sube la presi¾n, mßs nefrones mueren, lo que origina un cĒrculo vicioso que conduce, eventualmente, a la hipertensi¾n. Este proceso explica en forma simple el origen fetal de esta condici¾n (Fig. 4).
Figura 4. Desarrollo de la hipertensi¾n
En un estudio realizado en un peque±o grupo de ancianos, algunos con presi¾n normal y otros hipertensos, se observ¾ que en los normotensos el peso al nacer no tenĒan ninguna relaci¾n con la presi¾n sanguĒnea; en cambio, en los hipertensos, aunque hubieran sido tratados, los que tuvieron bajo peso al nacer tenĒan presiones mßs altas que aquellos con mayor peso al nacer. La industria farmacķutica deberĒa considerar estos datos, ya que demuestran que los hipertensos con antecedente de bajo peso al nacer son mucho mßs difĒciles de controlar con drogas. Esto se podrĒa explicar planteando que a los 70 a±os, todos los individuos que tienen menos nefrones desarrollarßn hipertensi¾n, si su carga genķtica les se±ala ese destino; en tanto que en los sujetos normotensos el peso de nacimiento es irrelevante, puesto que la presi¾n estß determinada por otros mecanismos no relacionados con este parßmetro.
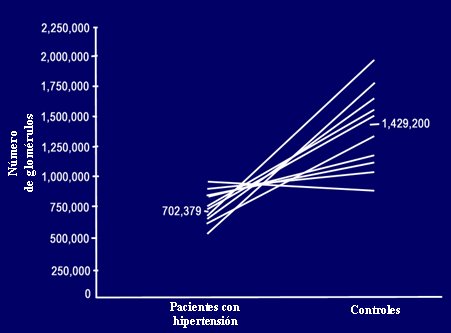
En un estudio alemßn, que se public¾ en NEJM, se compar¾ el n·mero de glomķrulos o nefrones en un grupo de 10 individuos hipertensos y un grupo de 10 individuos normales, todos fallecidos en accidentes de trßnsito. Tanto los hombres como las mujeres que habĒan sido hipertensos tenĒan menor cantidad de glomķrulos que aquellos sin hipertensi¾n (Fig. 5). Tambiķn se encontr¾ una diferencia significativa en el volumen glomerular, que era mayor en los sujetos con hipertensi¾n.
Figura 5. N·mero de glomķrulos en 10 pacientes con hipertensi¾n y 10 controles pareados
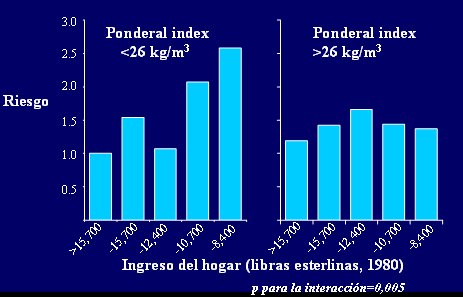
Figura 6. Tasa de riesgo para enfermedad coronaria (ingreso hospitalario o muerte) en 3.676 hombres
Renķ Dubos, en su libro Mirage of health (1987), se±al¾ que no se puede entender el efecto del ambiente sobre las personas si no se conoce la historia de vida de cada individuo. En este caso, esto significa que no se puede determinar el tipo de nutrici¾n que requieren los individuos, si no se conoce la historia nutricional de cada uno de ellos. No se puede decir: ōla grasa saturada es malaö; la oraci¾n correcta es: ōlas dietas ricas en grasas saturadas son malas para algunas personas, dependiendo de la experiencia nutricional que han tenido durante sus vidas, desde poco despuķs de la concepci¾nö. Durante muchos a±os se pens¾ que los genetistas podrĒan determinar quiķnes pueden consumir grasas saturadas y quiķnes no pueden hacerlo, pero este modelo era demasiado simple. Ahora existe un nuevo modelo, que incorpora los efectos de la nutrici¾n sobre la expresi¾n genķtica durante los primeros estadios del desarrollo.
Figura 7. Crecimiento de 357 ni±os que desarrollaron enfermedad coronaria en la edad adulta, en una cohorte de 4.630 ni±os nacidos en Helsinki
El crecimiento compensatorio acelerado postnatal tiene costos fisiol¾gicos y metab¾licos a largo plazo. Este fen¾meno ya se habĒa observado en animales, de modo que los granjeros sabĒan que si forzaban a los animales a crecer demasiado rßpido ķstos morirĒan, porque sus sistemas inmune, ¾seo, etc., no se desarrollarĒan lo suficiente.
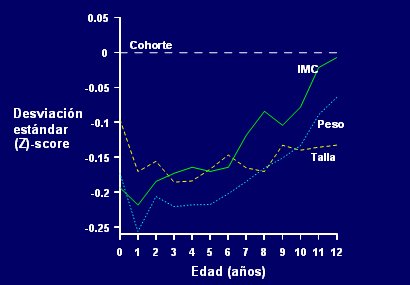
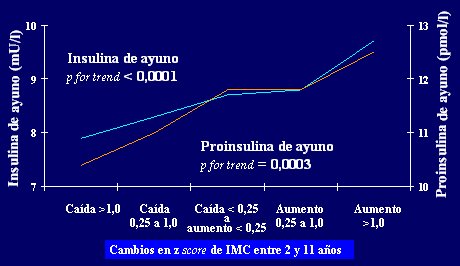
En la Fig. 8 se muestra a un grupo de hombres y mujeres de 62 a±os de edad, divididos en grupos seg·n la evoluci¾n de su Ēndice de masa corporal (IMC) entre los 2 y los 11 a±os de edad: los que disminuyeron su IMC en mßs de una desviaci¾n estßndar, los que aumentaron su IMC en mßs de una desviaci¾n estßndar y varios grupos intermedios. Cincuenta a±os despuķs, el rßpido incremento en el IMC se asocia a un aumento en la insulinemia y la proinsulina en ayuno, que son marcadores de resistencia a la insulina. Por lo tanto, la presencia de estos marcadores en el adulto no depende del grado de sobrepeso que tenga el individuo en ese momento, sino de la evoluci¾n de su IMC durante la ni±ez.
Figura 8. Medici¾n de resistencia a la insulina (ajustada por masa corporal actual) en 2003 hombres y mujeres de 62 a±os de edad
Con respecto al manejo del colesterol, siempre se pens¾ que los niveles elevados de este lĒpido se debĒan a dietas inapropiadas; de hecho, los mķdicos trataron durante mucho tiempo de reducir el colesterol de las personas mediante la dieta, lo que result¾ un fracaso y una pķrdida de tiempo: se puede cambiar el colesterol mediante estatinas, pero no mediante la dieta. El individuo debe aprender a manejar el colesterol y las grasas saturadas en un momento crĒtico de su vida; si no lo hace, tendrß alto riesgo de verse afectado por los problemas derivados del colesterol elevado.
En cuanto al ·ltimo punto, el coraz¾n estß estructuralmente completo en el momento del nacimiento; fue modelado, dentro del ·tero, por las mismas fuerzas contra las cuales tuvo que bombear: los vasos placentarios, que pueden haber conformado un sistema de alta o baja presi¾n, dependiendo, entre otros factores, de la nutrici¾n materna. La mayor parte de las muertes se debe a alg·n tipo de falla cardiaca, que sobreviene cuando los vasos coronarios no son capaces de suplir al m·sculo cardĒaco; en ese sentido no hay mucho que hacer, porque la circulaci¾n coronaria se forma antes de nacer y despuķs, prßcticamente no se modifica. En cambio, el rßpido aumento de peso durante la ni±ez puede empeorar la situaci¾n del coraz¾n, porque incrementa el estrķs contra el cual el ¾rgano debe trabajar. El coraz¾n estß configurado para un cuerpo en particular y si ķste crece mßs rßpido que lo esperado, la mayor demanda afectarß la estructura del coraz¾n; de hecho, se sabe que un ni±o peque±o al a±o de vida tendrß paredes cardĒacas mßs gruesas, cincuenta a±os despuķs, que un ni±o de peso normal al a±o de vida y que el tener un ventrĒculo izquierdo grueso es un factor de riesgo mayor para enfermedad coronaria. Existen s¾lo dos razones por las cuales los vasos sanguĒneos no pueden suministrar suficiente sangre al m·sculo cardĒaco: porque la pared es muy gruesa o porque el flujo sanguĒneo es muy peque±o, y ambas condiciones se establecen antes del a±o de vida.
Figura 9. FotografĒa de una familia durante la hambruna holandesa (1944)
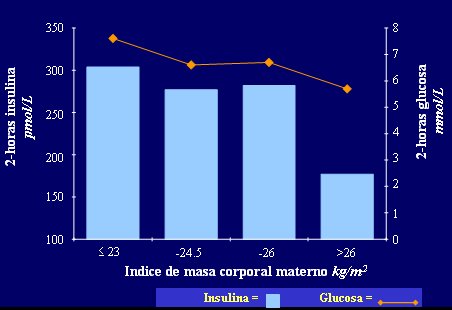
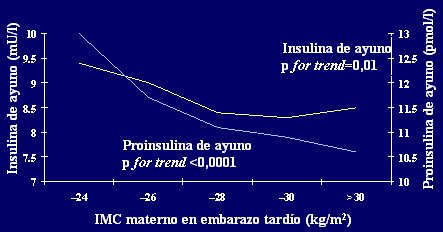
En China, en 1950, cuando Mao Tse Tung estaba a punto de entrar en la ciudad, las mujeres estaban dando a luz de manera habitual; en esa ķpoca los registros de los nacimientos eran muy detallados, de modo que se ha podido rastrear a los ni±os que nacieron en el Pekin Memorial Hospital hasta el dĒa de hoy y se encontr¾ que los hijos de las madres mßs delgadas tienen menor capacidad para regular la glucemia y mayores niveles de insulina (Fig. 10). Esta observaci¾n se ha repetido en otras poblaciones del mundo, entre ellas, la de Finlandia (Fig. 11).
Figura 10. Concentraciones medias de insulina, seg·n el Ēndice de masa corporal materno, a las 38 semanas de gestaci¾n (China, 1950)
Figura 11. Medici¾n de resistencia a la insulina (ajustada por masa corporal actual) en 2003 hombres y mujeres de 62 a±os de edad
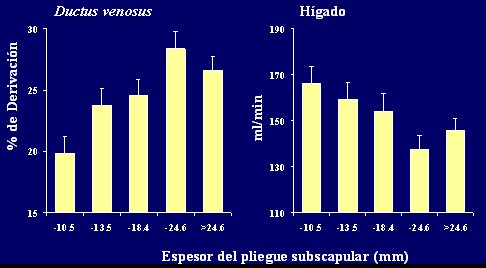
Figura 12. Efecto del espesor del pliegue cutßneo materno previo al embarazo sobre el flujo sanguĒneo a travķs del ductus venoso y el hĒgado
En este momento no se sabe de quķ manera este desvĒo reconoce el porcentaje de grasa materna. Se supone que si la sangre que viene desde la madre es pobre en proteĒnas y aminoßcidos, es mßs inteligente derivarla hacia el hĒgado fetal para que ķste pueda procesar estos aminoßcidos y producir las proteĒnas que el ni±o necesita; pero esta suposici¾n debe ser investigada y comprobada.
Hoy se sabe que el embri¾n humano es muy sensible a la nutrici¾n, que es capaz de reconocer el tipo de nutrientes que se le aportan y que, con esta base, configura su organismo para determinado tipo de nutrici¾n que recibirß en el resto de su vida. El embri¾n localiza precozmente a las cķlulas madre y decide quķ porcentaje de los nutrientes que recibe destinarß a la formaci¾n de la placenta y quķ porcentaje utilizarß para formarse a sĒ mismo. Esta decisi¾n se toma en el tercer dĒa de la vida intrauterina y puede ser la decisi¾n mßs importante de su vida: si se destinan muchas cķlulas a la placenta, ķsta competirß con el embri¾n por el alimento; si se destinan muy pocas, la placenta no se desarrollarß y el embri¾n morirß. C¾mo toma esta decisi¾n el embri¾n humano, quķ parßmetros de la madre considera y c¾mo los mide, no se sabe en absoluto: es uno mßs de la lista de temas sobre los cuales se debe investigar.
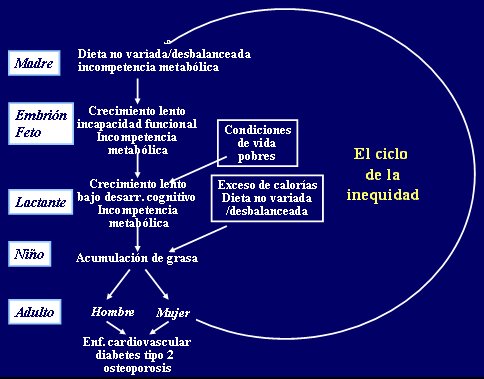
Figura 13. El cĒrculo de la inequidad
En este momento se estßn dando las condiciones para romper este cĒrculo, lo que serß posible en la medida en que se abandonen los prejuicios y se re·nan investigadores de distintas disciplinas. La pr¾xima reuni¾n internacional de la DOHAD (Developemental Origins of Health and Disease) se realizarß en Australia, en noviembre de 2007 y la subsiguiente se llevarß a cabo en Chile, durante el a±o 2009.
Medwave. A±o VII, No. 11, Diciembre 2007. Derechos Reservados.















 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de la conferencia dictada en el marco del XVII Congreso Chileno de Nutrici¾n, realizado en Iquique entre los dĒas 29 de noviembre al 2 de diciembre de 2006. El evento fue organizado por la Sociedad Chilena de Nutrici¾n, BromatologĒa y ToxicologĒa.
Presidente: Dr. Francisco Mardones Santander.
 Expositor:
David Barker[1]
Expositor:
David Barker[1]

Citaci¾n: Barker D. Mechanisms involved in fetal programming. Medwave 2007 Dic;7(11):e1097 doi: 10.5867/medwave.2007.11.1097
Fecha de publicaci¾n: 1/12/2007

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n