Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el marco del Congreso Conjunto de NefrologĒa, Hipertensi¾n y Trasplante 2006, Simposio Baxter, realizado en Valdivia entre los dĒas 4 al 7 de octubre de 2006. El evento fue organizado por la Sociedad Chilena de NefrologĒa, Hipertensi¾n y Trasplante. Secretaria Ejecutiva: Dra. Patricia Herrera. Secretario Ejecutivo Local: Dr. Claudio Flores.
El concepto de la dißlisis peritoneal (DP) aguda en pacientes con enfermedad renal cr¾nica es similar al de la dißlisis peritoneal en hemodißlisis cr¾nica, con la diferencia de que, en este caso, los pacientes que van a comenzar con dißlisis tienen una uremia muy elevada.
La primera raz¾n para iniciar la DP es que esta medida preserva mejor la funci¾n renal residual, como se demostr¾ en un estudio realizado por Lysaght, en el que esta funci¾n declin¾ con mßs rapidez en los pacientes en hemodißlisis que en los pacientes en dißlisis peritoneal (1). Lo mismo se observ¾ en una revisi¾n de varios estudios, tanto prospectivos como retrospectivos, que se public¾ en 2002 y que se resume en la Tabla I (2).
Tabla I. La dißlisis peritoneal mejora la preservaci¾n de la funci¾n renal residual (2).
Entre los beneficios de preservar la funci¾n renal (Fig. 1), es importante destacar que 1 ml/min de clearance de creatinina corresponde a 10 litros de clearance semanal. En 1980 daba lo mismo si los pacientes tenĒan un clearence de creatinina de 3 o de 5 ml/min, pero hoy se sabe que 1 ml de clearance es muy valioso para los pacientes, a tal punto que 1 ml/mm de mejorĒa en la filtraci¾n glomerular puede disminuir en 10% el riesgo relativo de muerte. La preservaci¾n de la funci¾n renal residual permite, ademßs, proporcionar funci¾n endocrina; mejorar la calidad de vida; aumentar el sodio total removido; mejorar el estado nutricional; tener una dieta e ingesta de agua mßs libres; controlar mejor el volumen y mejorar el clearence de beta2-microglubulina y de molķculas de tama±o medio (3).
Figura 1. Beneficios de preservar la funci¾n renal residual.
La segunda raz¾n para empezar con DP es que permite preservar el acceso vascular en situaciones de bacteremia, estenosis del catķter u otras complicaciones de ķste. La tercera raz¾n es que la cantidad de personal necesario para manejar a un determinado n·mero de pacientes es muy inferior con la DP: por ejemplo, el Aarhus University Hospital Skejby Hospital, de Dinamarca, durante 2004 hubo 110 pacientes en DP, los que fueron atendidos por 4 enfermeras; en cambio, se necesitaron 40 enfermeras por cada 100 pacientes en hemodißlisis. La ·ltima raz¾n para iniciar la DP es que mejora la calidad de vida, pues otorga a los pacientes mayor libertad que la hemodißlisis; estos ·ltimos pacientes necesitan tener una unidad de hemodißlisis cerca permanentemente, lo que los limita, por ejemplo, para viajar. En un estudio de Rubin, efectuado en 656 pacientes en DP o hemodißlisis que contestaron un cuestionario, se observaron los resultados siguientes: 70% de los pacientes en DP se mostraron satisfechos con la cantidad de informaci¾n recibida sobre el tratamiento; de los pacientes en hemodißlisis, s¾lo 25% estaban satisfechos (Fig.2). Asimismo, en tķrminos de impresi¾n general de bienestar, 85% de los pacientes en DP declararon que se sentĒan bien; la proporci¾n baj¾ a menos de 60% entre los pacientes en hemodißlisis (Fig. 3). (4)
Otro argumento para preferir la DP como primera elecci¾n es que mejora una serie de parßmetros en los pacientes con enfermedad cardiovascular, a saber: mejora el control del volumen; reduce la presi¾n; otorga mayor estabilidad hemodinßmica; normaliza el potasio; disminuye las arritmias; reduce el riesgo de contaminaci¾n; disminuye la incidencia de anemia, lo que se traduce en menor necesidad de eritropoyetina y de transfusiones sanguĒneas y evita el uso de anticoagulantes. Ademßs, el riesgo de contraer la hepatitis C es mucho menor con PD que con hemodißlisis, como lo demuestra el grßfico de la figura 4, que resume los resultados del estudio de Pereira sobre este aspecto (5).
En el Hospital Skejvy, de Dinamarca, en pacientes cr¾nicos que requieren tratamiento agudo, los cirujanos instalan el catķter, aunque no es tarea exclusiva de ellos; se utiliza anestesia local y un catķter Tenckhoff con doble cuff, sin antibi¾ticos profilßcticos, por norma del paĒs. El hospital cuenta con una indicaci¾n estßndar que se entrega a las enfermeras y que establece que para todos los pacientes el tiempo nocturno es de 12 horas y el tidal (marea) es de 50% a 75%; en cambio, hay diferencia en el volumen total seg·n el peso del paciente: 10 litros en los que pesan menos de 60 kg y 14 litros en los que pesan mßs de 60 kg; y en el volumen mßximo de infusi¾n, que es de 1,2 litros y 1,5 litros respectivamente. Para aplicar esta prescripci¾n no se necesita un nefr¾logo, s¾lo se necesita un cirujano y una enfermera.
Un aspecto interesante es que en este hospital se utiliza la dißlisis peritoneal ōen mareaö, o dißlisis tidal 50-75%, en la cual se infunde 1,2 litros, se drena 50 a 75% del volumen de infusi¾n y el resto se deja en la cavidad, es decir, se mantiene una cantidad de lĒquido constante en la cavidad abdominal, aunque se va a±adiendo y retirando peri¾dicamente la misma cantidad de lĒquido de dißlisis nuevo. Esto se hace porque algunos pacientes sienten mucho dolor con el vaciado total de la cavidad peritoneal y otras complicaciones mecßnicas, lo que se evita con la modalidad de marea. Son contraindicaciones para empezar la DP los cuadros siguientes: hipertensi¾n grave (PAD mayor de 120 mmHg), sobrehidrataci¾n (edema agudo de pulm¾n), hipercalemia con K mayor de 6,5 nmol/L, pericarditis urķmica, colitis urķmica y sangrado gastrointestinal. En la experiencia del expositor, la peritoneodißlisis ha tenido buenos resultados en pacientes con hipertensi¾n arterial grave y en pacientes con hipercalemia.
Polvsen public¾ los resultados del estudio retrospectivo efectuado en 52 pacientes, a los que se llam¾ casos, que entraron a este hospital en un lapso de dos a±os, entre enero de 2000 y junio de 2002 (5), por un cuadro que requiri¾ manejo agudo; los siguientes pacientes consecutivos que acudieron en forma planificada se consideraron como controles. En los casos, la PD aguda comenz¾ de inmediato, una vez instalado el catķter; en los controles planificados, la PD comenz¾ despuķs de doce dĒas de la inserci¾n. El prop¾sito del estudio fue comparar el resultado y las complicaciones de la dißlisis a corto plazo (3 meses), en ambos grupos. Al comparar los datos demogrßficos bßsicos (edad y sexo), n·mero de comorbilidades y niveles sķricos de creatinina, urea y alb·mina, se comprob¾ que los pacientes del grupo control eran de mayor edad y tenĒan mayor n·mero de comorbilidades, niveles mßs altos de urea y mßs bajos de alb·mina; es decir, eran pacientes mßs complicados, lo que era previsible, ya que eran agudos, pero que sin duda introduce un sesgo. En cuanto a las causas de insuficiencia renal terminal, no se encontr¾ grandes diferencias entre los grupos; la mßs significativa fue la mayor frecuencia de diabetes tipo 2 entre los pacientes agudos (Tabla II).
Los pacientes se clasificaron en transferidos desde hemodißlisis, derivados en forma temprana (conocidos mßs de 90 dĒas), derivados en forma tardĒa (conocidos entre 30 y 90 dĒas), y derivados en forma aguda (menos de 30 dĒas). Hubo diferencias significativas entre ambos grupos (Tabla III).
Tabla III. Procedencia del paciente al inicio de la peritoneodißlisis.
Las complicaciones se dividieron en infecciosas y mecßnicas. Las complicaciones infecciosas fueron similares: hubo 8 casos de peritonitis en ambos grupos; 2 y 3 infecciones del sitio de salida en los grupos agudo y planificado, respectivamente; es decir, no hubo diferencia en los riesgos de complicaci¾n infecciosa entre los dos grupos. En cambio, las complicaciones mecßnicas fueron mßs frecuentes en el grupo agudo, que tuvo 15 complicaciones de este tipo, frente a 4 en el grupo planificado (p menor de 0,01 en Tes. exacto de FISE). Los mayores problemas fueron la fuga subcutßnea, con 4 casos en el grupo agudo versus 0 casos en el grupo planificado, y el mal funcionamiento del catķter, con 8 y 3 casos respectivamente; asĒ, en 10 de los 15 pacientes en PD aguda que se complicaron hubo que reemplazar el catķter; en cambio, hubo que hacer lo mismo en s¾lo 2 de los 4 casos de pacientes complicados entre los de DP planificada (p < 0,02 en Tes. exacto de FISE).
En el mismo estudio, 3 pacientes del grupo agudo y 1 del grupo control presentaron derrame pleuroperitoneal o pleural, situaci¾n que no se podrĒa atribuir a la tķcnica de paciente agudo. La fuga subcutßnea sĒ se puede relacionar con la tķcnica por el volumen que se utiliza. Por este motivo se cambi¾ la prescripci¾n de volumen a 1,2 litros en pacientes con menos de 60 kilos y 1,5 litros a pacientes con mßs de 60 kilos. El mal funcionamiento se podrĒa atribuir a elementos psicol¾gicos, ya que los primeros pacientes fueron los mßs difĒciles. En suma, en los pacientes en periotoneodißlisis aguda la incidencia de complicaciones mecßnicas, como derrame pleural no relacionado con el comienzo agudo, fuga subcutßnea que se podrĒa deber al volumen que permanece en la cavidad y mal funcionamiento que se podrĒa atribuir a factores psicol¾gicos o catķter flotante, fue significativamente mayor. Los peligros del acceso para la dißlisis aguda son las eventuales complicaciones mecßnicas, infecciosas, tromb¾ticas o esten¾ticas. Entonces, es importante considerar la PD como un puente para la hemodißlisis y, eventualmente, para el trasplante renal; pero no hay que pensar en un catķter venoso central temporal como puente para la PD.
En cuanto a los resultados, no hubo diferencia significativa en los pacientes transferidos para hemodißlisis, que fueron 6 en el grupo con PD aguda y 5 en el grupo control, ni en el n·mero de trasplantados (1 y 2 respectivamente); pero sĒ la hubo en cuanto a muertes, ya que fallecieron 6 de los pacientes del grupo agudo y ninguno de los del grupo control (p menor de 0,05 en test exacto de Fisher). Es importante recordar que los pacientes agudos tenĒan mayor comorbilidad, urea mßs alta y alb·mina mßs baja. En resumen, entre los pacientes del grupo agudo la mortalidad fue significativamente mayor. Un detalle importante es que 6 pacientes se transfirieron desde hemodißlisis a DP y 4 de ellos murieron, lo que se explica porque se les transfiri¾ en momentos crĒticos de su cuadro, ya que las muertes no tuvieron relaci¾n con uremia, acidosis, hipercalemia, sobrehidrataci¾n ni otro elemento propio de una dißlisis inadecuada: si se excluye a estos pacientes transferidos desde hemodißlisis, no habrĒa diferencia en la mortalidad entre ambos grupos. La tasa de supervivencia de la tķcnica fue similar en ambos grupos: 85%, si se hace la correcci¾n por muertes y trasplante renal en el grupo de pacientes agudos; y tambiķn se observ¾ el mismo riesgo de transferencia a hemodißlisis.
Es interesante analizar lo que pas¾ con la urea, el potasio y la acidosis, recordando que se trata de pacientes agudos que inician la dißlisis peritoneal con valores de urea de 35 mmol/lt. Al cabo de tres dĒas (Fig. 5), estos valores disminuyeron a niveles que se consideraron controlables. En relaci¾n con la acidosis, los pacientes iniciaron PD aguda con el nivel de bicarbonato en 20 a 21 mmol/l y al cabo de tres dĒas el mismo nivel estaba en 24 a 25 mmol/lt, lo que se considera normal (Fig. 6). Con respecto al potasio, se observ¾ lo mismo: el promedio inicial fue de 4,1 mmol/ L y a la larga se logr¾ un buen resultado (Fig.7).
Figura 5. Urea sķrica (media y desviaci¾n estßndar) despuķs del inicio de la PD aguda.
Figura 6. Tasa de correcci¾n de la acidosis despuķs del inicio de la PD aguda.
Figura 7. Tasa de correcci¾n de la hipercalemia despuķs del inicio de la PD aguda.
La PD aguda es una opci¾n simple y segura para comenzar en forma aguda la dißlisis cr¾nica. Como inicio de una PD cr¾nica, la PD aguda es una forma eficiente de aumentar la utilizaci¾n de la terapia de DP en pacientes nuevos que comienzan la dißlisis. La PD y la hemodißlisis son terapias complementarias, no s¾lo en el paciente cr¾nico sino tambiķn en el agudo. La PD aguda de emergencia se debe usar en: pacientes pedißtricos en espera de un trasplante, ni±os con insuficiencia renal cr¾nica (IRC), adultos con IRC, adultos con deficiencia renal aguda, como puente hacia la hemodißlisis, en pacientes con infecci¾n del acceso vascular y en pacientes con IRC terminal, derivados tardĒamente.
Si se trata de enfermedad hepßtica cr¾nica, la ·nica salida es un trasplante, lo mismo que en la insuficiencia cardiaca cr¾nica; en cambio, en la insuficiencia renal cr¾nica, estßn las opciones de la hemodißlisis, la DP y el trasplante, y, si este ·ltimo no funciona, se puede ir a DP o a hemodißlisis y viceversa. Si se reconoce que estas terapias son complementarias, se podrß obtener el mßximo provecho de ellas.

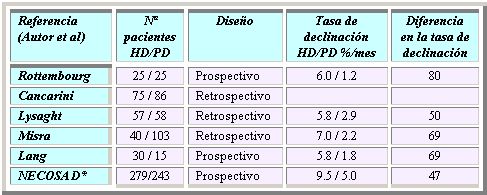 Tabla I. La dißlisis peritoneal mejora la preservaci¾n de la funci¾n renal residual (2).
Tabla I. La dißlisis peritoneal mejora la preservaci¾n de la funci¾n renal residual (2).

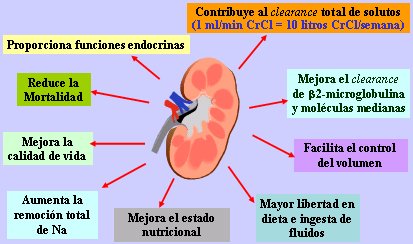 Figura 1. Beneficios de preservar la funci¾n renal residual.
Figura 1. Beneficios de preservar la funci¾n renal residual.

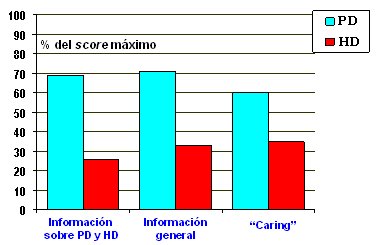 Figura 2. Satisfacci¾n con la cantidad de informaci¾n recibida: comparaci¾n entre pacientes en dißlisis peritoneal y en hemodißlisis (4).
Figura 2. Satisfacci¾n con la cantidad de informaci¾n recibida: comparaci¾n entre pacientes en dißlisis peritoneal y en hemodißlisis (4).

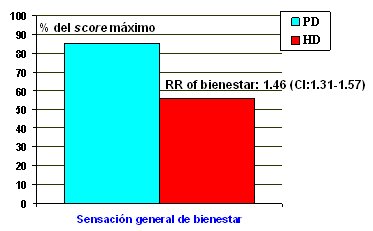 Figura 3. Impresi¾n de bienestar: comparaci¾n entre pacientes en dißlisis peritoneal y en hemodißlisis (4).
Figura 3. Impresi¾n de bienestar: comparaci¾n entre pacientes en dißlisis peritoneal y en hemodißlisis (4).

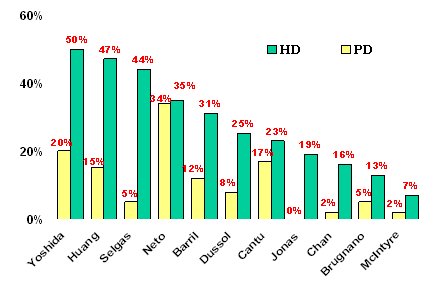 Figura 4. Prevalencia de anticuerpos contra el virus de la hepatitis C en pacientes en dißlisis, seg·n modalidad (5).
Figura 4. Prevalencia de anticuerpos contra el virus de la hepatitis C en pacientes en dißlisis, seg·n modalidad (5).

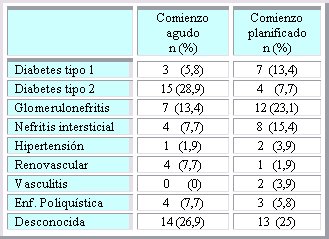 Tabla II. Causas de insuficiencia renal terminal: comparaci¾n entre pacientes que ingresaron a peritoneodißlisis en forma aguda o en forma planificada.
Tabla II. Causas de insuficiencia renal terminal: comparaci¾n entre pacientes que ingresaron a peritoneodißlisis en forma aguda o en forma planificada.

 Tabla III. Procedencia del paciente al inicio de la peritoneodißlisis.
Tabla III. Procedencia del paciente al inicio de la peritoneodißlisis.

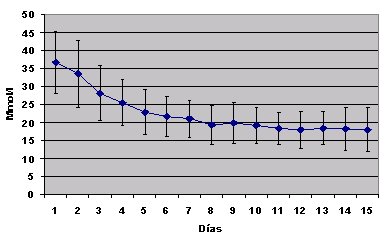 Figura 5. Urea sķrica (media y desviaci¾n estßndar) despuķs del inicio de la PD aguda.
Figura 5. Urea sķrica (media y desviaci¾n estßndar) despuķs del inicio de la PD aguda.

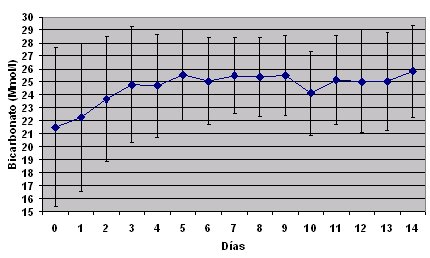 Figura 6. Tasa de correcci¾n de la acidosis despuķs del inicio de la PD aguda.
Figura 6. Tasa de correcci¾n de la acidosis despuķs del inicio de la PD aguda.

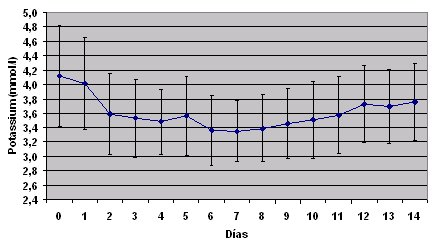 Figura 7. Tasa de correcci¾n de la hipercalemia despuķs del inicio de la PD aguda.
Figura 7. Tasa de correcci¾n de la hipercalemia despuķs del inicio de la PD aguda.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el marco del Congreso Conjunto de NefrologĒa, Hipertensi¾n y Trasplante 2006, Simposio Baxter, realizado en Valdivia entre los dĒas 4 al 7 de octubre de 2006. El evento fue organizado por la Sociedad Chilena de NefrologĒa, Hipertensi¾n y Trasplante. Secretaria Ejecutiva: Dra. Patricia Herrera. Secretario Ejecutivo Local: Dr. Claudio Flores.
 Expositor:
Josķ Divino[1]
Expositor:
Josķ Divino[1]

Citaci¾n: Divino J. Acute peritoneal dialysis in patients with chronic kidney disease. Medwave 2007 Mar;7(2):e1040 doi: 10.5867/medwave.2007.02.1040
Fecha de publicaci¾n: 1/3/2007

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n