En la investigación y tratamiento del paciente con microalbuminuria, se deben tomar las medidas siguientes:
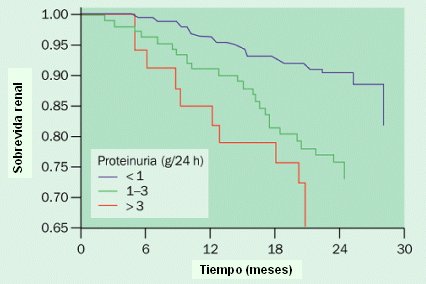
La microalbuminuria es un marcador de dańo renal y un testigo de nefropatía diabética precoz; se debe considerar como un mensaje del endotelio, en el sentido de que hay una disfunción generalizada que va progresando. Se sabe que la presencia de proteinuria es mala en toda nefropatía, como lo ilustra el gráfico de la Figura 1, en el que se muestra la sobrevida renal en los pacientes que presentan proteinuria menor de 1 gramo en 24 horas; entre 1 y 3 gramos en 24 horas; y más de 3 gramos en 24 horas; queda muy claro que, independiente de la etiología de la nefropatía, la presencia de proteinuria es un factor de mal pronóstico. Por eso, su detección es un pilar importante en las estrategias dirigidas a prevenir la progresión de la enfermedad.
Figura 1. Sobrevida renal según nivel de proteinuria.
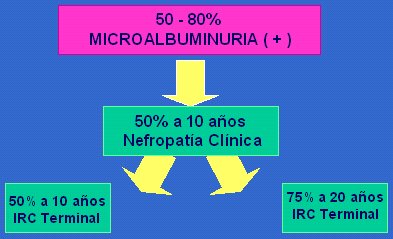
Cuando un paciente diabético tipo 1 tiene microalbuminuria, el riesgo de nefropatía es muy alto, sobre 80% (Fig. 2). En pacientes diabéticos tipo 2, el valor predictivo de la microalbuminuria es menor y fluctúa entre 20% y 45%, según la serie, lo que probablemente se deba a que estos enfermos fallecen antes, por causa cardiovascular; en otras palabras, si se eliminara la mortalidad por causa cardiovascular en los pacientes diabéticos tipo 2, probablemente aumentaría la oferta a diálisis, pero no seríamos capaces de absorberla.
Figura 2. Riesgo de progresión de nefropatía diabética tipo 1.
Los pilares de la terapia son el control glicémico (DCCT, UKPDS, Kumamoto Study); el control estrecho de la presión arterial (UKPDS, micro-HOPE, etc.); y la inhibición del sistema renina-angiotensina-aldosterona (Captopril Study, IRMA2, IDNT, RENAAL).
La estrategia dirigida a prevenir la progresión de la enfermedad comprende: diagnóstico e institución precoz del manejo; control de la presión arterial y de la proteinuria (que implica el uso de inhibidores de la ECA, boqueadores del receptor AT1, bloqueo dual con ECA y AT1), bloqueadores del calcio no dihidropiridínicos y, eventualmente, antagonistas de la aldosterona); restricción de la ingesta proteica; control del tabaquismo; tratamiento de la dislipidemia; control de la glicemia y de la obesidad; manejo de la hiperfosfemia y corrección de la acidosis; y también se plantea la necesidad de corregir precozmente la anemia y favorecer la quelación del plomo.
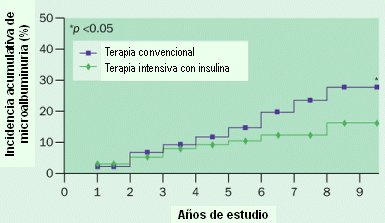
La utilidad del control metabólico estricto se ha establecido claramente en la prevención primaria y secundaria, en diabéticos tipo 1; en diabéticos tipo 2 también sería útil, según los resultados del estudio UKPDS y de un estudio japonés de menor cuantía. El objetivo es obtener cifras de hemoglobina glicosilada (HbA1c) menores de 7% (UKPDS). El control intensivo de la glicemia previene el desarrollo de nefropatía, como se demostró en un estudio realizado en diabéticos tipo 1, publicado en 2003 en The New England Journal of Medicine, en el que se observó que los pacientes que presentaban hemoglobina glicosilada de 6,9% o menos tenían menos incidencia acumulada de microalbuminuria, en comparación con los pacientes que recibieron terapia regular con insulina y con mal control metabólico (Fig. 3).
Figura 3. El control intensivo de la glicemia reduce el desarrollo de microalbuminuria.
En pacientes diabéticos tipo 2 no había una prueba tan clara hasta que se publicó el estudio UKPDS, realizado en Inglaterra en varios miles de pacientes diabéticos tipo 2 a quienes se siguió durante varios ańos. El estudio demostró que la hemoglobina glicosilada menor de 7% prevenía o reducía en 20% a 25% el desarrollo de todas las complicaciones microvasculares, una de las cuales es la nefropatía.
En el estudio UKPDS se estudió el efecto del control de la presión arterial en los pacientes diabéticos y se demostró claramente que el manejo adecuado con beta-bloqueadores o inhibidores de la enzima convertidora de angiotensina mejoraba significativamente los parámetros microvasculares, comparado con el control habitual. Los inhibidores de la enzima convertidora de angiotensina (IECA) o los bloqueadores de los receptores de angiotensina (AT1) retardan la progresión de la microalbuminuria y de la nefropatía clínica, por lo que son la primera elección farmacológica en caso de hipertensión arterial en estos pacientes. En teoría, están indicados en todo paciente con microalbuminuria positiva, aunque sea normotenso; es una recomendación tanto europea como estadounidense; en general, son bien tolerados. Después de iniciar la terapia conviene controlar el nivel de creatinina y potasio en forma precoz, a las dos semanas de tratamiento, ya que 10% a 15% de los pacientes diabéticos pueden presentar hiperaldosteronismo hipo-reninémico, a lo que se suma el hipoaldosterismo farmacológico causado por la inhibición del eje renina-angiotensina. Se debe advertir a los pacientes diabéticos e hipertensos que no consuman sales dietéticas si utilizan IECA, porque estas sales son ricas en potasio.
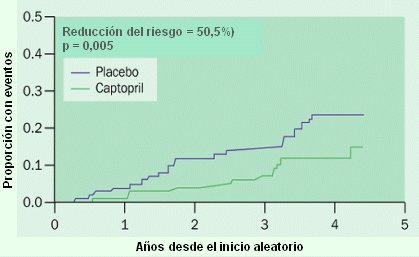
En 1992 se publicó la primera evidencia de la utilidad de los IECA, los que redujeron categóricamente la proporción de diabéticos tipo 1 que duplicaron sus niveles de creatinina o que necesitaron diálisis, al tercer o cuarto ańo de tratamiento. A partir de este resultado surgió una serie de trabajos sobre los IECA en pacientes diabéticos tipo 1 y tipo 2, con dosis y tiempos variables, con miras a determinar si este tratamiento podía controlar el desarrollo de nefropatía, o al menos retrasarlo, porque en esa época ya se vislumbraba el explosivo crecimiento de la nefropatía diabética como oferta de pacientes a diálisis (Fig. 4).
Figura 4. IECA en diabetes mellitus tipo 1.
Cuando se pusieron en boga los IECA, los interesados olvidaron que en la década de 1970 se había demostrado que el control de la presión arterial con tiazidas y beta-bloqueadores tipo Propanolol o Metildopa detenía en forma notoria la pendiente de caída de la velocidad de filtración glomerular, la que, con niveles de presión arterial próximos a 140/90 mmHg, era cercana a 1 ml/min/mes, mientras con estos fármacos se reducía a 0,29 y hasta 0,1 ml/min, lo que permitía retardar considerablemente la progresión de la nefropatía.
Un hecho llamativo es que los pacientes diabéticos tendrían una especial sensibilidad, desde el punto de vista de control de la presión y progresión, comparados con pacientes no diabéticos; sin embargo, este hallazgo inesperado no lo es tanto si se revisa el Informe de Hipertensión, estudio realizado hace mucho tiempo, que demostró el efecto beneficioso del control de la presión con felodipino, sobre la tasa de episodios cardiovasculares. En ese estudio, los pacientes diabéticos obtuvieron un beneficio mucho mayor que la población de pacientes no diabéticos, es decir que el control de la presión arterial ejercería efectos favorables, tanto en lo cardiovascular como en lo renal, y este efecto sería más notorio que en la población no diabética.
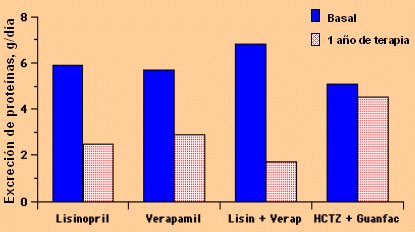
Una manera de objetivar el efecto del tratamiento es ver lo que pasa con la excreción de proteínas con la terapia. Si se compara los resultados de distintos fármacos sobre este parámetro (Fig. 5) se puede ver que el Lisinopril y el Verapamilo reducen en forma considerable la excreción proteica. Se ha planteado que el Verapamilo podría tener algún efecto independiente del control de la presión arterial, concretamente una acción estabilizante de la membrana basal glomerular; si esto se confirma con nuevos estudios, este fármaco se podría considerar como una alternativa cuando, por alguna razón, no se pueda efectuar bloqueo del eje renina-angiotensina.
Figura 5. Fármacos antihipertensivos y excreción proteica urinaria en nefropatía diabética.
En un estudio mucho más reciente, el IDNT (Irbesartan in Diabetic Nephropathy Trial), se comparó el efecto del IECA Irbesartán, Amlodipino y placebo en 1700 pacientes diabéticos tipo 2 y se demostró que el irbesartán reducía la progresión hacia insuficiencia renal y muerte en cerca de 20%. En cuanto a la duplicación de los niveles de creatinina, el irbesartán presentó un beneficio de alrededor de 25% en comparación con Amlodipino o placebo. En este estudio, el placebo y Amlodipino tuvieron los mismos resultados (Parving HH et al. N Engl J Med 2001; 345:870-878).
En forma casi simultánea apareció el estudio RENAAL (Reduction of Endpoints in NIDDM with the Angiotensin II Antagonist Losartan), en el que se evaluó, con una metodología similar, el efecto de Losartán en 1300 pacientes diabéticos tipo 2 a quienes se siguió durante 48 meses. El fármaco redujo la incidencia de nefropatía terminal en 28% y la combinación de nefropatía o muerte en 20%, en comparación con placebo (Brenner BM et al. N Engl J Med 2001;345(12):861-869). Por otra parte, en el estudio en colaboración de Lewis, con Captopril, y en los estudios REIN, con Ramipril, todos ellos controlados con placebo y efectuados con valores similares de presión arterial, también se comprobó una reducción significativa del riesgo de progresión a nefropatía terminal.
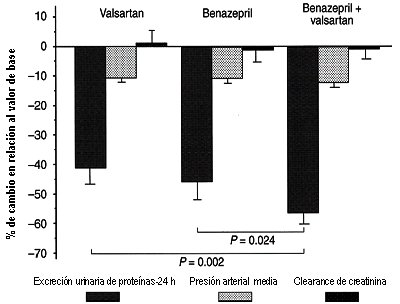
Con respecto a las ventajas del doble bloqueo de los receptores de angiotensina, en un estudio publicado en Kidney International, en el que se evaluó la excreción de proteínas en orina de 24 horas, en pacientes tratados con Valsartán o Benazepril, se observó una reducción similar en ambos grupos; pero al combinar ambos fármacos se obtuvo una reducción bastante mayor de la excreción de proteínas y una discreta reducción, no significativa, de la presión arterial, sin cambios importantes en la filtración glomerular, lo que significa que éste puede ser un camino interesante que seguir (Fig. 6).
Figura 6. Bloqueo dual en nefropatías proteinúricas (Campbell et al. Kidney Int 2003).
Los mecanismos que pueden explicar el efecto renoprotector de los IECA son la reducción de la presión arterial sistémica; reducción de la presión intraglomerular; aumento del flujo sanguíneo renal como reacción a la isquemia secundaria a la vasoconstricción renal; reducción de la proteinuria (en 45% en promedio); un efecto natriurético secundario a la inhibición del transporte de solutos inducido por AT-2 por el túbulo proximal; e inhibición de los efectos no hemodinámicos de la AT-2 sobre varios tipos de células, lo que reduce la proliferación, hipertrofia, expansión mesangial y síntesis de citoquinas y factores de crecimiento. Por esto, la AT-2 ya no se considera como un simple factor hemodinámico sino más bien como una citoquina proinflamatoria.
El control de la hipertensión arterial es un pilar importante en la estrategia del control de la progresión de la nefropatía diabética, lo que no significa que sea fácil; habitualmente se necesitan tres fármacos para lograr el objetivo de obtener una presión arterial de 125/75 mmHg (mínimo 130/80). Los fármacos que se recomiendan para lograr este objetivo son los bloqueadores de la ECA o de la AT-1, bloqueadores de canales de calcio no dihidropiridínicos, vasodilatadores y diuréticos (no monoterapia). En otras palabras, todo recurso vale. żCuáles son mejores? żLos IECA o los bloqueadores del receptor de AT-2? Numerosos trabajos, grandes y medianos, han demostrado que ambos tipos de fármacos tienen efectos equivalentes en el control de la hipertensión arterial y de la proteinuria en pacientes diabéticos tipo 2. Hasta el momento no ha aparecido un trabajo de seguimiento prolongado de un número grande de enfermos, en que se comparen ambos grupos.
En cuanto a si, para prevenir la progresión de la nefropatía diabética, es más eficaz el control de la presión arterial o el control de la glicemia, esta pregunta todavía no tiene una respuesta clara, pero hay argumentos en favor del control de la presión. Primero, los resultados del estudio UKPDS plantearían que el control de la presión arterial tiene más ventajas, en la prevención del desarrollo de complicaciones renales, que el control de la glicemia. Segundo, el control de la presión arterial retardaría la progresión del deterioro de la función renal a lo largo de toda la evolución de la nefropatía. Si se hace un intento de normalizar la glicemia cuando la función renal está en 25 a 28 ml/min, no se lograría nada, aparte de una eventual hipoglicemia; en cambio, el control de la presión arterial sería beneficioso durante todo el período de disfunción renal. En tercer lugar, es más fácil, en la práctica, lograr el control de la presión arterial que el de la glicemia.
Es probable que no importe tanto el fármaco como el valor de la presión arterial que se mida. En diabéticos tipo 1, parece claro que los IECA son más útiles que otros fármacos; pero en diabéticos tipo 2 los resultados son más discutibles y no está claro que los IECA sean superiores a otras terapias, excepto en los dos trabajos mencionados, los que no se refieren a IECA sino a bloqueadores del receptor de angiotensina. El valor práctico es que si la estrategia preventiva de progresión se basa en un IECA o en un inhibidor de receptor de angiotensina, va a llegar un momento en que se deberá suspender su uso, alrededor de 25 a 30 ml/min, cuando comience a aparecer hiperkalemia. Si entonces se piensa que no hay nada más que hacer, no se hará un esfuerzo por utilizar otras herramientas para controlar la presión arterial. Lo más importante es no renunciar al control de la presión por este motivo, sino recurrir a cualquier otra estrategia, por ejemplo, utilizar bloqueadores beta como Carvedilol o bloqueadores de los canales de calcio.
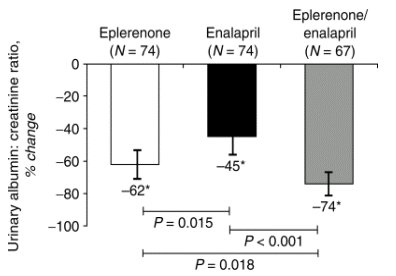
En un estudio reciente, también con bloqueo del eje renina-angiotensina, se investigó la utilidad de Eplerenona, bloqueador del receptor de aldosterona, y se observó que reducía de modo importante la excreción de proteínas, incluso más que Enalapril y sólo superada por la combinación de Eplerenona con Enalapril. En dicho estudio se observó mayor incidencia de hiperkalemia, como era previsible, pero se demostró que el bloqueo del receptor de aldosterona puede ser una herramienta adicional para continuar en la lucha por prevenir la progresión de la enfermedad (Fig. 7).
Figura 7. Bloqueo de aldosterona: evidencia en humanos.
La utilidad de la restricción proteica se ha demostrado claramente, en trabajos realizados en pacientes diabéticos tipo 1 y tipo 2. Esta medida está indicada en nefropatía clínica y consiste en administrar entre 0,6 y 0,8 g/kg/día, vigilando una eventual desnutrición. En la práctica, este aspecto es difícil, porque el paciente ya tiene restringidos los hidratos de carbono, por la diabetes, y la sal, por la hipertensión.
El abandono del tabaquismo es importante. Se ha demostrado que los pacientes diabéticos fumadores presentan mayor deterioro de la función renal que los diabéticos no fumadores. En un estudio publicado por Chuahirun se observa que los pacientes fumadores que iniciaron el estudio con un clearance de 102 ml/min, al término del estudio tenían 74 ml/min, es decir, habían perdido alrededor de 20 a 28 ml/min; en cambio, los no fumadores sólo habían perdido alrededor de 13 ml/min. Por lo tanto, desaconsejar el hábito de fumar es importante como parte de la estrategia para evitar la progresión, no sólo en nefropatía diabética (Chuahirun et al. Am J Kidney Dis, 2003).
El tratamiento hipolipemiante ha demostrado su utilidad en las nefropatías proteinúricas, una de las cuales es la nefropatía diabética, en términos de reducción de la caída de la velocidad de filtración glomerular. También se asocia a mayor reducción de la proteinuria, en nefropatía diabética y no diabética, como lo demuestra un metaanálisis de estudios en que se utilizaron estatinas, especialmente la atorvastatina (Fried et al. Kidney Int 2001).
En un estudio realizado en Suecia por Gaede, para evaluar la multi intervención en diabetes tipo 2, se demostró que el tratamiento intensificado, que incluía todos los aspectos descritos más arriba, redujo la incidencia de enfermedad cardiovascular en 53%; la nefropatía casi en 60%; la retinopatía en un porcentaje similar; y la polineuropatía autonómica en 63%. Estos resultados son muy buenos, pero se debe tomar en cuenta que son enfermos de estudio, es decir, tratados en forma precoz, en fases iniciales, probablemente pesquisados por la presencia de microalbuminuria positiva (Gaede P. NEJM, 2003, 348(5):383-393).
En un estudio realizado en Alemania se comprobó que los pacientes eran derivados al nefrólogo con nivel de creatinina de 29 ml/min, presión sistólica de 170 ml/min, hemoglobina glicosilada de 7,9 y colesterol LDL de 176 mg/dl, es decir, en condiciones desastrosas (Keller C. Deutsch Med Wochensch, 2000; 125 (9) :240-244).
El ideal es que los pacientes se deriven cuando tengan microalbuminuria persistente, con nivel de creatinina normal. Se debe recordar que el paciente diabético puede tener una creatinina de 1,1 o 1,2, en especial si es mujer, porque la nefropatía diabética pasa por un estado previo de hiperfiltración, de modo que con estos niveles se debe estudiar al paciente. También se debe derivar a los pacientes diabético hipertenso, a quienes tengan antecedentes familiares de nefropatía diabética o historia de episodios coronarios.
La triste realidad es que los pacientes llegan en estado de nefropatía diabética preterminal. En estos pacientes, el manejo parte por efectuar un doppler arterial de extremidades superiores e inferiores, para elegir el brazo que tenga la mejor arteria para la fístula, en caso de que necesite hemodiálisis; en ellos se debe efectuar el acceso vascular en forma precoz, con clearance de creatinina entre 20 y 25 ml/min, ya que en estos pacientes el desarrollo será lento y con un eventual fracaso del acceso vascular; se les debe derivar al oftalmólogo para fotocoagulación de los vasos de neoformación, que pueden sangrar cuando el paciente inicie hemodiálisis y se heparinice, y puede incluso quedar ciego; se debe realizar ecocardiograma 2 D, para investigar la posibilidad de cardiopatía isquémica; se debe iniciar en forma más precoz la hemodiálisis o peritoneodiálisis y convendría mantener el bloqueo del eje renina-angiotensina después del inicio de diálisis, aunque en la actualidad dicha medida está en investigación.
żSe puede prevenir la nefropatía diabética? Esta pregunta se está haciendo en todo el mundo. Para prevenir este problema se debe reconocer que existe y el éxito dependerá de la derivación precoz y de la suma de varios pequeńos éxitos, en cuanto al control de la presión y de la glicemia, en el marco de una política que apoye esta vital tarea. En este contexto, se debe saber que en Chile, la nefropatía diabética no se ha incorporado dentro del plan AUGE.







 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Expositor:
Antonio Saffie Ibáńez[1]
Expositor:
Antonio Saffie Ibáńez[1]

Citación: Saffie A. Prevention and progression of diabetic nephropathy II: treatment. Medwave 2006 Mar;6(2):e1886 doi: 10.5867/medwave.2006.02.1886
Fecha de publicación: 1/3/2006

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión