 Para Descargar PDF debe Abrir sesión.
Para Descargar PDF debe Abrir sesión.
Palabras clave: Idiopathic retroperitoneal fibrosis, secondary retroperitoneal fibrosis, abdominal pain, uretheral obstruction
Introducción: la primera descripción de obstrucción ureteral extrínseca por un proceso de fibrosis retroperitoneal se efectuó en 1905. En poco más de un siglo sólo se han reportado unos 800 casos de esta patología. Caso clínico: se reporta el caso de un paciente femenino de 55 ańos, que cursa con dolor abdominal difuso de larga evolución, acompańado de náusea, vómito, fiebre de 38°C e hipertensión de 160/100 mmHg. Se realiza tomografía axial computarizada observándose masa retroperitoneal que produce obstrucción de uréteres. Se realiza laparotomía exploradora con toma de biopsia y liberación de uréteres. El análisis histopatológico demuestra la presencia de fibrosis retroperitoneal, una entidad patológica poco frecuente, cuyo diagnóstico requiere un alto índice de sospecha en base a los hallazgos clínicos, de laboratorio y de gabinete. Revisión de la literatura: no se han formulado definiciones claras de los diferentes trastornos que se incluyen en el espectro de la fibrosis retroperitoneal, debido a lo infrecuente de esta enfermedad. Por esta razón hoy se carece de criterios diagnósticos y de una clasificación coherente de las diferentes formas que puede adoptar la enfermedad. Sin embargo, ante la sospecha de una fibrosis retroperitoneal se debe distinguir entre una forma idiopática y una secundaria, por las diferentes implicaciones para el tratamiento. Conclusión: la fibrosis retroperitoneal es un diagnóstico diferencial ante la presencia de dolor abdominal difuso asociado a síntomas de compresión ureteral o de grandes vasos.
En 1905 J. Albarran hizo la primera descripción de la obstrucción ureteral extrínseca por un proceso de fibrosis retroperitoneal. En 1948 John K. Ormond realizó una descripción completa de la fibrosis retroperitoneal en la literatura anglosajona y en 1957 Raper FR reportó la primera serie de esta enfermedad con siete casos[1],[2]. Hasta 2002 se habían descrito poco más de 800 casos de fibrosis retroperitoneal[3]. A continuación presentamos un caso de una paciente de 55 años con fibrosis retroperitoneal idiopática.
Se trata de una paciente femenina de 55 años de edad, con antecedente de tabaquismo y dolor articular crónico sin diagnóstico establecido. Inicia su padecimiento seis meses previos a su ingreso con dolor abdominal difuso, de leve intensidad y remisión espontánea a los dos días. Dos días antes de su ingreso se reinicia el dolor en hemiabdomen superior de mayor intensidad, con irradiación hacia la región dorso-lumbar, acompañado de náusea y vómito gastrobiliar, además de fiebre de 38°C.
A su ingreso presentó una presión arterial de 160/100 mmHg negando antecedentes de hipertensión, con facies de dolor, palidez de tegumentos, con regular estado de hidratación. Su abdomen presenta resistencia muscular voluntaria, con dolor intenso a la palpación de cuadrante superior derecho, signos de Murphy y Giordano derecho positivos. En los exámenes de laboratorio se observó una leucocitosis leve (12.100 células/mm3), elevación de urea y creatinina y examen general de orina con leve albuminuria. Se realizó ultrasonido de hígado y vía biliar sin alteraciones, con rastreo renal reportando crecimiento de ambas siluetas renales.
Al persistir presión arterial elevada, se sospecha una obstrucción de vasos renales y se solicita una tomografía axial computarizada. En la tomografía axial computarizada se identificó una masa retroperitoneal que producía obstrucción de uréteres (Figuras 1 y 2), por lo que se decidió realizar canulación con catéter doble J bilateral. Luego se efectuó laparotomía para liberación de los mismos. En la cirugía se observó un retroperitoneo de consistencia dura, desde L1 hasta la región sacra y a ambos lados abarcando ambos uréteres. Se realizó la liberación de uréteres y se tomaron biopsias de retroperitoneo y de ganglios retroperitoneales.
El examen histopatológico reportó la presencia de fibroblastos rodeados de abundantes fibras de colágeno, además de inflamación crónica inespecífica consistente con fibrosis retroperitoneal (Figura 3). Después de la cirugía se inició terapia esteroidea a base de prednisona, 60 mg diarios por un mes y posteriormente 20 mg diarios por 6 meses. Un año después de la cirugía, no se han presentado más alteraciones en la función renal ni de la presión arterial, por lo que no se ha indicado nueva tomografía ni reinicio del tratamiento con prednisona.
Figura 3. Microfotografía donde se identifican fibroblastos embebidos en fibras de colágeno.
El término fibrosis retroperitoneal se utiliza generalmente para referirse a una entidad clínico-anatomopatológica que se caracteriza por la presencia de tejido esclerótico en el retroperitoneo periaórtico y periilíaco[4]. La prevalencia estimada de la fibrosis retroperitoneal es de 0,2 a 2 casos por 100.000[3],[5], mientras que la incidencia anual es de 0,1-0,5 casos por cada 100.000 habitantes[4],[6] . Hay un predomino del género masculino en la fibrosis retroperitoneal de 2-3:1 respecto a las mujeres[7],[8],[9]. La edad de presentación típica es en la quinta y sexta décadas de vida[1],[5], [7],[10].
Se pueden distinguir tres grupos de fibrosis retroperitoneal:
Tabla I. Fármacos relacionados con fibrosis retroperitoneal.
Tabla II. Causas de fibrosis retroperitoneal secundaria.
Al parecer, la fibrosis retroperitoneal idiopática podría ser causada por una reacción alérgica a los componentes lipídicos de la pared aórtica[12]. El ceroide, un polímero insoluble de lípidos y proteínas oxidados, parece ser el antígeno blanco. De hecho, se pueden encontrar anticuerpos circulantes contra el ceroide en más del 90% de los pacientes con fibrosis retroperitoneal[3],[9]. Una vez que se produce el adelgazamiento o la rotura de la media de la aorta, los antígenos son procesados por los macrófagos de la adventicia[4]. Los antígenos son presentados a los linfocitos, lo que produce una activación de los mismos y la producción de autoanticuerpos. Ello inicia la respuesta inflamatoria, con la llegada de células de defensa al área de aterosclerosis y liberación de numerosas citocinas, factores de crecimiento y sustancias profibrinogénicas. Los macrófagos secretan factor de crecimiento fibroblástico y los linfocitos T secretan factor de crecimiento fibroblástico y factor estimulante de la síntesis de colágeno, lo que resulta en la proliferación de fibroblastos y fibrosis[9].
Se ha planteado la posibilidad de que las células plasmáticas portadoras de IgG4 desempeñen un papel patogénico en la fibrosis retroperitoneal idiopática[4]. Con todo, algunos sujetos ancianos muestran IgG frente al ceroide sin expresión de la enfermedad, lo que puede indicar que hay una respuesta inmunológica de grado diverso o que se trata de un epifenómeno de la fibrosis retroperitoneal[1],[13].
El depósito de hemosiderina en algunas placas fibróticas indica una hemorragia retroperitoneal previa que podría contribuir al proceso de fibrosis[8]. También se ha supuesto que el consumo prolongado de metisergida (siendo antagonista de la serotonina), causa un efecto de rebote en la liberación de serotonina. A su vez, la serotonina tiene efectos profibróticos y esto podría ser responsable del desarrollo de la fibrosis retroperitoneal[14]. De hecho, la metisergida se ha relacionado con 12% de los casos de fibrosis retroperitoneal[8]. En el caso de los cánceres relacionados con fibrosis retroperitoneal podrían producir compuestos fibrogénicos, como serotonina y factores de crecimiento. Finalmente, la fibrosis retroperitoneal puede resultar como una respuesta esclerótica a la radioterapia, a las infecciones, a los traumatismos o las lesiones quirúrgicas[4].
Los signos y síntomas están relacionados con el atrapamiento y compresión de los uréteres, vena cava inferior, aorta y sus ramas o vasos gonadales[8]. Inicialmente se presenta con síntomas inespecíficos como dolor difuso de espalda baja, flanco o abdomen en 80 a 100% de los casos, con aparición insidiosa e intensidad progresivamente creciente debido a la obstrucción ureteral[3],[8],[11]. En consecuencia, los síntomas están en relación con la oliguria y la uremia[4], con presencia de hipertensión arterial (de 50 a 60%)[3], anemia, alteraciones de los líquidos y electrolitos[4], malestar general (25%), náusea y vómito (3%), infección urinaria (6%), cólico renal (10%), hematuria (3%) y oclusión intestinal (10%)[11]. Puede existir polaquiuria y disuria, incluso en ausencia de una infección de la vía urinaria.
Los síntomas secundarios a la obstrucción de la vía urinaria son más frecuentes debido a que la obstrucción de los dos uréteres se presenta en el 50% o más de los casos. Dicha obstrucción puede ser simultanea o metacrónica[4]. La presencia de anorexia (13%), fiebre leve (3%) y pérdida de peso (13%)[11] podrían ser un reflejo de la naturaleza inflamatoria sistémica de la enfermedad[4].
La compresión de la vena cava inferior causa edema de los miembros inferiores o escroto, o tromboflebitis profunda de las piernas, mientras que la afección de los vasos y linfáticos gonadales puede resultar en hidroceles, molestia escrotal[8] y disfunción eréctil[4]. Aunque la tromboflebitis se puede presentar en el 6% de los casos[11], el resto de estos últimos síntomas son menos frecuentes[4]. La compresión de la aorta y arterias iliacas comunes produce claudicación y gangrena de las extremidades inferiores. La estenosis de las arterias renales puede producir hipertensión renovascular, mientras que la oclusión de las arterias mesentéricas superior e inferior pueden producir isquemia intestinal[8]. En etapas tardías puede presentarse insuficiencia renal aguda por obstrucción ureteral[3],[7],[11].
La fibrosis extraperitoneal junto con enfermedades y fenómenos autoinmunes se presenta entre el 8 y 15% de los casos de fibrosis retroperitoneal en forma de fibrosis mediastinal, tiroiditis de Riedel, pseudotumor orbitario fibrótico, periarteritis de las arterias coronarias, nódulos hialinos pulmonares, colangeítis esclerosante, sialoadenitis crónica y fibrosis periarticular[3],[4],[7],[8] . Es menos frecuente la asociación de fibrosis retroperitoneal con lupus eritematoso sistémico, enfermedad de Crohn, artritis, púrpura de Henoch-Schönlein, espondilitis anquilosante, poliarteritis nodosa, granulomatosis de Wegener[14], arteritis de Takayasu, cirrosis biliar primaria, sarcoidosis, contractura de Dupuytren, enfermedad de Peyronie[1], enfermedad de Weber-Christian sistémica (paniculitis no supurativa), escleroderma, mesenteritis esclerosante y pancreatitis crónica de origen autoinmune[15] [16],[17],[18].
El diagnóstico de la fibrosis retroperitoneal tiene cierta dificultad en la práctica clínica. La fibrosis retroperitoneal carece de criterios diagnósticos establecidos, así que el diagnóstico se realiza con signos clínicos sugestivos, junto con exámenes de laboratorio y estudios de imagen compatibles[10].
No hay estudios de laboratorio específicos para la fibrosis retroperitoneal, aunque puede observarse piuria (60% de los casos), proteinuria (40%), índice de sedimentación eritrocitario elevado (entre 80 y 90% de los casos), hipergammaglobulinemia policlonal[3],[14] , algún grado de compromiso renal (más del 75% de los casos)[8], hipoalbuminemia, anemia normocrómica y normocítica, trombocitosis leve, autoanticuerpos contra músculo liso[7], anticuerpos antinucleares (hasta 60% de los casos) y factor reumatoide (probablemente una alteración general de la autotolerancia). Puede haber elevación de otros autoanticuerpos cuando hay relación con otras enfermedades, como los anticuerpos anticitoplasma de neutrófilos (relacionados con la granulomatosis de Wegener o la poliangeítis), anticuerpos antitiroglobulina y microsomales antitiroideos (tiroiditis autoinmunitaria), anticuerpos contra dsADN (lupus eritematoso sistémico) y los antígenos Ro(SSA)/La(SSB) (síndrome de Sjögren). Por otro lado, el valor de la proteína C reactiva suele estar sumamente elevado. Recientemente se han observado concentraciones séricas elevadas de IgG4 y abundancia de células plasmáticas portadoras de IgG4 en los infiltrados inflamatorios presentes en las zonas afectadas por la enfermedad. Esto ha llevado a algunos investigadores a acuñar el término de “síndrome de hiper-IgG4”[4].
La urografía excretora se basa en la presencia de una triada clásica que consiste en el retraso en la excreción del medio de contraste con hidronefrosis unilateral (20% de los casos) o bilateral (68% de los casos) e hidrouréter proximal secundaria a la afección ureteral, desviación medial del tercio medio de ambos uréteres, y estrechamiento de la luz ureteral a nivel vertebral L4-L5. No obstante, la desviación medial del uréter, considerado como un signo clásico de la fibrosis retroperitoneal en pielografía, puede observarse en el 20% de los individuos no afectados[6].
El ultrasonido generalmente muestra una masa retroperitoneal para-aórtica o en el espacio perirrenal, hipoecoica, bien definida, la cual se asocia con hidronefrosis o dilatación ureteral proximal[11]. La masa se observa hipoecoica o anecoica, bien delimitada, aunque con bordes irregularmente contorneados. Se debe evaluar integralmente la columna lumbar prevertebral y paravertebral para evaluar plenamente la presencia y extensión de la reacción fibrótica[6]. La hidronefrosis es bilateral en 60%, unilateral en 20% y no está presente en el resto[11]. La ultrasonografía tiene una sensibilidad global para la detección de la fibrosis retroperitoneal de sólo 25%[6], aunque puede utilizarse para monitorizar la extensión de la hidronefrosis y evaluar de forma indirecta la respuesta al tratamiento[4].
La tomografía axial computarizada puede mostrar una masa que generalmente inicia a nivel del hilio renal y se limita a la región lumbar. En las fibrosis retroperitoneal no malignas, el borde anterior se encuentra claramente delimitado y pobremente en el margen posterior. Esta masa tiende a envolver la aorta y la vena cava, pero sin desplazarlas[11] aunque sí produce una desviación medial y compresión extrínseca de los uréteres[4]. Generalmente, el centro de la fibrosis se encuentra en el nivel de la bifurcación aórtica[6], pero es rara la extensión hasta la pelvis o hacia duodeno, páncreas e incluso mediastino. La densidad de la masa en la tomografía axial computarizada es similar a la del músculo y con contraste intravenoso la placa en etapas tempranas es más vascular y muestra un buen realce, mientras que en las etapas tardías, la placa es avascular y tiene poco realce[6],[11]. Sin embargo, la reacción fibrosa no puede ser fácilmente apreciable en la tomografía axial computarizada. Se ha informado que un tercio de los pacientes con fibrosis retroperitoneal quirúrgicamente probada no tenía anomalía alguna en la tomografía axial computarizada[6].
La resonancia magnética puede mostrar engrosamiento de las cápsulas renales, una masa bien definida alrededor de la aorta, además de datos de aortitis (estenosis y engrosamiento y anormalidades estructurales en la pared de los vasos)[6]. La diferenciación entre la fibrosis retroperitoneal maligna y no maligna puede ser factible con la resonancia magnética. La fibrosis retroperitoneal benigna consta de una masa retroperitoneal más homogénea y de más baja intensidad en la señal de T2. Una fibrosis retroperitoneal maligna posee un margen mal definido, una masa heterogénea y una mayor intensidad de señal en T2 que en T1[11].
No se han formulado definiciones claras de los diferentes trastornos que se incluyen en el espectro de la fibrosis retroperitoneal. Esta falta de claridad probablemente se debe al hecho de que la fibrosis retroperitoneal es una enfermedad muy poco frecuente, por lo que actualmente se carece de criterios diagnósticos y de una clasificación coherente de las diferentes formas que puede adoptar la enfermedad. Sin embargo, ante la sospecha de una fibrosis retroperitoneal se debe hacer una distinción entre una forma idiopática y una secundaria de la enfermedad, debido a sus diferentes implicaciones para el tratamiento[4].
El diagnóstico de certeza para la fibrosis retroperitoneal es la biopsia del tejido fibrótico[19]. En la evaluación macroscópica, la placa fibrótica tiene una consistencia de madera color blanco grisáceo, con un borde anterior bien delimitado, pero el posterior es difícil de separar del resto de la estructuras. La placa usualmente está centrada en la superficie de las vertebras lumbares bajas[5],[8]. Esta placa rodea la aorta y la vena cava inferior y sólo en 10% de los casos afecta a la pelvis entre los vasos iliacos[20].
Ormond dividió a la enfermedad en tres etapas evolutivas con diferentes hallazgos microscópicos:
El tratamiento de la fibrosis retroperitoneal inicialmente es médico y se basa en la suspensión de los fármacos sospechosos de producir la agresión[12] y el uso empírico de esteroides en las fases tempranas en dosis de 40 a 60 mg por día (1 mg/kg/día) durante 6 a 8 semanas. Si se controla el cuadro agudo, se mantiene la dosis de prednisona de 10 mg por día por un período de 12 a 18 meses. Posteriormente se mantiene vigilancia del paciente cada 3 a 6 meses[3]. El uso de esteroide tiene una mejor respuesta en los casos de fibrosis retroperitoneal idiopática, además de ser más útiles en la fase inicial de la fibrosis retroperitoneal, no así en la fase madura y de escara cuando hay poca respuesta celular[5].
En etapas iniciales de la fibrosis retroperitoneal la obstrucción ureteral frecuentemente es unilateral y la respuesta a los esteroides es adecuada. Sin embargo en etapa tardía el curso clínico es más serio, hay escasa respuesta a los esteroides e incluso al tratamiento quirúrgico debido a la presencia de una fibrosis bien establecida y afección ureteral bilateral. Si no hay respuesta al esteroide se puede intentar el uso de inmunosupresores como la ciclosporina, la azatioprina y la ciclofosfamida, aunque la acción de estas dos últimas es retrasada y tienen una gran toxicidad, además de existir poca experiencia en su uso[5],[12]. La respuesta observada en el manejo con prednisona 0,5 mg/kg/día por un mes y reducción gradual hasta una dosis de mantenimiento de 10 a5 mg/día por 18 meses, junto con azatioprina a dosis de 1,5 mg/kg/día por 16 meses, es del 100%[22] . Se ha descrito el uso de esteroide asociado a colchicina (0,5 mg cada 12 horas por 2 años) por su efecto antifibrótico y antiinflamatoria con buenos resultados. Su uso evita dosis elevadas de esteroides o inmunosupresores y tiene buenos resultados[23].
En tiempos recientes ha tomado una mayor importancia el tamoxifeno, un antiestrógeno que inhibiría el crecimiento de los fibroblastos y la producción de diversas citocinas[5]. Se ha reportado una rápida mejoría en la función renal por fibrosis retroperitoneal usando cirugía y tamoxifeno, con éxito a largo plazo (hasta 4 años de seguimiento) y pocos efectos colaterales. La respuesta observada en pacientes tratados con prednisona a 1 mg/kg/día por 1 mes y reducción hasta una dosis de mantenimiento de 10-5 mg/día por 15 meses, asociado con tamoxifeno 20 a 40 mg/día por 18 meses ha sido del 94%. Sin embargo, cabe mencionar que todas estas respuestas al tratamiento médico se basan en pequeñas series de casos y otros anecdóticos, por lo que su papel aún está por investigarse con un mayor número de pacientes[22] .
El manejo quirúrgico debe estar encaminado a la incisión de la masa fibrosa con liberación de los uréteres o cualquier otro órgano envuelto por la fibrosis[21] . La ureterólisis e intraperitonealización del uréter y/o envolvimiento de los uréteres en el epiplón ha sido ampliamente usada, aunque tiene una recidiva de hasta 22%[22] . En caso de daño irreparable del uréter, puede realizarse resección ureteral con anastomosis primaria, autotransplante, uso de injerto de vena espermática, interposición ileal, ureteroneocistostomía y reimplantación ureteral[12]. La nefrostomía percutánea o la colocación de catéteres doble J son manejos temporales de la insuficiencia renal aguda obstructiva. Los stents se reservan para pacientes con fibrosis retroperitoneal maligna o con alto riesgo con la realización de la cirugía[21] . El índice de éxito con la cirugía urológica consistente únicamente en la ureterólisis es de 73%, con los esteroides es de 86% y con la combinación de ambos de 73%. La combinación de esteroides y otros agentes inmunosupresores permiten una mejoría en 97% de los casos de fibrosis retroperitoneal[10].
El pronóstico depende de un diagnóstico temprano de la enfermedad e inicio del tratamiento médico antes de que se presenten los cambios irreversibles en uno o ambos riñones. En pacientes con fibrosis retroperitoneal idiopática sin compromiso renal el pronóstico es excelente, con éxito a largo plazo de más de 90%[11]. Se debe mantener un monitoreo de los pacientes con fibrosis retroperitoneal debido a que la enfermedad puede recurrir dentro de los 5 años después del diagnóstico, aunque se han reportado casos raros de recurrencia después de 10 años de seguimiento[22] . El pronóstico es más pobre en pacientes con fibrosis retroperitoneal maligna, con una supervivencia media de 3 a 6 meses después de establecido el diagnóstico[11].
Se concluye que la fibrosis retroperitoneal debe ser parte del diagnóstico diferencial ante la presencia de dolor abdominal difuso asociado a síntomas de compresión ureteral o de grandes vasos. La realización de estudios tomográficos puede servir para establecer la sospecha, aunque el diagnóstico de certeza es la exploración quirúrgica con toma de biopsia, así como el tratamiento adecuado de los uréteres envueltos por la compresión de la fibrosis retroperitoneal. El establecimiento del período de evolución debe determinar si el manejo será de predominio médico basado en esteroides o si los resultados serán mejores con un abordaje quirúrgico.
Los autores han completado el formulario de declaración de conflictos de intereses del ICMJE traducido al castellano por Medwave, y declaran no haber recibido financiamiento para la realización del artículo; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado, en los últimos tres años; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. El formulario puede ser solicitado contactando al autor responsable.
Los autores obtuvieron el consentimiento informado de los parientes del sujeto del estudio, para el uso de los datos y la posterior publicación de los resultados en Medwave. El formulario puede ser solicitado contactando al autor responsable.

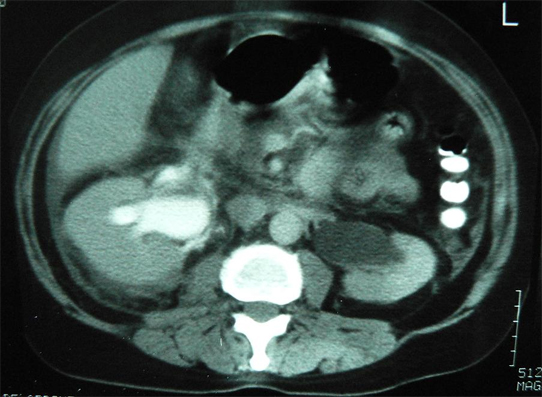 Figura 1. Placa de tomografía axial computarizada en la que se observa dilatación del sistema pielocalicial importante en ambos rińones.
Figura 1. Placa de tomografía axial computarizada en la que se observa dilatación del sistema pielocalicial importante en ambos rińones.

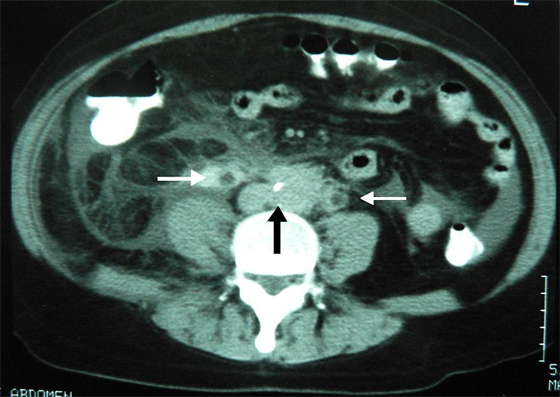 Figura 2. Placa de tomografía axial computarizada en la que se observa intensa reacción alrededor de ambos uréteres dilatados (flechas blancas), así como pérdida de la anatomía en torno a la vena cava inferior y aorta (flecha negra).
Figura 2. Placa de tomografía axial computarizada en la que se observa intensa reacción alrededor de ambos uréteres dilatados (flechas blancas), así como pérdida de la anatomía en torno a la vena cava inferior y aorta (flecha negra).

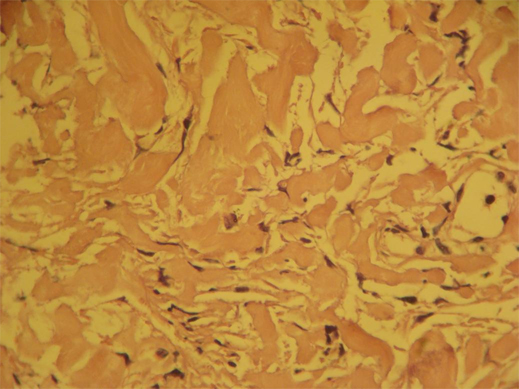 Figura 3. Microfotografía donde se identifican fibroblastos embebidos en fibras de colágeno.
Figura 3. Microfotografía donde se identifican fibroblastos embebidos en fibras de colágeno.

 Tabla I. Fármacos relacionados con fibrosis retroperitoneal.
Tabla I. Fármacos relacionados con fibrosis retroperitoneal.

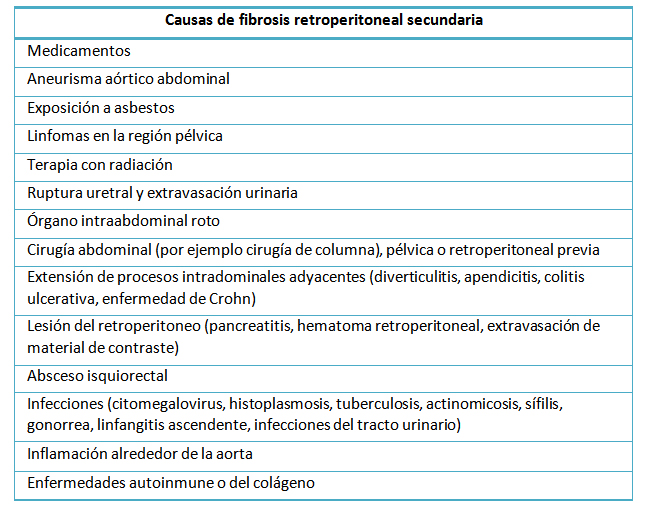 Tabla II. Causas de fibrosis retroperitoneal secundaria.
Tabla II. Causas de fibrosis retroperitoneal secundaria.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Introduction. The first description of extrinsic uretheral obstruction by retroperitoneal fibrosis occurred in 1905. In little more than a century, about 800 cases of this disease have been reported. Case description. We report the case of a female 55 year-old patient who presents with diffuse abdominal pain of long duration, nausea, vomiting, fever of 38°C and hypertension of 160/100 mmHg. A CT scan is performed that shows a retroperitoneal mass that obstructs the urethers. Exploratory laparotomy was performed, urethers were released and biopsy was taken. Pathology analysis showed the presence of retroperitoneal fibrosis, a rare pathological entity whose diagnosis requires a high index of suspicion based on clinical, imaging and laboratory workup. Literature review. There are no clear definitions of the variety of disorders that are included in the spectrum of retroperitoneal fibrosis, due to the rarity of this condition. Consequently, we lack diagnostic criteria and a consistent classification of the different forms that it may adopt. However, when there is suspicion of retroperitoneal fibrosis, the first step is to establish whether it is idiopathic or secondary, as there will be treatment implications. Conclusion. Retroperitoneal fibrosis should be considered in the differential diagnosis whenever diffuse abdominal pain is associated with uretheral or great vessels compression.
 Autores:
José Francisco Camacho[1], Juan Carlos Helú[2,3], Alfonso Valenzuela [3], Juan Francisco Hidalgo[4]
Autores:
José Francisco Camacho[1], Juan Carlos Helú[2,3], Alfonso Valenzuela [3], Juan Francisco Hidalgo[4]

Citación: Camacho JF, Helú JC, Valenzuela A, Hidalgo JF. Retroperitoneal fibrosis: case report and literature review. Medwave 2013;13(8):e5795 doi: 10.5867/medwave.2013.08.5795
Fecha de envío: 3/9/2013
Fecha de aceptación: 23/9/2013
Fecha de publicación: 27/9/2013
Origen: no solicitado
Tipo de revisión: con revisión por tres pares revisores, a doble ciego

Nos complace que usted tenga interés en comentar uno de nuestros artículos. Su comentario será publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la dirección editorial considera que su comentario es: ofensivo en algún sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas políticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisión por pares.
Aún no hay comentarios en este artículo.
Para comentar debe iniciar sesión
 Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
Medwave publica las vistas HTML y descargas PDF por artículo, junto con otras métricas de redes sociales.
 Wu J, Catalano E, Coppola D. Retroperitoneal fibrosis (Ormond's disease): clinical pathologic study of eight cases. Cancer Control. 2002 Sep-Oct;9(5):432-7. | PubMed |
Wu J, Catalano E, Coppola D. Retroperitoneal fibrosis (Ormond's disease): clinical pathologic study of eight cases. Cancer Control. 2002 Sep-Oct;9(5):432-7. | PubMed | Pérez OI, Lizarralde ZL, de Pierola BF, García AL, Crespo CI. Fibrosis retroperitoneal secundaria a neoplasia gástrica. Actas Urol Esp. 2008 Mar;32(3):345-7. | CrossRef | PubMed |
Pérez OI, Lizarralde ZL, de Pierola BF, García AL, Crespo CI. Fibrosis retroperitoneal secundaria a neoplasia gástrica. Actas Urol Esp. 2008 Mar;32(3):345-7. | CrossRef | PubMed | Monev S. Idiopathic retroperitoneal fibrosis: prompt diagnosis preserves organ function. Cleve Clin J Med. 2002 Feb;69(2):160-6. | CrossRef | PubMed |
Monev S. Idiopathic retroperitoneal fibrosis: prompt diagnosis preserves organ function. Cleve Clin J Med. 2002 Feb;69(2):160-6. | CrossRef | PubMed | Vaglio A, Palmisano A, Corradi D, Salvarani C, Buzio C. Retroperitoneal fibrosis: evolving concepts. Rheum Dis Clin North Am. 2007 Nov;33(4):803-17, vi-vii. | CrossRef | PubMed |
Vaglio A, Palmisano A, Corradi D, Salvarani C, Buzio C. Retroperitoneal fibrosis: evolving concepts. Rheum Dis Clin North Am. 2007 Nov;33(4):803-17, vi-vii. | CrossRef | PubMed | Mańero C, Navas-Parejo A, Prados MD, García-Valdecasas J, Hornos C, Espigares MJ, et al. Fracaso renal agudo obstructivo por masa retroperitoneal. Nefrologia. 2004;24 Suppl 3:49-55. | PubMed |
Mańero C, Navas-Parejo A, Prados MD, García-Valdecasas J, Hornos C, Espigares MJ, et al. Fracaso renal agudo obstructivo por masa retroperitoneal. Nefrologia. 2004;24 Suppl 3:49-55. | PubMed | Cronin CG, Lohan DG, Blake MA, Roche C, McCarthy P, Murphy JM. Retroperitoneal fibrosis: a review of clinical features and imaging findings. AJR Am J Roentgenol. 2008 Aug;191(2):423-31. | CrossRef | PubMed |
Cronin CG, Lohan DG, Blake MA, Roche C, McCarthy P, Murphy JM. Retroperitoneal fibrosis: a review of clinical features and imaging findings. AJR Am J Roentgenol. 2008 Aug;191(2):423-31. | CrossRef | PubMed | Amis ES Jr. Retroperitoneal fibrosis. AJR Am J Roentgenol. 1991 Aug;157(2):321-9. | CrossRef | PubMed |
Amis ES Jr. Retroperitoneal fibrosis. AJR Am J Roentgenol. 1991 Aug;157(2):321-9. | CrossRef | PubMed | Demko TM, Diamond JR, Groff J. Obstructive nephropathy as a result of retroperitoneal fibrosis: a review of its pathogenesis and associations. J Am Soc Nephrol. 1997 Apr;8(4):684-8. | PubMed |
Demko TM, Diamond JR, Groff J. Obstructive nephropathy as a result of retroperitoneal fibrosis: a review of its pathogenesis and associations. J Am Soc Nephrol. 1997 Apr;8(4):684-8. | PubMed | Castro-Iglesias N, Belhassen-García M, Velasco-Tirado V, Carpio-Pérez A, Inés-Revuelta S, Martín-Barba S, et al. Ormond's disease: Experience with five cases. Reumatol Clin. 2010 Jul-Aug;6(4):199-202. | CrossRef | PubMed |
Castro-Iglesias N, Belhassen-García M, Velasco-Tirado V, Carpio-Pérez A, Inés-Revuelta S, Martín-Barba S, et al. Ormond's disease: Experience with five cases. Reumatol Clin. 2010 Jul-Aug;6(4):199-202. | CrossRef | PubMed | Vivas I, Nicolás AI, Velázquez P, Elduayen B, Fernández-Villa T, Martínez-Cuesta A. Retroperitoneal fibrosis: typical and atypical manifestations. Br J Radiol. 2000 Feb;73(866):214-22. | PubMed |
Vivas I, Nicolás AI, Velázquez P, Elduayen B, Fernández-Villa T, Martínez-Cuesta A. Retroperitoneal fibrosis: typical and atypical manifestations. Br J Radiol. 2000 Feb;73(866):214-22. | PubMed | Marzano A, Trapani A, Leone N, Actis GC, Rizzetto M. Treatment of idiopathic retroperitoneal fibrosis using cyclosporin. Ann Rheum Dis. 2001 Apr;60(4):427-8. | CrossRef | PubMed | PMC |
Marzano A, Trapani A, Leone N, Actis GC, Rizzetto M. Treatment of idiopathic retroperitoneal fibrosis using cyclosporin. Ann Rheum Dis. 2001 Apr;60(4):427-8. | CrossRef | PubMed | PMC | Keith DS, Larson TS. Idiopathic retroperitoneal fibrosis. J Am Soc Nephrol. 1993 May;3(11):1748-52. | PubMed |
Keith DS, Larson TS. Idiopathic retroperitoneal fibrosis. J Am Soc Nephrol. 1993 May;3(11):1748-52. | PubMed | Bilici A, Karadag B, Doventas A, Erdincler DS, Cetinkaya S, Ogut G, et al. Retroperitoneal fibrosis caused by pergolide in a patient with Parkinson's disease. Neth J Med. 2004 Nov;62(10):389-92. | PubMed |
Bilici A, Karadag B, Doventas A, Erdincler DS, Cetinkaya S, Ogut G, et al. Retroperitoneal fibrosis caused by pergolide in a patient with Parkinson's disease. Neth J Med. 2004 Nov;62(10):389-92. | PubMed | Kamisawa T, Chen PY, Tu Y, Nakajima H, Egawa N. Autoimmune pancreatitis metachronously associated with retroperitoneal fibrosis with IgG4-positive plasma cell infiltration. World J Gastroenterol. 2006 May 14;12(18):2955-7. | PubMed |
Kamisawa T, Chen PY, Tu Y, Nakajima H, Egawa N. Autoimmune pancreatitis metachronously associated with retroperitoneal fibrosis with IgG4-positive plasma cell infiltration. World J Gastroenterol. 2006 May 14;12(18):2955-7. | PubMed | Ng NK, Bong JJ, Williamson RC. Lymphoplasmacytic sclerosing pancreatitis and retroperitoneal fibrosis. HPB Surg. 2008;2008:719513. | PubMed |
Ng NK, Bong JJ, Williamson RC. Lymphoplasmacytic sclerosing pancreatitis and retroperitoneal fibrosis. HPB Surg. 2008;2008:719513. | PubMed | Fukukura Y, Fujiyoshi F, Nakamura F, Hamada H, Nakajo M. Autoimmune pancreatitis associated with idiopathic retroperitoneal fibrosis. AJR Am J Roentgenol. 2003 Oct;181(4):993-5. | CrossRef | PubMed |
Fukukura Y, Fujiyoshi F, Nakamura F, Hamada H, Nakajo M. Autoimmune pancreatitis associated with idiopathic retroperitoneal fibrosis. AJR Am J Roentgenol. 2003 Oct;181(4):993-5. | CrossRef | PubMed | Schultz O, Schuchmann S, Burmester GR, Buttgereit F. Case number 26: systemic idiopathic fibrosis associated with aortitis. Ann Rheum Dis. 2003 May;62(5):486. | CrossRef | PubMed | PMC |
Schultz O, Schuchmann S, Burmester GR, Buttgereit F. Case number 26: systemic idiopathic fibrosis associated with aortitis. Ann Rheum Dis. 2003 May;62(5):486. | CrossRef | PubMed | PMC | Park BK, Kim SH, Moon MH. Idiopathic presacral retroperitoneal fibrosis: report of two cases. Br J Radiol. 2003 Aug;76(908):570-3. | CrossRef | PubMed |
Park BK, Kim SH, Moon MH. Idiopathic presacral retroperitoneal fibrosis: report of two cases. Br J Radiol. 2003 Aug;76(908):570-3. | CrossRef | PubMed | Takahashi J, Wakamatsu Y, Okude J, Gohda T, Sanefuji Y, Sasaki S, et al. Idiopathic retroperitoneal fibrosis in a patient suspected of impending rupture of the abdominal aortic aneurysm. Ann Thorac Cardiovasc Surg. 2008 Feb;14(1):55-9. | PubMed |
Takahashi J, Wakamatsu Y, Okude J, Gohda T, Sanefuji Y, Sasaki S, et al. Idiopathic retroperitoneal fibrosis in a patient suspected of impending rupture of the abdominal aortic aneurysm. Ann Thorac Cardiovasc Surg. 2008 Feb;14(1):55-9. | PubMed | Torella M, De Santo LS, Della Corte A, Esposito S, Onorati F, Nappi G, et al. Extensive retroperitoneal fibrosis with duodenal and ureteral obstruction associated with giant inflammatory aneurysm of the abdominal aorta. Tex Heart Inst J. 2003;30(4):311-3. | PubMed | PMC |
Torella M, De Santo LS, Della Corte A, Esposito S, Onorati F, Nappi G, et al. Extensive retroperitoneal fibrosis with duodenal and ureteral obstruction associated with giant inflammatory aneurysm of the abdominal aorta. Tex Heart Inst J. 2003;30(4):311-3. | PubMed | PMC |