Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso Te¾rico y Seminarios de OncologĒa Bßsica, organizado por el Centro de OncologĒa Preventiva de la Universidad de Chile durante los dĒas 3 de abril y 7 de agosto de 2002.
Editor CientĒfico: Dr. Josķ Manuel Ojeda.
El cßncer de pulm¾n da cuenta de 170.000 nuevos casos cada a±o. Menos del 15% de los pacientes sobrevivirßn a esta enfermedad (1), a pesar de la tecnologĒa refinada en la cirugĒa y avances en radioterapia y quimioterapia.
Los cßnceres de pulm¾n son divididos, seg·n la anatomĒa patol¾gica, en cuatro variedades que incluyen: cßncer no cķlulas peque±as (NSCLC) con tres subtipos: adenocarcinoma, cßncer de cķlulas escamosas y cßncer indiferenciado de cķlulas grandes, y cßncer indiferenciado de cķlulas peque±as (SCLC).
Los pacientes con NSCLC en etapas tempranas son tratados con cirugĒa y los de etapas tardĒas con radioterapia y/o quimioterapia. La sobrevida a dos a±os para pacientes en Estadio III es de 20% y 5% en Estadio IV. Las cifras de sobrevida han permanecido sin cambios por muchos a±os. La identificaci¾n de nuevas terapias menos t¾xicas es fundamental para mejorar las actuales estrategias de tratamiento y el desarrollo de estas nuevas terapias dependerß de la biologĒa molecular de estos tumores. Numerosos estudios indican que el mecanismo de muerte celular inducido por radioterapia y quimioterapia es la apoptosis. Muchos de los genes implicados en la apoptosis han sido identificados y muchos estßn mutados o alterados. Muchos tumores resistentes a la radio y quimioterapia tambiķn son resistentes a la apoptosis en cultivos in vitro. En los a±os recientes ha quedado claro que el cßncer es causado por mutaciones de DNA que ocurren secuencialmente en el tiempo.
La patogķnesis molecular del SCLC y NSCLC es diferente (2). Algunas de estas alteraciones pueden servir de blanco para nuevos agentes de terapia. Ellas son:
Esta clasificaci¾n es artificial ya que existe sobreposici¾n en muchos aspectos de estas terapias.
Los principales componentes de la vĒa de se±ales de la cķlula, tales como proteĒna tirosin kinasa (PTKs), proteĒna kinasa C (PKC) y los sistemas de proteĒna kinasa activada por ras(MAPK), estßn alterados en las cķlulas de cßncer de pulm¾n por oncogenes, ya sea por sobreexpresi¾n o mutaci¾n, llevando a una desrregulaci¾n en las se±ales celulares y la proliferaci¾n celular.
PTKs
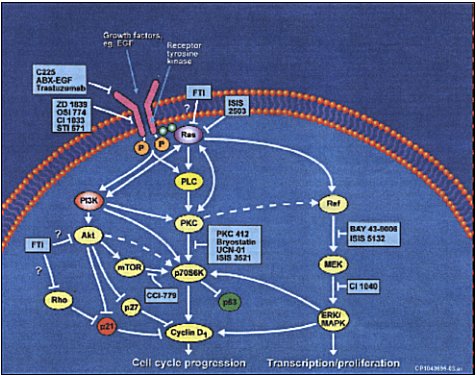
PTKs es una gran familia de oncogenes dominantes. Los dos mayores grupos son: receptor tirosin kinasa y no receptor tirosin kinasa. Los receptores tirosin kinasa (RTKs) son glicoproteĒnas, la uni¾n del ligando a RTKs induce oligodimerizaci¾n del receptor, autofosforilßndose. Posteriormente ocurren cambios conformacionales, uniones y activaci¾n de molķculas rĒo abajo, tales como fosfolipasa C (PLC), kinasa 3 fosfoinosititida (PI3K) y ras (Figura 1).
Figura 1. Cambios conformacionales.
La actividad de los RTKs estß controlada en cķlulas normales en reposo. En tumores malignos, genes que codifican para estos receptores escapan de los mecanismos intracelulares regulatorios.
Los RTKs han sido organizados en familias. Las variadas subfamilias incluyen los receptores del factor de crecimiento epidermal (EGFR), factor de crecimiento derivado de las plaquetas (PDGF), VEGF, factor de crecimiento de fibroblastos y factor de crecimiento del hepatocito.
EGFR difiere de los otros RTKs en que es codificada en el cromosoma 7p11 a 13. Otros tres miembros de esta familia, HER2, HER3 y HER4 (llamados tambiķn erbB2, erbB3, erbB4) son conocidos. Miembros de la familia de EGFR y sus ligandos son sobreexpresados o expresados de forma autocrina en un gran n·mero de tipos tumorales, incluyendo cßncer pancreßtico, pulm¾n, ovario, renal, gßstrico, hepatocelular y mama. EGFR sirve como receptor predominante para m·ltiples distintos ligandos incluyendo EGF, factor transformante de crecimiento alfa, anfirregulina y el factor de crecimiento que une heparina. La mayor funci¾n de estos otros receptores parece estar en los efectores rĒo abajo de cada uno de ķstos, fosforilan y modulan las se±ales de cada uno de los otros pares especĒficos. La uni¾n de un ligando, produce dimerizaci¾n y la subsecuente fosforilaci¾n de proteĒnas traduciendo proliferaci¾n celular y se±ales de sobrevida a travķs de ras/MAPK y PI3K/Akt (4)
Cetuximab(C225) y ABX-EGF: Uno de los agentes es el mAb quimķrico rat¾n-humano 225 (C225). Inhibe completamente la activaci¾n de EGF-RTK, causando una detenci¾n del ciclo celular en G1 produciendo un aumento de los niveles de p27KIP1 y la inhibici¾n de la actividad de la ciclina dependiente de kinasa (cdk2) (5). C225 mostr¾ actividad sinķrgica antitumoral con agentes como cisplatino, doxorrubicina, topotecßn y paclitaxel. Estudios fase I han establecido la seguridad de la administraci¾n. Datos de estudios Fase II indican que la actividad antitumoral estß aumentada al usarse en combinaci¾n con quimioterapia.
ABX-EGF: es una inmunoglobulina humanizada mAb que se une especĒficamente a EGFR humano con alta afinidad. Los modelos de estudio tumoral demuestran una erradicaci¾n completa de grandes tumores. No hay efecto en tumores EGFR negativos.
Trastuzumab y una vacuna peptĒdica quimķrica MVF-HER2 cķlula B (628-647): el protooncogen HER2/neu codifica la glicoproteĒna receptor transmembrana 185Kd (p185) con actividad intrĒnseca tirosin kinasa. Cuando la proteĒna HER2/neu estß activa, puede interactuar con muchas proteĒnas diferentes tales como PLC y la vĒa ras/MAPK (6).
Estß sobreexpresada en aproximadamente 30% de los NSCLC, predominantemente en adenocarcinoma y tambiķn en SCLC. Se ha relacionado con sobrevida mßs corta en SCLC avanzado.
La angiogķnesis estß tambiķn implicada como mecanismo de agresi¾n inducido por HER2/neu porque la sobreexpresi¾n de p185 resulta en una expresi¾n aumentada del mRNA de VEGF con inducci¾n y mejoramiento de la secreci¾n de VEGF. Dando un aumento en la propensi¾n de metßstasis a distancia y ademßs un aumento de la secreci¾n de metaloproteinasas (7).
Estudios recientes han indicado que la sobreexpresi¾n de p185 estß asociada con aumento en la resistencia a una amplia variedad de quimioterßpicos, incluyendo: cisplatino, etop¾sido, doxorrubicina y placlitaxel (8).
Trastuzumab: es un anticuerpo monoclonal recombinante humanizado contra el receptor HER2, con actividad demostrada en cßncer de mama metastßsico. En cķlulas cultivadas que expresan altos niveles de HER2, trastuzumab causa una detenci¾n del crecimiento en GoG1 del ciclo celular.
En lĒneas celulares de cßncer de pulm¾n, la inhibici¾n ocurri¾ s¾lo en lĒneas celulares con la expresi¾n de HER2/neu (9). Estos datos sugieren que el tratamiento de cķlulas que sobreexpresan HER2 es antiproliferativo y la citostasis puede resultar de la inhibici¾n de la progresi¾n del ciclo celular. Anticuerpos anti HER2 tambiķn median la citotoxicidad dependiente de complemento y/o citotoxicidad celular dependiente de anticuerpos. En estudios preclĒnicos precoces, Slamon et al demostraron interacciones entre trastuzumab y los agentes anticancerĒgenos. La interacci¾n sinķrgica de trastuzumab con los agentes alquilantes, anßlogos de platino e inhibidores de topoisomerasa II asĒ como la interacci¾n aditiva con taxanos, antraciclinas y algunos antimetabolitos en cķlulas de cßncer de mama con sobreexpresi¾n de HER2/neu, guiaron a estudios clĒnicos. Aunque datos preclĒnicos muestran una inhibici¾n aditiva de lĒneas celulares de cßncer de pulm¾n que sobreexpresan HER2/neu con la combinaci¾n de trastuzumab y otros agentes citot¾xicos, los resultados de la combinaci¾n de quimioterapia con trastuzumab en pacientes con NSCLC cuyos tumores sobreexpresan HER2/neu son desalentadores. Esto se puede relacionar con el grado de expresi¾n de HER2/neu en NSCLC y la heterogenicidad de su expresi¾n en los pacientes tratados.
Induce inmunidad activa, sin embargo, no es claro si los humanos pueden montar una respuesta inmune efectiva con estrategias de vacuna basadas en proteĒnas o cķlulas, porque HER2 es un antĒgeno propio no mutado. Ademßs, algunos anticuerpos estimulan mßs que inhiben el crecimiento de tumores humanos y las vacunas HER2 presentan m·ltiples epĒtopes que podrĒan dar una respuesta humoral contraproducente.
MVF-HER2(628-647): Es una vacuna pķptido quimķrico cķlulas B que incorpora epĒtope del linfocito T helper dando altos tĒtulos de anticuerpos a HER2 (10). Estos anticuerpos obtenidos tuvieron una actividad antitumoral in vitro y previnieron el desarrollo tumoral in vivo.

 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Este texto completo es la transcripci¾n editada y revisada de una conferencia dictada en el Curso Te¾rico y Seminarios de OncologĒa Bßsica, organizado por el Centro de OncologĒa Preventiva de la Universidad de Chile durante los dĒas 3 de abril y 7 de agosto de 2002.
Editor CientĒfico: Dr. Josķ Manuel Ojeda.
 Expositora:
Elsa Cabrera Acosta[1]
Expositora:
Elsa Cabrera Acosta[1]

Citaci¾n: Cabrera E. New therapies in lung cancer I. Medwave 2002 Dic;2(11):e3501 doi: 10.5867/medwave.2002.11.3501
Fecha de publicaci¾n: 1/12/2002

Nos complace que usted tenga interķs en comentar uno de nuestros artĒculos. Su comentario serß publicado inmediatamente. No obstante, Medwave se reserva el derecho a eliminarlo posteriormente si la direcci¾n editorial considera que su comentario es: ofensivo en alg·n sentido, irrelevante, trivial, contiene errores de lenguaje, contiene arengas polĒticas, obedece a fines comerciales, contiene datos de alguna persona en particular, o sugiere cambios en el manejo de pacientes que no hayan sido publicados previamente en alguna revista con revisi¾n por pares.
A·n no hay comentarios en este artĒculo.
Para comentar debe iniciar sesi¾n