Resumen
INTRODUCCIÓN
Es común que los pacientes en estado terminal tengan una reducida ingesta de líquidos, lo que muchas veces repercute en una necesidad de mayor apoyo médico. Sin embargo, no está claro si esta medida tiene un impacto clínico real.
MÉTODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios y preparamos una tabla de resumen de los resultados utilizando el método GRADE.
RESULTADOS Y CONCLUSIONES
Concluimos que la administración de hidratación parenteral podría hacer poca o ninguna diferencia en la sobrevida y en la calidad de vida de los pacientes oncológicos terminales, y que no está claro si tiene algún otro beneficio porque la certeza de la evidencia es muy baja.
Problema
La ingesta reducida de líquidos en pacientes con cáncer en etapa terminal constituye un evento frecuente. Puede ser atribuida a diferentes factores, algunos propios de la enfermedad (por ejemplo, obstrucción por neoplasia) como a náuseas o debilidad generalizada. Por lo mismo, es común que estos pacientes desarrollen signos clínicos de deshidratación.
Se desconoce si la hidratación parenteral en estos pacientes ayuda a prolongar la vida o a disminuir los síntomas, o si acaso conlleva más riesgos que beneficios tales como complicaciones locales en sitio de punción (eritema, edema, dolor), o a nivel sistémico (edema, insuficiencia cardiaca congestiva, etc).
Metodos
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas y reanalizamos los datos de los estudios primarios. Con esta información, generamos un resumen estructurado denominado FRISBEE (Friendly Summaries of Body of Evidence using Epistemonikos), siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios cuando sea posible, una tabla de resumen de resultados con el método GRADE y una sección de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
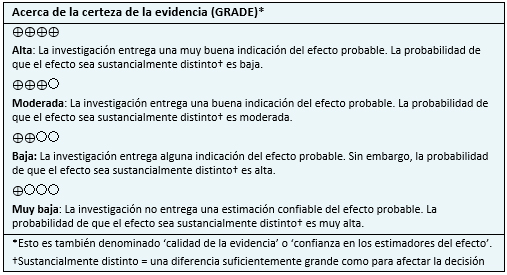
Acerca del conjunto de evidencia para esta pregunta
|
Cuál es la evidencia |
Encontramos cuatro revisiones sistemáticas [1],[2],[3],[4] que |
|
Qué tipo de pacientes incluyeron los estudios* |
Todos los ensayos incluyeron pacientes con cáncer terminal, deshidratación clínica e ingesta reducida de líquidos. Dos ensayos [5],[6] incluyeron pacientes mayores de 18 años y el ensayo restante [7] no lo especificó. |
|
Qué tipo de intervenciones incluyeron los estudios* |
Dos ensayos [5],[6] evaluaron hidratación parenteral con solución salina (1 litro) SC versus placebo (definido como solución salina 100 cc SC). Un ensayo [7] evaluó hidratación parenteral con dextrosa 5% + 140 mEq/L NaCl SC versus ninguna intervención. |
|
Qué tipo de desenlaces midieron |
Los ensayos midieron múltiples desenlaces, pero las revisiones sistemáticas identificadas los agruparon de la siguiente manera: signos clínicos de deshidratación, sed, delirium, sobrevida, calidad de vida y complicaciones. |
* La información sobre los estudios primarios es extraída desde las revisiones sistemáticas identificadas, no directamente desde los estudios, a menos que se especifique lo contrario.
Cuál es la evidencia
Resumen de los resultados
La información sobre los efectos de la hidratación parenteral está basada en tres ensayos aleatorizados [5],[6],[7] que incluyen 230 pacientes.
Dos ensayos [5],[6] reportaron el desenlace deshidratación clínica (definida como los síntomas: fatiga, mioclonías, sedación, alucinaciones) (180 pacientes). Un ensayo [7] midió el desenlace sed (50 pacientes). Dos ensayos [5],[7] (179 pacientes) evaluaron el desenlace delirium (de acuerdo a Memorial Delirium Assessment Scale o MDAS) , un ensayo [5] (129 pacientes) midió el desenlace sobrevida (a 17 días) y calidad de vida (de acuerdo a scores FACIT-F y FACIT-G). Dos ensayos [6],[7] (101 pacientes) midieron el desenlace efectos adversos locales del sitio de punción (dolor, edema).
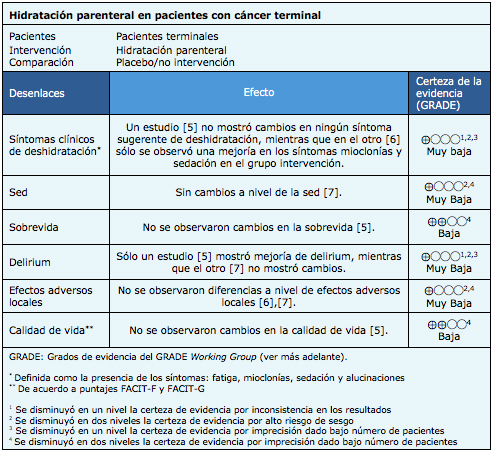
El resumen de los resultados es el siguiente:
- No está claro si la hidratación parenteral tiene algún beneficio sobre los síntomas clínicos de deshidratación en pacientes oncológicos terminales, porque la certeza de la evidencia es muy baja.
- No está claro si la hidratación parenteral disminuye la sed en pacientes oncológicos terminales, porque la certeza de la evidencia es muy baja
- La hidratación parenteral podría tener poco o ningún efecto en la sobrevida de los pacientes oncológicos terminales, pero la certeza de la evidencia es baja.
- No está claro si la hidratación parenteral previene el delirium en pacientes oncológicos terminales, porque la certeza de la evidencia es muy baja
- No está claro si la hidratación parenteral conlleva mayores efectos adversos locales en pacientes oncológicos terminales, porque la certeza de la evidencia es muy baja
- La hidratación parenteral podría hacer poca o ninguna diferencia en la calidad de vida de pacientes oncológicos terminales, pero la certeza de la evidencia es baja.
Otras consideraciones para la toma de decisión
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Consideraciones de recursos |
|
| Qué piensan los pacientes y sus tratantes |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Cómo realizamos este resumen
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
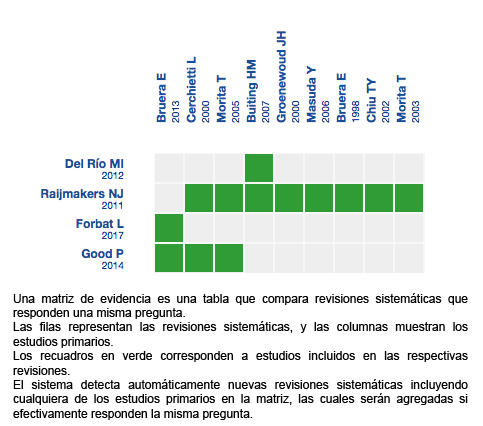
Siga el enlace para acceder a la versión interactiva: Hidratación parenteral en pacientes terminales
Notas
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en la página web de Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más precoz.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta.
Este artículo es parte del proyecto síntesis de evidencia de Epistemonikos. Se elabora con una metodología preestablecida, siguiendo rigurosos estándares metodológicos y proceso de revisión por pares interno. Cada uno de estos artículos corresponde a un resumen, denominado FRISBEE (Friendly Summary of Body of Evidence using Epistemonikos), cuyo principal objetivo es sintetizar el conjunto de evidencia de una pregunta específica, en un formato amigable a los profesionales clínicos. Sus principales recursos se basan en la matriz de evidencia de Epistemonikos y análisis de resultados usando metodología GRADE. Mayores detalles de los métodos para elaborar este FRISBEE están descritos aquí (http://dx.doi.org/10.5867/medwave.2014.06.5997)
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

INTRODUCCIÓN
Es común que los pacientes en estado terminal tengan una reducida ingesta de líquidos, lo que muchas veces repercute en una necesidad de mayor apoyo médico. Sin embargo, no está claro si esta medida tiene un impacto clínico real.
MÉTODOS
Para responder esta pregunta utilizamos Epistemonikos, la mayor base de datos de revisiones sistemáticas en salud, la cual es mantenida mediante búsquedas en múltiples fuentes de información, incluyendo MEDLINE, EMBASE, Cochrane, entre otras. Extrajimos los datos desde las revisiones identificadas, reanalizamos los datos de los estudios primarios y preparamos una tabla de resumen de los resultados utilizando el método GRADE.
RESULTADOS Y CONCLUSIONES
Concluimos que la administración de hidratación parenteral podría hacer poca o ninguna diferencia en la sobrevida y en la calidad de vida de los pacientes oncológicos terminales, y que no está claro si tiene algún otro beneficio porque la certeza de la evidencia es muy baja.
 Authors:
José Canihuante[1,2], Pedro Pérez[2,3]
Authors:
José Canihuante[1,2], Pedro Pérez[2,3]
Affiliation:
[1] Facultad de Medicina, Pontificia Universidad Católica de Chile, Santiago, Chile
[2] Proyecto Epistemonikos, Santiago, Chile
[3] Departamento de Medicina Interna, Facultad de Medicina, Pontificia Universidad Católica de Chile, Santiago, Chile
E-mail: peperezc@gmail.com
Author address:
[1] Centro Evidencia UC Pontificia Universidad Católica de Chile Centro de Innovación UC Anacleto Angelini Avda.Vicuńa Mackenna 4860 Macul Santiago Chile

Citation: Canihuante J, Pérez P. Is parenteral hydration beneficial in terminally ill cancer patients?. Medwave 2018 Ene-Feb;18(1):e7149 doi: 10.5867/medwave.2018.01.7149
Submission date: 23/11/2017
Acceptance date: 20/12/2017
Publication date: 12/2/2018
Origin: This article is a product of the Evidence Synthesis Project of Epistemonikos Fundation, in collaboration with Medwave for its publication.
Type of review: Non-blinded peer review by members of the methodological team of Epistemonikos Evidence Synthesis Project.

Comments (0)
We are pleased to have your comment on one of our articles. Your comment will be published as soon as it is posted. However, Medwave reserves the right to remove it later if the editors consider your comment to be: offensive in some sense, irrelevant, trivial, contains grammatical mistakes, contains political harangues, appears to be advertising, contains data from a particular person or suggests the need for changes in practice in terms of diagnostic, preventive or therapeutic interventions, if that evidence has not previously been published in a peer-reviewed journal.
No comments on this article.
To comment please log in
 Medwave provides HTML and PDF download counts as well as other harvested interaction metrics.
Medwave provides HTML and PDF download counts as well as other harvested interaction metrics. There may be a 48-hour delay for most recent metrics to be posted.

- Raijmakers NJ, van Zuylen L, Costantini M, Caraceni A, Clark J, Lundquist G, Voltz R, Ellershaw JE, van der Heide A; OPCARE9. Artificial nutrition and hydration in the last week of life in cancer patients. A systematic literatura review of practices and effects. Ann Oncol. 2011 Jul;22(7):1478-86. | CrossRef | PubMed |
- Good P, Richard R, Syrmis W, Jenkins-Marsh S, Stephens J. Medically assisted hydration for adult palliative care patients. Cochrane Database Syst Rev. 2014 Apr 23;(4):CD006273. | CrossRef | PubMed |
- Del Río MI, Shand B, Bonati P, Palma A, Maldonado A, Taboada P, Nervi F. Hydration and nutrition at the end of life: a systematic review of emotional impact, perceptions, and decision-making among patients, family, and health care staff. Psychooncology. 2012 Sep;21(9):913-21. | CrossRef | PubMed |
- Forbat L, Kunicki N, Chapman M, Lovell C. How and why are subcutaneous fluids administered in an advanced illness population: a systematic review. J Clin Nurs. 2017 May;26(9-10):1204-1216. | CrossRef | PubMed |
- Bruera E, Hui D, Dalal S, Torres-Vigil I, Trumble J, Roosth J, Krauter S, Strickland C, Unger K, Palmer JL, Allo J, Frisbee-Hume S, Tarleton K. Parenteral hydration in patients with advanced cancer: a multicenter, double-blind, placebo-controlled randomized trial. J Clin Oncol. 2013 Jan 1;31(1):111-8. | CrossRef | PubMed | PMC |
- Bruera E, Sala R, Rico MA, Moyano J, Centeno C, Willey J, Palmer JL. Effects of parenteral hydration in terminally ill cancer patients: a preliminary study. J Clin Oncol. 2005 Apr 1;23(10):2366-71. | PubMed |
- Cerchietti L, Navigante A, Sauri A, Palazzo F. Hypodermoclysis for control of dehydration in terminal-stage cancer. Int J Palliat Nurs. 2000 Sep;6(8):370-4. | PubMed |
- Bosshard G, Nilstun T, Bilsen J, Norup M, Miccinesi G, van Delden JJ, Faisst K, van der Heide A; European End-of-Life Consortium. Forgoing treatment at the end of life in 6 European countries. Arch Intern Med. 2005 Feb 28;165(4):401-7. | PubMed |
- Bruera E, Belzile M, Watanabe S, Fainsinger RL. Volume of hydration in terminal cancer patients. Support Care Cancer. 1996 Mar;4(2):147-50. | PubMed |
- Bruera E, Pruvost M, Schoeller T, Montejo G, Watanabe S. Proctoclysis for hydration of terminally ill cancer patients. J Pain Symptom Manage. 1998 Apr;15(4):216-9. | PubMed |
- Buiting HM, van Delden JJ, Rietjens JA, Onwuteaka-Philipsen BD, Bilsen J, Fischer S, Löfmark R, Miccinesi G, Norup M, van der Heide A; EURELD-Consortium. Forgoing artificial nutrition or hydration in patients nearing death in six European countries. J Pain Symptom Manage. 2007 Sep;34(3):305-14. Epub 2007 Jul 2. | PubMed |
- Byron E, Gastmans C, Diercks de Casterlé B. Decisionmaking about artificial feeding in end-of-life care: literatura review. J Adv Nurs 2008;63:2–14.
- Chiu TY, Hu WY, Chuang RB, Chen CY. Nutrition and hydration for terminal cancer patients in Taiwan. Support Care Cancer. 2002 Nov;10(8):630-6. Epub 2002 Sep 18. | PubMed |
- Chiu TY, Hu WY, Chuang RB, Cheng YR, Chen CY, Wakai S. Terminal cancer patients' wishes and influencing factors toward the provision of artificial nutrition and hydration in Taiwan. J Pain Symptom Manage. 2004 Mar;27(3):206-14. | PubMed |
- Claisse L, Grosshans C & Passadori Y (2005) The use of hypodermoclysis in palliative care. European Journal of Palliative Care 12, 243–246.
- Dasgupta M, Binns MA, Rochon PA. Subcutaneous fluid infusion in a long-term care setting. J Am Geriatr Soc. 2000 Jul;48(7):795-9. | PubMed |
- Fainsinger RL, MacEachern T, Miller MJ, Bruera E, Spachynski K, Kuehn N, Hanson J. The use of hypodermoclysis for rehydration in terminally ill cancer patients. J Pain Symptom Manage. 1994 Jul;9(5):298-302. | PubMed |
- Fins JJ, Miller FG, Acres CA, Bacchetta MD, Huzzard LL, Rapkin BD. End-of-life decision-making in the hospital: current practice and future prospects. J Pain Symptom Manage. 1999 Jan;17(1):6-15. | PubMed |
- Gonçalves JF, Alvarenga M, Silva A. The last forty-eight hours of life in a Portuguese palliative care unit: does it differ from elsewhere? J Palliat Med. 2003 Dec;6(6):895-900. | PubMed |
- Groenewoud JH, van der Heide A, Kester JG, de Graaff CL, van der Wal G, van der Maas PJ. A nationwide study of decisions to forego life-prolonging treatment in Dutch medical practice. Arch Intern Med. 2000 Feb 14;160(3):357-63. | PubMed |
- Hanson LC, Garrett JM, Lewis C, Phifer N, Jackman A, Carey TS. Physicians' expectations of benefit from tube feeding. J Palliat Med. 2008 Oct;11(8):1130-4. | CrossRef | PubMed | PMC |
- Hawkins C. Anorexia and anxiety in advanced malignancy: the relative problem. J Hum Nutr Diet 2000;13:113–117.
- Holden CM. Anorexia in the terminally ill cancer patient: the emotional impact on the patient and the family. Hosp J. 1991;7(3):73-84. | PubMed |
- Lanuke K, Fainsinger RL. Hydration management in palliative care settings--a survey of experts. J Palliat Care. 2003 Winter;19(4):278-9. | PubMed |
- Lanuke K, Fainsinger RL, DeMoissac D. Hydration management at the end of life. J Palliat Med. 2004 Apr;7(2):257-63. | PubMed |
- Ke LS, Chiu TY, Lo SS, Hu WY. Knowledge, attitudes, and behavioral intentions of nurses toward providing artificial nutrition and hydration for terminal cáncer patients in Taiwan. Cancer Nurs. 2008 Jan-Feb;31(1):67-76. | CrossRef | PubMed |
- Masuda Y, Noguchi H, Kuzuya M, Inoue A, Hirakawa Y, Iguchi A, Uemura K. Comparison of medical treatments for the dying in a hospice and a geriatric hospital in Japan. J Palliat Med. 2006 Feb;9(1):152-60. | PubMed |
- McClement SE, Degner LF, Harlos MS. Family beliefs regarding the nutritional care of a terminally ill relative: a qualitative study. J Palliat Med. 2003 Oct;6(5):737-48. | PubMed |
- McClement SE, Degner LF, Harlos M. Family responses to declining intake and weight loss in a terminally ill relative. Part 1: fighting back. J Palliat Care. 2004 Summer;20(2):93-100. | PubMed |
- Meares CJ. Primary caregiver perceptions of intake cessation in patients who are terminally Ill. Oncol Nurs Forum. 1997 Nov-Dec;24(10):1751-7. | PubMed |
- Mercadante S, Ferrera P, Girelli D, Casuccio A. Patients' and relatives' perceptions about intravenous and subcutaneous hydration. J Pain Symptom Manage. 2005 Oct;30(4):354-8. | PubMed |
- Miyashita M, Morita T, Shima Y, Kimura R, Takahashi M, Adachi I. Nurse views of the adequacy of decision making and nurse distress regarding artificial hydration for terminally ill cancer patients: a nationwide survey. Am J Hosp Palliat Care. 2007 Dec-2008 Jan;24(6):463-9. Epub 2007 Jun 29. | PubMed |
- Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Association between hydration volume and symptoms in terminally ill cáncer patients with abdominal malignancies. Ann Oncol. 2005 Apr;16(4):640-7. Epub 2005 Jan 31. | PubMed |
- Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Artificial hydration therapy, laboratory findings, and fluid balance in terminally ill patients with abdominal malignancies. J Pain Symptom Manage. 2006 Feb;31(2):130-9. | PubMed |
- Morita T, Tei Y, Inoue S. Agitated terminal delirium and association with partial opioid substitution and hydration. J Palliat Med. 2003 Aug;6(4):557-63. | PubMed |
- Morita T, Shima Y, Adachi I; Japan Palliative Oncology Study Group. Attitudes of Japanese physicians toward terminal dehydration: a nationwide survey. J Clin Oncol. 2002 Dec 15;20(24):4699-704. | PubMed |
- Morita T, Tsunoda J, Inoue S, Chihara S. Perceptions and decision-making on rehydration of terminally ill cancer patients and family members. Am J Hosp Palliat Care. 1999 May-Jun;16(3):509-16. | PubMed |
- Musgrave CF, Bartal N, Opstad J. Intravenous hydration for terminal patients: what are the attitudes of Israeli terminal patients, their families, and their health professionals? J Pain Symptom Manage. 1996 Jul;12(1):47-51. | PubMed |
- Oh DY, Kim JH, Lee SH, Kim DW, Im SA, Kim TY, Heo DS, Bang YJ, Kim NK. Artificial nutrition and hydration in terminal cancer patients: the real and the ideal. Support Care Cancer. 2007 Jun;15(6):631-6. Epub 2006 Nov 11. | PubMed |
- Oi-Ling K, Man-Wah DT, Kam-Hung DN. Symptom distress as rated by advanced cancer patients, caregivers and physicians in the last week of life. Palliat Med. 2005 Apr;19(3):228-33. | PubMed |
- Orrevall Y, Tishelman C, Herrington MK, Permert J. The path from oral nutrition to home parenteral nutrition: a qualitative interview study of the experiences of advanced cancer patients and their families. Clin Nutr. 2004Dec;23(6):1280-7. | PubMed |
- Parkash R, Burge F. The family's perspective on issues of hydration in terminal care. J Palliat Care. 1997 Winter;13(4):23-7. | PubMed |
- Roeline H, Pasman W, Mei The A, Onwuteaka-Philipsen B, Ribbe M, Van der Wal G. Participants in the decisión making on artificial nutrition and hydration to demented nursing home patients: a qualitative study. J Aging Stud 2004;18:321–335.
- Poole K, Froggatt K. Loss of weight and loss of appetite in advanced cancer: a problem for the patient, the carer, or the health professional? Palliat Med. 2002 Nov;16(6):499-506. | PubMed |
- Sato K, Miyashita M, Morita T, Sanjo M, Shima Y, Uchitomi Y. Quality of end-of-life treatment for cancer patients in general wards and the palliative care unit at a regional cancer center in Japan: a retrospective chart review. Support Care Cancer. 2008 Feb;16(2):113-22. Epub 2007 Oct 5. | PubMed |
- Shega JW, Hougham GW, Cox-Hayley D, Sachs GA, Stocking CB. Advanced dementia and feeding tubes: do physician factors contribute to state variation? J Am Geriatr Soc. 2004 Jul;52(7):1217-8. | PubMed |
- Shega JW, Hougham GW, Stocking CB, Cox-Hayley D, Sachs GA. Barriers to limiting the practice of feeding tube placement in advanced dementia. J Palliat Med. 2003 Dec;6(6):885-93. | PubMed |
- Shragge JE, Wismer WV, Olson KL, Baracos VE. Shifting to conscious control: psychosocial and dietary management of anorexia by patients with advanced cancer. Palliat Med. 2007 Apr;21(3):227-33. | PubMed |
- Sprung CL, Maia P, Bulow HH, Ricou B, Armaganidis A, Baras M, Wennberg E, Reinhart K, Cohen SL, Fries DR, Nakos G, Thijs LG; Ethicus Study Group. The importance of religious affiliation and culture on end-of-life decisions in European intensive care units. Intensive Care Med. 2007 Oct;33(10):1732-9. Erratum in: Intensive Care Med. 2007 Oct;33(10):1859. | PubMed |
- Strasser F, Binswanger J, Cerny T, Kesselring A. Fighting a losing battle: eating-related distress of men with advanced cancer and their female partners. A mixed-methods study. Palliat Med. 2007 Mar;21(2):129-37. | PubMed |
- van der Riet P, Good P, Higgins I, Sneesby L. Palliative care professionals' perceptions of nutrition and hydration at the end of life. Int J Palliat Nurs. 2008 Mar;14(3):145-51. | PubMed |
- van Wigcheren PT, Onwuteaka-Philipsen BD, Pasman HR, Ooms ME, Ribbe MW, van der Wal G. Starting artificial nutrition and hydration in patients with dementia in The Netherlands: frequencies, patient characteristics and decision-making process. Aging Clin Exp Res. 2007 Feb;19(1):26-33. | PubMed |
- Viola RA. Studying Fluid Status and the Dying: The Challenge of Clinical Research in Palliative Care [MSc thesis]. Canada: University of Ottawa, 1997.
- Waller A, Hershkowitz M, Adunsky A. The effect of intravenous fluid infusion on blood and urine parameters of hydration and on state of consciousness in terminal cancer patients. Am J Hosp Palliat Care. 1994 Nov-Dec;11(6):22-7. | PubMed |
- Worobec G, Brown MK. Hypodermoclysis therapy. In a chronic care hospital setting. J Gerontol Nurs. 1997 Jun;23(6):23-8. | PubMed |
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Palliative Care 2017 [cited November 12, 2017].
 Raijmakers NJ, van Zuylen L, Costantini M, Caraceni A, Clark J, Lundquist G, Voltz R, Ellershaw JE, van der Heide A; OPCARE9. Artificial nutrition and hydration in the last week of life in cancer patients. A systematic literatura review of practices and effects. Ann Oncol. 2011 Jul;22(7):1478-86. | CrossRef | PubMed |
Raijmakers NJ, van Zuylen L, Costantini M, Caraceni A, Clark J, Lundquist G, Voltz R, Ellershaw JE, van der Heide A; OPCARE9. Artificial nutrition and hydration in the last week of life in cancer patients. A systematic literatura review of practices and effects. Ann Oncol. 2011 Jul;22(7):1478-86. | CrossRef | PubMed | Good P, Richard R, Syrmis W, Jenkins-Marsh S, Stephens J. Medically assisted hydration for adult palliative care patients. Cochrane Database Syst Rev. 2014 Apr 23;(4):CD006273. | CrossRef | PubMed |
Good P, Richard R, Syrmis W, Jenkins-Marsh S, Stephens J. Medically assisted hydration for adult palliative care patients. Cochrane Database Syst Rev. 2014 Apr 23;(4):CD006273. | CrossRef | PubMed | Del Río MI, Shand B, Bonati P, Palma A, Maldonado A, Taboada P, Nervi F. Hydration and nutrition at the end of life: a systematic review of emotional impact, perceptions, and decision-making among patients, family, and health care staff. Psychooncology. 2012 Sep;21(9):913-21. | CrossRef | PubMed |
Del Río MI, Shand B, Bonati P, Palma A, Maldonado A, Taboada P, Nervi F. Hydration and nutrition at the end of life: a systematic review of emotional impact, perceptions, and decision-making among patients, family, and health care staff. Psychooncology. 2012 Sep;21(9):913-21. | CrossRef | PubMed | Forbat L, Kunicki N, Chapman M, Lovell C. How and why are subcutaneous fluids administered in an advanced illness population: a systematic review. J Clin Nurs. 2017 May;26(9-10):1204-1216. | CrossRef | PubMed |
Forbat L, Kunicki N, Chapman M, Lovell C. How and why are subcutaneous fluids administered in an advanced illness population: a systematic review. J Clin Nurs. 2017 May;26(9-10):1204-1216. | CrossRef | PubMed | Bruera E, Hui D, Dalal S, Torres-Vigil I, Trumble J, Roosth J, Krauter S, Strickland C, Unger K, Palmer JL, Allo J, Frisbee-Hume S, Tarleton K. Parenteral hydration in patients with advanced cancer: a multicenter, double-blind, placebo-controlled randomized trial. J Clin Oncol. 2013 Jan 1;31(1):111-8. | CrossRef | PubMed | PMC |
Bruera E, Hui D, Dalal S, Torres-Vigil I, Trumble J, Roosth J, Krauter S, Strickland C, Unger K, Palmer JL, Allo J, Frisbee-Hume S, Tarleton K. Parenteral hydration in patients with advanced cancer: a multicenter, double-blind, placebo-controlled randomized trial. J Clin Oncol. 2013 Jan 1;31(1):111-8. | CrossRef | PubMed | PMC | Bruera E, Sala R, Rico MA, Moyano J, Centeno C, Willey J, Palmer JL. Effects of parenteral hydration in terminally ill cancer patients: a preliminary study. J Clin Oncol. 2005 Apr 1;23(10):2366-71. | PubMed |
Bruera E, Sala R, Rico MA, Moyano J, Centeno C, Willey J, Palmer JL. Effects of parenteral hydration in terminally ill cancer patients: a preliminary study. J Clin Oncol. 2005 Apr 1;23(10):2366-71. | PubMed | Cerchietti L, Navigante A, Sauri A, Palazzo F. Hypodermoclysis for control of dehydration in terminal-stage cancer. Int J Palliat Nurs. 2000 Sep;6(8):370-4. | PubMed |
Cerchietti L, Navigante A, Sauri A, Palazzo F. Hypodermoclysis for control of dehydration in terminal-stage cancer. Int J Palliat Nurs. 2000 Sep;6(8):370-4. | PubMed | Bosshard G, Nilstun T, Bilsen J, Norup M, Miccinesi G, van Delden JJ, Faisst K, van der Heide A; European End-of-Life Consortium. Forgoing treatment at the end of life in 6 European countries. Arch Intern Med. 2005 Feb 28;165(4):401-7. | PubMed |
Bosshard G, Nilstun T, Bilsen J, Norup M, Miccinesi G, van Delden JJ, Faisst K, van der Heide A; European End-of-Life Consortium. Forgoing treatment at the end of life in 6 European countries. Arch Intern Med. 2005 Feb 28;165(4):401-7. | PubMed | Bruera E, Belzile M, Watanabe S, Fainsinger RL. Volume of hydration in terminal cancer patients. Support Care Cancer. 1996 Mar;4(2):147-50. | PubMed |
Bruera E, Belzile M, Watanabe S, Fainsinger RL. Volume of hydration in terminal cancer patients. Support Care Cancer. 1996 Mar;4(2):147-50. | PubMed | Bruera E, Pruvost M, Schoeller T, Montejo G, Watanabe S. Proctoclysis for hydration of terminally ill cancer patients. J Pain Symptom Manage. 1998 Apr;15(4):216-9. | PubMed |
Bruera E, Pruvost M, Schoeller T, Montejo G, Watanabe S. Proctoclysis for hydration of terminally ill cancer patients. J Pain Symptom Manage. 1998 Apr;15(4):216-9. | PubMed | Buiting HM, van Delden JJ, Rietjens JA, Onwuteaka-Philipsen BD, Bilsen J, Fischer S, Löfmark R, Miccinesi G, Norup M, van der Heide A; EURELD-Consortium. Forgoing artificial nutrition or hydration in patients nearing death in six European countries. J Pain Symptom Manage. 2007 Sep;34(3):305-14. Epub 2007 Jul 2. | PubMed |
Buiting HM, van Delden JJ, Rietjens JA, Onwuteaka-Philipsen BD, Bilsen J, Fischer S, Löfmark R, Miccinesi G, Norup M, van der Heide A; EURELD-Consortium. Forgoing artificial nutrition or hydration in patients nearing death in six European countries. J Pain Symptom Manage. 2007 Sep;34(3):305-14. Epub 2007 Jul 2. | PubMed | Byron E, Gastmans C, Diercks de Casterlé B. Decisionmaking about artificial feeding in end-of-life care: literatura review. J Adv Nurs 2008;63:2–14.
Byron E, Gastmans C, Diercks de Casterlé B. Decisionmaking about artificial feeding in end-of-life care: literatura review. J Adv Nurs 2008;63:2–14.  Chiu TY, Hu WY, Chuang RB, Chen CY. Nutrition and hydration for terminal cancer patients in Taiwan. Support Care Cancer. 2002 Nov;10(8):630-6. Epub 2002 Sep 18. | PubMed |
Chiu TY, Hu WY, Chuang RB, Chen CY. Nutrition and hydration for terminal cancer patients in Taiwan. Support Care Cancer. 2002 Nov;10(8):630-6. Epub 2002 Sep 18. | PubMed | Chiu TY, Hu WY, Chuang RB, Cheng YR, Chen CY, Wakai S. Terminal cancer patients' wishes and influencing factors toward the provision of artificial nutrition and hydration in Taiwan. J Pain Symptom Manage. 2004 Mar;27(3):206-14. | PubMed |
Chiu TY, Hu WY, Chuang RB, Cheng YR, Chen CY, Wakai S. Terminal cancer patients' wishes and influencing factors toward the provision of artificial nutrition and hydration in Taiwan. J Pain Symptom Manage. 2004 Mar;27(3):206-14. | PubMed | Claisse L, Grosshans C & Passadori Y (2005) The use of hypodermoclysis in palliative care. European Journal of Palliative Care 12, 243–246.
Claisse L, Grosshans C & Passadori Y (2005) The use of hypodermoclysis in palliative care. European Journal of Palliative Care 12, 243–246.  Dasgupta M, Binns MA, Rochon PA. Subcutaneous fluid infusion in a long-term care setting. J Am Geriatr Soc. 2000 Jul;48(7):795-9. | PubMed |
Dasgupta M, Binns MA, Rochon PA. Subcutaneous fluid infusion in a long-term care setting. J Am Geriatr Soc. 2000 Jul;48(7):795-9. | PubMed | Fainsinger RL, MacEachern T, Miller MJ, Bruera E, Spachynski K, Kuehn N, Hanson J. The use of hypodermoclysis for rehydration in terminally ill cancer patients. J Pain Symptom Manage. 1994 Jul;9(5):298-302. | PubMed |
Fainsinger RL, MacEachern T, Miller MJ, Bruera E, Spachynski K, Kuehn N, Hanson J. The use of hypodermoclysis for rehydration in terminally ill cancer patients. J Pain Symptom Manage. 1994 Jul;9(5):298-302. | PubMed | Fins JJ, Miller FG, Acres CA, Bacchetta MD, Huzzard LL, Rapkin BD. End-of-life decision-making in the hospital: current practice and future prospects. J Pain Symptom Manage. 1999 Jan;17(1):6-15. | PubMed |
Fins JJ, Miller FG, Acres CA, Bacchetta MD, Huzzard LL, Rapkin BD. End-of-life decision-making in the hospital: current practice and future prospects. J Pain Symptom Manage. 1999 Jan;17(1):6-15. | PubMed | Gonçalves JF, Alvarenga M, Silva A. The last forty-eight hours of life in a Portuguese palliative care unit: does it differ from elsewhere? J Palliat Med. 2003 Dec;6(6):895-900. | PubMed |
Gonçalves JF, Alvarenga M, Silva A. The last forty-eight hours of life in a Portuguese palliative care unit: does it differ from elsewhere? J Palliat Med. 2003 Dec;6(6):895-900. | PubMed | Groenewoud JH, van der Heide A, Kester JG, de Graaff CL, van der Wal G, van der Maas PJ. A nationwide study of decisions to forego life-prolonging treatment in Dutch medical practice. Arch Intern Med. 2000 Feb 14;160(3):357-63. | PubMed |
Groenewoud JH, van der Heide A, Kester JG, de Graaff CL, van der Wal G, van der Maas PJ. A nationwide study of decisions to forego life-prolonging treatment in Dutch medical practice. Arch Intern Med. 2000 Feb 14;160(3):357-63. | PubMed | Hanson LC, Garrett JM, Lewis C, Phifer N, Jackman A, Carey TS. Physicians' expectations of benefit from tube feeding. J Palliat Med. 2008 Oct;11(8):1130-4. | CrossRef | PubMed | PMC |
Hanson LC, Garrett JM, Lewis C, Phifer N, Jackman A, Carey TS. Physicians' expectations of benefit from tube feeding. J Palliat Med. 2008 Oct;11(8):1130-4. | CrossRef | PubMed | PMC | Hawkins C. Anorexia and anxiety in advanced malignancy: the relative problem. J Hum Nutr Diet 2000;13:113–117.
Hawkins C. Anorexia and anxiety in advanced malignancy: the relative problem. J Hum Nutr Diet 2000;13:113–117.  Holden CM. Anorexia in the terminally ill cancer patient: the emotional impact on the patient and the family. Hosp J. 1991;7(3):73-84. | PubMed |
Holden CM. Anorexia in the terminally ill cancer patient: the emotional impact on the patient and the family. Hosp J. 1991;7(3):73-84. | PubMed | Lanuke K, Fainsinger RL. Hydration management in palliative care settings--a survey of experts. J Palliat Care. 2003 Winter;19(4):278-9. | PubMed |
Lanuke K, Fainsinger RL. Hydration management in palliative care settings--a survey of experts. J Palliat Care. 2003 Winter;19(4):278-9. | PubMed | Lanuke K, Fainsinger RL, DeMoissac D. Hydration management at the end of life. J Palliat Med. 2004 Apr;7(2):257-63. | PubMed |
Lanuke K, Fainsinger RL, DeMoissac D. Hydration management at the end of life. J Palliat Med. 2004 Apr;7(2):257-63. | PubMed | Ke LS, Chiu TY, Lo SS, Hu WY. Knowledge, attitudes, and behavioral intentions of nurses toward providing artificial nutrition and hydration for terminal cáncer patients in Taiwan. Cancer Nurs. 2008 Jan-Feb;31(1):67-76. | CrossRef | PubMed |
Ke LS, Chiu TY, Lo SS, Hu WY. Knowledge, attitudes, and behavioral intentions of nurses toward providing artificial nutrition and hydration for terminal cáncer patients in Taiwan. Cancer Nurs. 2008 Jan-Feb;31(1):67-76. | CrossRef | PubMed | Masuda Y, Noguchi H, Kuzuya M, Inoue A, Hirakawa Y, Iguchi A, Uemura K. Comparison of medical treatments for the dying in a hospice and a geriatric hospital in Japan. J Palliat Med. 2006 Feb;9(1):152-60. | PubMed |
Masuda Y, Noguchi H, Kuzuya M, Inoue A, Hirakawa Y, Iguchi A, Uemura K. Comparison of medical treatments for the dying in a hospice and a geriatric hospital in Japan. J Palliat Med. 2006 Feb;9(1):152-60. | PubMed | McClement SE, Degner LF, Harlos MS. Family beliefs regarding the nutritional care of a terminally ill relative: a qualitative study. J Palliat Med. 2003 Oct;6(5):737-48. | PubMed |
McClement SE, Degner LF, Harlos MS. Family beliefs regarding the nutritional care of a terminally ill relative: a qualitative study. J Palliat Med. 2003 Oct;6(5):737-48. | PubMed | McClement SE, Degner LF, Harlos M. Family responses to declining intake and weight loss in a terminally ill relative. Part 1: fighting back. J Palliat Care. 2004 Summer;20(2):93-100. | PubMed |
McClement SE, Degner LF, Harlos M. Family responses to declining intake and weight loss in a terminally ill relative. Part 1: fighting back. J Palliat Care. 2004 Summer;20(2):93-100. | PubMed | Meares CJ. Primary caregiver perceptions of intake cessation in patients who are terminally Ill. Oncol Nurs Forum. 1997 Nov-Dec;24(10):1751-7. | PubMed |
Meares CJ. Primary caregiver perceptions of intake cessation in patients who are terminally Ill. Oncol Nurs Forum. 1997 Nov-Dec;24(10):1751-7. | PubMed | Mercadante S, Ferrera P, Girelli D, Casuccio A. Patients' and relatives' perceptions about intravenous and subcutaneous hydration. J Pain Symptom Manage. 2005 Oct;30(4):354-8. | PubMed |
Mercadante S, Ferrera P, Girelli D, Casuccio A. Patients' and relatives' perceptions about intravenous and subcutaneous hydration. J Pain Symptom Manage. 2005 Oct;30(4):354-8. | PubMed | Miyashita M, Morita T, Shima Y, Kimura R, Takahashi M, Adachi I. Nurse views of the adequacy of decision making and nurse distress regarding artificial hydration for terminally ill cancer patients: a nationwide survey. Am J Hosp Palliat Care. 2007 Dec-2008 Jan;24(6):463-9. Epub 2007 Jun 29. | PubMed |
Miyashita M, Morita T, Shima Y, Kimura R, Takahashi M, Adachi I. Nurse views of the adequacy of decision making and nurse distress regarding artificial hydration for terminally ill cancer patients: a nationwide survey. Am J Hosp Palliat Care. 2007 Dec-2008 Jan;24(6):463-9. Epub 2007 Jun 29. | PubMed | Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Association between hydration volume and symptoms in terminally ill cáncer patients with abdominal malignancies. Ann Oncol. 2005 Apr;16(4):640-7. Epub 2005 Jan 31. | PubMed |
Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Association between hydration volume and symptoms in terminally ill cáncer patients with abdominal malignancies. Ann Oncol. 2005 Apr;16(4):640-7. Epub 2005 Jan 31. | PubMed | Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Artificial hydration therapy, laboratory findings, and fluid balance in terminally ill patients with abdominal malignancies. J Pain Symptom Manage. 2006 Feb;31(2):130-9. | PubMed |
Morita T, Hyodo I, Yoshimi T, Ikenaga M, Tamura Y, Yoshizawa A, Shimada A, Akechi T, Miyashita M, Adachi I; Japan Palliative Oncology Study Group. Artificial hydration therapy, laboratory findings, and fluid balance in terminally ill patients with abdominal malignancies. J Pain Symptom Manage. 2006 Feb;31(2):130-9. | PubMed | Morita T, Tei Y, Inoue S. Agitated terminal delirium and association with partial opioid substitution and hydration. J Palliat Med. 2003 Aug;6(4):557-63. | PubMed |
Morita T, Tei Y, Inoue S. Agitated terminal delirium and association with partial opioid substitution and hydration. J Palliat Med. 2003 Aug;6(4):557-63. | PubMed | Morita T, Shima Y, Adachi I; Japan Palliative Oncology Study Group. Attitudes of Japanese physicians toward terminal dehydration: a nationwide survey. J Clin Oncol. 2002 Dec 15;20(24):4699-704. | PubMed |
Morita T, Shima Y, Adachi I; Japan Palliative Oncology Study Group. Attitudes of Japanese physicians toward terminal dehydration: a nationwide survey. J Clin Oncol. 2002 Dec 15;20(24):4699-704. | PubMed | Morita T, Tsunoda J, Inoue S, Chihara S. Perceptions and decision-making on rehydration of terminally ill cancer patients and family members. Am J Hosp Palliat Care. 1999 May-Jun;16(3):509-16. | PubMed |
Morita T, Tsunoda J, Inoue S, Chihara S. Perceptions and decision-making on rehydration of terminally ill cancer patients and family members. Am J Hosp Palliat Care. 1999 May-Jun;16(3):509-16. | PubMed | Musgrave CF, Bartal N, Opstad J. Intravenous hydration for terminal patients: what are the attitudes of Israeli terminal patients, their families, and their health professionals? J Pain Symptom Manage. 1996 Jul;12(1):47-51. | PubMed |
Musgrave CF, Bartal N, Opstad J. Intravenous hydration for terminal patients: what are the attitudes of Israeli terminal patients, their families, and their health professionals? J Pain Symptom Manage. 1996 Jul;12(1):47-51. | PubMed | Oh DY, Kim JH, Lee SH, Kim DW, Im SA, Kim TY, Heo DS, Bang YJ, Kim NK. Artificial nutrition and hydration in terminal cancer patients: the real and the ideal. Support Care Cancer. 2007 Jun;15(6):631-6. Epub 2006 Nov 11. | PubMed |
Oh DY, Kim JH, Lee SH, Kim DW, Im SA, Kim TY, Heo DS, Bang YJ, Kim NK. Artificial nutrition and hydration in terminal cancer patients: the real and the ideal. Support Care Cancer. 2007 Jun;15(6):631-6. Epub 2006 Nov 11. | PubMed | Oi-Ling K, Man-Wah DT, Kam-Hung DN. Symptom distress as rated by advanced cancer patients, caregivers and physicians in the last week of life. Palliat Med. 2005 Apr;19(3):228-33. | PubMed |
Oi-Ling K, Man-Wah DT, Kam-Hung DN. Symptom distress as rated by advanced cancer patients, caregivers and physicians in the last week of life. Palliat Med. 2005 Apr;19(3):228-33. | PubMed | Orrevall Y, Tishelman C, Herrington MK, Permert J. The path from oral nutrition to home parenteral nutrition: a qualitative interview study of the experiences of advanced cancer patients and their families. Clin Nutr. 2004Dec;23(6):1280-7. | PubMed |
Orrevall Y, Tishelman C, Herrington MK, Permert J. The path from oral nutrition to home parenteral nutrition: a qualitative interview study of the experiences of advanced cancer patients and their families. Clin Nutr. 2004Dec;23(6):1280-7. | PubMed | Parkash R, Burge F. The family's perspective on issues of hydration in terminal care. J Palliat Care. 1997 Winter;13(4):23-7. | PubMed |
Parkash R, Burge F. The family's perspective on issues of hydration in terminal care. J Palliat Care. 1997 Winter;13(4):23-7. | PubMed | Roeline H, Pasman W, Mei The A, Onwuteaka-Philipsen B, Ribbe M, Van der Wal G. Participants in the decisión making on artificial nutrition and hydration to demented nursing home patients: a qualitative study. J Aging Stud 2004;18:321–335.
Roeline H, Pasman W, Mei The A, Onwuteaka-Philipsen B, Ribbe M, Van der Wal G. Participants in the decisión making on artificial nutrition and hydration to demented nursing home patients: a qualitative study. J Aging Stud 2004;18:321–335.  Poole K, Froggatt K. Loss of weight and loss of appetite in advanced cancer: a problem for the patient, the carer, or the health professional? Palliat Med. 2002 Nov;16(6):499-506. | PubMed |
Poole K, Froggatt K. Loss of weight and loss of appetite in advanced cancer: a problem for the patient, the carer, or the health professional? Palliat Med. 2002 Nov;16(6):499-506. | PubMed | Sato K, Miyashita M, Morita T, Sanjo M, Shima Y, Uchitomi Y. Quality of end-of-life treatment for cancer patients in general wards and the palliative care unit at a regional cancer center in Japan: a retrospective chart review. Support Care Cancer. 2008 Feb;16(2):113-22. Epub 2007 Oct 5. | PubMed |
Sato K, Miyashita M, Morita T, Sanjo M, Shima Y, Uchitomi Y. Quality of end-of-life treatment for cancer patients in general wards and the palliative care unit at a regional cancer center in Japan: a retrospective chart review. Support Care Cancer. 2008 Feb;16(2):113-22. Epub 2007 Oct 5. | PubMed | Shega JW, Hougham GW, Cox-Hayley D, Sachs GA, Stocking CB. Advanced dementia and feeding tubes: do physician factors contribute to state variation? J Am Geriatr Soc. 2004 Jul;52(7):1217-8. | PubMed |
Shega JW, Hougham GW, Cox-Hayley D, Sachs GA, Stocking CB. Advanced dementia and feeding tubes: do physician factors contribute to state variation? J Am Geriatr Soc. 2004 Jul;52(7):1217-8. | PubMed | Shega JW, Hougham GW, Stocking CB, Cox-Hayley D, Sachs GA. Barriers to limiting the practice of feeding tube placement in advanced dementia. J Palliat Med. 2003 Dec;6(6):885-93. | PubMed |
Shega JW, Hougham GW, Stocking CB, Cox-Hayley D, Sachs GA. Barriers to limiting the practice of feeding tube placement in advanced dementia. J Palliat Med. 2003 Dec;6(6):885-93. | PubMed | Shragge JE, Wismer WV, Olson KL, Baracos VE. Shifting to conscious control: psychosocial and dietary management of anorexia by patients with advanced cancer. Palliat Med. 2007 Apr;21(3):227-33. | PubMed |
Shragge JE, Wismer WV, Olson KL, Baracos VE. Shifting to conscious control: psychosocial and dietary management of anorexia by patients with advanced cancer. Palliat Med. 2007 Apr;21(3):227-33. | PubMed | Sprung CL, Maia P, Bulow HH, Ricou B, Armaganidis A, Baras M, Wennberg E, Reinhart K, Cohen SL, Fries DR, Nakos G, Thijs LG; Ethicus Study Group. The importance of religious affiliation and culture on end-of-life decisions in European intensive care units. Intensive Care Med. 2007 Oct;33(10):1732-9. Erratum in: Intensive Care Med. 2007 Oct;33(10):1859. | PubMed |
Sprung CL, Maia P, Bulow HH, Ricou B, Armaganidis A, Baras M, Wennberg E, Reinhart K, Cohen SL, Fries DR, Nakos G, Thijs LG; Ethicus Study Group. The importance of religious affiliation and culture on end-of-life decisions in European intensive care units. Intensive Care Med. 2007 Oct;33(10):1732-9. Erratum in: Intensive Care Med. 2007 Oct;33(10):1859. | PubMed | Strasser F, Binswanger J, Cerny T, Kesselring A. Fighting a losing battle: eating-related distress of men with advanced cancer and their female partners. A mixed-methods study. Palliat Med. 2007 Mar;21(2):129-37. | PubMed |
Strasser F, Binswanger J, Cerny T, Kesselring A. Fighting a losing battle: eating-related distress of men with advanced cancer and their female partners. A mixed-methods study. Palliat Med. 2007 Mar;21(2):129-37. | PubMed | van der Riet P, Good P, Higgins I, Sneesby L. Palliative care professionals' perceptions of nutrition and hydration at the end of life. Int J Palliat Nurs. 2008 Mar;14(3):145-51. | PubMed |
van der Riet P, Good P, Higgins I, Sneesby L. Palliative care professionals' perceptions of nutrition and hydration at the end of life. Int J Palliat Nurs. 2008 Mar;14(3):145-51. | PubMed | van Wigcheren PT, Onwuteaka-Philipsen BD, Pasman HR, Ooms ME, Ribbe MW, van der Wal G. Starting artificial nutrition and hydration in patients with dementia in The Netherlands: frequencies, patient characteristics and decision-making process. Aging Clin Exp Res. 2007 Feb;19(1):26-33. | PubMed |
van Wigcheren PT, Onwuteaka-Philipsen BD, Pasman HR, Ooms ME, Ribbe MW, van der Wal G. Starting artificial nutrition and hydration in patients with dementia in The Netherlands: frequencies, patient characteristics and decision-making process. Aging Clin Exp Res. 2007 Feb;19(1):26-33. | PubMed | Viola RA. Studying Fluid Status and the Dying: The Challenge of Clinical Research in Palliative Care [MSc thesis]. Canada: University of Ottawa, 1997.
Viola RA. Studying Fluid Status and the Dying: The Challenge of Clinical Research in Palliative Care [MSc thesis]. Canada: University of Ottawa, 1997.  Waller A, Hershkowitz M, Adunsky A. The effect of intravenous fluid infusion on blood and urine parameters of hydration and on state of consciousness in terminal cancer patients. Am J Hosp Palliat Care. 1994 Nov-Dec;11(6):22-7. | PubMed |
Waller A, Hershkowitz M, Adunsky A. The effect of intravenous fluid infusion on blood and urine parameters of hydration and on state of consciousness in terminal cancer patients. Am J Hosp Palliat Care. 1994 Nov-Dec;11(6):22-7. | PubMed | Worobec G, Brown MK. Hypodermoclysis therapy. In a chronic care hospital setting. J Gerontol Nurs. 1997 Jun;23(6):23-8. | PubMed |
Worobec G, Brown MK. Hypodermoclysis therapy. In a chronic care hospital setting. J Gerontol Nurs. 1997 Jun;23(6):23-8. | PubMed | National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Palliative Care 2017 [cited November 12, 2017].
National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines): Palliative Care 2017 [cited November 12, 2017]. Systematization of initiatives in sexual and reproductive health about good practices criteria in response to the COVID-19 pandemic in primary health care in Chile
Clinical, psychological, social, and family characterization of suicidal behavior in Chilean adolescents: a multiple correspondence analysis








