Resumen
Durante un episodio de sepsis, el fenómeno de respuesta inflamatoria sistémica desencadena una serie de mecanismos procoagulantes. Se ha planteado que el uso de proteína C activada podría tener un rol en el manejo de esta patología, pero no existe consenso al respecto. Utilizando la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en múltiples bases de datos, identificamos siete revisiones sistemáticas que en conjunto incluyen 35 estudios primarios, de los cuales seis corresponden a estudios aleatorizados. Realizamos un metanálisis y tablas de resumen de los resultados utilizando el método GRADE. Concluimos que el uso de proteína C activada en cuadros sépticos probablemente no disminuye la tasa de mortalidad y aumenta la tasa de eventos hemorrágicos.
Problema
La sepsis continúa siendo la principal causa de morbimortalidad en unidades de cuidados intensivos en todo el mundo. Su incidencia ha ido en aumento, con mayores complicaciones y con agentes infecciosos más resistentes. Si bien se ha observado cierta tendencia a la disminución de la mortalidad gracias a algunas intervenciones, las herramientas terapéuticas efectivas siguen siendo limitadas.
La proteína C humana es una glicoproteína dependiente de la vitamina K, estructuralmente similar a otras proteínas que afectan a la coagulación de la sangre, tales como la protrombina, Factor VII, Factor IX y Factor X. Se piensa que jugaría un papel importante regulando la anticoagulación, inflamación, muerte celular y manteniendo la permeabilidad de las paredes de los vasos sanguíneos.
La compañía farmacéutica que producía este fármaco lo retiró del mercado en 2011.
Métodos
Utilizamos la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en múltiples bases de datos, para identificar revisiones sistemáticas y sus estudios primarios incluidos. Con esta información generamos un resumen estructurado, siguiendo un formato preestablecido, que incluye mensajes clave, un resumen del conjunto de evidencia (presentado como matriz de evidencia en Epistemonikos), metanálisis del total de los estudios, tablas de resumen de resultados con el método GRADE, y tabla de otras consideraciones para la toma de decisión.
|
Mensajes clave
|
Acerca del conjunto de evidencia para esta pregunta
|
Cuál es la evidencia. |
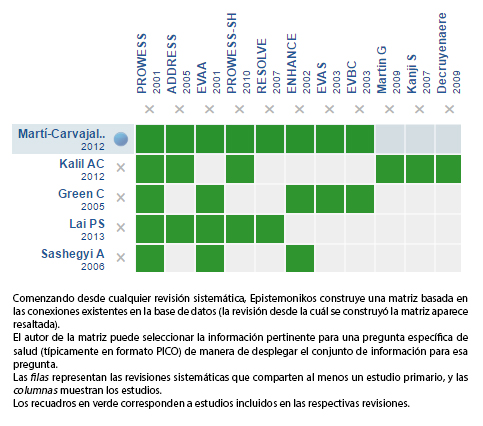
Encontramos siete revisiones sistemáticas [1],[2],[3],[4],[5],[6],[7], que incluyen 35 estudios primarios [8],[9], |
|
Qué tipo de pacientes incluyeron los estudios |
Respecto a los tipos de pacientes, cabe destacar que los seis estudios fueron realizados con posterioridad al año 1991, año que se realiza el primer Consensus Definitions for Sepsis and Septic Shock, por lo que la definición y graduación de la severidad de la sepsis es homogénea entre los diversos estudios. |
|
Qué tipo de intervenciones incluyeron los estudios |
En cuatro de los seis estudios, el tipo de proteína C activada utilizada fue drotrecogin alfa-activada [8],[11],[12],[13] y en dos fue proteína C activada humana (rhAPC) [9],[10]. La vía de administración fue endovenosa en todos los estudios Respecto a la dosis utilizada, cinco utilizaron una dosis estándar de 24 μg/kg/hora por un total de 96 horas [8], [10],[11],[12],[13]. Un estudio utilizó dosis variables y tiempo distinto a las 96 horas [9]. Todos los estudios compararon contra placebo o tratamiento estándar. |
|
Qué tipo de desenlaces midieron |
Las distintas revisiones sistemáticas identificadas agruparon los desenlaces de la siguiente forma:
|
Resumen de los resultados
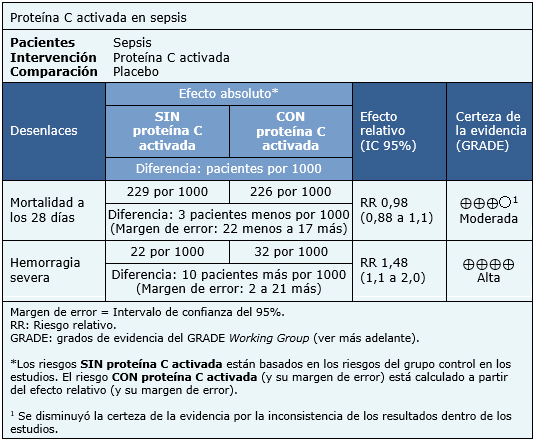
La información sobre los efectos de la proteína C activada en la sepsis está basada en seis estudios aleatorizados que incluyen 6781 pacientes. Todos los estudios midieron el desenlace mortalidad a los 28 días y hemorragia severa. El resumen de los resultados es el siguiente:
- El uso de proteína C activada en pacientes con sepsis probablemente no disminuye la tasa de mortalidad. La certeza de la evidencia es moderada.
- El uso de proteína C activada en pacientes con sepsis aumenta la tasa de hemorragia severa durante la hospitalización. La certeza de la evidencia es alta.

Otras consideraciones para la toma de decisión
|
A quién se aplica y a quién no se aplica esta evidencia |
|
| Sobre los desenlaces incluidos en este resumen |
|
| Balance riesgo/beneficio y certeza de la evidencia |
|
| Qué piensan los pacientes y sus tratantes |
|
| Consideraciones de recursos |
|
| Diferencias entre este resumen y otras fuentes |
|
| ¿Puede que cambie esta información en el futuro? |
|
Cómo realizamos este resumen
Mediante métodos automatizados y colaborativos recopilamos toda la evidencia relevante para la pregunta de interés y la presentamos en una matriz de evidencia.
Siga el enlace para acceder a la versión interactiva: Proteína C activada recombinante para el tratamiento de la sepsis
Notas
Si con posterioridad a la publicación de este resumen se publican nuevas revisiones sistemáticas sobre este tema, en la parte superior de la matriz se mostrará un aviso de “nueva evidencia”. Si bien el proyecto contempla la actualización periódica de estos resúmenes, los usuarios están invitados a comentar en Medwave o contactar a los autores mediante correo electrónico si creen que hay evidencia que motive una actualización más rápida.
Luego de crear una cuenta en Epistemonikos, al guardar las matrices recibirá notificaciones automáticas cada vez que exista nueva evidencia que potencialmente responda a esta pregunta. El detalle de los métodos para elaborar este resumen están descritos aquí: http://dx.doi.org/10.5867/medwave.2014.06.5997.
La Fundación Epistemonikos es una organización que busca acercar la información a quienes toman decisiones en salud, mediante el uso de tecnologías. Su principal desarrollo es la base de datos Epistemonikos (www.epistemonikos.org).
Los resúmenes de evidencia siguen un riguroso proceso de revisión por pares interno.
Declaración de conflictos de intereses
Los autores declaran no tener conflictos de intereses con la materia de este artículo.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

Durante un episodio de sepsis, el fenómeno de respuesta inflamatoria sistémica desencadena una serie de mecanismos procoagulantes. Se ha planteado que el uso de proteína C activada podría tener un rol en el manejo de esta patología, pero no existe consenso al respecto. Utilizando la base de datos Epistemonikos, la cual es mantenida mediante búsquedas en múltiples bases de datos, identificamos siete revisiones sistemáticas que en conjunto incluyen 35 estudios primarios, de los cuales seis corresponden a estudios aleatorizados. Realizamos un metanálisis y tablas de resumen de los resultados utilizando el método GRADE. Concluimos que el uso de proteína C activada en cuadros sépticos probablemente no disminuye la tasa de mortalidad y aumenta la tasa de eventos hemorrágicos.
 Authors:
Juan Alvarado[1,2], Ricardo Castro[2,3]
Authors:
Juan Alvarado[1,2], Ricardo Castro[2,3]
Affiliation:
[1] Facultad de Medicina, Pontificia Universidad Católica de Chile, Santiago, Chile
[2] Proyecto Epistemonikos, Santiago, Chile
[3] Departamento de Medicina Intensiva, Facultad de Medicina, Pontificia Universidad Católica de Chile, Santiago, Chile
E-mail: rcastro@med.puc.cl
Author address:
[1] Facultad de Medicina Pontificia Universidad Católica de Chile Lira 63 Santiago Centro Chile

Citation: Alvarado J, Castro R. What is the role of recombinant activated protein C in the management of sepsis?. Medwave 2016; 16(Suppl5):e6801 doi: 10.5867/medwave.2016.6801
Publication date: 20/12/2016

Comments (0)
We are pleased to have your comment on one of our articles. Your comment will be published as soon as it is posted. However, Medwave reserves the right to remove it later if the editors consider your comment to be: offensive in some sense, irrelevant, trivial, contains grammatical mistakes, contains political harangues, appears to be advertising, contains data from a particular person or suggests the need for changes in practice in terms of diagnostic, preventive or therapeutic interventions, if that evidence has not previously been published in a peer-reviewed journal.
No comments on this article.
To comment please log in
 Medwave provides HTML and PDF download counts as well as other harvested interaction metrics.
Medwave provides HTML and PDF download counts as well as other harvested interaction metrics. There may be a 48-hour delay for most recent metrics to be posted.

- Costa V, Brophy JM. Drotrecogin alfa (activated) in severe sepsis: a systematic review and new cost-effectiveness analysis. BMC Anesthesiol. 2007 Jun 25;7:5 | PubMed |
- Green C, Dinnes J, Takeda A, Shepherd J, Hartwell D, Cave C, Payne E, Cuthbertson BH. Clinical effectiveness and cost-effectiveness of drotrecogin alfa (activated) (Xigris) for the treatment of severe sepsis in adults: a systematic review and economic evaluation. Health Technol Assess. 2005 Mar;9(11):1-126, iii-iv | PubMed |
- Kalil AC, LaRosa SP. Effectiveness and safety of drotrecogin alfa (activated) for severe sepsis: a meta-analysis and metaregression. Lancet Infect Dis. 2012 Sep;12(9):678-86 | CrossRef | PubMed |
- Lai PS, Matteau A, Iddriss A, Hawes JC, Ranieri V, Thompson BT. An updated meta-analysis to understand the variable efficacy of drotrecogin alfa (activated) in severe sepsis and septic shock. Minerva Anestesiol. 2013 Jan;79(1):33-43. | PubMed |
- Martí-Carvajal AJ, Solŕ I, Gluud C, Lathyris D, Cardona AF. Human recombinant protein C for severe sepsis and septic shock in adult and paediatric patients. Cochrane Database Syst Rev. 2012 Dec 12;12:CD004388 | CrossRef | PubMed |
- Sashegyi A, Trzaskoma BL, Nelson DR, Williams MD, Macias W. International INtegrated Database for the Evaluation of severe sePsis and drotrecogin alfa (activated) THerapy: component trials and statistical methods for INDEPTH. Curr Med Res Opin. 2006 May;22(5):1001-12 | PubMed |
- Wiedermann CJ, Kaneider NC. A meta-analysis of controlled trials of recombinant human activated protein C therapy in patients with sepsis. BMC Emerg Med. 2005 Oct 14;5:7 | PubMed |
- Abraham E, Laterre PF, Garg R, Levy H, Talwar D, Trzaskoma BL, François B, Guy JS, Brückmann M, Rea-Neto A, Rossaint R, Perrotin D, Sablotzki A, Arkins N, Utterback BG, Macias WL; Administration of Drotrecogin Alfa (Activated) in Early Stage Severe Sepsis (ADDRESS) Study Group.. Drotrecogin alfa (activated) for adults with severe sepsis and a low risk of death. N Engl J Med. 2005 Sep 29;353(13):1332-41 | PubMed |
- Bernard GR, Vincent JL, Laterre PF, LaRosa SP, Dhainaut JF, Lopez-Rodriguez A, Steingrub JS, Garber GE, Helterbrand JD, Ely EW, Fisher CJ Jr; Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group.. Efficacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med. 2001 Mar 8;344(10):699-709 | PubMed |
- Bernard GR, Ely EW, Wright TJ, Fraiz J, Stasek JE Jr, Russell JA, Mayers I, Rosenfeld BA, Morris PE, Yan SB, Helterbrand JD. Safety and dose relationship of recombinant human activated protein C for coagulopathy in severe sepsis. Crit Care Med. 2001 Nov;29(11):2051-9 | PubMed |
- Dhainaut JF, Antonelli M, Wright P, Desachy A, Reignier J, Lavoue S, Charpentier J, Belger M, Cobas-Meyer M, Maier C, Mignini MA, Janes J. Extended drotrecogin alfa (activated) treatment in patients with prolonged septic shock. Intensive Care Med. 2009 Jul;35(7):1187-95 | CrossRef | PubMed |
- Nadel S, Goldstein B, Williams MD, Dalton H, Peters M, Macias WL, Abd-Allah SA, Levy H, Angle R, Wang D, Sundin DP, Giroir B; REsearching severe Sepsis and Organ dysfunction in children: a gLobal perspective (RESOLVE) study group. Drotrecogin alfa (activated) in children with severe sepsis: a multicentre phase III randomised controlled trial. Lancet. 2007 Mar 10;369(9564):836-43 | PubMed |
- PROWESS SHOCK Steering Committee., Thompson BT, Ranieri VM, Finfer S, Barie PS, Dhainaut JF, Douglas IS, Gĺrdlund B, Marshall JC, Rhodes A. Statistical analysis plan of PROWESS SHOCK study. Intensive Care Med. 2010 Nov;36(11):1972-3. | CrossRef | PubMed |
- Martin G, Brunkhorst FM, Janes JM, Reinhart K, Sundin DP, Garnett K, Beale R. The international PROGRESS registry of patients with severe sepsis: drotrecogin alfa (activated) use and patient outcomes. Crit Care. 2009;13(3):R103 | CrossRef | PubMed |
- Lindenauer PK, Rothberg MB, Nathanson BH, Pekow PS, Steingrub JS. Activated protein C and hospital mortality in septic shock: a propensity-matched analysis. Crit Care Med. 2010 Apr;38(4):1101-7 | CrossRef | PubMed |
- Kanji S, Perreault MM, Chant C, Williamson D, Burry L. Evaluating the use of Drotrecogin alfa (activated) in adult severe sepsis: a Canadian multicenter observational study. Intensive Care Med. 2007 Mar;33(3):517-23 | PubMed |
- Decruyenaere J, De Backer D, Spapen H, Laterre PF, Raemaekers J, Rogiers P, Trine H, Sartral M, Haentjens T, Wagner T. 90-day follow-up of patients treated with Drotrecogin Alfa (activated) for severe sepsis: a Belgian open label study. Acta Clin Belg. 2009 Jan-Feb;64(1):16-22 | PubMed |
- Hecksher CA, Lacerda HR, Maciel MA. Characteristics and outcomes of patients treated with drotrecogin alpha and other interventions of the "Surviving Sepsis" campaign in clinical practice. Rev Bras Ter Intensiva. 2008 Jun;20(2):135-43. | PubMed |
- Gentry CA, Gross KB, Sud B, Drevets DA. Adverse outcomes associated with the use of drotrecogin alfa (activated) in patients with severe sepsis and baseline bleeding precautions. Crit Care Med. 2009 Jan;37(1):19-25 | CrossRef | PubMed |
- Bertolini G, Rossi C, Anghileri A, Livigni S, Addis A, Poole D. Use of Drotrecogin alfa (activated) in Italian intensive care units: the results of a nationwide survey. Intensive Care Med. 2007 Mar;33(3):426-34 | PubMed |
- Anger KE, Degrado JR, Greenwood BC, Cohen SA, Szumita PM. Evaluation of recombinant activated protein C for severe sepsis at a tertiary academic medical center. Therapeutics and clinical risk management. 2013;9:277-84. | Link |
- Bollinger J, Coley K, Rea R, Saul M. Outcomes in patients with recombinant human activated protein c at an academic medical center versus the ENHANCE US trial. Crit Care Med 2006; 34: A111. | Link |
- Wheeler A, Steingrub J, Schmidt GA, Sanchez P, Jacobi J, Linde-Zwirble W, Bates B, Qualy RL, Woodward B, Zeckel M. A retrospective observational study of drotrecogin alfa (activated) in adults with severe sepsis: comparison with a controlled clinical trial. Crit Care Med. 2008 Jan;36(1):14-23 | PubMed |
- Spriet I, Meersseman W, Wilmer A, Meyfroidt G, Casteels M, Willems L. Evaluation of drotrecogin alpha use in a Belgian university hospital. Pharm World Sci. 2006 Oct;28(5):290-5 | PubMed |
- Rowan KM, Welch CA, North E, Harrison DA. Drotrecogin alfa (activated): real-life use and outcomes for the UK. Crit Care. 2008;12(2):R58 | CrossRef | PubMed |
- Higgins TL, Steingrub JS, Tereso GJ, Tidswell MA, McGee WT. Drotrecogin alfa (activated) in sepsis: initial experience with patient selection, cost, and clinical outcomes. J Intensive Care Med. 2005 Nov-Dec;20(6):339-45 | PubMed |
- Ridley S, Lwin A, Wyncoll D, Lippett S, Watson D, Gunning K, Higgins D. Drotrecogin alfa (activated): diffusion from clinical trials to clinical practice. Eur J Anaesthesiol. 2008 Mar;25(3):211-6 | PubMed |
- Sadaka F, O'Brien J, Migneron M, Stortz J, Vanston A, Taylor RW. Activated protein C in septic shock: a propensity-matched analysis. Crit Care. 2011;15(2):R89 | CrossRef | PubMed |
- Ferrer R, Artigas A, Suarez D, Palencia E, Levy MM, Arenzana A, Pérez XL, Sirvent JM; Edusepsis Study Group.. Effectiveness of treatments for severe sepsis: a prospective, multicenter, observational study. Am J Respir Crit Care Med. 2009 Nov 1;180(9):861-6 | CrossRef | PubMed |
- Kübler A, Mayzner-Zawadzka E, Durek G, Gaszynski W, Karpel E, Mikaszewska-Sokolewicz M, Majak P. Results of severe sepsis treatment program using recombinant human activated protein C in Poland. Med Sci Monit. 2006 Mar;12(3):CR107-12 | PubMed |
- Maurice A, Seguin P, Aguillon D, Chanavaz C, Mallédant Y. [Activated protein C treatment: experience about 23 patients in the operative period]. Ann Fr Anesth Reanim. 2005 Apr;24(4):343-6 | PubMed |
- Dhainaut JF, Payet S, Vallet B, França LR, Annane D, Bollaert PE, Le Tulzo Y, Runge I, Malledant Y, Guidet B, Le Lay K, Launois R; PREMISS Study Group. Cost-effectiveness of activated protein C in real-life clinical practice. Crit Care. 2007;11(5):R99 | PubMed |
- Vincent JL, Bernard GR, Beale R, Doig C, Putensen C, Dhainaut JF, Artigas A, Fumagalli R, Macias W, Wright T, Wong K, Sundin DP, Turlo MA, Janes J. Drotrecogin alfa (activated) treatment in severe sepsis from the global open-label trial ENHANCE: further evidence for survival and safety and implications for early treatment. Crit Care Med. 2005 Oct;33(10):2266-77 | PubMed |
- Vincent JL, Laterre PF, Decruyenaere J, Spapen H, Raemaekers J, Damas F, Rogiers P, Sartral M, Haentjens T, Nelson D, Janes J. A registry of patients treated with drotrecogin alfa (activated) in Belgian intensive care units an observational study. Acta Clin Belg. 2008 Jan-Feb;63(1):25-30 | PubMed |
- Ernst FR, Johnston JA, Pulgar S, He J, Ball DE, Young JK, Cooper LM. Timing of drotrecogin alfa (activated) initiation in treatment of severe sepsis: a database cohort study of hospital mortality, length of stay, and costs. Curr Med Res Opin. 2007 Jan;23(1):235-44 | PubMed |
- Eli Lilly. An open label study of drotrecogin alfa (activated) in adult patients with severe sepsis and multiple organ dysfunctions, a phase IV protocol. 2006; Summary ID 7159: 1–6. | Link |
- Macchiavello L, Ellis G, Bowden S, Smithies M. A large, single-centre UK registry of drotrecogin alfa-activated use. Crit Care 2007; 11 (suppl 2): 58. | Link |
- Steingrub JS, Cheatham ML, Woodward B, Wang HT, Effron MB; XEUS Investigators.. A prospective, observational study of Xigris Use in the United States (XEUS). J Crit Care. 2010 Dec;25(4):660.e9-16 | CrossRef | PubMed |
- Bernard GR, Vincent JL, Laterre PF, et al, and the Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group. Effi cacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med 2001; 344: 699–709. | CrossRef | PubMed | Link |
- Bernard GR, Macias WL, Joyce DE,Williams MD, Bailey J, Vincent JL. Safety assessment of drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis. Critical Care 2003;7(2):155–63. | PubMed |
- Bernard G, Margolis B, Shanies H, Ely E, Wheeler A, Levy H. Efficacy and safety of References 66 drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis: report from a single open-label trial in the United States 2002. | Link |
- Eli Lilly. Xigris NICE submission: drotrecogin alfa (activated) for severe sepsis. Basingstoke: Eli Lilly; 2003. | Link |
- Dr. R. Phillip Dellinger; Dr. Mitchell M.Levy; Dr. Andrew Rhodes; Dr. Djillali Annane et al. Campańa para sobrevivir a la sepsis: recomendaciones internacionales para el tratamiento de sepsis grave y shock séptico, 2012: Crit Care Med 2013; Febrero de 2013 Volumen 41. | CrossRef | Link |
 Costa V, Brophy JM. Drotrecogin alfa (activated) in severe sepsis: a systematic review and new cost-effectiveness analysis. BMC Anesthesiol. 2007 Jun 25;7:5 | PubMed |
Costa V, Brophy JM. Drotrecogin alfa (activated) in severe sepsis: a systematic review and new cost-effectiveness analysis. BMC Anesthesiol. 2007 Jun 25;7:5 | PubMed | Green C, Dinnes J, Takeda A, Shepherd J, Hartwell D, Cave C, Payne E, Cuthbertson BH. Clinical effectiveness and cost-effectiveness of drotrecogin alfa (activated) (Xigris) for the treatment of severe sepsis in adults: a systematic review and economic evaluation. Health Technol Assess. 2005 Mar;9(11):1-126, iii-iv | PubMed |
Green C, Dinnes J, Takeda A, Shepherd J, Hartwell D, Cave C, Payne E, Cuthbertson BH. Clinical effectiveness and cost-effectiveness of drotrecogin alfa (activated) (Xigris) for the treatment of severe sepsis in adults: a systematic review and economic evaluation. Health Technol Assess. 2005 Mar;9(11):1-126, iii-iv | PubMed | Kalil AC, LaRosa SP. Effectiveness and safety of drotrecogin alfa (activated) for severe sepsis: a meta-analysis and metaregression. Lancet Infect Dis. 2012 Sep;12(9):678-86 | CrossRef | PubMed |
Kalil AC, LaRosa SP. Effectiveness and safety of drotrecogin alfa (activated) for severe sepsis: a meta-analysis and metaregression. Lancet Infect Dis. 2012 Sep;12(9):678-86 | CrossRef | PubMed | Lai PS, Matteau A, Iddriss A, Hawes JC, Ranieri V, Thompson BT. An updated meta-analysis to understand the variable efficacy of drotrecogin alfa (activated) in severe sepsis and septic shock. Minerva Anestesiol. 2013 Jan;79(1):33-43. | PubMed |
Lai PS, Matteau A, Iddriss A, Hawes JC, Ranieri V, Thompson BT. An updated meta-analysis to understand the variable efficacy of drotrecogin alfa (activated) in severe sepsis and septic shock. Minerva Anestesiol. 2013 Jan;79(1):33-43. | PubMed | Martí-Carvajal AJ, Solŕ I, Gluud C, Lathyris D, Cardona AF. Human recombinant protein C for severe sepsis and septic shock in adult and paediatric patients. Cochrane Database Syst Rev. 2012 Dec 12;12:CD004388 | CrossRef | PubMed |
Martí-Carvajal AJ, Solŕ I, Gluud C, Lathyris D, Cardona AF. Human recombinant protein C for severe sepsis and septic shock in adult and paediatric patients. Cochrane Database Syst Rev. 2012 Dec 12;12:CD004388 | CrossRef | PubMed | Sashegyi A, Trzaskoma BL, Nelson DR, Williams MD, Macias W. International INtegrated Database for the Evaluation of severe sePsis and drotrecogin alfa (activated) THerapy: component trials and statistical methods for INDEPTH. Curr Med Res Opin. 2006 May;22(5):1001-12 | PubMed |
Sashegyi A, Trzaskoma BL, Nelson DR, Williams MD, Macias W. International INtegrated Database for the Evaluation of severe sePsis and drotrecogin alfa (activated) THerapy: component trials and statistical methods for INDEPTH. Curr Med Res Opin. 2006 May;22(5):1001-12 | PubMed | Wiedermann CJ, Kaneider NC. A meta-analysis of controlled trials of recombinant human activated protein C therapy in patients with sepsis. BMC Emerg Med. 2005 Oct 14;5:7 | PubMed |
Wiedermann CJ, Kaneider NC. A meta-analysis of controlled trials of recombinant human activated protein C therapy in patients with sepsis. BMC Emerg Med. 2005 Oct 14;5:7 | PubMed | Abraham E, Laterre PF, Garg R, Levy H, Talwar D, Trzaskoma BL, François B, Guy JS, Brückmann M, Rea-Neto A, Rossaint R, Perrotin D, Sablotzki A, Arkins N, Utterback BG, Macias WL; Administration of Drotrecogin Alfa (Activated) in Early Stage Severe Sepsis (ADDRESS) Study Group.. Drotrecogin alfa (activated) for adults with severe sepsis and a low risk of death. N Engl J Med. 2005 Sep 29;353(13):1332-41 | PubMed |
Abraham E, Laterre PF, Garg R, Levy H, Talwar D, Trzaskoma BL, François B, Guy JS, Brückmann M, Rea-Neto A, Rossaint R, Perrotin D, Sablotzki A, Arkins N, Utterback BG, Macias WL; Administration of Drotrecogin Alfa (Activated) in Early Stage Severe Sepsis (ADDRESS) Study Group.. Drotrecogin alfa (activated) for adults with severe sepsis and a low risk of death. N Engl J Med. 2005 Sep 29;353(13):1332-41 | PubMed | Bernard GR, Vincent JL, Laterre PF, LaRosa SP, Dhainaut JF, Lopez-Rodriguez A, Steingrub JS, Garber GE, Helterbrand JD, Ely EW, Fisher CJ Jr; Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group.. Efficacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med. 2001 Mar 8;344(10):699-709 | PubMed |
Bernard GR, Vincent JL, Laterre PF, LaRosa SP, Dhainaut JF, Lopez-Rodriguez A, Steingrub JS, Garber GE, Helterbrand JD, Ely EW, Fisher CJ Jr; Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group.. Efficacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med. 2001 Mar 8;344(10):699-709 | PubMed | Bernard GR, Ely EW, Wright TJ, Fraiz J, Stasek JE Jr, Russell JA, Mayers I, Rosenfeld BA, Morris PE, Yan SB, Helterbrand JD. Safety and dose relationship of recombinant human activated protein C for coagulopathy in severe sepsis. Crit Care Med. 2001 Nov;29(11):2051-9 | PubMed |
Bernard GR, Ely EW, Wright TJ, Fraiz J, Stasek JE Jr, Russell JA, Mayers I, Rosenfeld BA, Morris PE, Yan SB, Helterbrand JD. Safety and dose relationship of recombinant human activated protein C for coagulopathy in severe sepsis. Crit Care Med. 2001 Nov;29(11):2051-9 | PubMed | Dhainaut JF, Antonelli M, Wright P, Desachy A, Reignier J, Lavoue S, Charpentier J, Belger M, Cobas-Meyer M, Maier C, Mignini MA, Janes J. Extended drotrecogin alfa (activated) treatment in patients with prolonged septic shock. Intensive Care Med. 2009 Jul;35(7):1187-95 | CrossRef | PubMed |
Dhainaut JF, Antonelli M, Wright P, Desachy A, Reignier J, Lavoue S, Charpentier J, Belger M, Cobas-Meyer M, Maier C, Mignini MA, Janes J. Extended drotrecogin alfa (activated) treatment in patients with prolonged septic shock. Intensive Care Med. 2009 Jul;35(7):1187-95 | CrossRef | PubMed | Nadel S, Goldstein B, Williams MD, Dalton H, Peters M, Macias WL, Abd-Allah SA, Levy H, Angle R, Wang D, Sundin DP, Giroir B; REsearching severe Sepsis and Organ dysfunction in children: a gLobal perspective (RESOLVE) study group. Drotrecogin alfa (activated) in children with severe sepsis: a multicentre phase III randomised controlled trial. Lancet. 2007 Mar 10;369(9564):836-43 | PubMed |
Nadel S, Goldstein B, Williams MD, Dalton H, Peters M, Macias WL, Abd-Allah SA, Levy H, Angle R, Wang D, Sundin DP, Giroir B; REsearching severe Sepsis and Organ dysfunction in children: a gLobal perspective (RESOLVE) study group. Drotrecogin alfa (activated) in children with severe sepsis: a multicentre phase III randomised controlled trial. Lancet. 2007 Mar 10;369(9564):836-43 | PubMed | PROWESS SHOCK Steering Committee., Thompson BT, Ranieri VM, Finfer S, Barie PS, Dhainaut JF, Douglas IS, Gĺrdlund B, Marshall JC, Rhodes A. Statistical analysis plan of PROWESS SHOCK study. Intensive Care Med. 2010 Nov;36(11):1972-3. | CrossRef | PubMed |
PROWESS SHOCK Steering Committee., Thompson BT, Ranieri VM, Finfer S, Barie PS, Dhainaut JF, Douglas IS, Gĺrdlund B, Marshall JC, Rhodes A. Statistical analysis plan of PROWESS SHOCK study. Intensive Care Med. 2010 Nov;36(11):1972-3. | CrossRef | PubMed | Martin G, Brunkhorst FM, Janes JM, Reinhart K, Sundin DP, Garnett K, Beale R. The international PROGRESS registry of patients with severe sepsis: drotrecogin alfa (activated) use and patient outcomes. Crit Care. 2009;13(3):R103 | CrossRef | PubMed |
Martin G, Brunkhorst FM, Janes JM, Reinhart K, Sundin DP, Garnett K, Beale R. The international PROGRESS registry of patients with severe sepsis: drotrecogin alfa (activated) use and patient outcomes. Crit Care. 2009;13(3):R103 | CrossRef | PubMed | Lindenauer PK, Rothberg MB, Nathanson BH, Pekow PS, Steingrub JS. Activated protein C and hospital mortality in septic shock: a propensity-matched analysis. Crit Care Med. 2010 Apr;38(4):1101-7 | CrossRef | PubMed |
Lindenauer PK, Rothberg MB, Nathanson BH, Pekow PS, Steingrub JS. Activated protein C and hospital mortality in septic shock: a propensity-matched analysis. Crit Care Med. 2010 Apr;38(4):1101-7 | CrossRef | PubMed | Kanji S, Perreault MM, Chant C, Williamson D, Burry L. Evaluating the use of Drotrecogin alfa (activated) in adult severe sepsis: a Canadian multicenter observational study. Intensive Care Med. 2007 Mar;33(3):517-23 | PubMed |
Kanji S, Perreault MM, Chant C, Williamson D, Burry L. Evaluating the use of Drotrecogin alfa (activated) in adult severe sepsis: a Canadian multicenter observational study. Intensive Care Med. 2007 Mar;33(3):517-23 | PubMed | Decruyenaere J, De Backer D, Spapen H, Laterre PF, Raemaekers J, Rogiers P, Trine H, Sartral M, Haentjens T, Wagner T. 90-day follow-up of patients treated with Drotrecogin Alfa (activated) for severe sepsis: a Belgian open label study. Acta Clin Belg. 2009 Jan-Feb;64(1):16-22 | PubMed |
Decruyenaere J, De Backer D, Spapen H, Laterre PF, Raemaekers J, Rogiers P, Trine H, Sartral M, Haentjens T, Wagner T. 90-day follow-up of patients treated with Drotrecogin Alfa (activated) for severe sepsis: a Belgian open label study. Acta Clin Belg. 2009 Jan-Feb;64(1):16-22 | PubMed | Hecksher CA, Lacerda HR, Maciel MA. Characteristics and outcomes of patients treated with drotrecogin alpha and other interventions of the "Surviving Sepsis" campaign in clinical practice. Rev Bras Ter Intensiva. 2008 Jun;20(2):135-43. | PubMed |
Hecksher CA, Lacerda HR, Maciel MA. Characteristics and outcomes of patients treated with drotrecogin alpha and other interventions of the "Surviving Sepsis" campaign in clinical practice. Rev Bras Ter Intensiva. 2008 Jun;20(2):135-43. | PubMed | Gentry CA, Gross KB, Sud B, Drevets DA. Adverse outcomes associated with the use of drotrecogin alfa (activated) in patients with severe sepsis and baseline bleeding precautions. Crit Care Med. 2009 Jan;37(1):19-25 | CrossRef | PubMed |
Gentry CA, Gross KB, Sud B, Drevets DA. Adverse outcomes associated with the use of drotrecogin alfa (activated) in patients with severe sepsis and baseline bleeding precautions. Crit Care Med. 2009 Jan;37(1):19-25 | CrossRef | PubMed | Bertolini G, Rossi C, Anghileri A, Livigni S, Addis A, Poole D. Use of Drotrecogin alfa (activated) in Italian intensive care units: the results of a nationwide survey. Intensive Care Med. 2007 Mar;33(3):426-34 | PubMed |
Bertolini G, Rossi C, Anghileri A, Livigni S, Addis A, Poole D. Use of Drotrecogin alfa (activated) in Italian intensive care units: the results of a nationwide survey. Intensive Care Med. 2007 Mar;33(3):426-34 | PubMed | Anger KE, Degrado JR, Greenwood BC, Cohen SA, Szumita PM. Evaluation of recombinant activated protein C for severe sepsis at a tertiary academic medical center. Therapeutics and clinical risk management. 2013;9:277-84. | Link |
Anger KE, Degrado JR, Greenwood BC, Cohen SA, Szumita PM. Evaluation of recombinant activated protein C for severe sepsis at a tertiary academic medical center. Therapeutics and clinical risk management. 2013;9:277-84. | Link | Bollinger J, Coley K, Rea R, Saul M. Outcomes in patients with recombinant human activated protein c at an academic medical center versus the ENHANCE US trial. Crit Care Med 2006; 34: A111. | Link |
Bollinger J, Coley K, Rea R, Saul M. Outcomes in patients with recombinant human activated protein c at an academic medical center versus the ENHANCE US trial. Crit Care Med 2006; 34: A111. | Link | Wheeler A, Steingrub J, Schmidt GA, Sanchez P, Jacobi J, Linde-Zwirble W, Bates B, Qualy RL, Woodward B, Zeckel M. A retrospective observational study of drotrecogin alfa (activated) in adults with severe sepsis: comparison with a controlled clinical trial. Crit Care Med. 2008 Jan;36(1):14-23 | PubMed |
Wheeler A, Steingrub J, Schmidt GA, Sanchez P, Jacobi J, Linde-Zwirble W, Bates B, Qualy RL, Woodward B, Zeckel M. A retrospective observational study of drotrecogin alfa (activated) in adults with severe sepsis: comparison with a controlled clinical trial. Crit Care Med. 2008 Jan;36(1):14-23 | PubMed | Spriet I, Meersseman W, Wilmer A, Meyfroidt G, Casteels M, Willems L. Evaluation of drotrecogin alpha use in a Belgian university hospital. Pharm World Sci. 2006 Oct;28(5):290-5 | PubMed |
Spriet I, Meersseman W, Wilmer A, Meyfroidt G, Casteels M, Willems L. Evaluation of drotrecogin alpha use in a Belgian university hospital. Pharm World Sci. 2006 Oct;28(5):290-5 | PubMed | Rowan KM, Welch CA, North E, Harrison DA. Drotrecogin alfa (activated): real-life use and outcomes for the UK. Crit Care. 2008;12(2):R58 | CrossRef | PubMed |
Rowan KM, Welch CA, North E, Harrison DA. Drotrecogin alfa (activated): real-life use and outcomes for the UK. Crit Care. 2008;12(2):R58 | CrossRef | PubMed | Higgins TL, Steingrub JS, Tereso GJ, Tidswell MA, McGee WT. Drotrecogin alfa (activated) in sepsis: initial experience with patient selection, cost, and clinical outcomes. J Intensive Care Med. 2005 Nov-Dec;20(6):339-45 | PubMed |
Higgins TL, Steingrub JS, Tereso GJ, Tidswell MA, McGee WT. Drotrecogin alfa (activated) in sepsis: initial experience with patient selection, cost, and clinical outcomes. J Intensive Care Med. 2005 Nov-Dec;20(6):339-45 | PubMed | Ridley S, Lwin A, Wyncoll D, Lippett S, Watson D, Gunning K, Higgins D. Drotrecogin alfa (activated): diffusion from clinical trials to clinical practice. Eur J Anaesthesiol. 2008 Mar;25(3):211-6 | PubMed |
Ridley S, Lwin A, Wyncoll D, Lippett S, Watson D, Gunning K, Higgins D. Drotrecogin alfa (activated): diffusion from clinical trials to clinical practice. Eur J Anaesthesiol. 2008 Mar;25(3):211-6 | PubMed | Sadaka F, O'Brien J, Migneron M, Stortz J, Vanston A, Taylor RW. Activated protein C in septic shock: a propensity-matched analysis. Crit Care. 2011;15(2):R89 | CrossRef | PubMed |
Sadaka F, O'Brien J, Migneron M, Stortz J, Vanston A, Taylor RW. Activated protein C in septic shock: a propensity-matched analysis. Crit Care. 2011;15(2):R89 | CrossRef | PubMed | Ferrer R, Artigas A, Suarez D, Palencia E, Levy MM, Arenzana A, Pérez XL, Sirvent JM; Edusepsis Study Group.. Effectiveness of treatments for severe sepsis: a prospective, multicenter, observational study. Am J Respir Crit Care Med. 2009 Nov 1;180(9):861-6 | CrossRef | PubMed |
Ferrer R, Artigas A, Suarez D, Palencia E, Levy MM, Arenzana A, Pérez XL, Sirvent JM; Edusepsis Study Group.. Effectiveness of treatments for severe sepsis: a prospective, multicenter, observational study. Am J Respir Crit Care Med. 2009 Nov 1;180(9):861-6 | CrossRef | PubMed | Kübler A, Mayzner-Zawadzka E, Durek G, Gaszynski W, Karpel E, Mikaszewska-Sokolewicz M, Majak P. Results of severe sepsis treatment program using recombinant human activated protein C in Poland. Med Sci Monit. 2006 Mar;12(3):CR107-12 | PubMed |
Kübler A, Mayzner-Zawadzka E, Durek G, Gaszynski W, Karpel E, Mikaszewska-Sokolewicz M, Majak P. Results of severe sepsis treatment program using recombinant human activated protein C in Poland. Med Sci Monit. 2006 Mar;12(3):CR107-12 | PubMed | Maurice A, Seguin P, Aguillon D, Chanavaz C, Mallédant Y. [Activated protein C treatment: experience about 23 patients in the operative period]. Ann Fr Anesth Reanim. 2005 Apr;24(4):343-6 | PubMed |
Maurice A, Seguin P, Aguillon D, Chanavaz C, Mallédant Y. [Activated protein C treatment: experience about 23 patients in the operative period]. Ann Fr Anesth Reanim. 2005 Apr;24(4):343-6 | PubMed | Dhainaut JF, Payet S, Vallet B, França LR, Annane D, Bollaert PE, Le Tulzo Y, Runge I, Malledant Y, Guidet B, Le Lay K, Launois R; PREMISS Study Group. Cost-effectiveness of activated protein C in real-life clinical practice. Crit Care. 2007;11(5):R99 | PubMed |
Dhainaut JF, Payet S, Vallet B, França LR, Annane D, Bollaert PE, Le Tulzo Y, Runge I, Malledant Y, Guidet B, Le Lay K, Launois R; PREMISS Study Group. Cost-effectiveness of activated protein C in real-life clinical practice. Crit Care. 2007;11(5):R99 | PubMed | Vincent JL, Bernard GR, Beale R, Doig C, Putensen C, Dhainaut JF, Artigas A, Fumagalli R, Macias W, Wright T, Wong K, Sundin DP, Turlo MA, Janes J. Drotrecogin alfa (activated) treatment in severe sepsis from the global open-label trial ENHANCE: further evidence for survival and safety and implications for early treatment. Crit Care Med. 2005 Oct;33(10):2266-77 | PubMed |
Vincent JL, Bernard GR, Beale R, Doig C, Putensen C, Dhainaut JF, Artigas A, Fumagalli R, Macias W, Wright T, Wong K, Sundin DP, Turlo MA, Janes J. Drotrecogin alfa (activated) treatment in severe sepsis from the global open-label trial ENHANCE: further evidence for survival and safety and implications for early treatment. Crit Care Med. 2005 Oct;33(10):2266-77 | PubMed | Vincent JL, Laterre PF, Decruyenaere J, Spapen H, Raemaekers J, Damas F, Rogiers P, Sartral M, Haentjens T, Nelson D, Janes J. A registry of patients treated with drotrecogin alfa (activated) in Belgian intensive care units an observational study. Acta Clin Belg. 2008 Jan-Feb;63(1):25-30 | PubMed |
Vincent JL, Laterre PF, Decruyenaere J, Spapen H, Raemaekers J, Damas F, Rogiers P, Sartral M, Haentjens T, Nelson D, Janes J. A registry of patients treated with drotrecogin alfa (activated) in Belgian intensive care units an observational study. Acta Clin Belg. 2008 Jan-Feb;63(1):25-30 | PubMed | Ernst FR, Johnston JA, Pulgar S, He J, Ball DE, Young JK, Cooper LM. Timing of drotrecogin alfa (activated) initiation in treatment of severe sepsis: a database cohort study of hospital mortality, length of stay, and costs. Curr Med Res Opin. 2007 Jan;23(1):235-44 | PubMed |
Ernst FR, Johnston JA, Pulgar S, He J, Ball DE, Young JK, Cooper LM. Timing of drotrecogin alfa (activated) initiation in treatment of severe sepsis: a database cohort study of hospital mortality, length of stay, and costs. Curr Med Res Opin. 2007 Jan;23(1):235-44 | PubMed | Eli Lilly. An open label study of drotrecogin alfa (activated) in adult patients with severe sepsis and multiple organ dysfunctions, a phase IV protocol. 2006; Summary ID 7159: 1–6. | Link |
Eli Lilly. An open label study of drotrecogin alfa (activated) in adult patients with severe sepsis and multiple organ dysfunctions, a phase IV protocol. 2006; Summary ID 7159: 1–6. | Link | Macchiavello L, Ellis G, Bowden S, Smithies M. A large, single-centre UK registry of drotrecogin alfa-activated use. Crit Care 2007; 11 (suppl 2): 58. | Link |
Macchiavello L, Ellis G, Bowden S, Smithies M. A large, single-centre UK registry of drotrecogin alfa-activated use. Crit Care 2007; 11 (suppl 2): 58. | Link | Steingrub JS, Cheatham ML, Woodward B, Wang HT, Effron MB; XEUS Investigators.. A prospective, observational study of Xigris Use in the United States (XEUS). J Crit Care. 2010 Dec;25(4):660.e9-16 | CrossRef | PubMed |
Steingrub JS, Cheatham ML, Woodward B, Wang HT, Effron MB; XEUS Investigators.. A prospective, observational study of Xigris Use in the United States (XEUS). J Crit Care. 2010 Dec;25(4):660.e9-16 | CrossRef | PubMed | Bernard GR, Vincent JL, Laterre PF, et al, and the Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group. Effi cacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med 2001; 344: 699–709. | CrossRef | PubMed | Link |
Bernard GR, Vincent JL, Laterre PF, et al, and the Recombinant human protein C Worldwide Evaluation in Severe Sepsis (PROWESS) study group. Effi cacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med 2001; 344: 699–709. | CrossRef | PubMed | Link | Bernard GR, Macias WL, Joyce DE,Williams MD, Bailey J, Vincent JL. Safety assessment of drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis. Critical Care 2003;7(2):155–63. | PubMed |
Bernard GR, Macias WL, Joyce DE,Williams MD, Bailey J, Vincent JL. Safety assessment of drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis. Critical Care 2003;7(2):155–63. | PubMed | Bernard G, Margolis B, Shanies H, Ely E, Wheeler A, Levy H. Efficacy and safety of References 66 drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis: report from a single open-label trial in the United States 2002. | Link |
Bernard G, Margolis B, Shanies H, Ely E, Wheeler A, Levy H. Efficacy and safety of References 66 drotrecogin alfa (activated) in the treatment of adult patients with severe sepsis: report from a single open-label trial in the United States 2002. | Link | Eli Lilly. Xigris NICE submission: drotrecogin alfa (activated) for severe sepsis. Basingstoke: Eli Lilly; 2003. | Link |
Eli Lilly. Xigris NICE submission: drotrecogin alfa (activated) for severe sepsis. Basingstoke: Eli Lilly; 2003. | Link |Systematization of initiatives in sexual and reproductive health about good practices criteria in response to the COVID-19 pandemic in primary health care in Chile
Clinical, psychological, social, and family characterization of suicidal behavior in Chilean adolescents: a multiple correspondence analysis








