Introducción
Los estudios de cohorte corresponden a diseños observacionales en los que se sigue en el tiempo a un grupo de sujetos que tienen una o varias características comunes. En estos diseños se realizan mediciones periódicas para ver si aparece algún desenlace, evento o enfermedad en estudio[1],[2],[3],[4]. Existe un origen histórico para su denominación, en las legiones romanas se llamaba cohorte (cohors) a seis centurias de soldados marchando en el campo de batalla hacia diferentes destinos, los que variaban según el grupo al que pertenecían[2],[5]. Esta situación es muy similar a lo que sucede en este tipo de diseño, en que grupos de individuos avanzan hacia un desenlace cuya frecuencia puede estar determinada por uno o más factores a los que están expuestos.
El diseño es parecido al de los ensayos clínicos, considerados los más adecuados para la inferencia causal[13] . No obstante, una gran diferencia es que la exposición ocurre naturalmente, siendo determinada por preferencias, decisiones clínicas u otras condiciones. En los ensayos clínicos, lo último es asignado directamente por el investigador[6].
Bajo esta perspectiva, las cohortes se consideran diseños prospectivos y analíticos[2],[3]. Sin embargo, también es posible encontrar versiones retrospectivas, en las que los investigadores recolectan datos existentes entre pacientes que presentaron o no un desenlace. Dado que existe un proceso de seguimiento desde una exposición a un evento, la denominación cohorte también aplica a este último diseño. La gran diferencia con los estudios de casos y los controles, es que las cohortes a contrastar son separadas sobre la base de la exposición a un factor y no al desenlace. Una tercera variante, la ambidireccional, implica una recolección de datos en ambas direcciones que toma datos existentes, por ejemplo en fichas clínicas, y luego realiza seguimiento a los pacientes incluidos hasta el desarrollo de un evento.
Ambas cohortes deberían ser similares en todos los aspectos relevantes, situación muy difícil de lograr en estos estudios por su naturaleza observacional. Esto las hace susceptibles a sesgos de confusión, en los que otras variables, distintas a la exposición en estudio, puedan explicar los resultados[6].
En la Tabla I presentamos una comparación entre los aspectos positivos y las complejidades que presenta el diseño de cohorte.
Tabla I. Cuadro comparativo ventajas/desventajas del diseńo de cohorte.
Seleccionando la muestra
La adecuada selección de los participantes, el registro riguroso de los eventuales factores de exposición y el control periódico y objetivo de la aparición de eventos, constituyen la clave del buen desarrollo de este tipo de estudios[2],[3],[4].
Los individuos pueden corresponder a una población general, como fue el estudio Framingham que aportó información clave sobre factores de riesgo cardiovascular14-26, o de grupos sociales específicos[7],[8],[9],[11],[12], como una cohorte de 40.633 médicos ingleses que estableció la asociación entre tabaquismo y varios eventos de interés[10],[27],[28],[29],[30],[31],[32],[33].
Una cohorte también puede ser seleccionada debido a una exposición específica como contaminación ambiental, radiaciones, o peligros ocupacionales. En estos casos, en que no pueden evaluarse experimentalmente por razones éticas, es el diseño ideal[4].
Aspectos sobre la calidad
El primer aspecto a evaluar en un estudio de cohortes es la similitud de los grupos contrastados. Ello se logra mediante la tabla de características de los individuos estudiados, que debiera reportarse en todo estudio de esta naturaleza. En caso de existir desbalances, ciertas técnicas estadísticas de análisis multivariado, como las regresiones, permitirán ajustar los análisis a las diferencias entre grupos.
En septiembre de 2004 se realizó un panel de expertos que emitió una lista de verificación consensuada para reportar estudios observacionales, denominada iniciativa STROBE (STrengthening the Reporting of OBservational studies in Epidemiology). Se trata de una lista de chequeo para el título, resumen, introducción y las secciones de métodos, resultados y discusión de los artículos[35]. La iniciativa STROBE está concebida para ser una lista de comprobación del reporte y en ningún caso es un instrumento para probar la calidad del estudio observacional. Para ello existen otras herramientas[36].
Luego, el investigador debe entregar las medidas de asociación relacionadas con sus hipótesis primarias y secundarias, proveyendo datos crudos suficientes como para que cualquier lector pueda confirmar las medidas de asociación informadas[4]. Es preferible reportar medidas de asociación con intervalos de confianza del 95% en lugar de valores p de contraste de hipótesis[34].
Estableciendo asociaciones
Las medidas de asociación en estudios de cohorte pueden expresarse como probabilidades (riesgos), cuando todos los individuos son seguidos por el mismo periodo de tiempo. También pueden expresarse como tasas cuando el seguimiento de los sujetos no es el mismo, usando una medida de personas/tiempo en el denominador. La forma de cálculo de estas medidas se muestra en la Figura 1.
Así, como en los ensayos clínicos, es deseable que los estudios de cohorte resguarden una potencia estadística suficiente para detectar las asociaciones que esperan detectar.
Figura 1. Principales medidas de riesgo en estudios longitudinales.
Síntesis
Los estudios de cohorte son diseños observacionales que han aportado enormemente al conocimiento biomédico. Tienen limitaciones inherentes, por lo que los lectores deben asegurarse que suficientes medidas de control, como con los sesgos de confusión, sean provistas por los investigadores.
Existen guías estandarizadas que asisten en la evaluación de la calidad, tanto del reporte como de la investigación misma.
Notas
Declaración de conflictos de intereses
Los autores han completado el formulario de declaración de conflictos de intereses del ICMJE traducido al castellano por Medwave, y declaran no haber recibido financiamiento para la realización del artículo; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado, en los últimos tres años; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. Los formularios pueden ser solicitados contactando al autor responsable.

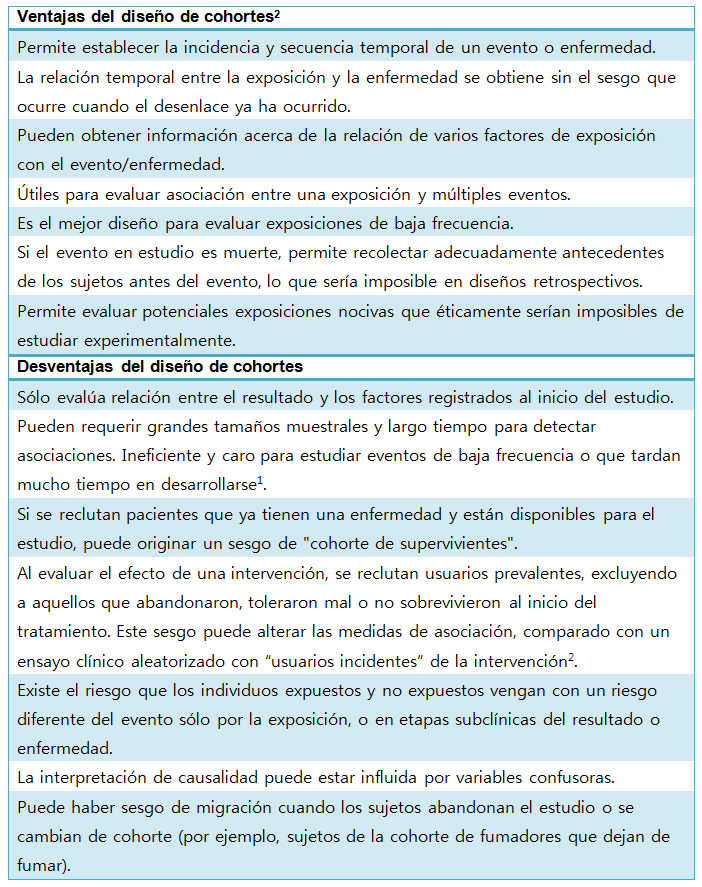 Tabla I. Cuadro comparativo ventajas/desventajas del diseńo de cohorte.
Tabla I. Cuadro comparativo ventajas/desventajas del diseńo de cohorte.

 Figura 1. Principales medidas de riesgo en estudios longitudinales.
Figura 1. Principales medidas de riesgo en estudios longitudinales.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Authors:
Eva Madrid Aris[1], Felipe Martínez Lomakin[1,2]
Authors:
Eva Madrid Aris[1], Felipe Martínez Lomakin[1,2]
Affiliation:
[1] Centro de Investigaciones Biomédicas, Escuela de Medicina, Universidad de Valparaíso, Chile
[2] M.Sc. Programme in Evidence-Based Healthcare, University of Oxford
E-mail: eva.madrid@uv.cl
Author address:
[1] Hontaneda 2664
Edificio Dr. Bruno Günther Schaffeld
Valparaíso

Citation: Madrid E, Martínez F. . Medwave 2014;14(1):e5877 doi: 10.5867/medwave.2014.01.5877
Submission date: 25/12/2013
Acceptance date: 25/12/2013
Publication date: 2/1/2014

Comments (0)
We are pleased to have your comment on one of our articles. Your comment will be published as soon as it is posted. However, Medwave reserves the right to remove it later if the editors consider your comment to be: offensive in some sense, irrelevant, trivial, contains grammatical mistakes, contains political harangues, appears to be advertising, contains data from a particular person or suggests the need for changes in practice in terms of diagnostic, preventive or therapeutic interventions, if that evidence has not previously been published in a peer-reviewed journal.
No comments on this article.
To comment please log in
 Medwave provides HTML and PDF download counts as well as other harvested interaction metrics.
Medwave provides HTML and PDF download counts as well as other harvested interaction metrics. There may be a 48-hour delay for most recent metrics to be posted.

- Grimes DA, Schulz KF. An overview of clinical research: the lay of the land. Lancet. 2002 Jan 5;359(9300):57-61. | CrossRef | PubMed |
- Grimes DA, Schulz KF. Cohort studies: marching towards outcomes. Lancet. 2002 Jan 26;359(9303):341-5. | CrossRef | PubMed |
- Cummings SR, Newman TB, Hulley SB. Designing a cohort study. En: Designing clinical research. Philadelphia, PA: Lippincott Williams & Wilkins, 2005:97-106.
- Dos Santos Silva I. Cancer Epidemiology: Principles and Methods. Lyon, France: International Agency for Research on Cancer, 1999.
- César CJ. La Guerra de las Galias: Alianza Editorial, 2002.
- Carlson MD, Morrison RS. Study design, precision, and validity in observational studies. J Palliat Med. 2009 Jan;12(1):77-82. | CrossRef | PubMed | PMC |
- Beasley RP, Hwang LY, Lin CC, Chien CS. Hepatocellular carcinoma and hepatitis B virus. Lancet. 1981 Nov;2(8256):1129-33. | CrossRef | PubMed |
- D'Agostino RB Sr, Vasan RS, Pencina MJ, Wolf PA, Cobain M, Massaro JM, et al. General cardiovascular risk profile for use in primary care: the Framingham Heart Study. Circulation. 2008 Feb 12;117(6):743-53. | CrossRef | PubMed |
- Beral V, Hermon C, Kay C, Hannaford P, Darby S, Reeves G. Mortality associated with oral contraceptive use: 25 year follow up of cohort of 46 000 women from Royal College of General Practitioners' oral contraception study. BMJ. 1999 Jan 9;318(7176):96-100. | CrossRef | PubMed | PMC |
- Doll R, Peto R, Boreham J, Sutherland I. Mortality from cancer in relation to smoking: 50 years observations on British doctors. Br J Cancer. 2005 Feb 14;92(3):426-9. | CrossRef | PubMed | PMC |
- Eriksson JG, Forsén T, Tuomilehto J, Osmond C, Barker DJ. Early growth and coronary heart disease in later life: longitudinal study. BMJ. 2001 Apr 21;322(7292):949-53. | CrossRef | PubMed | PMC |
- Barker DJ, Forsén T, Uutela A, Osmond C, Eriksson JG. Size at birth and resilience to effects of poor living conditions in adult life: longitudinal study. BMJ. 2001 Dec 1;323(7324):1273-6. | CrossRef | PubMed | PMC |
- Rubin DB. The design versus the analysis of observational studies for causal effects: parallels with the design of randomized trials. StatMed. 2007 Jan 15;26(1):20-36. | CrossRef | PubMed |
- Kim KS, Owen WL, Williams D, Adams-Campbell LL. A comparison between BMI and Conicity index on predicting coronary heart disease: the Framingham heart study. Ann Epidemiol. 2000 Oct;10(7):424-31. | CrossRef | PubMed |
- Kannel WB, McGee D, Gordon T. A general cardiovascular risk profile: the Framingham Study. Am J Cardiol. 1976 Jul;38(1):46-51. | CrossRef | PubMed |
- Truett J, Cornfield J, Kannel W. A multivariate analysis of the risk of coronary heart disease in Framingham. J Chronic Dis. 1967 Jul;20(7):511-24. | CrossRef | PubMed |
- Parikh NI, Pencina MJ, Wang TJ, Benjamin EJ, Lanier KJ, Levy D, et al. A risk score for predicting near-term incidence of hypertension: the Framingham Heart Study. Ann InternMed. 2008 Jan 15;148(2):102-10. | CrossRef | PubMed |
- Wolf PA, Kannel WB, Sorlie P, McNamara P. Asymptomatic carotid bruit and risk of stroke. The Framingham study.JAMA. 1981 Apr 10;245(14):1442-5. | CrossRef | PubMed |
- Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke: the Framingham Study. Stroke. 1991 Aug;22(8):983-8. | CrossRef | PubMed |
- Stokes J 3rd, Kannel WB, Wolf PA, D'Agostino RB, Cupples LA. Blood pressure as a risk factor for cardiovascular disease. The Framingham Study--30 years of follow-up. Hypertension. 1989 May;13(5 Suppl):I13-8. | CrossRef | PubMed |
- Kannel WB. CHD risk factors: a Framingham study update. HospPract (Off Ed). 1990 Jul 15;25(7):119-27, 130. | PubMed |
- Kannel WB, Castelli WP, McNamara PM. Cigarette smoking and risk of coronary heart disease. Epidemiologic clues to pathogensis. The Framingham Study. Natl Cancer InstMonogr. 1968 Jun;28:9-20. | PubMed |
- Wolf PA, D'Agostino RB, Kannel WB, Bonita R, Belanger AJ. Cigarette smoking as a risk factor for stroke. The Framingham study. JAMA. 1988 Feb 19;259(7):1025-9. | CrossRef | PubMed |
- Kannel WB, McGee DL. Diabetes and cardiovascular risk factors: the Framingham study. Circulation. 1979 Jan;59(1):8-13. | CrossRef | PubMed |
- Franklin SS, Larson MG, Khan SA, Wong ND, Leip EP, Kannel WB, et al. Does the relation of blood pressure to coronary heart disease risk change with aging? The Framingham Heart Study. Circulation. 2001 Mar 6;103(9):1245-9. | CrossRef | PubMed |
- D'Agostino RB, Kannel WB, Belanger AJ, Sytkowski PA. Trends in CHD and risk factors at age 55-64 in the Framingham Study. Int J Epidemiol. 1989;18(3 Suppl 1):S67-72. | CrossRef | PubMed |
- Doll R, Peto R, Hall E, Wheatley K, Gray R. Alcohol and coronary heart disease reduction among British doctors: confounding or causality? Eur Heart J. 1997 Jan;18(1):23-5. | CrossRef | PubMed |
- Doll R, Peto R. Cigarette smoking and bronchial carcinoma: dose and time relationships among regular smokers and lifelong non-smokers. J Epidemiol Community Health. 1978 Dec;32(4):303-13. | CrossRef | PubMed | PMC |
- Doll R, Peto R. Mortality among doctors in different occupations. Br Med J. 1977 Jun 4;1(6074):1433-6. | CrossRef | PubMed | PMC |
- Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to alcohol consumption: a prospective study among male British doctors. Int J Epidemiol. 2005 Feb;34(1):199-204. | CrossRef | PubMed |
- Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to smoking: 50 years' observations on male British doctors. BMJ. 2004 Jun 26;328(7455):1519. | CrossRef | PubMed | PMC |
- Schauffler HH, D'Agostino RB, Kannel WB. Risk for cardiovascular disease in the elderly and associated Medicare costs: the Framingham Study. Am J Prev Med. 1993 May-Jun;9(3):146-54. | PubMed |
- Doll R, Peto R, Boreham J, Sutherland I. Smoking and dementia in male British doctors: prospective study.BMJ. 2000 Apr;320(7242):1097-102. | CrossRef | PubMed | PMC |
- Sackett DL, Deeks JJ, Altman DG. Down withodds ratios! Evidence-based Medicine. Sep-Oct 1996;6(1):164-66. | Link |
- von Elm E, Altman DG, Egger M, Pocock SJ, Gřtzsche PC, Vandenbroucke JP. The Strengthening the reporting of observational studies in epidemiology (STROBE) statement: guidelines for reporting observational studies. Lancet. 2007 Oct 20;370(9596):1453-7. | CrossRef | PubMed |
- Sanderson S, Tatt ID, Higgins JP. Tools for assessing quality and susceptibility to bias in observational studies in epidemiology: a systematic review and annotated bibliography. Int J Epidemiol. 2007 Jun;36(3):666-76. | CrossRef | PubMed |
 Grimes DA, Schulz KF. An overview of clinical research: the lay of the land. Lancet. 2002 Jan 5;359(9300):57-61. | CrossRef | PubMed |
Grimes DA, Schulz KF. An overview of clinical research: the lay of the land. Lancet. 2002 Jan 5;359(9300):57-61. | CrossRef | PubMed | Grimes DA, Schulz KF. Cohort studies: marching towards outcomes. Lancet. 2002 Jan 26;359(9303):341-5. | CrossRef | PubMed |
Grimes DA, Schulz KF. Cohort studies: marching towards outcomes. Lancet. 2002 Jan 26;359(9303):341-5. | CrossRef | PubMed | Cummings SR, Newman TB, Hulley SB. Designing a cohort study. En: Designing clinical research. Philadelphia, PA: Lippincott Williams & Wilkins, 2005:97-106.
Cummings SR, Newman TB, Hulley SB. Designing a cohort study. En: Designing clinical research. Philadelphia, PA: Lippincott Williams & Wilkins, 2005:97-106.  Dos Santos Silva I. Cancer Epidemiology: Principles and Methods. Lyon, France: International Agency for Research on Cancer, 1999.
Dos Santos Silva I. Cancer Epidemiology: Principles and Methods. Lyon, France: International Agency for Research on Cancer, 1999.  César CJ. La Guerra de las Galias: Alianza Editorial, 2002.
César CJ. La Guerra de las Galias: Alianza Editorial, 2002.  Carlson MD, Morrison RS. Study design, precision, and validity in observational studies. J Palliat Med. 2009 Jan;12(1):77-82. | CrossRef | PubMed | PMC |
Carlson MD, Morrison RS. Study design, precision, and validity in observational studies. J Palliat Med. 2009 Jan;12(1):77-82. | CrossRef | PubMed | PMC | Beasley RP, Hwang LY, Lin CC, Chien CS. Hepatocellular carcinoma and hepatitis B virus. Lancet. 1981 Nov;2(8256):1129-33. | CrossRef | PubMed |
Beasley RP, Hwang LY, Lin CC, Chien CS. Hepatocellular carcinoma and hepatitis B virus. Lancet. 1981 Nov;2(8256):1129-33. | CrossRef | PubMed | D'Agostino RB Sr, Vasan RS, Pencina MJ, Wolf PA, Cobain M, Massaro JM, et al. General cardiovascular risk profile for use in primary care: the Framingham Heart Study. Circulation. 2008 Feb 12;117(6):743-53. | CrossRef | PubMed |
D'Agostino RB Sr, Vasan RS, Pencina MJ, Wolf PA, Cobain M, Massaro JM, et al. General cardiovascular risk profile for use in primary care: the Framingham Heart Study. Circulation. 2008 Feb 12;117(6):743-53. | CrossRef | PubMed | Beral V, Hermon C, Kay C, Hannaford P, Darby S, Reeves G. Mortality associated with oral contraceptive use: 25 year follow up of cohort of 46 000 women from Royal College of General Practitioners' oral contraception study. BMJ. 1999 Jan 9;318(7176):96-100. | CrossRef | PubMed | PMC |
Beral V, Hermon C, Kay C, Hannaford P, Darby S, Reeves G. Mortality associated with oral contraceptive use: 25 year follow up of cohort of 46 000 women from Royal College of General Practitioners' oral contraception study. BMJ. 1999 Jan 9;318(7176):96-100. | CrossRef | PubMed | PMC | Doll R, Peto R, Boreham J, Sutherland I. Mortality from cancer in relation to smoking: 50 years observations on British doctors. Br J Cancer. 2005 Feb 14;92(3):426-9. | CrossRef | PubMed | PMC |
Doll R, Peto R, Boreham J, Sutherland I. Mortality from cancer in relation to smoking: 50 years observations on British doctors. Br J Cancer. 2005 Feb 14;92(3):426-9. | CrossRef | PubMed | PMC | Eriksson JG, Forsén T, Tuomilehto J, Osmond C, Barker DJ. Early growth and coronary heart disease in later life: longitudinal study. BMJ. 2001 Apr 21;322(7292):949-53. | CrossRef | PubMed | PMC |
Eriksson JG, Forsén T, Tuomilehto J, Osmond C, Barker DJ. Early growth and coronary heart disease in later life: longitudinal study. BMJ. 2001 Apr 21;322(7292):949-53. | CrossRef | PubMed | PMC | Barker DJ, Forsén T, Uutela A, Osmond C, Eriksson JG. Size at birth and resilience to effects of poor living conditions in adult life: longitudinal study. BMJ. 2001 Dec 1;323(7324):1273-6. | CrossRef | PubMed | PMC |
Barker DJ, Forsén T, Uutela A, Osmond C, Eriksson JG. Size at birth and resilience to effects of poor living conditions in adult life: longitudinal study. BMJ. 2001 Dec 1;323(7324):1273-6. | CrossRef | PubMed | PMC | Rubin DB. The design versus the analysis of observational studies for causal effects: parallels with the design of randomized trials. StatMed. 2007 Jan 15;26(1):20-36. | CrossRef | PubMed |
Rubin DB. The design versus the analysis of observational studies for causal effects: parallels with the design of randomized trials. StatMed. 2007 Jan 15;26(1):20-36. | CrossRef | PubMed | Kim KS, Owen WL, Williams D, Adams-Campbell LL. A comparison between BMI and Conicity index on predicting coronary heart disease: the Framingham heart study. Ann Epidemiol. 2000 Oct;10(7):424-31. | CrossRef | PubMed |
Kim KS, Owen WL, Williams D, Adams-Campbell LL. A comparison between BMI and Conicity index on predicting coronary heart disease: the Framingham heart study. Ann Epidemiol. 2000 Oct;10(7):424-31. | CrossRef | PubMed | Kannel WB, McGee D, Gordon T. A general cardiovascular risk profile: the Framingham Study. Am J Cardiol. 1976 Jul;38(1):46-51. | CrossRef | PubMed |
Kannel WB, McGee D, Gordon T. A general cardiovascular risk profile: the Framingham Study. Am J Cardiol. 1976 Jul;38(1):46-51. | CrossRef | PubMed | Truett J, Cornfield J, Kannel W. A multivariate analysis of the risk of coronary heart disease in Framingham. J Chronic Dis. 1967 Jul;20(7):511-24. | CrossRef | PubMed |
Truett J, Cornfield J, Kannel W. A multivariate analysis of the risk of coronary heart disease in Framingham. J Chronic Dis. 1967 Jul;20(7):511-24. | CrossRef | PubMed | Parikh NI, Pencina MJ, Wang TJ, Benjamin EJ, Lanier KJ, Levy D, et al. A risk score for predicting near-term incidence of hypertension: the Framingham Heart Study. Ann InternMed. 2008 Jan 15;148(2):102-10. | CrossRef | PubMed |
Parikh NI, Pencina MJ, Wang TJ, Benjamin EJ, Lanier KJ, Levy D, et al. A risk score for predicting near-term incidence of hypertension: the Framingham Heart Study. Ann InternMed. 2008 Jan 15;148(2):102-10. | CrossRef | PubMed | Wolf PA, Kannel WB, Sorlie P, McNamara P. Asymptomatic carotid bruit and risk of stroke. The Framingham study.JAMA. 1981 Apr 10;245(14):1442-5. | CrossRef | PubMed |
Wolf PA, Kannel WB, Sorlie P, McNamara P. Asymptomatic carotid bruit and risk of stroke. The Framingham study.JAMA. 1981 Apr 10;245(14):1442-5. | CrossRef | PubMed | Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke: the Framingham Study. Stroke. 1991 Aug;22(8):983-8. | CrossRef | PubMed |
Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke: the Framingham Study. Stroke. 1991 Aug;22(8):983-8. | CrossRef | PubMed | Stokes J 3rd, Kannel WB, Wolf PA, D'Agostino RB, Cupples LA. Blood pressure as a risk factor for cardiovascular disease. The Framingham Study--30 years of follow-up. Hypertension. 1989 May;13(5 Suppl):I13-8. | CrossRef | PubMed |
Stokes J 3rd, Kannel WB, Wolf PA, D'Agostino RB, Cupples LA. Blood pressure as a risk factor for cardiovascular disease. The Framingham Study--30 years of follow-up. Hypertension. 1989 May;13(5 Suppl):I13-8. | CrossRef | PubMed | Kannel WB. CHD risk factors: a Framingham study update. HospPract (Off Ed). 1990 Jul 15;25(7):119-27, 130. | PubMed |
Kannel WB. CHD risk factors: a Framingham study update. HospPract (Off Ed). 1990 Jul 15;25(7):119-27, 130. | PubMed | Kannel WB, Castelli WP, McNamara PM. Cigarette smoking and risk of coronary heart disease. Epidemiologic clues to pathogensis. The Framingham Study. Natl Cancer InstMonogr. 1968 Jun;28:9-20. | PubMed |
Kannel WB, Castelli WP, McNamara PM. Cigarette smoking and risk of coronary heart disease. Epidemiologic clues to pathogensis. The Framingham Study. Natl Cancer InstMonogr. 1968 Jun;28:9-20. | PubMed | Wolf PA, D'Agostino RB, Kannel WB, Bonita R, Belanger AJ. Cigarette smoking as a risk factor for stroke. The Framingham study. JAMA. 1988 Feb 19;259(7):1025-9. | CrossRef | PubMed |
Wolf PA, D'Agostino RB, Kannel WB, Bonita R, Belanger AJ. Cigarette smoking as a risk factor for stroke. The Framingham study. JAMA. 1988 Feb 19;259(7):1025-9. | CrossRef | PubMed | Kannel WB, McGee DL. Diabetes and cardiovascular risk factors: the Framingham study. Circulation. 1979 Jan;59(1):8-13. | CrossRef | PubMed |
Kannel WB, McGee DL. Diabetes and cardiovascular risk factors: the Framingham study. Circulation. 1979 Jan;59(1):8-13. | CrossRef | PubMed | Franklin SS, Larson MG, Khan SA, Wong ND, Leip EP, Kannel WB, et al. Does the relation of blood pressure to coronary heart disease risk change with aging? The Framingham Heart Study. Circulation. 2001 Mar 6;103(9):1245-9. | CrossRef | PubMed |
Franklin SS, Larson MG, Khan SA, Wong ND, Leip EP, Kannel WB, et al. Does the relation of blood pressure to coronary heart disease risk change with aging? The Framingham Heart Study. Circulation. 2001 Mar 6;103(9):1245-9. | CrossRef | PubMed | D'Agostino RB, Kannel WB, Belanger AJ, Sytkowski PA. Trends in CHD and risk factors at age 55-64 in the Framingham Study. Int J Epidemiol. 1989;18(3 Suppl 1):S67-72. | CrossRef | PubMed |
D'Agostino RB, Kannel WB, Belanger AJ, Sytkowski PA. Trends in CHD and risk factors at age 55-64 in the Framingham Study. Int J Epidemiol. 1989;18(3 Suppl 1):S67-72. | CrossRef | PubMed | Doll R, Peto R, Hall E, Wheatley K, Gray R. Alcohol and coronary heart disease reduction among British doctors: confounding or causality? Eur Heart J. 1997 Jan;18(1):23-5. | CrossRef | PubMed |
Doll R, Peto R, Hall E, Wheatley K, Gray R. Alcohol and coronary heart disease reduction among British doctors: confounding or causality? Eur Heart J. 1997 Jan;18(1):23-5. | CrossRef | PubMed | Doll R, Peto R. Cigarette smoking and bronchial carcinoma: dose and time relationships among regular smokers and lifelong non-smokers. J Epidemiol Community Health. 1978 Dec;32(4):303-13. | CrossRef | PubMed | PMC |
Doll R, Peto R. Cigarette smoking and bronchial carcinoma: dose and time relationships among regular smokers and lifelong non-smokers. J Epidemiol Community Health. 1978 Dec;32(4):303-13. | CrossRef | PubMed | PMC | Doll R, Peto R. Mortality among doctors in different occupations. Br Med J. 1977 Jun 4;1(6074):1433-6. | CrossRef | PubMed | PMC |
Doll R, Peto R. Mortality among doctors in different occupations. Br Med J. 1977 Jun 4;1(6074):1433-6. | CrossRef | PubMed | PMC | Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to alcohol consumption: a prospective study among male British doctors. Int J Epidemiol. 2005 Feb;34(1):199-204. | CrossRef | PubMed |
Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to alcohol consumption: a prospective study among male British doctors. Int J Epidemiol. 2005 Feb;34(1):199-204. | CrossRef | PubMed | Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to smoking: 50 years' observations on male British doctors. BMJ. 2004 Jun 26;328(7455):1519. | CrossRef | PubMed | PMC |
Doll R, Peto R, Boreham J, Sutherland I. Mortality in relation to smoking: 50 years' observations on male British doctors. BMJ. 2004 Jun 26;328(7455):1519. | CrossRef | PubMed | PMC | Schauffler HH, D'Agostino RB, Kannel WB. Risk for cardiovascular disease in the elderly and associated Medicare costs: the Framingham Study. Am J Prev Med. 1993 May-Jun;9(3):146-54. | PubMed |
Schauffler HH, D'Agostino RB, Kannel WB. Risk for cardiovascular disease in the elderly and associated Medicare costs: the Framingham Study. Am J Prev Med. 1993 May-Jun;9(3):146-54. | PubMed | Doll R, Peto R, Boreham J, Sutherland I. Smoking and dementia in male British doctors: prospective study.BMJ. 2000 Apr;320(7242):1097-102. | CrossRef | PubMed | PMC |
Doll R, Peto R, Boreham J, Sutherland I. Smoking and dementia in male British doctors: prospective study.BMJ. 2000 Apr;320(7242):1097-102. | CrossRef | PubMed | PMC | Sackett DL, Deeks JJ, Altman DG. Down withodds ratios! Evidence-based Medicine. Sep-Oct 1996;6(1):164-66. | Link |
Sackett DL, Deeks JJ, Altman DG. Down withodds ratios! Evidence-based Medicine. Sep-Oct 1996;6(1):164-66. | Link |Systematization of initiatives in sexual and reproductive health about good practices criteria in response to the COVID-19 pandemic in primary health care in Chile
Clinical, psychological, social, and family characterization of suicidal behavior in Chilean adolescents: a multiple correspondence analysis








