El carcinoma de células escamosas de la cavidad oral es el cáncer más relevante para los cirujanos dentistas. Es uno de los 10 cánceres más comunes en el planeta, con una detección clínica tardía, pobre pronóstico, con alterativas terapéuticas de alto costo y desfigurantes [1]. Lamentablemente, hasta el día de hoy no se cuenta con biomarcadores específicos para la enfermedad.
El término biomarcador corresponde a una amplia subcategoría de signos médicos que se pueden medir de forma precisa y reproducible. Los biomarcadores corresponden a características cuantificables de los procesos biológicos [2]. En general, éstos pueden clasificarse en:
i) Farmacodinámicos: indicadores de la interacción de un fármaco y su blanco.
ii) Pronósticos: indican el curso probable de una enfermedad.
iii) Predictivos: pacientes con probabilidades de responder a un tratamiento en particular [3].
Con el florecimiento de la era de las ómicas, miles de potenciales biomarcadores han sido identificados y publicados. Ello supone un aumento de oportunidades para mejores diagnósticos, desarrollo de tratamientos más eficaces y un mejor pronóstico para el cáncer. Pese a lo auspicioso de las ómicas, en 2011 se estimaba que más de 150 mil manuscritos documentaban igual o superior número de biomarcadores. Sin embargo, hasta esa fecha menos de 100 fueron validados en la práctica clínica rutinaria [4]. Sumado a lo anterior, recientemente el proyecto del Atlas del Genoma del Cáncer mostró que una gran batería de información genómica y proteómica no mejoraba el potencial pronóstico de las variables clínicas en pacientes con diferentes tipos de cáncer [5].
Ciertamente los potenciales biomarcadores deben recorrer un difícil camino para colaborar con la clínica y beneficiar a los pacientes. Las mayores limitaciones que debe resolver el proceso investigativo para la determinación de los candidatos son las fallas en el diseño, ejecución e instrumentos de medición del estudio y en el campo de la validación, la pobre sensibilidad y especificidad [3]. A ello se puede sumar la dificultad financiera para conducir estudios de largo aliento y lograr las validaciones, la presión productiva hacia los equipos de investigación (resultados en corto tiempo), y el desencuentro de la ciencia básica con la clínica (carencia de integración y fisiopatología de sistemas).
Para mejorar la calidad de investigación en biomarcadores, la Early Detection Research Network del National Cancer Institute de Estados Unidos, dispone de guías para el diseño de estudios (http://edrn.nci.nih.gov/researchers/study-design-guidance-tools). De acuerdo con estas publicaciones, por ejemplo, si se quiere identificar biomarcadores en saliva de pacientes con riesgo o diagnóstico de cáncer oral (un área promisoria en la investigación del carcinoma de células escamosas de la cavidad oral), las muestras biológicas sólo podrían ser descongeladas una vez desde que fueron recolectadas y luego deben ser descartadas.
Conforme a directrices recientes, para que un candidato a biomarcador llegue potencialmente a la clínica debe necesariamente recorrer los siguientes pasos:
i) Validación analítica del ensayo para el biomarcador.
ii) Validación clínica para el test del biomarcador.
iii) Demostración del valor clínico de las pruebas para el biomarcador.
iv) Aprobación regulatoria [6].
¿Qué oportunidades ofrece el carcinoma de células escamosas de la cavidad oral a biomarcadores emergentes? Pese a que la cavidad oral es un territorio anatómico relativamente accesible para el examen, el cáncer oral se diagnostica en etapas clínicas avanzadas, lo que es un desafío y una llamada de atención para la comunidad odontológica. La detección del carcinoma de células escamosas de la cavidad oral es eminentemente visual y la confirmación es histopatológica. La evidencia actual muestra que esto no basta, lo que justifica la necesidad de biomarcadores.
La Figura 1 resume la “historia natural” del carcinoma de células escamosas de la cavidad oral. La exposición de la mucosa oral a un conjunto de factores de riesgo como el tabaco, el alcohol, el virus de papiloma humano, la radiación solar (exposoma) y su interacción (interactoma), genera queratinocitos aberrantes con ventajas ecológicas sobre el resto del microambiente. La inestabilidad génica creciente crea un campo de susceptibilidad para la neoplasia maligna, que puede ser representada por lesiones precursoras epiteliales. Éstas, finalmente abarcan completamente los estratos celulares hasta la degradación de la membrana basal y la invasión.
Figura 1. Historia natural del carcinoma de células escamosas de la cavidad oral.
Es esta historia natural la que presenta ventanas para el abordaje del carcinoma de células escamosas de la cavidad oral y el origen de los biomarcadores. La “historia natural” del cáncer oral permite el estudio de diferentes fases en la progresión de la neoplasia maligna. Una de las oportunidades está dada por la generación de un campo etiológico, influenciado por los factores de riesgo y sus interacciones, que promueve un estado de susceptibilidad. El paso de este estado de susceptibilidad hacia un campo cancerizable, otorga otra oportunidad de estudio. Una vez establecida la invasión, desde el diagnóstico de cáncer oral pueden emerger biomarcadores pronósticos y predictivos.
En este contexto, algunas de las preguntas que podrían o deberían ser respondidas, son: ¿Qué características cuantificables son representativas de un epitelio susceptible al carcinoma de células escamosas de la cavidad oral? ¿Se puede monitorear el paso de un estado de susceptibilidad a un campo epitelial cancerizable? ¿Es posible registrar procesos biológicos previos a las aberraciones moleculares? ¿Son las aberraciones moleculares permanentes, pese a la terapia? La boca aporta un acceso poco dificultoso para estas directrices.
Para quienes trabajan con biología molecular del cáncer oral, cursando día a día con la búsqueda biomarcadores tumorales, pretendiendo un mejor conocimiento del comportamiento tumoral, éstas son preguntas permanentes. Por nombrar una ómica, la proteómica está constantemente repensando sus diseños experimentales y buscando la validación. Es altamente probable que en un futuro cercano disminuyan las publicaciones presentando potenciales biomarcadores y aumenten aquellas con alguna oportunidad clínica. Es lo que pretenden diferentes grupos de estudios de biomarcadores. Es lo que muchos esperamos para el cáncer oral.
Notas
Declaración de conflictos de intereses
El autor ha completado el formulario de declaración de potenciales conflictos de intereses del ICMJE y declara no tener intereses en conflicto con la materia de este artículo.

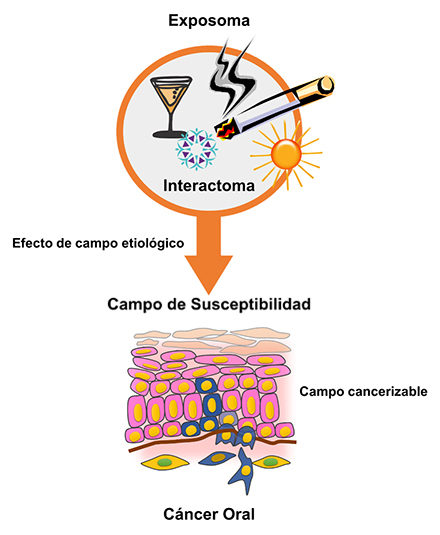 Figura 1. Historia natural del carcinoma de células escamosas de la cavidad oral.
Figura 1. Historia natural del carcinoma de células escamosas de la cavidad oral.
 Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave está bajo una licencia Creative Commons Atribución-NoComercial 3.0 Unported. Esta licencia permite el uso, distribución y reproducción del artículo en cualquier medio, siempre y cuando se otorgue el crédito correspondiente al autor del artículo y al medio en que se publica, en este caso, Medwave.

 Author:
César Rivera[1,2]
Author:
César Rivera[1,2]
Affiliation:
[1] Facultad de Ciencias de la Salud, Departamento de Ciencias Básicas Biomédicas, Universidad de Talca (UTALCA), Talca, Chile
[2] Centro Nacional de Investigación en Energía y Materiales (CNPEM), Laboratorio Nacional de Biociencias (LNBio), Campinas, Săo Paulo, Brasil
E-mail: contacto@cesarrivera.cl
Author address:
[1] Universidad de Talca Campus Norte, Laboratorio de Morfología
Avenida Lircay S/N
Talca
3460000
Región del Maule
Chile

Citation: Rivera C. Opportunities for biomarkers with potential clinical use in oral cancer. Medwave 2015 Jul;15(6):e6182 doi: 10.5867/medwave.2015.06.6186
Submission date: 9/5/2015
Acceptance date: 8/7/2015
Publication date: 20/7/2015
Origin: not requested
Type of review: reviewed by two external peer reviewers, double-blind

Comments (0)
We are pleased to have your comment on one of our articles. Your comment will be published as soon as it is posted. However, Medwave reserves the right to remove it later if the editors consider your comment to be: offensive in some sense, irrelevant, trivial, contains grammatical mistakes, contains political harangues, appears to be advertising, contains data from a particular person or suggests the need for changes in practice in terms of diagnostic, preventive or therapeutic interventions, if that evidence has not previously been published in a peer-reviewed journal.
No comments on this article.
To comment please log in
 Medwave provides HTML and PDF download counts as well as other harvested interaction metrics.
Medwave provides HTML and PDF download counts as well as other harvested interaction metrics. There may be a 48-hour delay for most recent metrics to be posted.

- Rivera C, Venegas B. Histological and molecular aspects of oral squamous cell carcinoma (Review). Oncol Lett. 2014;8(1):7-11. | PubMed |
- Strimbu K, Tavel JA. What are biomarkers? Curr Opin HIV AIDS. 2010;5(6):463-6. | PubMed |
- Drucker E, Krapfenbauer K. Pitfalls and limitations in translation from biomarker discovery to clinical utility in predictive and personalised medicine. EPMA J. 2013;4(1):7. | PubMed |
- Poste G. Bring on the biomarkers. Nature. 2011;469(7329):156-7. | PubMed |
- Yuan Y, Van Allen EM, Omberg L, Wagle N, Amin-Mansour A, Sokolov A, et al. Assessing the clinical utility of cancer genomic and proteomic data across tumor types. Nat Biotechnol. 2014;32(7):644-52. | PubMed |
- Duffy MJ, Sturgeon CM, Soletormos G, Barak V, Molina R, Hayes DF, et al. Validation of New Cancer Biomarkers: A Position Statement from the European Group on Tumor Markers. Clin Chem. 2015 Jun;61(6):809-820. | PubMed |
 Rivera C, Venegas B. Histological and molecular aspects of oral squamous cell carcinoma (Review). Oncol Lett. 2014;8(1):7-11. | PubMed |
Rivera C, Venegas B. Histological and molecular aspects of oral squamous cell carcinoma (Review). Oncol Lett. 2014;8(1):7-11. | PubMed | Drucker E, Krapfenbauer K. Pitfalls and limitations in translation from biomarker discovery to clinical utility in predictive and personalised medicine. EPMA J. 2013;4(1):7. | PubMed |
Drucker E, Krapfenbauer K. Pitfalls and limitations in translation from biomarker discovery to clinical utility in predictive and personalised medicine. EPMA J. 2013;4(1):7. | PubMed | Yuan Y, Van Allen EM, Omberg L, Wagle N, Amin-Mansour A, Sokolov A, et al. Assessing the clinical utility of cancer genomic and proteomic data across tumor types. Nat Biotechnol. 2014;32(7):644-52. | PubMed |
Yuan Y, Van Allen EM, Omberg L, Wagle N, Amin-Mansour A, Sokolov A, et al. Assessing the clinical utility of cancer genomic and proteomic data across tumor types. Nat Biotechnol. 2014;32(7):644-52. | PubMed | Duffy MJ, Sturgeon CM, Soletormos G, Barak V, Molina R, Hayes DF, et al. Validation of New Cancer Biomarkers: A Position Statement from the European Group on Tumor Markers. Clin Chem. 2015 Jun;61(6):809-820. | PubMed |
Duffy MJ, Sturgeon CM, Soletormos G, Barak V, Molina R, Hayes DF, et al. Validation of New Cancer Biomarkers: A Position Statement from the European Group on Tumor Markers. Clin Chem. 2015 Jun;61(6):809-820. | PubMed |Systematization of initiatives in sexual and reproductive health about good practices criteria in response to the COVID-19 pandemic in primary health care in Chile
Clinical, psychological, social, and family characterization of suicidal behavior in Chilean adolescents: a multiple correspondence analysis








