Key Words: amiodarone, pulmonary fibrosis, acute pulmonary toxicity
Resumen
Se sabe que la amiodarona, un potente antiarrĒtmico, causa toxicidad pulmonar. La neumonitis intersticial cr¾nica es la presentaci¾n mßs com·n. Sin embargo, la toxicidad pulmonar aguda es rara y provoca una mayor mortalidad. Se presenta un paciente de 61 a±os con fibrilaci¾n auricular persistente que, tras tratamiento por un mes con amiodarona vĒa oral a dosis baja de impregnaci¾n de 400 miligramos al dĒa, desarroll¾ toxicidad pulmonar aguda secundaria al antiarrĒtmico confirmada por radiografĒa y tomografĒa. Su caso tuvo resoluci¾n despuķs de la suspensi¾n del fßrmaco y tratamiento con esteroides.
|
Ideas clave
|
Introducción
La amiodarona es un potente antiarrítmico yodado del benzofurano que comenzó a usarse en 1967, primero como antianginoso y luego como antiarrítmico. Se aplicó en la profilaxis y tratamiento de arritmias ventriculares y supraventriculares. Su actividad antiarrítmica se debe a una prolongación del periodo refractario y del potencial de acción en el tejido miocárdico, incluyéndose como clase III en la clasificación de Vaughan-William[1].
Este fármaco tiene una vida media de 30 a 60 días y una elevada solubilidad en lípidos, con una amplia gama de efectos adversos. La concentración de la amiodarona en el pulmón es de 100 a 500 veces mayor que en el suero, con un aclaramiento en los tejidos bastante lento. Esto se demuestra en las autopsias, en donde se observa que la amiodarona puede permanecer en el pulmón hasta un año después de finalizado el tratamiento[2].
La incidencia de toxicidad pulmonar crónica (forma insidiosa que aparece luego de dos meses de tratamiento con una dosis mayor de 400 miligramos al día)[3], se encuentra en un rango de 10 a 15%[1]. No obstante, la toxicidad pulmonar aguda (que simula una neumonía) es rara y solo se evidencia en casos reportados de manera aislada[2],[3],[4],[5],[6].
Se presenta el caso de un paciente que desarrolló toxicidad pulmonar aguda por amiodarona, después de un mes de iniciado el tratamiento con dosis baja de impregnación. El objetivo del presente reporte radica en comunicar que esta toxicidad puede estar presente en periodos cortos y a bajas dosis de tratamiento con la amiodarona. También busca exponer una breve revisión de esta reacción adversa, considerada como la más grave entre las ocasionadas por este fármaco.
Reporte de caso
Se presenta un paciente de 61 años de edad, del sexo masculino, con antecedentes de salud anterior, obesidad abdominal, sin hábitos tóxicos ni antecedentes laborales de riesgo, sin medicación previa. Acudió a consulta por disnea a moderados esfuerzos y palpitaciones de tres semanas de evolución, sin otra sintomatología referida. Al examen físico se detectaron ruidos cardiacos taquiarrítmicos con una frecuencia de 154 latidos por minuto, sin otro dato de interés. Se diagnosticó una fibrilación auricular persistente y se indicó tratamiento ambulatorio con amiodarona vía oral a dosis baja de impregnación de 400 miligramos al día asociado a carvedilol (6,25 miligramos), media tableta al día y anticoagulación con warfarina.
Al mes de tratamiento el paciente acudió con empeoramiento de la disnea a los mínimos esfuerzos, tos seca pertinaz, sin otra sintomatología referida. Al examen físico presentó murmullo vesicular disminuido globalmente y crepitantes diseminados en ambos campos pulmonares, manteniendo la fibrilación auricular con respuesta ventricular rápida. Se detectó ligera leucocitosis con discreta desviación a la izquierda. Velocidad de sedimentación globular en 33 milímetros por segundo. Se evalúa por servicio de Medicina Interna y se interpreta como una insuficiencia cardiaca de debut y bronconeumonía bacteriana extrahospitalaria (Figura 1 A).
Figura 1. RadiografĒa de t¾rax posteroanterior.
Se le indica tratamiento con cefuroxima intravenosa y azitromicina vía oral, así como furosemida intravenosa en altas dosis, manteniendo la anticoagulación y el tratamiento con amiodarona vía oral.
A los cuatro días de tratamiento el paciente empeora aún más la tos y la disnea. Se le traslada a la Unidad de Cuidados Coronarios. Se realiza ecocardiograma que muestra una aceptable función sistólica biventricular y aurículas no remodeladas. Ese mismo día, se realiza urgente una tomografía computarizada de pulmón que muestra opacidades de aspecto inflamatorio con tractos fibrosos bibasales y engrosamientos septales que confieren el aspecto de patrón en “vidrio deslustrado“, lo que sugirió la posibilidad de una enfermedad pulmonar intersticial (Figura 2 A), y se sospecha la presencia de toxicidad pulmonar aguda secundaria a amiodarona.
Figura 2. TomografĒa axial computarizada de t¾rax simple (ventana de pulm¾n).
Al quinto día de iniciado el tratamiento, se suspendió la administración de amiodarona, furosemida y los antimicrobianos anteriormente referidos. Se inició tratamiento con hidrocortizona a una dosis de 100 milígramos intravenosa cada seis horas, así como control de la frecuencia ventricular asociando la digoxina (0,25 miligramos, media tableta al día por vía oral) al carvedilol. A los 10 días de suspendida la amiodarona y de recibir tratamiento con hidrocortizona, el paciente mejoró notablemente el cuadro respiratorio, con disminución de la tos y mejoría de la clase funcional. En ese momento se realizó análisis de factor reumatoide que fue negativo. Se tomó radiografía posteroanterior evolutiva que muestra una mejoría notable de las radio opacidades (Figura 1 B). En la tomografía simple evolutiva de 64 cortes realizada en ese momento, se observó una marcada mejoría pos tratamiento; aunque con persistencia del patrón en “vidrio deslustrado” y finos tractos fibrosos hacia la periferia (Figura 3 A). A los 15 días de estadía intrahospitalaria se realizó una espirometría que mostró un patrón restrictivo leve. El paciente egresó con tratamiento con prednisona a razón de un miligramo por kilogramo vía oral durante un mes. Actualmente se mantiene con clase funcional II.
Discusión
La toxicidad pulmonar por amiodarona se relaciona con varios factores: la edad y la dosis acumulada total, la duración del tratamiento, así como el sexo masculino, la historia previa de enfermedad respiratoria o de cirugía cardiotorácica, entre otros[5]. El mecanismo de daño puede ser directo (tóxico celular), indirecto de tipo autoinmune o por bloqueo del metabolismo de los fosfolípidos, con acúmulo anormal tanto en el intersticio como en los neumocitos tipo II, en los que se produce una hiperplasia. Por lo tanto, el mecanismo fisiopatológico de la amiodarona consiste en una acción combinada del fármaco junto con células T citotóxicas y la hiperplasia de los neumocitos tipo II, que darán lugar a una desestructuración del parénquima normal del pulmón[7].
Los pacientes con dosis acumuladas mayores o iguales a100 gramos o iguales o superiores a 400 miligramos al día durante más de dos meses, o 200 miligramos al día durante dos años, forman un grupo de alto riesgo[8]. La dosis de impregnación con amiodarona de 400 miligramos al día empleada en este paciente puede considerarse baja, si se tiene en cuenta que en los periodos iniciales se emplea una dosis de impregnación mayor (de 1000 a 1200 miligramos al día por un periodo de 5 a 15 días en la mayoría de los centros)[6], lo que sumado al corto periodo de tiempo (un mes) en que el paciente desarrolló la toxicidad pulmonar, confiere peculiaridad a este caso. Sobre todo, si se tiene en cuenta que la duración del tratamiento puede ser un factor de riesgo de mayor peso respecto a la dosis acumulada. En otros casos aislados[9],[10] se ha reportado la toxicidad pulmonar aguda en un periodo menor de dos semanas[9], e incluso en 48 horas, tras recibir una dosis total de 1500 miligramos intravenoso[10].
La tomografía de tórax es una herramienta esencial para el diagnóstico de toxicidad pulmonar por amiodarona, con hallazgos bien definidos que incluyen cambios pulmonares parenquimatosos, engrosamiento septal, fibrosis intersticial, opacidades intersticiales, alveolares y pleuroparenquimatosas. Otros hallazgos relacionados son imágenes difusas en vidrio despulido (generalmente bilaterales); panal de abejas y bronquiectasias por tracción[11], como en el caso que se reporta.
Ante un paciente con este cuadro clínico deben descartarse otras enfermedades, como los compromisos respiratorios reumatológicos o la neumonía eosinofílica. Sin embargo, el paciente no tenía síntomas o signos al examen físico que sugiriesen una enfermedad reumatológica y el factor reumatoide fue negativo, si bien no se disponían en el centro de anticuerpos para enfermedades autoinmunes. Además, no tuvo antecedentes de fiebre y el conteo sérico de eosinófilos fue normal. El diagnóstico precoz, la retirada del fármaco y el tratamiento con esteroides puede resolver la toxicidad pulmonar por amiodarona en dos a cuatro semanas, ya que la fibrosis pulmonar es reversible cuando se detecta oportunamente[12], como en el presente caso.
La novedad del caso que se presenta radica en la concientización de que, si bien es infrecuente, la toxicidad pulmonar aguda por amiodarona debe tenerse en cuenta en un paciente con exacerbación de síntomas respiratorios que se encuentre tomando este medicamento, a pesar del corto tiempo de iniciado el tratamiento y el empleo de dosis bajas de impregnación.
Esta reacción adversa fue comunicada al Sistema Nacional de Farmacovigilancia[13],y según los criterios de causalidad se catalogó el caso con una relación de causalidad probable.
Notas
Roles de autoría
JOCR, AAYQ: realizaron la atención clínica del paciente y escribieron, revisaron y editaron el manuscrito. JDLN: realizó, recopiló y editó las imágenes radiológicas tomadas al paciente. Todos los autores realizaron aportes críticos a la redacción del manuscrito y aprobaron la versión final del mismo.
Conflictos de intereses
Los autores han completado el formulario de declaración de conflictos de intereses del ICMJE, y declaran no haber recibido financiamiento para la realización del reporte; no tener relaciones financieras con organizaciones que podrían tener intereses en el artículo publicado; y no tener otras relaciones o actividades que podrían influir sobre el artículo publicado. Los formularios pueden ser solicitados contactando al autor responsable o a la dirección editorial de la Revista.
Financiamiento
Los autores declaran que no existió ninguna fuente de financiamiento externo.
Consideraciones éticas
El consentimiento informado solicitado por Medwave para la publicación de este reporte de caso, incluyendo las imágenes mostradas, ha sido firmado por el paciente. Los autores declaran que se respetó la privacidad del paciente según las normas de CIOMS, de privacidad de los datos recolectados. Una copia del consentimiento informado fue remitida a la dirección editorial de la revista.

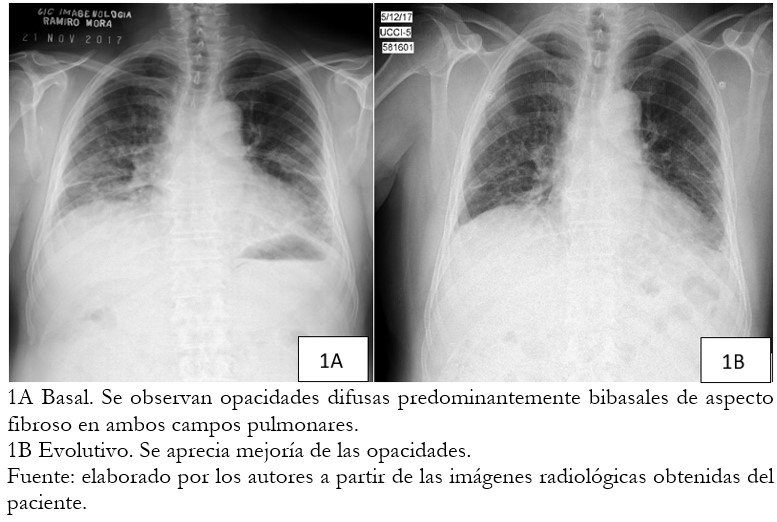 Figura 1. RadiografĒa de t¾rax posteroanterior.
Figura 1. RadiografĒa de t¾rax posteroanterior.

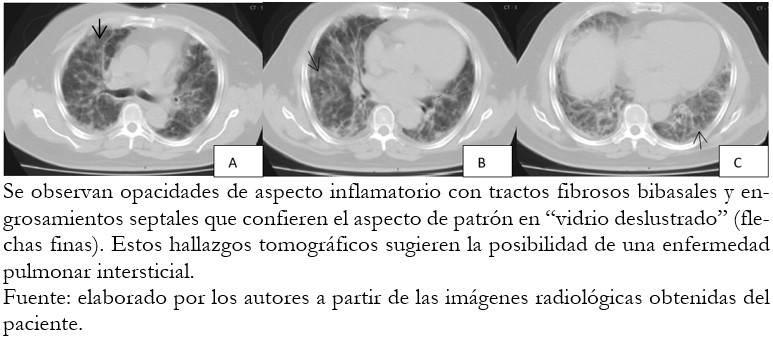 Figura 2. TomografĒa axial computarizada de t¾rax simple (ventana de pulm¾n).
Figura 2. TomografĒa axial computarizada de t¾rax simple (ventana de pulm¾n).

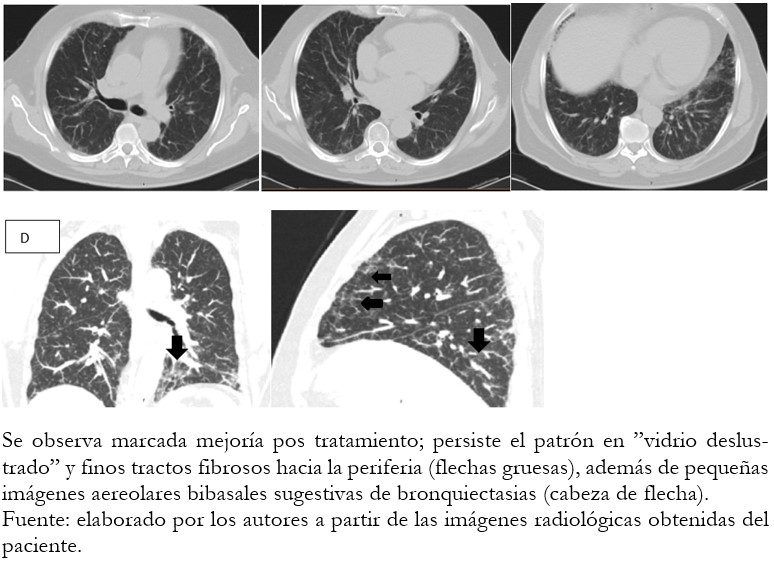 Figura 3. TomografĒa axial computarizada simple evolutiva con reconstrucciones coronales y sagitales.
Figura 3. TomografĒa axial computarizada simple evolutiva con reconstrucciones coronales y sagitales.
 Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.
Esta obra de Medwave estß bajo una licencia Creative Commons Atribuci¾n-NoComercial 3.0 Unported. Esta licencia permite el uso, distribuci¾n y reproducci¾n del artĒculo en cualquier medio, siempre y cuando se otorgue el crķdito correspondiente al autor del artĒculo y al medio en que se publica, en este caso, Medwave.

Se sabe que la amiodarona, un potente antiarrĒtmico, causa toxicidad pulmonar. La neumonitis intersticial cr¾nica es la presentaci¾n mßs com·n. Sin embargo, la toxicidad pulmonar aguda es rara y provoca una mayor mortalidad. Se presenta un paciente de 61 a±os con fibrilaci¾n auricular persistente que, tras tratamiento por un mes con amiodarona vĒa oral a dosis baja de impregnaci¾n de 400 miligramos al dĒa, desarroll¾ toxicidad pulmonar aguda secundaria al antiarrĒtmico confirmada por radiografĒa y tomografĒa. Su caso tuvo resoluci¾n despuķs de la suspensi¾n del fßrmaco y tratamiento con esteroides.
 Authors:
Julio O Cabrera-Rego[1], Josķ D Luzurriaga Navas[2], Alberto A Yanes Quintana[1]
Authors:
Julio O Cabrera-Rego[1], Josķ D Luzurriaga Navas[2], Alberto A Yanes Quintana[1]
Affiliation:
[1] Unidad de Cuidados Coronarios Intensivos, Hospital Manuel Fajardo, La Habana, Cuba
[2] Departamento de ImagenologĒa, Hospital Manuel Fajardo, La Habana, Cuba
E-mail: jocabrera@infomed.sld.cu
Author address:
[1] Zapata y D, Vedado, Plaza de La Revoluci¾n La Habana, Cuba C¾digo postal: 10400

Citation: Cabrera-Rego JO, Luzurriaga Navas JD, Yanes Quintana AA. Acute amiodarone pulmonary toxicity with low impregnation dose: case report. Medwave 2020;20(7):e7996 doi: 10.5867/medwave.2020.07.7996
Submission date: 16/1/2020
Acceptance date: 25/7/2020
Publication date: 14/8/2020
Origin: Not commissioned
Type of review: Amiodarone, Pulmonary fibrosis, Acute pulmonary toxicity

Comments (0)
We are pleased to have your comment on one of our articles. Your comment will be published as soon as it is posted. However, Medwave reserves the right to remove it later if the editors consider your comment to be: offensive in some sense, irrelevant, trivial, contains grammatical mistakes, contains political harangues, appears to be advertising, contains data from a particular person or suggests the need for changes in practice in terms of diagnostic, preventive or therapeutic interventions, if that evidence has not previously been published in a peer-reviewed journal.
No comments on this article.
To comment please log in
 Medwave provides HTML and PDF download counts as well as other harvested interaction metrics.
Medwave provides HTML and PDF download counts as well as other harvested interaction metrics. There may be a 48-hour delay for most recent metrics to be posted.

- Exp¾sito ME, Fernßndez V, San Miguel MT. Fibrosis pulmonar asociada a amiodarona. A prop¾sito de un caso. Farm Hosp. 1995;19(6):371-3. [On line]. | Link |
- Kaya SB, Deger S, Hacievliyagil SS, Aytemur ZA. Acute amiodarone toxicity causing respiratory failure. Rev Assoc Med Bras (1992). 2017 Mar;63(3):210-212. | CrossRef | PubMed |
- Singh VK, Maheshwari V. Acute Respiratory Distress Syndrome Complicated by Amiodarone Induced Pulmonary Fibrosis: Don't Let Your Guard Down. J Clin Diagn Res. 2017 Apr;11(4):UD01-UD02. | CrossRef | PubMed |
- Lohiya RV, Pethe MP. Early Recognition of Acute Pneumonitis in Amiodarone Treatment. Heart Views. 2018 Jul-Sep;19(3):109-113. | CrossRef | PubMed |
- Abuzaid A, Saad M, Ayan M, Kabach A, Haddad TM, Smer A, et al. Acute Amiodarone Pulmonary Toxicity after Drug Holiday: A Case Report and Review of the Literature. Case Rep Cardiol. 2015;2015:927438. | CrossRef | PubMed |
- Range FT, Hilker E, Breithardt G, Buerke B, Lebiedz P. Amiodarone-induced pulmonary toxicity--a fatal case report and literature review. Cardiovasc Drugs Ther. 2013 Jun;27(3):247-54. | CrossRef | PubMed |
- Lancha-DomĒnguez J, RamĒrez-Sßnchez MM, Pßez-Rubio MI. Toxicidad pulmonar asociada a tratamiento con amiodarona. Rev Esp Casos Clin Med Intern (RECCMI). 2019; 4(2):57-60. | CrossRef |
- Schwaiblmair M, Berghaus T, Haeckel T, Wagner T, von Scheidt W. Amiodarone-induced pulmonary toxicity: an under-recognized and severe adverse effect? Clin Res Cardiol. 2010 Nov;99(11):693-700. | CrossRef | PubMed |
- Kharabsheh S, Abendroth CS, Kozak M. Fatal pulmonary toxicity occurring within two weeks of initiation of amiodarone. Am J Cardiol. 2002 Apr 1;89(7):896-8. | CrossRef | PubMed |
- Subban V, Kalidoss L, Lakshmanan A, Ajit MS. Acute amiodarone pulmonary toxicity in a patient with acute anterior wall myocardial infarction and ventricular tachycardia. Sahel Med J. 2013;16(4):165-7. | CrossRef |
- Bahena-L¾pez E, Bucio-Reta E, Bahena-L¾pez JP. Toxicidad pulmonar por amiodarona. Rev Invest Med Sur Mex. 2015;22(4):214-7. [On line]. | Link |
- Sßnchez S, Zamora E, Hoyos N, Naranjo A, Al Nakeeb Z, Gir¾n RM. Fibrosis pulmonar por amiodarona. Rev Patol Respir. 2006;9(2):77-80. [On line]. | Link |
- Jimķnez L¾pez G, Alonso Orta I. Normas y procedimientos de trabajo del Sistema Cubano de Farmacovigilancia. La Habana: Ministerio de Salud P·blica (MINSAP), Direcci¾n Nacional de Medicamentos y Equipos Mķdicos; 2012.
 Exp¾sito ME, Fernßndez V, San Miguel MT. Fibrosis pulmonar asociada a amiodarona. A prop¾sito de un caso. Farm Hosp. 1995;19(6):371-3. [On line]. | Link |
Exp¾sito ME, Fernßndez V, San Miguel MT. Fibrosis pulmonar asociada a amiodarona. A prop¾sito de un caso. Farm Hosp. 1995;19(6):371-3. [On line]. | Link | Kaya SB, Deger S, Hacievliyagil SS, Aytemur ZA. Acute amiodarone toxicity causing respiratory failure. Rev Assoc Med Bras (1992). 2017 Mar;63(3):210-212. | CrossRef | PubMed |
Kaya SB, Deger S, Hacievliyagil SS, Aytemur ZA. Acute amiodarone toxicity causing respiratory failure. Rev Assoc Med Bras (1992). 2017 Mar;63(3):210-212. | CrossRef | PubMed | Singh VK, Maheshwari V. Acute Respiratory Distress Syndrome Complicated by Amiodarone Induced Pulmonary Fibrosis: Don't Let Your Guard Down. J Clin Diagn Res. 2017 Apr;11(4):UD01-UD02. | CrossRef | PubMed |
Singh VK, Maheshwari V. Acute Respiratory Distress Syndrome Complicated by Amiodarone Induced Pulmonary Fibrosis: Don't Let Your Guard Down. J Clin Diagn Res. 2017 Apr;11(4):UD01-UD02. | CrossRef | PubMed | Lohiya RV, Pethe MP. Early Recognition of Acute Pneumonitis in Amiodarone Treatment. Heart Views. 2018 Jul-Sep;19(3):109-113. | CrossRef | PubMed |
Lohiya RV, Pethe MP. Early Recognition of Acute Pneumonitis in Amiodarone Treatment. Heart Views. 2018 Jul-Sep;19(3):109-113. | CrossRef | PubMed | Abuzaid A, Saad M, Ayan M, Kabach A, Haddad TM, Smer A, et al. Acute Amiodarone Pulmonary Toxicity after Drug Holiday: A Case Report and Review of the Literature. Case Rep Cardiol. 2015;2015:927438. | CrossRef | PubMed |
Abuzaid A, Saad M, Ayan M, Kabach A, Haddad TM, Smer A, et al. Acute Amiodarone Pulmonary Toxicity after Drug Holiday: A Case Report and Review of the Literature. Case Rep Cardiol. 2015;2015:927438. | CrossRef | PubMed | Range FT, Hilker E, Breithardt G, Buerke B, Lebiedz P. Amiodarone-induced pulmonary toxicity--a fatal case report and literature review. Cardiovasc Drugs Ther. 2013 Jun;27(3):247-54. | CrossRef | PubMed |
Range FT, Hilker E, Breithardt G, Buerke B, Lebiedz P. Amiodarone-induced pulmonary toxicity--a fatal case report and literature review. Cardiovasc Drugs Ther. 2013 Jun;27(3):247-54. | CrossRef | PubMed | Lancha-DomĒnguez J, RamĒrez-Sßnchez MM, Pßez-Rubio MI. Toxicidad pulmonar asociada a tratamiento con amiodarona. Rev Esp Casos Clin Med Intern (RECCMI). 2019; 4(2):57-60. | CrossRef |
Lancha-DomĒnguez J, RamĒrez-Sßnchez MM, Pßez-Rubio MI. Toxicidad pulmonar asociada a tratamiento con amiodarona. Rev Esp Casos Clin Med Intern (RECCMI). 2019; 4(2):57-60. | CrossRef | Schwaiblmair M, Berghaus T, Haeckel T, Wagner T, von Scheidt W. Amiodarone-induced pulmonary toxicity: an under-recognized and severe adverse effect? Clin Res Cardiol. 2010 Nov;99(11):693-700. | CrossRef | PubMed |
Schwaiblmair M, Berghaus T, Haeckel T, Wagner T, von Scheidt W. Amiodarone-induced pulmonary toxicity: an under-recognized and severe adverse effect? Clin Res Cardiol. 2010 Nov;99(11):693-700. | CrossRef | PubMed | Kharabsheh S, Abendroth CS, Kozak M. Fatal pulmonary toxicity occurring within two weeks of initiation of amiodarone. Am J Cardiol. 2002 Apr 1;89(7):896-8. | CrossRef | PubMed |
Kharabsheh S, Abendroth CS, Kozak M. Fatal pulmonary toxicity occurring within two weeks of initiation of amiodarone. Am J Cardiol. 2002 Apr 1;89(7):896-8. | CrossRef | PubMed | Subban V, Kalidoss L, Lakshmanan A, Ajit MS. Acute amiodarone pulmonary toxicity in a patient with acute anterior wall myocardial infarction and ventricular tachycardia. Sahel Med J. 2013;16(4):165-7. | CrossRef |
Subban V, Kalidoss L, Lakshmanan A, Ajit MS. Acute amiodarone pulmonary toxicity in a patient with acute anterior wall myocardial infarction and ventricular tachycardia. Sahel Med J. 2013;16(4):165-7. | CrossRef | Bahena-L¾pez E, Bucio-Reta E, Bahena-L¾pez JP. Toxicidad pulmonar por amiodarona. Rev Invest Med Sur Mex. 2015;22(4):214-7. [On line]. | Link |
Bahena-L¾pez E, Bucio-Reta E, Bahena-L¾pez JP. Toxicidad pulmonar por amiodarona. Rev Invest Med Sur Mex. 2015;22(4):214-7. [On line]. | Link | Sßnchez S, Zamora E, Hoyos N, Naranjo A, Al Nakeeb Z, Gir¾n RM. Fibrosis pulmonar por amiodarona. Rev Patol Respir. 2006;9(2):77-80. [On line]. | Link |
Sßnchez S, Zamora E, Hoyos N, Naranjo A, Al Nakeeb Z, Gir¾n RM. Fibrosis pulmonar por amiodarona. Rev Patol Respir. 2006;9(2):77-80. [On line]. | Link | Jimķnez L¾pez G, Alonso Orta I. Normas y procedimientos de trabajo del Sistema Cubano de Farmacovigilancia. La Habana: Ministerio de Salud P·blica (MINSAP), Direcci¾n Nacional de Medicamentos y Equipos Mķdicos; 2012.
Jimķnez L¾pez G, Alonso Orta I. Normas y procedimientos de trabajo del Sistema Cubano de Farmacovigilancia. La Habana: Ministerio de Salud P·blica (MINSAP), Direcci¾n Nacional de Medicamentos y Equipos Mķdicos; 2012. Systematization of initiatives in sexual and reproductive health about good practices criteria in response to the COVID-19 pandemic in primary health care in Chile
Clinical, psychological, social, and family characterization of suicidal behavior in Chilean adolescents: a multiple correspondence analysis








